Содержание
- 2. Раздел 1 Закон поглощения света
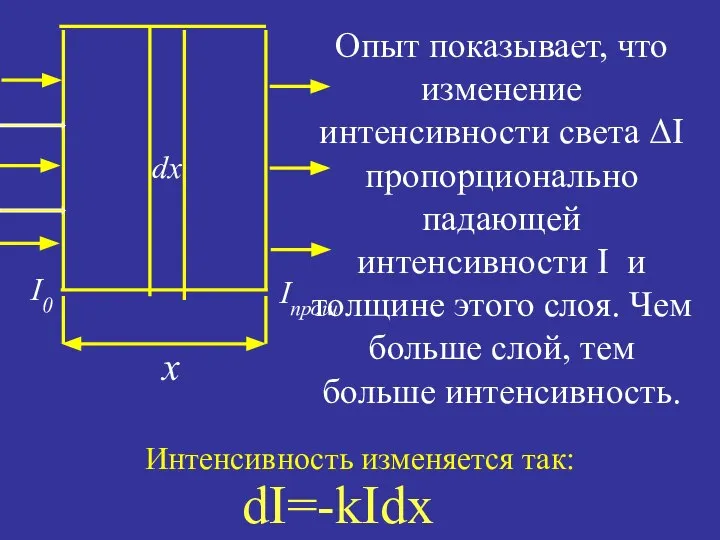
- 3. Опыт показывает, что изменение интенсивности света ΔI пропорционально падающей интенсивности I и толщине этого слоя. Чем
- 4. dI = - kIdx = - kdx S = - kSdx ln I = - k
- 5. Iпрош = Io – закон поглощения света (закон Бугера) Коэффициент k называют показатель поглощения. Измеряется в
- 6. К = αс – закон Бера α - удельный показатель поглощения; с – концентрация; α зависит
- 7. Отношение Iпрош. к I0 Т = = – коэффициент пропускания D = lg = - lg
- 8. Определив зависимость D от λ, можно узнать тип вещества, то есть провести качественный анализ. Зная коэффициенты
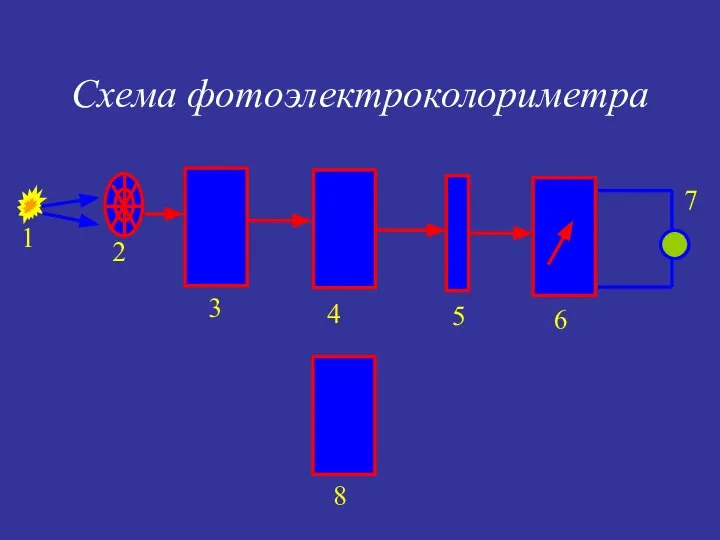
- 9. Схема фотоэлектроколориметра 1 2 3 4 5 6 7 8
- 10. 1-источник света 2-линза 3-светофильтр 4-кювета с растворителем 5-фотометрический клин 6-фотоэлемент 7-микроамперметр 8-кювета с раствором
- 11. Передвигая оптический клин , можно изменять силу тока , в частности , установить ее равной 100
- 12. Раздел 2 Рассеяние света
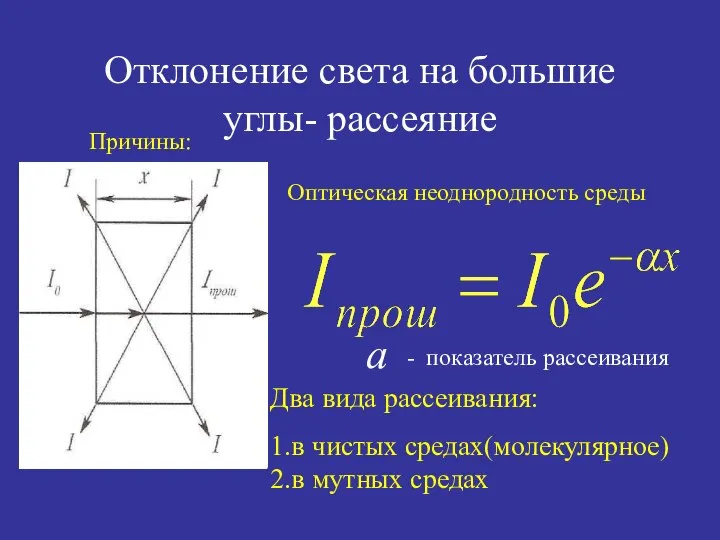
- 13. Отклонение света на большие углы- рассеяние Причины: Оптическая неоднородность среды - показатель рассеивания Два вида рассеивания:
- 14. Молекулярное рассеивание наблюдается ,если d где d-размер неоднородности(частиц), а λ -длина волны (в воздухе ,в воде
- 15. Раздел 3 Оптические спектры атомов
- 16. Впервые происхождение спектров атомов смог объяснить Нильс Бор. Постулаты Бора 1.Электроны в атоме могут находиться только
- 17. 2.При переходе атома из одного состояния в другое, он излучает или поглощает квант электромагнитной энергии. hν
- 18. Найдем радиусы стационарных орбит электронов Потенциальная энергия электрона Кинетическая энергия Полная энергия электрона в атоме всегда
- 19. Полная энергия электрона в стационарных состояниях где
- 20. Полная энергия электрона равна: Е = - E0/ E0 = 13,6 эВ; n – номер орбиты
- 21. У каждого атома свой номер (z), следовательно, набор возможных энергетических состояний у каждого атома и элемента
- 22. РАЗДЕЛ 4 Спектр атома водорода.
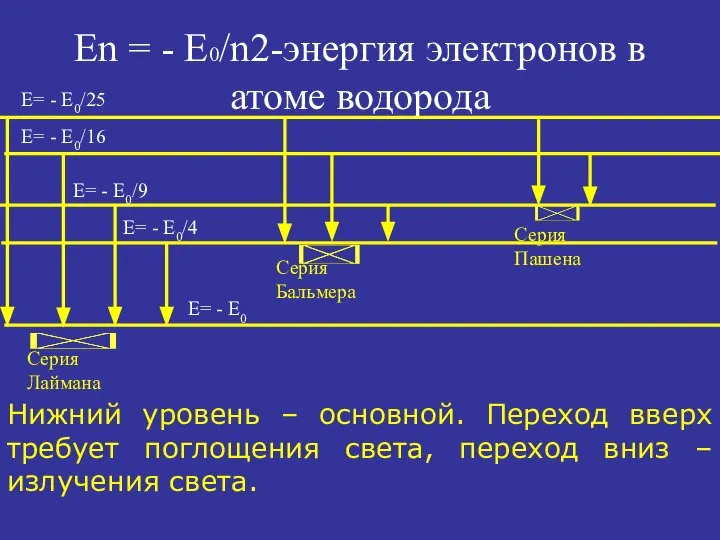
- 23. Еn = - E0/n2-энергия электронов в атоме водорода Нижний уровень – основной. Переход вверх требует поглощения
- 24. Частоты спектральных линий ν = (Ек – Еn)/h = где n = 1, 2, 3, 4…;
- 25. Основные спектральные серии водорода Спектральная серия – группа линий в спектре веществ, которым соответствуют переходы электронов
- 26. 2.Серия Бальмера n = 2 k ≥ 3 ν = лежит в видимой области спектра Серия
- 27. РАЗДЕЛ 5 Спектры сложных атомов.
- 28. Энергия электронов в сложных атомах зависит не только от главного квантового числа (h), но и от
- 29. По принципу Паули в одном квантовом состоянии в атоме может находиться не более одного электрона. Последовательность
- 30. Переходы между уровнями подразделяются: а) излучательные (оптические) – поглощения будут возникать при переходе электронов из основного
- 31. Оптические переходы подчиняются правилам отбора: Δl = ± 1 S = 0. Энергоуровни, переходы из которых
- 32. РАЗДЕЛ 6 Спектры молекул.
- 33. Е мол. = Еэл. дв. + Екол. дв. + Евращ., где Екол. дв - колебательное движение
- 34. Спектры поглощения возникают при переходах молекулы из нижних подуровней основных состояний в верхние состояния. Испускание происходит
- 35. Спектры люминесценции молекул не совпадают по положению со спектрами поглощения, а смещены относительно их в сторону
- 36. РАЗДЕЛ 7 Виды спектров.
- 37. = ν = Электронно-колебательные-вращательные. Электронные спектры ΔЕэл ≠ 0 ΔЕкол ≠ 0 ΔЕвращ ≠ 0 2.Колебательно-
- 38. РАЗДЕЛ 8 Люминесценция
- 39. Если атом или молекула совершает оптический переход из возбуждения в основное состояние, то испускаемое излучение называют
- 40. а) фотолюминесценция – возбуждение поглощения электромагнитной энергией; б) катодолюминесценция - возбуждение электрическим ударом; в) электролюминесценция -
- 41. г) рентгенолюминесценция – возбуждение рентгеновскими лучами. д) химилюминесценция – возбуждение в результате химической реакции. А +
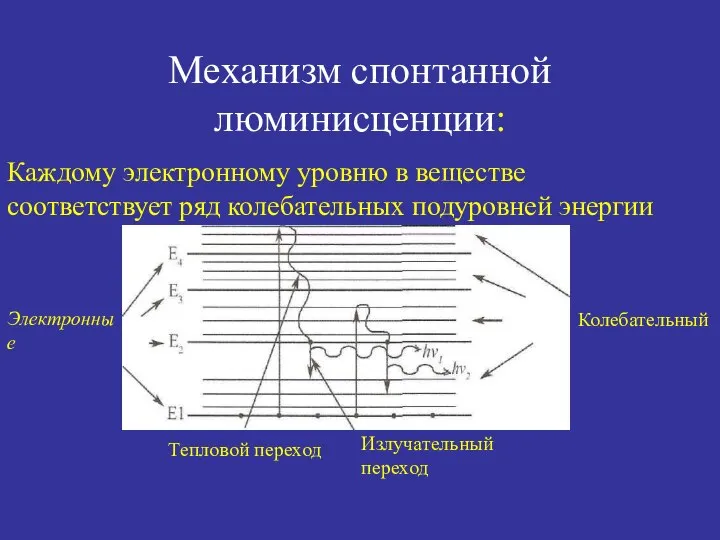
- 42. Механизм спонтанной люминисценции: Каждому электронному уровню в веществе соответствует ряд колебательных подуровней энергии Электронные Тепловой переход
- 43. Эти кванты (hv) и представляют собой кванты люминисценции. А различие их энергии определяет спектр люминисценции. Таким
- 44. Характеристики и законы люминисценции Спектр возбуждения - это зависимость возбуждающего люминисценцию света от длины волны Спектр
- 45. Если изменяется электронная энергия , то спектр называется электронно-колебательно-вращательным Электронные: полосы которых расположены в ультрафиолетовой ,
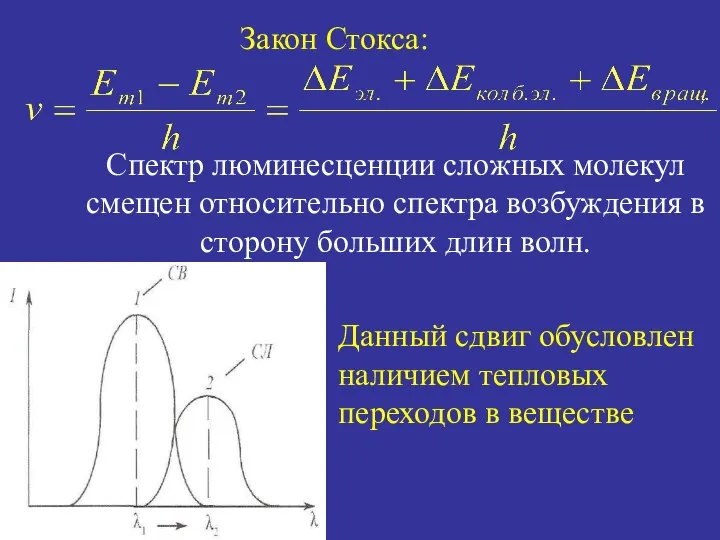
- 46. Спектр люминесценции сложных молекул смещен относительно спектра возбуждения в сторону больших длин волн. Данный сдвиг обусловлен
- 47. Закон Вавилова: Спектр люминисценции сложных молекул является характеристикой вещества и не зависит от длины волны возбуждающего
- 48. Квантовый выход люминиценции: Это отношение числа квантов излучаемых веществом к числу поглощенных квантов возбуждающего света. если
- 49. После прекращения возбуждения Iлюм. уменьшается по закону: Iлюм. = I0 τ - длительность люминесценции определяет время,
- 50. В зависимости от того, что помещают в фокальную плоскость (7), различают следующие приборы: если стеклянная пластинка,
- 51. -если узкую щель, то получаем монохромат – прибор для улавливания узкого спектрального диапазона излучения. -спектрометр(в фокальной
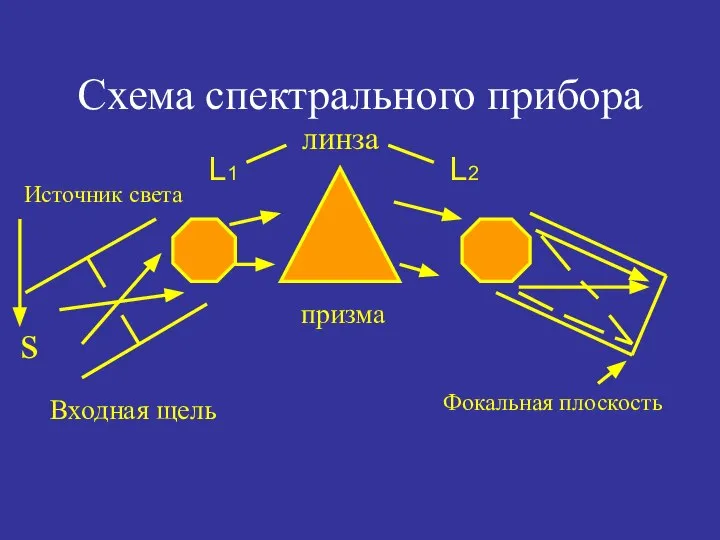
- 52. Схема спектрального прибора s Входная щель призма Фокальная плоскость Источник света линза L1 L2
- 53. Применение в медицине Например в санитарии проверяют доброкачественность мяса . Измеряется люминисценция белкового экстракта. Свет люминисценции
- 54. Вторичная люминисценция биологических объектов Вещества, которыми подкрашиваются биологические объекты, называются люминофорами. Существуют два вида люминофоров. 1.Если
- 56. Лукьяница Владимир Васильевич доцент кафедры физики
- 57. ЛАЗЕРЫ ИСПОЛЬЗОВАНИЕ В МЕДИЦИНЕ И ИХ
- 58. Введение. Свойства лазерного излучения Раздел 1. Устройство, принципы работы и классификация лазеров Раздел 2. Преимущества полупроводниковых
- 59. СВОЙСТВА ЛАЗЕРНОГО ИЗЛУЧЕНИЯ
- 60. 1. Высокая направленность или малая расходимость лазерного луча (несколько угловых минут) 2. Монохроматичность (λ=const, Δλ≈0,01нм) 3.
- 61. УСТРОЙСТВО, ПРИНЦИПЫ РАБОТЫ И КЛАССИФИКАЦИЯ ЛАЗЕРОВ
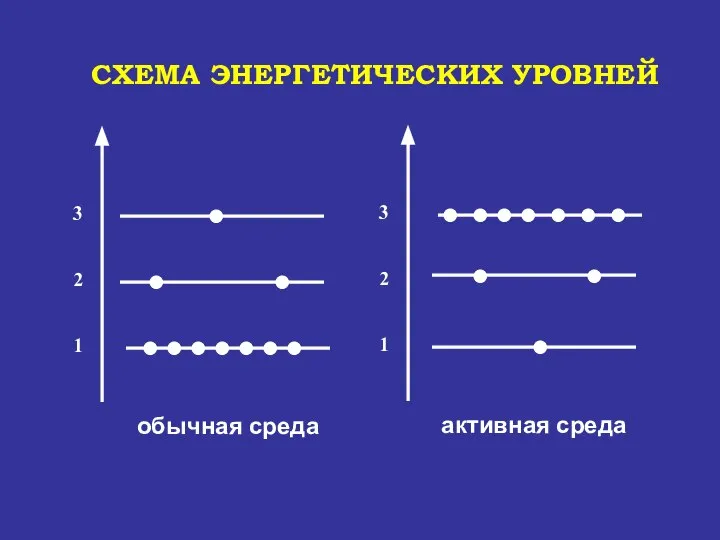
- 62. СХЕМА ЭНЕРГЕТИЧЕСКИХ УРОВНЕЙ
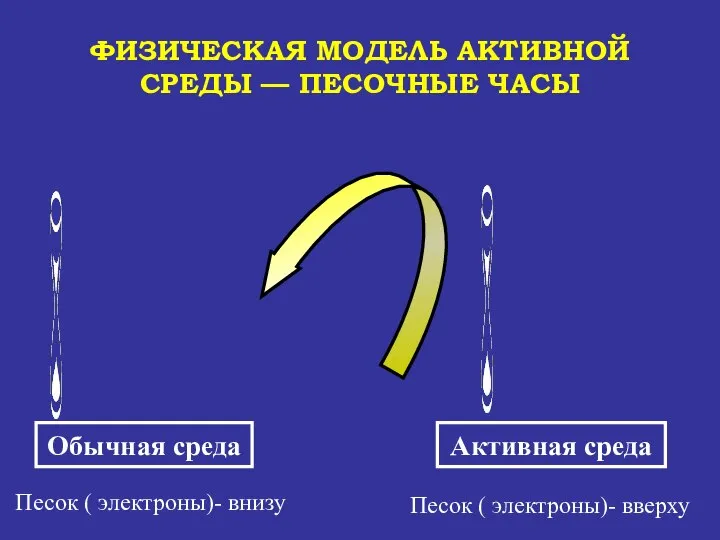
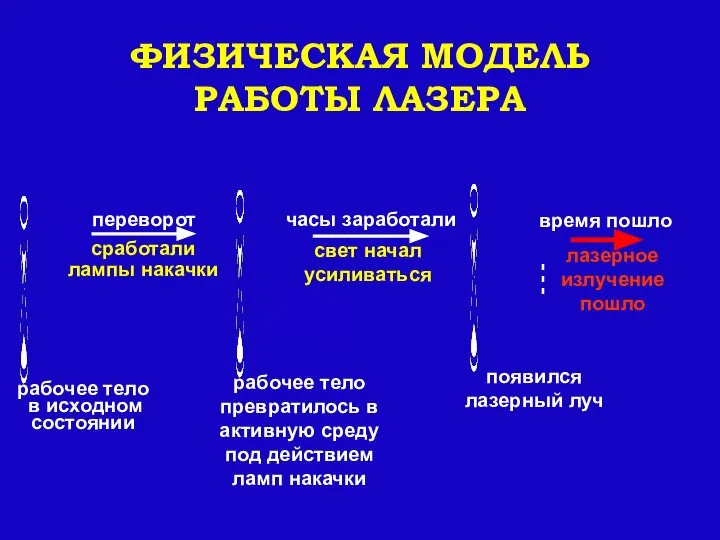
- 63. ФИЗИЧЕСКАЯ МОДЕЛЬ АКТИВНОЙ СРЕДЫ — ПЕСОЧНЫЕ ЧАСЫ Обычная среда Песок ( электроны)- внизу Активная среда Песок
- 64. Нет, давай сходим в кино Пойдем в библиотеку
- 65. Идем на дискотеку
- 66. Посмотри на эту малышку
- 67. Она что, читать сюда пришла? Нет, вместо библиотеки её занесло сюда «вынужденным излучением»
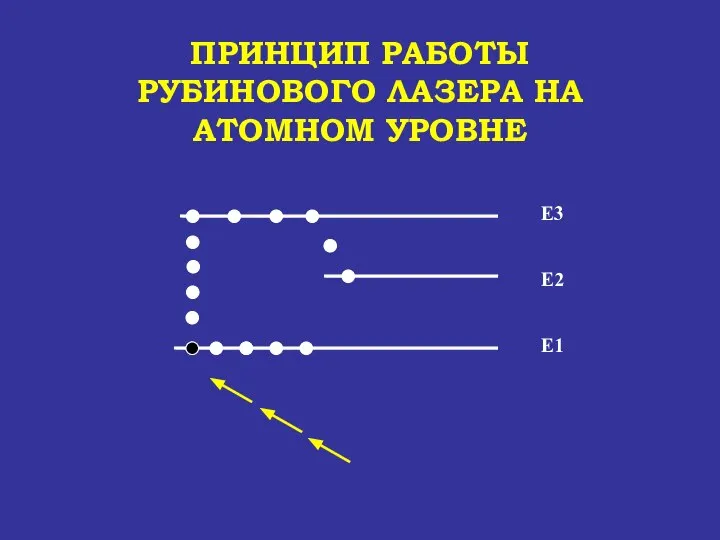
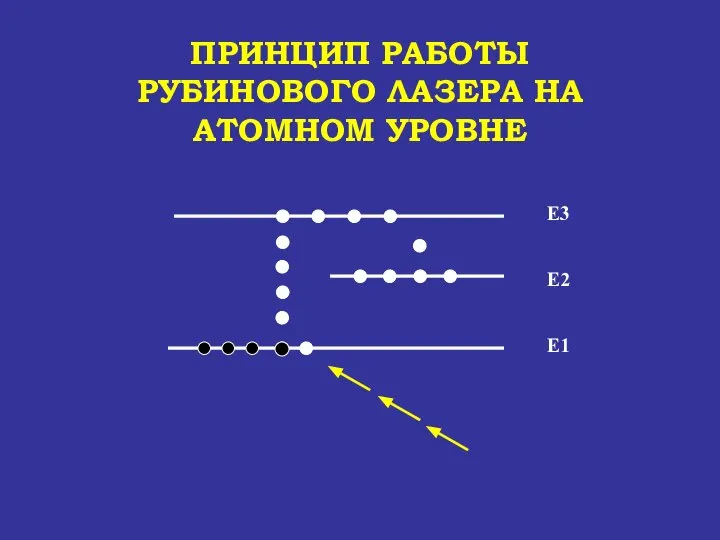
- 68. ПРИНЦИП РАБОТЫ РУБИНОВОГО ЛАЗЕРА НА АТОМНОМ УРОВНЕ Е1 Е2 Е3
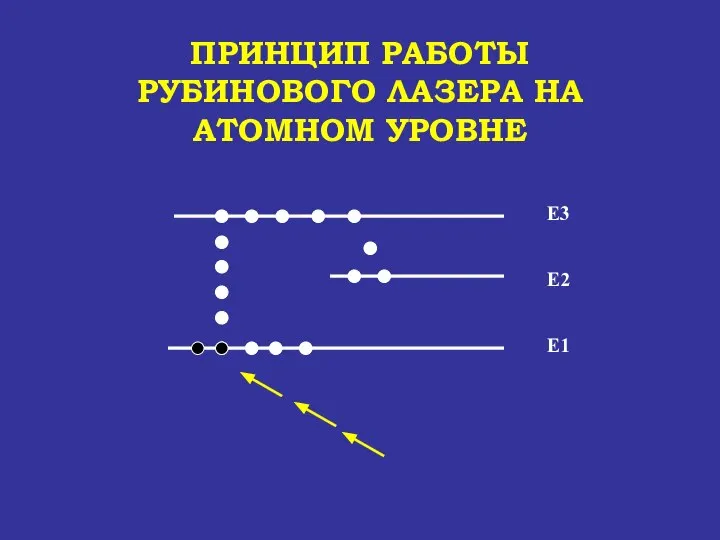
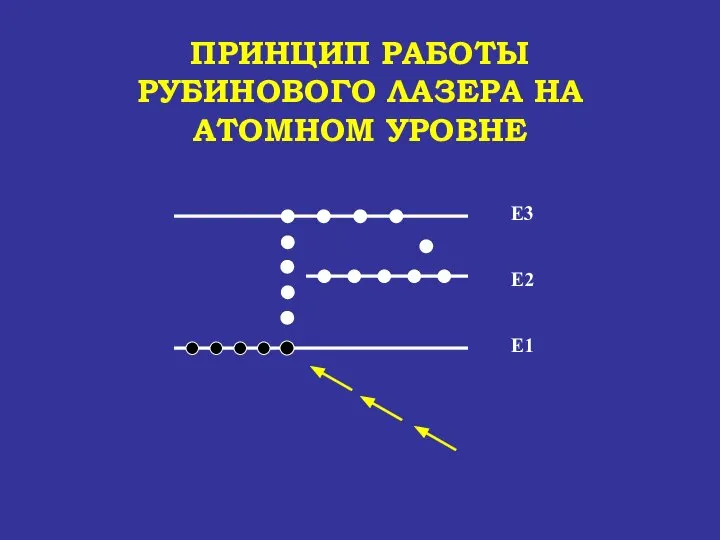
- 69. ПРИНЦИП РАБОТЫ РУБИНОВОГО ЛАЗЕРА НА АТОМНОМ УРОВНЕ Е1 Е2 Е3
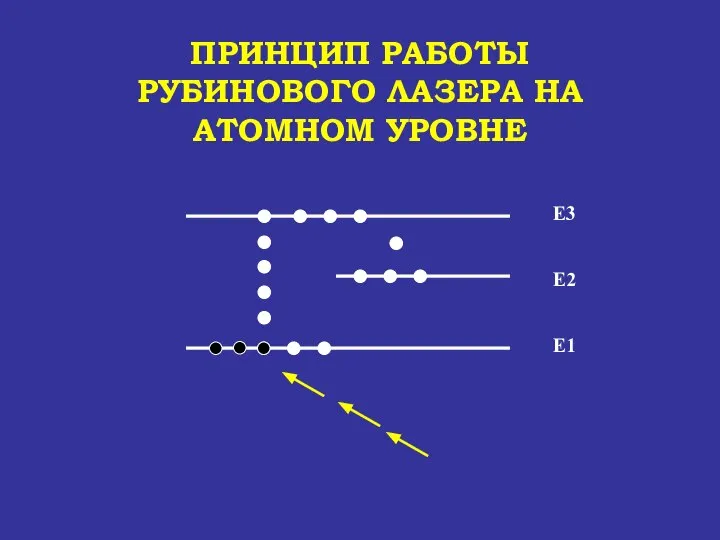
- 70. ПРИНЦИП РАБОТЫ РУБИНОВОГО ЛАЗЕРА НА АТОМНОМ УРОВНЕ Е1 Е2 Е3
- 71. ПРИНЦИП РАБОТЫ РУБИНОВОГО ЛАЗЕРА НА АТОМНОМ УРОВНЕ Е1 Е2 Е3
- 72. ПРИНЦИП РАБОТЫ РУБИНОВОГО ЛАЗЕРА НА АТОМНОМ УРОВНЕ Е1 Е2 Е3
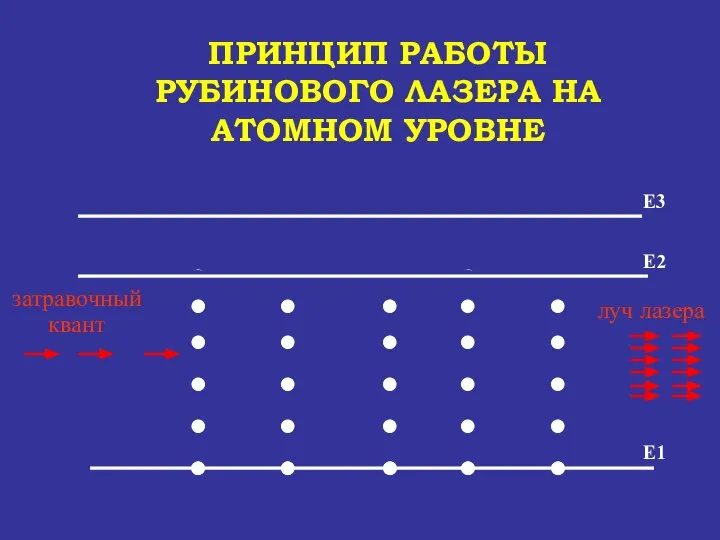
- 73. ПРИНЦИП РАБОТЫ РУБИНОВОГО ЛАЗЕРА НА АТОМНОМ УРОВНЕ Е1 Е2 Е3 затравочный квант луч лазера
- 74. УСИЛЕНИЕ СВЕТА АКТИВНОЙ СРЕДОЙ
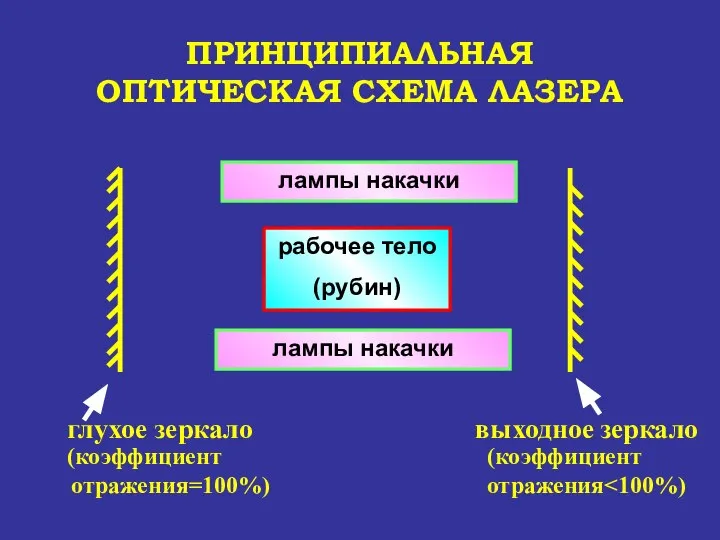
- 75. ПРИНЦИПИАЛЬНАЯ ОПТИЧЕСКАЯ СХЕМА ЛАЗЕРА рабочее тело (рубин)
- 76. НАЗНАЧЕНИЕ ОСНОВНЫХ ЭЛЕМЕНТОВ ЛАЗЕРА 1. Рабочее тело (акивная среда) генерирует и усиливает лазерное излучение (свет) 2.
- 77. НАЗНАЧЕНИЕ ОСНОВНЫХ ЭЛЕМЕНТОВ ЛАЗЕРА 3. Резонатор а) посредством отражения света от зеркал искусственно удлиняет путь L
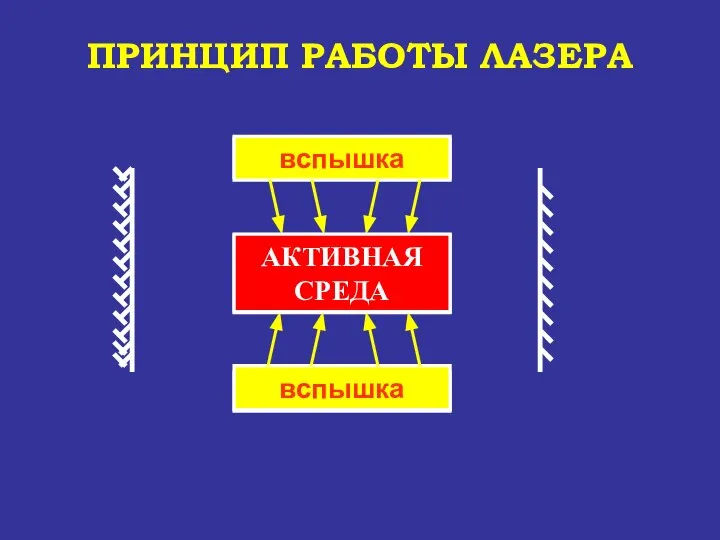
- 78. ПРИНЦИП РАБОТЫ ЛАЗЕРА РАБОЧЕЕ ТЕЛО
- 79. ПРИНЦИП РАБОТЫ ЛАЗЕРА РАБОЧЕЕ ТЕЛО АКТИВНАЯ СРЕДА
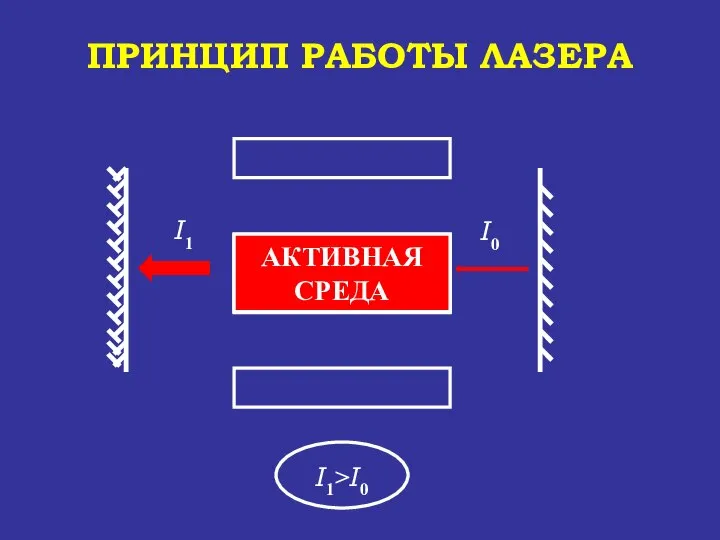
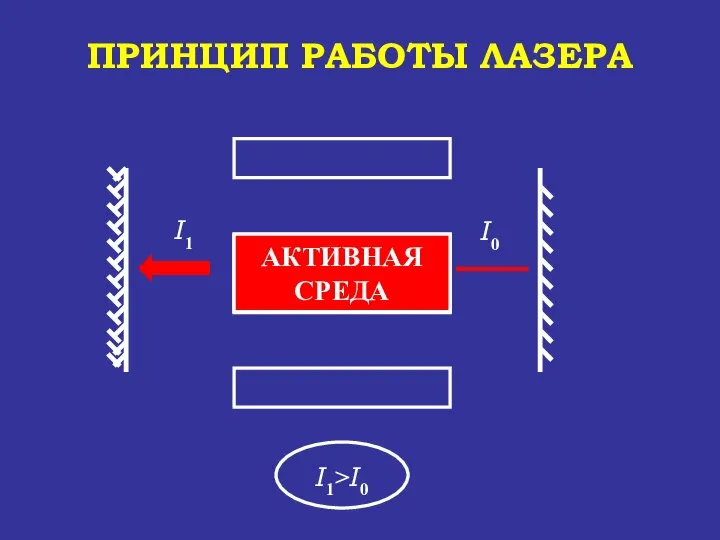
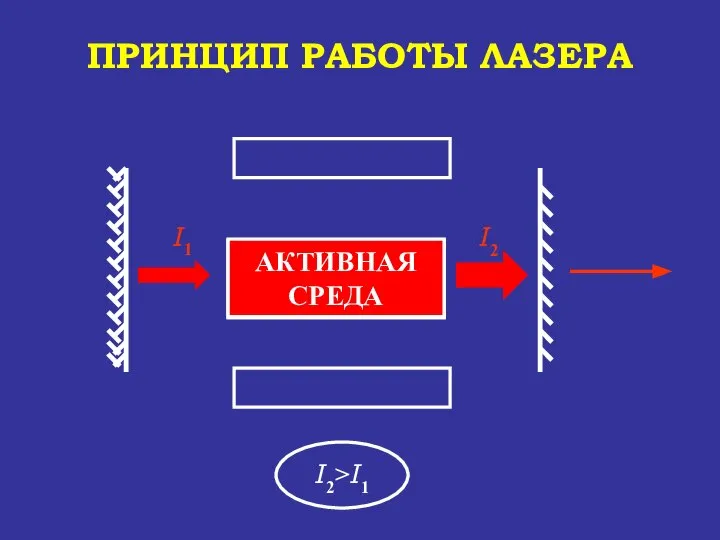
- 80. АКТИВНАЯ СРЕДА УСИЛЕНИЕ СВЕТА АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА
- 81. АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА УСИЛЕНИЕ СВЕТА АКТИВНАЯ СРЕДА
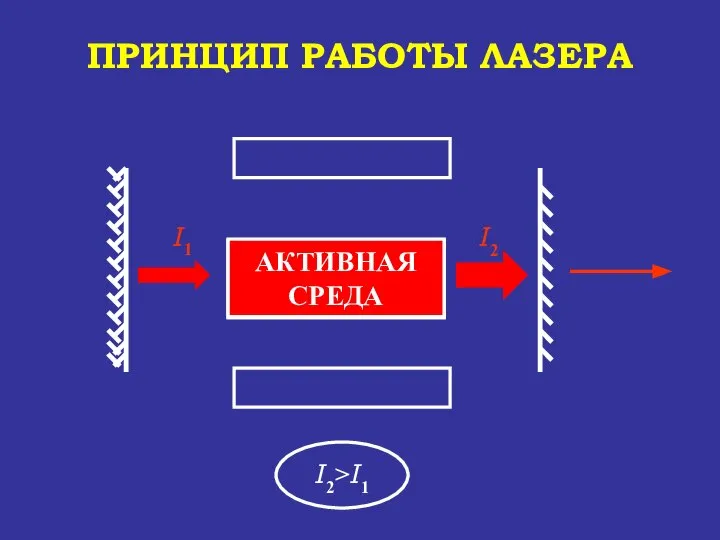
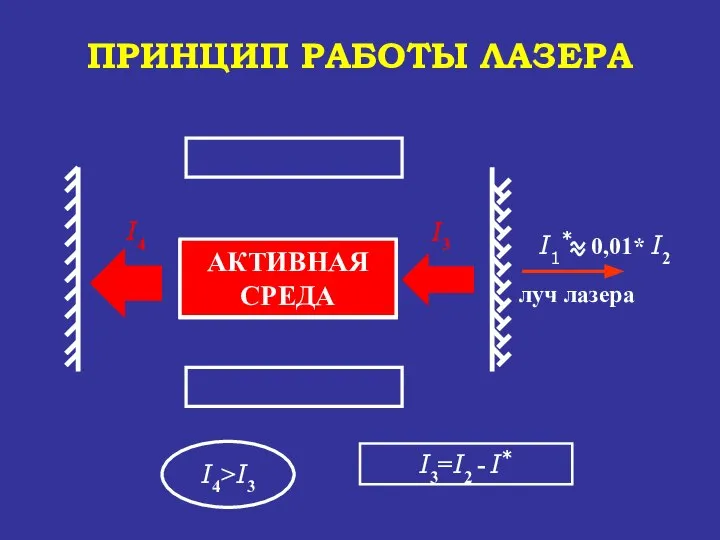
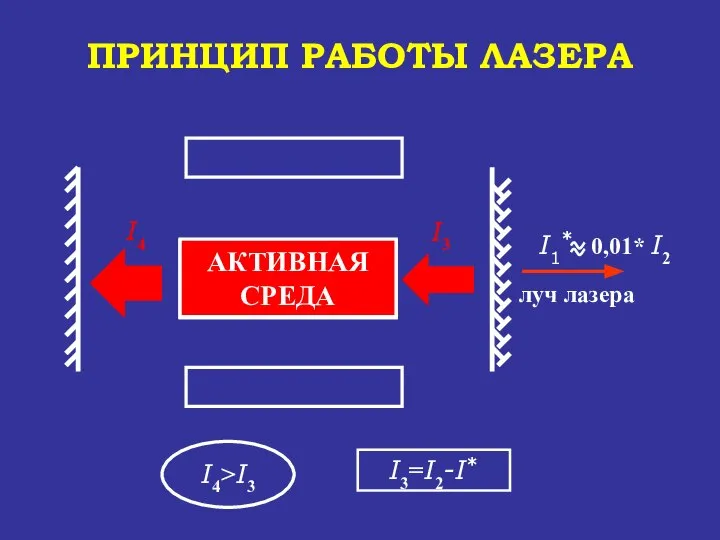
- 82. АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА луч лазера I1* 0,01* I2 I3=I2 - I* УСИЛЕНИЕ СВЕТА АКТИВНАЯ
- 83. АКТИВНАЯ СРЕДА АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА луч лазера I2* 0,01* I5 I2* >I1* УСИЛЕНИЕ СВЕТА
- 84. И так далее до истощения активной среды (I*=const). Затем опять срабатывают лампы накачки, которые поддерживают активную
- 85. ПРИНЦИП РАБОТЫ ЛАЗЕРА РАБОЧЕЕ ТЕЛО
- 86. ПРИНЦИП РАБОТЫ ЛАЗЕРА РАБОЧЕЕ ТЕЛО АКТИВНАЯ СРЕДА
- 87. АКТИВНАЯ СРЕДА УСИЛЕНИЕ СВЕТА АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА
- 88. АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА УСИЛЕНИЕ СВЕТА АКТИВНАЯ СРЕДА
- 89. АКТИВНАЯ СРЕДА ПРИНЦИП РАБОТЫ ЛАЗЕРА луч лазера I1* 0,01* I2 I3=I2-I* УСИЛЕНИЕ СВЕТА АКТИВНАЯ СРЕДА
- 90. ФИЗИЧЕСКАЯ МОДЕЛЬ РАБОТЫ ЛАЗЕРА
- 91. ПРЕИМУЩЕСТВА ПОЛУПРОВОДНИКОВОГО ЛАЗЕРА
- 92. 1. Малые габариты (размеры), что обусловлено использованием не ламп, а p-n-переходов для накачки 3. Высокий КПД
- 93. ПРИМЕНЕНИЕ ЛАЗЕРОВ В КЛИНИКЕ
- 94. а) лазерные приборы иммунологических реакций, нефелометры, спектрофотометры б) исследования микроциркуляции крови в различных органах и тканях
- 97. стимуляция обменных процессов и активация механизмов саногенеза (используются низкоэнергетические приборы). Время зонального воздействия определяется из формулы:
- 98. ТЕРАПЕВТИЧЕСКОЕ ДЕЙСТВИЕ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ 1. Противовоспалительное 2. Обезболивающее 3. Спазмолитическое 5. Стиммулирующее обменные и регенеративные процессы
- 99. МЕХАНИЗМЫ ЛАЗЕРНОГО ВОЗДЕЙСТВИЯ
- 100. ОСНОВНЫЕ КОНЦЕПЦИИ, ОБЪЯСНЯЮЩИЕ МЕХАНИЗМЫ ЛАЗЕРНОГО ВОЗДЕЙСТВИЯ 1. Теория поглощения 2. Нейрорефлекторная теория 3. Теория резонансного волнового
- 101. ТЕХНИКА БЕЗОПАСНОСТИ
- 102. ЛАЗЕРНАЯ БЕЗОПАСНОСТЬ По степени опасности лазеры делятся на 4 класса: I - безопасные (излучение не опасно
- 103. СПОСОБЫ ЗАЩИТЫ ОТ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ 1. Коллективные: телевизионные системы; защитные экраны, бленды и диафрагмы; системы блокировки
- 104. ДЕМОНСТРАЦИОННЫЕ ОПЫТЫ
- 105. КОНТРОЛЬНЫЕ ВОПРОСЫ
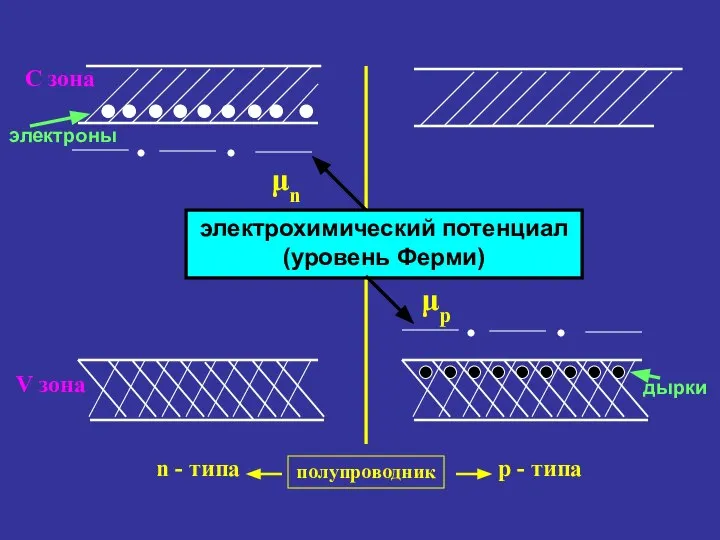
- 106. электрохимический потенциал (уровень Ферми) С зона электроны V зона дырки μn μp
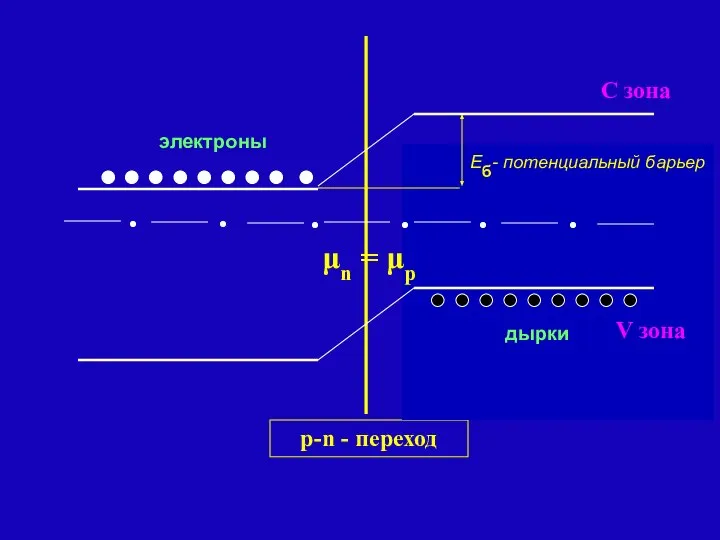
- 107. электроны p-n - переход μn = μp
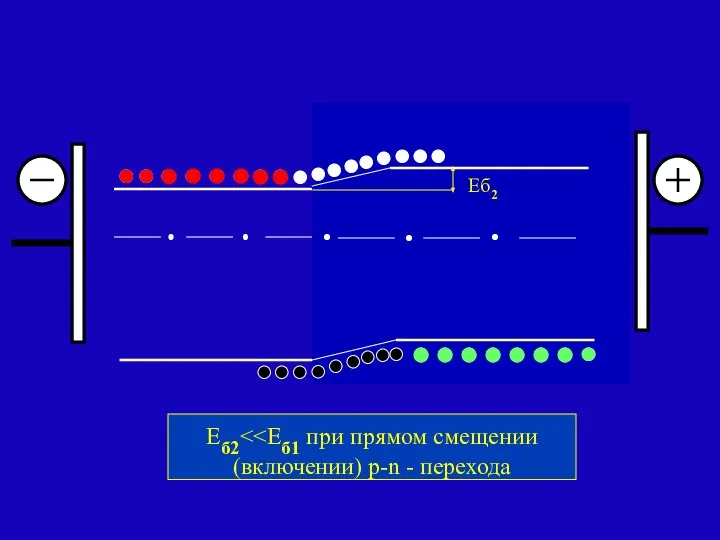
- 108. p-n - переход Еб1 Еб2
- 110. Скачать презентацию
















































































 Валы и оси
Валы и оси Ближнепольная оптическая спектроскопия
Ближнепольная оптическая спектроскопия История создания пылесоса. «От швабры до пылесоса-робота»
История создания пылесоса. «От швабры до пылесоса-робота» Аттестационная работа. Бурение нефтяных и газовых скважин. Методика расчета утяжеленных бурильных труб
Аттестационная работа. Бурение нефтяных и газовых скважин. Методика расчета утяжеленных бурильных труб влажность воздуха
влажность воздуха Рентгеновское излучение
Рентгеновское излучение Петрофизика. Физико-механические свойства горных пород
Петрофизика. Физико-механические свойства горных пород МОУ «Котельниковская средняя общеобразовательная школа №1 имени Героя Советского Союза Л. Д. Чурилова. МОУ «Котельниковская сред
МОУ «Котельниковская средняя общеобразовательная школа №1 имени Героя Советского Союза Л. Д. Чурилова. МОУ «Котельниковская сред Устройство подвески Лада Веста
Устройство подвески Лада Веста Какая сила движет электрическими приборами
Какая сила движет электрическими приборами Введение в магнитостатику. Сила Лоренца
Введение в магнитостатику. Сила Лоренца Простые механизмы. Рычаг
Простые механизмы. Рычаг Аттестация 1-2012. Вопросы теста
Аттестация 1-2012. Вопросы теста Презентация по физике "Законы сохранения" - скачать бесплатно
Презентация по физике "Законы сохранения" - скачать бесплатно Тепловое излучение и люминесценция
Тепловое излучение и люминесценция Инвариантность модуля скорости света в вакууме. Постулаты Эйнштейна. Пространство и время специальной теории. Занятие №77
Инвариантность модуля скорости света в вакууме. Постулаты Эйнштейна. Пространство и время специальной теории. Занятие №77 Проблемное обучение на уроках физики
Проблемное обучение на уроках физики Входной контроль 1. Одно и то же вещество может находиться только А) в твёрдом состоянии К) в жидком состоянии С) в газообразном со
Входной контроль 1. Одно и то же вещество может находиться только А) в твёрдом состоянии К) в жидком состоянии С) в газообразном со Распределение напряжений вокруг скважины
Распределение напряжений вокруг скважины Решение задачи изгиба многослойной упругопластической пластины
Решение задачи изгиба многослойной упругопластической пластины Дыбыс күшейту аппараттуралары
Дыбыс күшейту аппараттуралары Методы моментов. Метод сферических гармоник. Уравнение переноса в Р1-приближении. Диффузионное приближение
Методы моментов. Метод сферических гармоник. Уравнение переноса в Р1-приближении. Диффузионное приближение Презентация Применение конденсаторов
Презентация Применение конденсаторов  Двойной электрон-ядерный резонанс. Введение в теорию кристаллического поля
Двойной электрон-ядерный резонанс. Введение в теорию кристаллического поля Электроемкость и конденсаторы
Электроемкость и конденсаторы Модель сечения выведения для быстрых нейтронов. Сечение выведения гетерогенных сред. Основные предположения
Модель сечения выведения для быстрых нейтронов. Сечение выведения гетерогенных сред. Основные предположения Кипение. Температура кипения
Кипение. Температура кипения Основные уравнения движения жидкостей
Основные уравнения движения жидкостей