Содержание
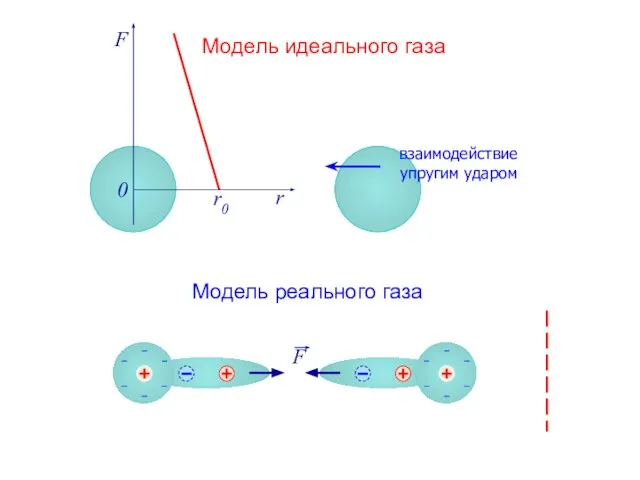
- 2. F r r0 0 Модель идеального газа Модель реального газа взаимодействие упругим ударом
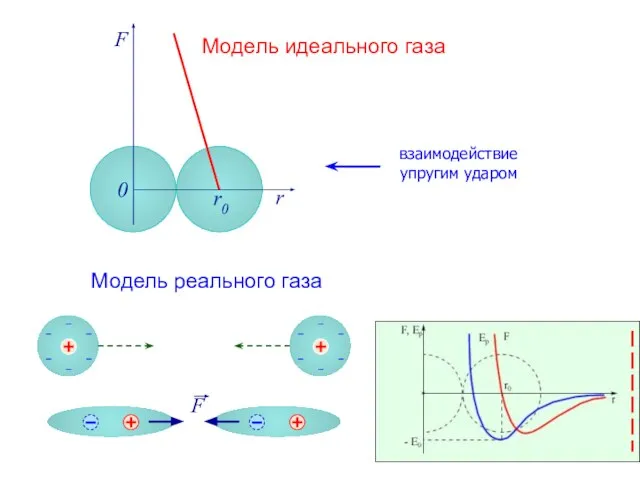
- 3. F r r0 0 Модель идеального газа Модель реального газа взаимодействие упругим ударом
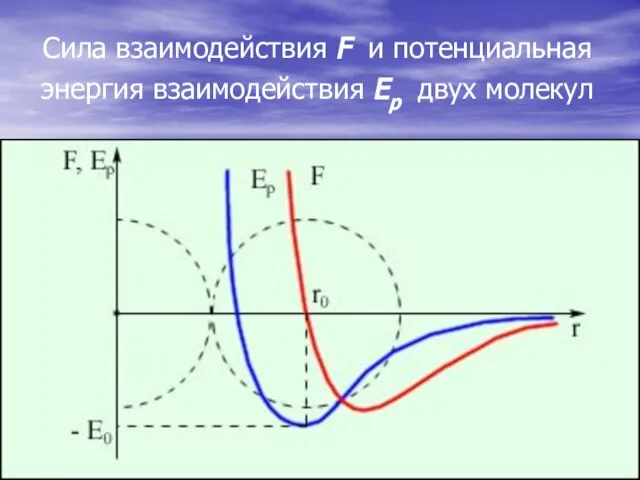
- 4. Сила взаимодействия F и потенциальная энергия взаимодействия Eр двух молекул
- 5. Модель Ван-дер-Ваальса Уравнение Ван-дер-Ваальса Ван-дер-Ваальс (van der Waals) Ян (1837 – 1923) Модель идеального газа:
- 6. Реальные газы. Жидкости. Твердые тела Конденсация реального газа. Изотермы Ван-дер-Ваальса
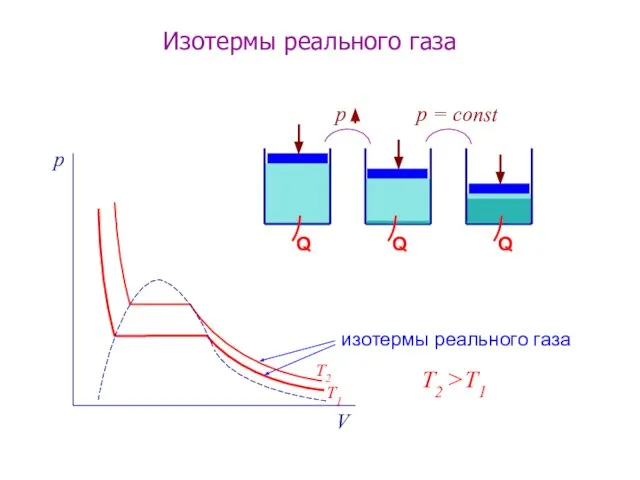
- 7. изотермы реального газа р = const Изотермы реального газа T2 >T1
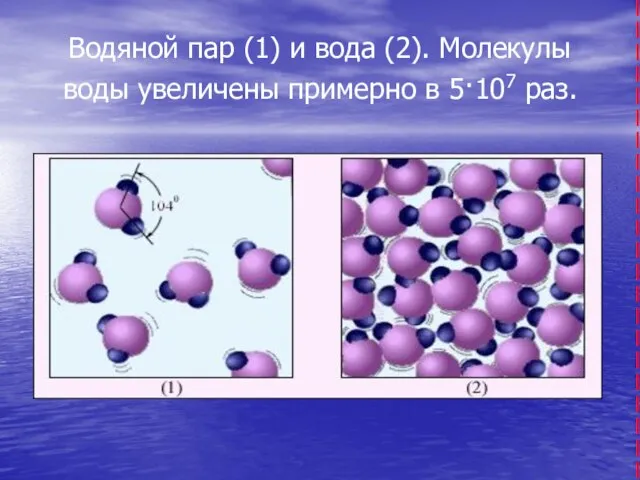
- 8. Водяной пар (1) и вода (2). Молекулы воды увеличены примерно в 5·107 раз.
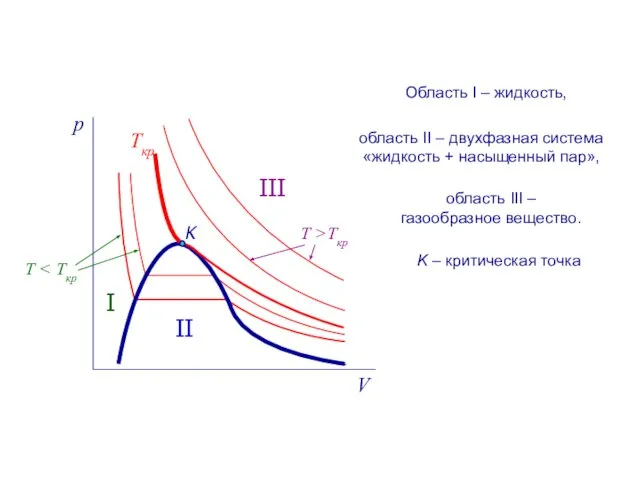
- 9. Ткр K I II III область II – двухфазная система «жидкость + насыщенный пар», Область I
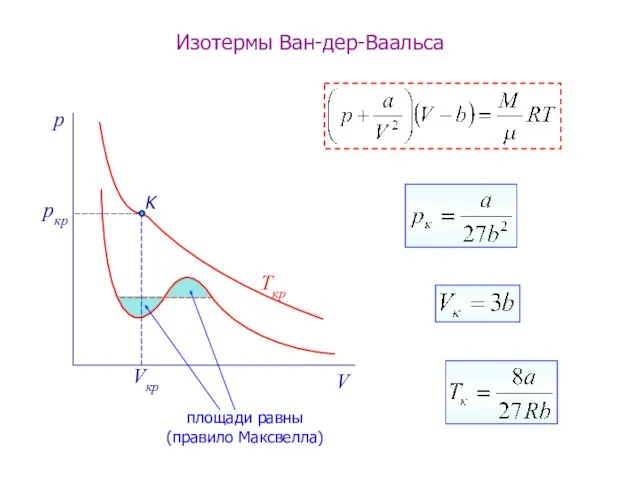
- 10. p V pкр Vкр Ткр Изотермы Ван-дер-Ваальса K площади равны (правило Максвелла)
- 11. Реальные газы. Жидкости . Твердые тела Область двухфазных состояний. Равновесие фаз. Критическое состояние
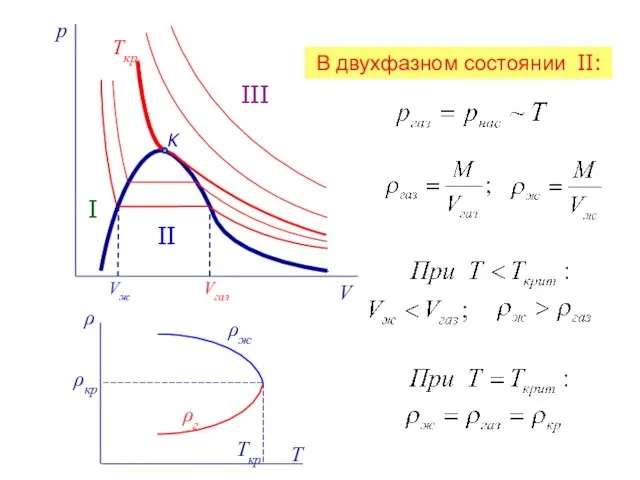
- 12. Ткр K I II III Tкр ρкр ρж ρг В двухфазном состоянии II:
- 13. Определение: теплота, идущая на изменение фазового состояния вещества, называется теплотой фазового превращения или скрытой теплотой перехода
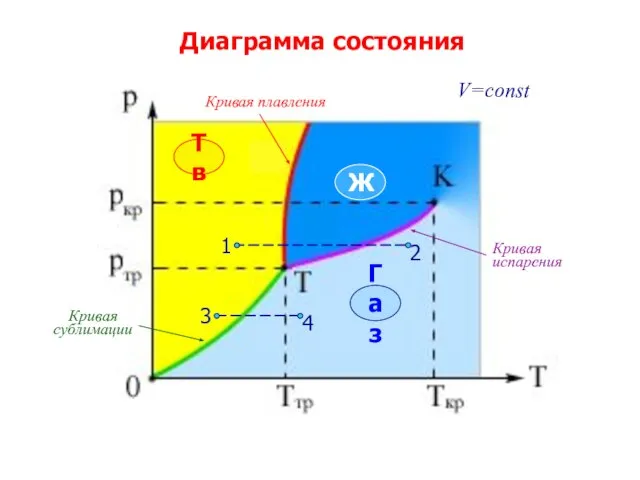
- 14. Диаграмма состояния Тв Ж Газ V=const
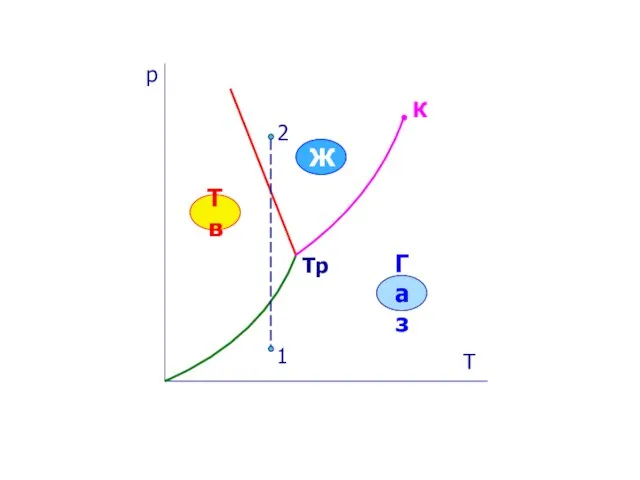
- 15. р Т К Тр Тв Ж Газ
- 16. Реальные газы. Жидкости . Твердые тела Дырочная модель жидкости
- 17. В кристаллах – дальний порядок В жидкостях – ближний порядок микрополости – «дырки» (~ 10% V)
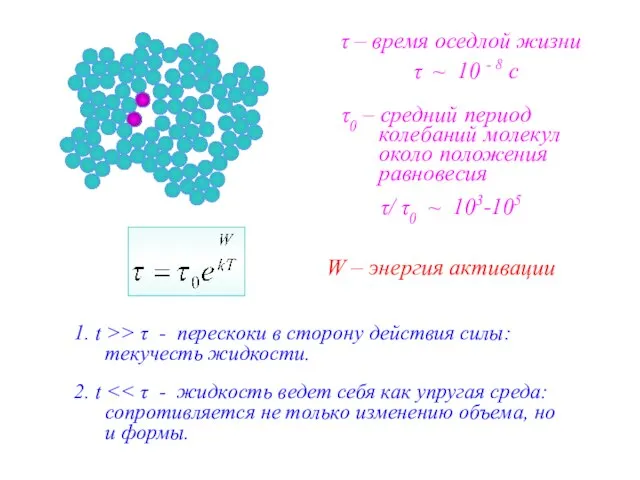
- 18. τ – время оседлой жизни τ0 – средний период колебаний молекул около положения равновесия W –
- 19. Реальные газы. Жидкости . Твердые тела Кристаллы. Классическая теория теплоемкости кристаллов. Закон Дюлонга-Пти
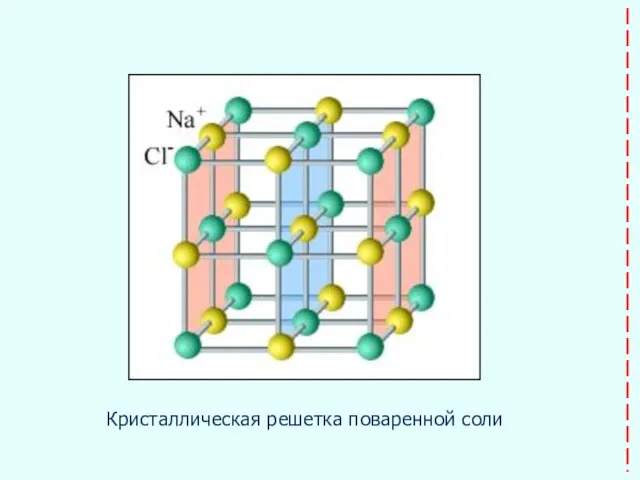
- 20. Кристаллическая решетка поваренной соли
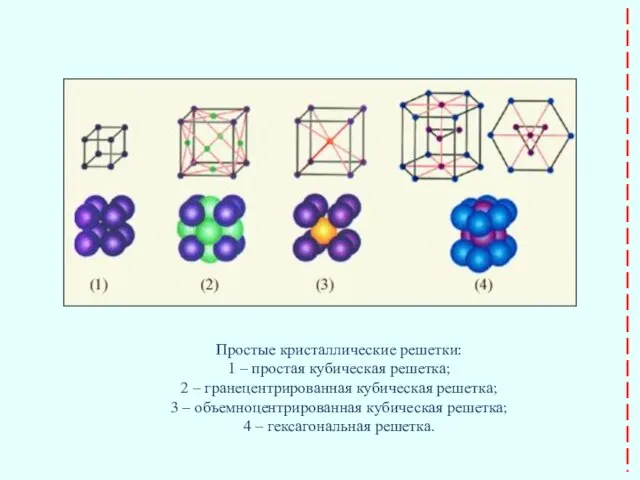
- 21. Простые кристаллические решетки: 1 – простая кубическая решетка; 2 – гранецентрированная кубическая решетка; 3 – объемноцентрированная
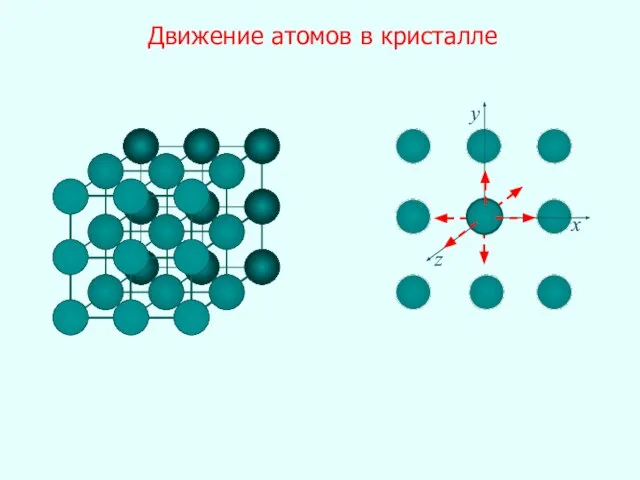
- 22. Движение атомов в кристалле x y z
- 23. x y z Движение атомов в кристалле
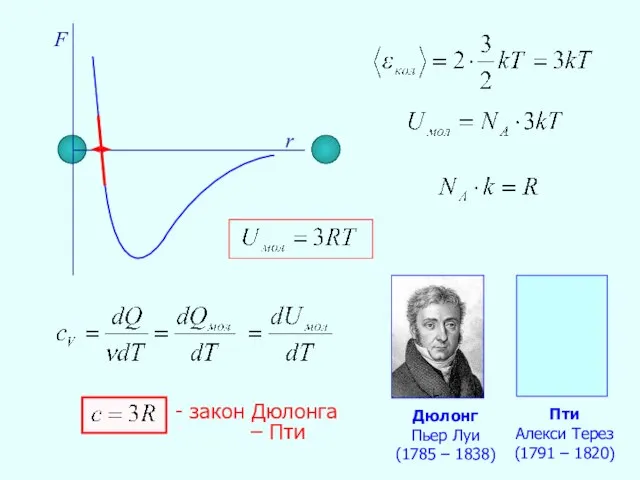
- 24. F r - закон Дюлонга – Пти Дюлонг Пьер Луи (1785 – 1838) Пти Алекси Терез
- 26. Скачать презентацию








 Термодинамика биологических процессов
Термодинамика биологических процессов Учебный курс
Учебный курс  Электромеханический переключатель
Электромеханический переключатель Физические модели. Постановка задачи
Физические модели. Постановка задачи Аккумулятор (лат. accumulator — жинақтауыш) - химиялық реакция энергиясын электр энергиясына айналдыратын аспап; ол электржәне
Аккумулятор (лат. accumulator — жинақтауыш) - химиялық реакция энергиясын электр энергиясына айналдыратын аспап; ол электржәне Плавание судов
Плавание судов Сообщающиеся сосуды
Сообщающиеся сосуды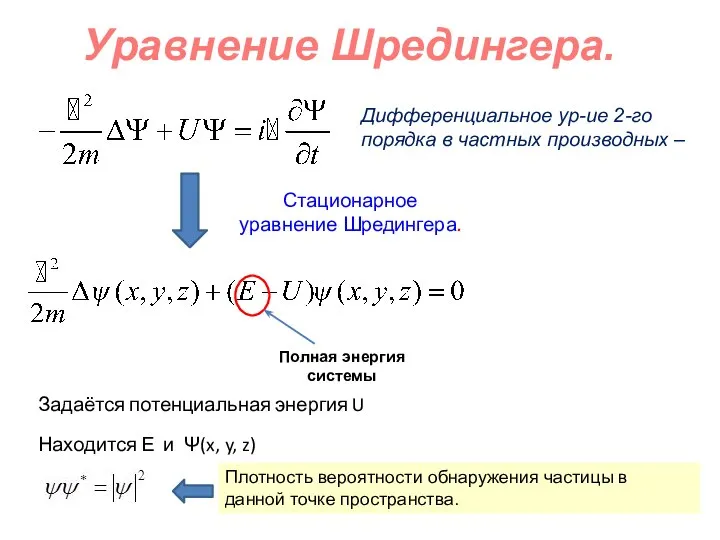 Уравнение Шредингера. Квантовые числа
Уравнение Шредингера. Квантовые числа Помехи в каналах связи
Помехи в каналах связи Элекромагнитная индукция
Элекромагнитная индукция Найзағайдың түрлері
Найзағайдың түрлері Механическое движение. Физика 7 класс
Механическое движение. Физика 7 класс Лазерная технология
Лазерная технология Методы астрофизическиx исследований (МАФИ)
Методы астрофизическиx исследований (МАФИ) Элементы квантовой механики
Элементы квантовой механики Плоский изгиб. Расчет на прочность
Плоский изгиб. Расчет на прочность Физика 8 класс
Физика 8 класс  Содержание Атомная физика 1.Строение атома (Резерфода) 2.Модель атома водорода по Бору 3.Квантовые постулаты Бора 4.Испускание и п
Содержание Атомная физика 1.Строение атома (Резерфода) 2.Модель атома водорода по Бору 3.Квантовые постулаты Бора 4.Испускание и п Режимы работы электродвигателей по нагреву
Режимы работы электродвигателей по нагреву Формирование познавательных интересов у учащихся на уроках физики
Формирование познавательных интересов у учащихся на уроках физики Сила трения
Сила трения Решение задач кинетическая и потенциальная энергия
Решение задач кинетическая и потенциальная энергия Резка металла
Резка металла Презентация по физике "Транспорт веществ в организме человека. Диффузия. Осмос" - скачать
Презентация по физике "Транспорт веществ в организме человека. Диффузия. Осмос" - скачать  Вклад Ломоносова в изучение физики и астрономии.
Вклад Ломоносова в изучение физики и астрономии. Механический электрогенератор
Механический электрогенератор Эксперимент – как метод обучения естественным наукам
Эксперимент – как метод обучения естественным наукам Понятие динамической системы станка. Динамическое качество станка. Основные задачи динамики станков
Понятие динамической системы станка. Динамическое качество станка. Основные задачи динамики станков