Содержание
- 2. в абсорбционных машинах, в испарителях и конденсаторах при наличии в хладагенте неконденсирующихся газов-примесей, в контактных аппаратах
- 3. ТМО Лекция 17 Основные положения Массообмен (перенос массы, массоперенос) – процесс, в результате которого вещество переносится
- 4. ТМО Лекция 16 Массовая доля компонента в смеси: Объёмная (мольная) доля для идеальных газов: Связь: ПРИМЕР.
- 5. Молекулярная диффузия – самопроизвольный процесс переноса массы в неподвижных жидких, газообразных и твердых средах, обусловленный движением
- 6. Концентрационная диффузия – молекулярный перенос массы происходит в системе, в различных точках которой температура и давление
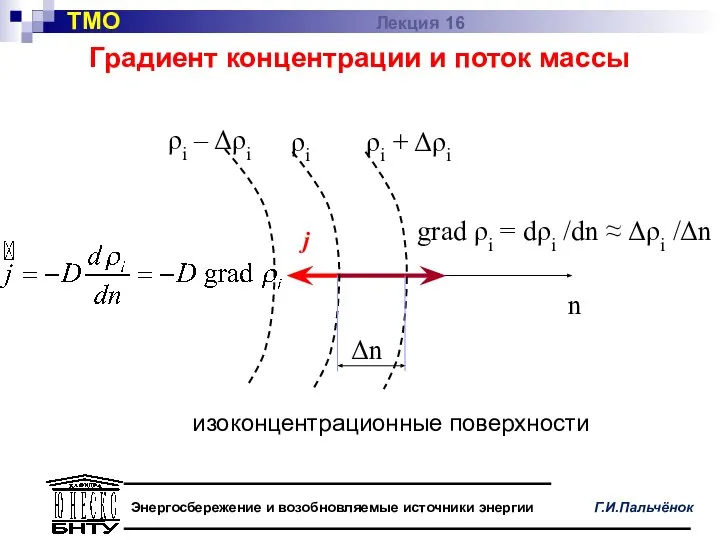
- 7. Градиент концентрации и поток массы ТМО Лекция 16
- 8. В отсутствие источников (стоков) массы (например, при химических реакциях) изменение массы (количества вещества), содержащегося в элементарном
- 9. ТМО Лекция 17 Термодиффузионное отношение: Dт – к-т термодиффузии, м2/с Термодиффузия (эффект Соре) – молекулярный перенос
- 10. Следствие явления термодиффузии – диффузионный термоэффект Дюфо: возникновение разности температур в изначально изотермической смеси газов в
- 11. Бародиффузия – эффект молекулярного переноса массы в системе, в различных точках которой концентрации компонентов и температура
- 12. Суммарная плотность молекулярного потока массы: ТМО Лекция 16
- 13. Коэффициент молекулярной диффузии Рассматривается изотермическая и изобарическая бинарная (2 компонента) смесь газов. Формула Сазерленда-Косова для к-та
- 14. D0 12 ·104 м2/с (Т0 = 273 К; Р0 = 1,01.105 Па = 760 мм рт.
- 15. Коэффициент молекулярной диффузии в многокомпонентной смеси Для приближённых оценок при малых различиях в молекулярных массах компонентов
- 16. Плотность потока массы в движущейся среде (смеси) можно записать в форме закона Фика, введя в него
- 17. В диффузионном пограничном слое толщиной δ у поверхности раздела фаз доминирует молекулярный механизм переноса массы вдоль
- 18. Число Шервуда (диффузионное число Нуссельта)– безразмерный коэффициент массоотдачи Число Шмидта (диффузионное число Прандтля) – критерий подобия
- 19. Диффузионное число Пекле – отношение между скоростями конвективного и диффузионного переноса массы ТП Лекция 18
- 20. Кинетические коэффициенты молекулярного переноса тепла, массы, импульса в идеальных газах a ≈ D ≈ ν ≈
- 21. Коэффициенты турбулентного переноса wy' – пульсационная скорость вдоль оси у, м/с; l' – масштаб турбулентности ~
- 22. Касательное напряжение трения на стенке: – при обтекании пластины – при течении в трубе круглого сечения
- 23. Аналогия Чилтона – Колберна в выражение аналогии Рейнольдса введена эмпирическая поправка на влияние чисел Прандтля и
- 24. ТМО Лекция 17 Система дифференциальных уравнений погран. слоя
- 25. Теплообмен Массообмен ТМО Лекция 16 Испарение жидкости на поверхности раздела фаз приводит к появлению конвективного потока
- 27. Скачать презентацию























 Формирование понятия «энергия»
Формирование понятия «энергия» Механический электрогенератор
Механический электрогенератор Без имени-0318-0337-drwg_1(12) CH(ru)
Без имени-0318-0337-drwg_1(12) CH(ru) Давление твердых тел, жидкостей и газов
Давление твердых тел, жидкостей и газов Теория механизмов и машин. Лекция 5
Теория механизмов и машин. Лекция 5 Урок физики в 8 классе «Кипение»
Урок физики в 8 классе «Кипение»  Механические колебания и волны. Колебательное движение. Свободные колебания
Механические колебания и волны. Колебательное движение. Свободные колебания Решение задач по теме Движение
Решение задач по теме Движение Влияние солнечных рентгеновских вспышек на изменения атмосферного электрического поля и прохождение волн СДВ диапазона
Влияние солнечных рентгеновских вспышек на изменения атмосферного электрического поля и прохождение волн СДВ диапазона История создания ядерного оружия. Испытания ядерного оружия.
История создания ядерного оружия. Испытания ядерного оружия.  Исследование возможности накопления энергии из высоковольтного разряда
Исследование возможности накопления энергии из высоковольтного разряда Екологічні проблеми ядерної енергетики Ядерна енергетика.
Екологічні проблеми ядерної енергетики Ядерна енергетика. Открытие нейтронов и протонов
Открытие нейтронов и протонов Биопотенциалы покоя. Генерация и распространение потенциала действия. (Лекция 5)
Биопотенциалы покоя. Генерация и распространение потенциала действия. (Лекция 5) Решение задач
Решение задач Полет на Марс – Что ждет добровольцев?
Полет на Марс – Что ждет добровольцев?  Презентация по физике "Педагогические технологии при обучении физике: преподавание, развивающее ученика" - скачать
Презентация по физике "Педагогические технологии при обучении физике: преподавание, развивающее ученика" - скачать  Атмосферное давление на разных высотах. Манометры
Атмосферное давление на разных высотах. Манометры Презентация_
Презентация_ Поршневой жидкостный насос. Водопровод
Поршневой жидкостный насос. Водопровод Первый закон термодинамики
Первый закон термодинамики Второй закон Ньютона дистанционное обучение
Второй закон Ньютона дистанционное обучение Фізіка з асновамі геафізікі
Фізіка з асновамі геафізікі Твоя первая модель. Как выбрать модель самолета
Твоя первая модель. Как выбрать модель самолета Волновая оптика. Поляризация света. Тепловое излучение (Лекция 3)
Волновая оптика. Поляризация света. Тепловое излучение (Лекция 3) Показатели надежности электроснабжения
Показатели надежности электроснабжения Плазмалық технологиялардың физикалық негіздері
Плазмалық технологиялардың физикалық негіздері Электрические явления. 8 класс
Электрические явления. 8 класс