Содержание
- 2. МОЛЕКУЛЯРНАЯ ФИЗИКА ТЕРМОДИНАМИКА Т П У Сегодня *
- 3. Тема 7. ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА РЕАЛЬНЫХ ГАЗОВ 7.1. Реальные газы 7.2. Силы Ван-дер-Ваальса 7.2. Вывод уравнения Ван-дер-Ваальса
- 4. 7.1. Реальные газы Как известно, уравнение состояния устанавливает связь между давлением Р, объемом V, температурой T
- 5. Уравнение Менделеева – Клапейрона - самое простое, надежное и известное уравнение состояния идеального газа. Реальные газы
- 6. Для газов с низкой температурой сжиже-ния (He, H2, Ne и даже N2, O2, Ar, CO, CH4)
- 7. Первая поправка в уравнении состояния идеального газа рассматривает собственный объем, занимаемый молекулами реального газа. В уравнении
- 8. При понижении температуры межмолекулярное взаимодействие в реальных газах приводит к конденсации (образование жидкости). Межмолекулярное притяжение эквивалентно
- 9. Наибольшее распространение вследствие простоты и физической наглядности получило уравнение Ван-дер-Ваальса (1873). Ван-дер-Ваальс дал функциональную интерпретацию внутреннего
- 10. С учетом этих соображений уравнение состояния идеального газа преобразуется в уравнение Ван-дер-Ваальса: или для одного моля
- 11. Ян-Дидерик Ван-дер-Ваальс (1837 – 1923), голландский физик. Его докторская диссертация, посвященная непрерывности газообразного и жидкого состояний,
- 12. Помимо Нобелевской премии, Ван-дер-Ваальс получил почетную докторскую степень Кембриджского университета. Кроме того, он являлся членом Нидерландской
- 13. Реальные газы – газы, свойства которых зависят от взаимодействия молекул. В обычных условиях, когда средняя потенциальная
- 14. 7.2. Силы Ван-дер-Ваальса Я.Д. Ван-дер-Ваальс для объяснения свойств реальных газов и жидкостей, предположил, что на малых
- 15. Межмолекулярные взаимодей-ствия имеют электрическую природу и складываются из: сил притяжения (ориентационных, индукционных, дисперсионных) и сил отталкивания.
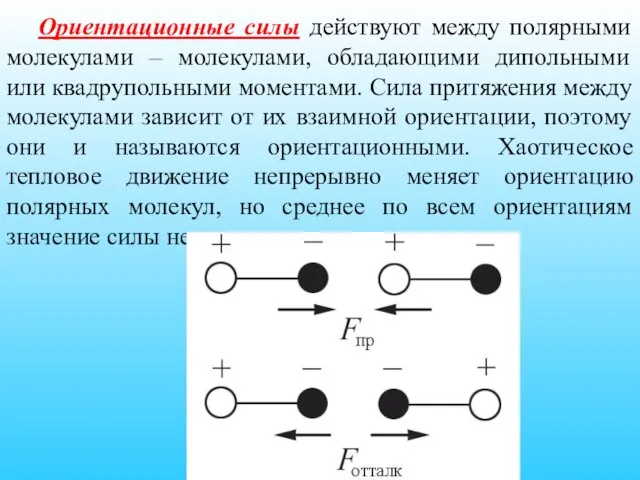
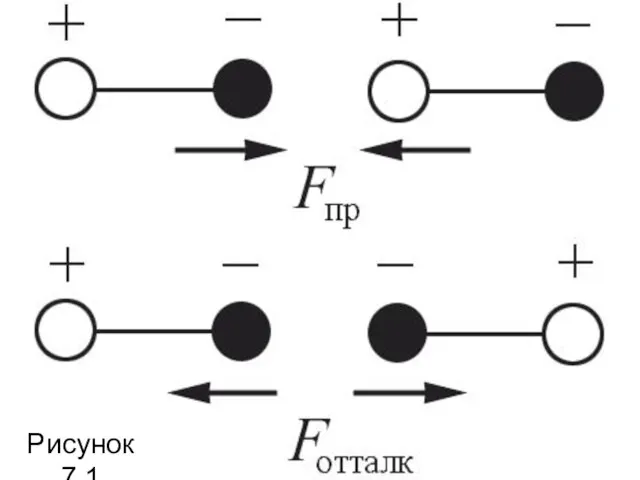
- 16. Ориентационные силы действуют между полярными молекулами – молекулами, обладающими дипольными или квадрупольными моментами. Сила притяжения между
- 17. Рисунок 7.1
- 18. Среднее значение потенциальной энергии ориентационного межмолекулярного взаимодействия равно Uор(r) ~ p1 p2 r−6, где p1, p2
- 19. Индукционные (поляризационные) силы действуют между полярной и неполярной молекулами, а также между полярными молекулами. Полярная молекула
- 20. Дисперсионное молекулярное взаимодействие возникает благодаря виртуальному нарушению электронейтральности молекулы в отдельные моменты времени. Мгновенный диполь поляризует
- 21. Данное взаимодействие называется дисперсионным, его энергия определяется поляризуемостью молекул α1, α2: U(r) ~ α1α2 r –6,
- 22. Отметим, что все три силы и энергии одинаковым образом убывают с расстоянием: F = Fор +
- 23. Силы отталкивания действуют между молекулами на очень малых расстояниях, когда происходит взаимодействие электронных оболочек атомов, входящих
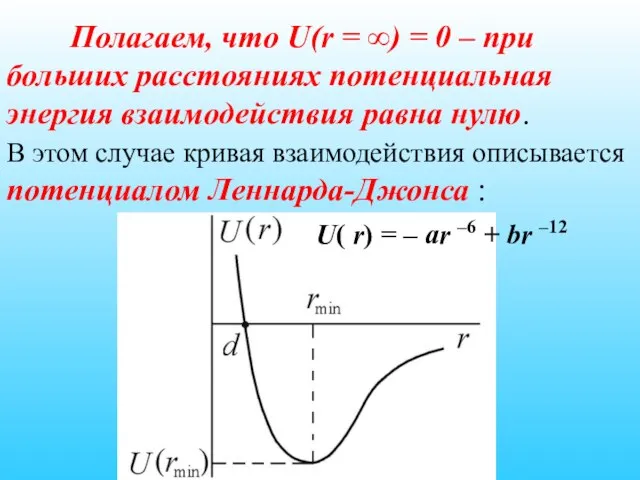
- 24. Полагаем, что U(r = ∞) = 0 – при больших расстояниях потенциальная энергия взаимодействия равна нулю.
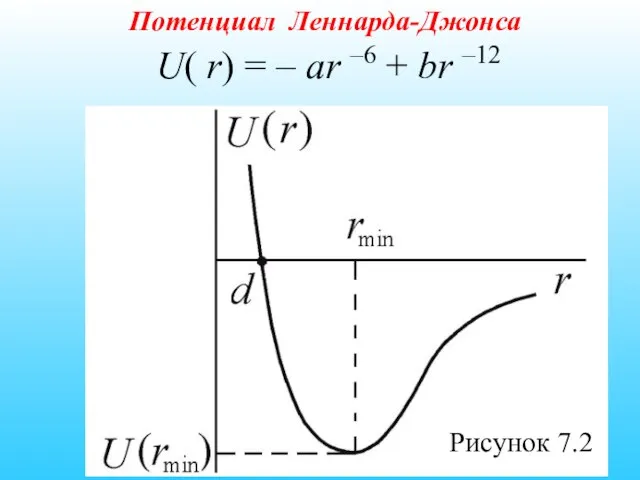
- 25. U( r) = – ar –6 + br –12 Рисунок 7.2 Потенциал Леннарда-Джонса
- 26. Глубина потенциала равна U(rmin) = –a2/4b при rmin = (2b/a)1/6 – расстоянии, соответствующем наибольшей энергии связи
- 27. 7.3. Вывод уравнения Ван-дер-Ваальса Уравнение Ван-дер-Ваальса – одно из первых уравнений состояния реального газа, которое было
- 28. Учтем влияние конечных размеров молекул на уравнение состояния реального газа. Давление определяется средней кинетической энергией теплового
- 29. В результате в сосуде, содержащем N молекул конечных размеров, область объемом (N/2)4π(2r)3/3 = 4NVмолек будет недоступна
- 30. Объем, доступный точечным молекулам, будет равен V − b, а давление, оказываемое на стенки сосуда, определяется
- 31. Для ν = m/μ молей газа уравнение состояния газа с учетом конечного размера молекул примет вид:
- 32. Рассмотрим влияние сил притяжения на уравнение состояния идеального газа. Будем считать для простоты частицы газа точечными.
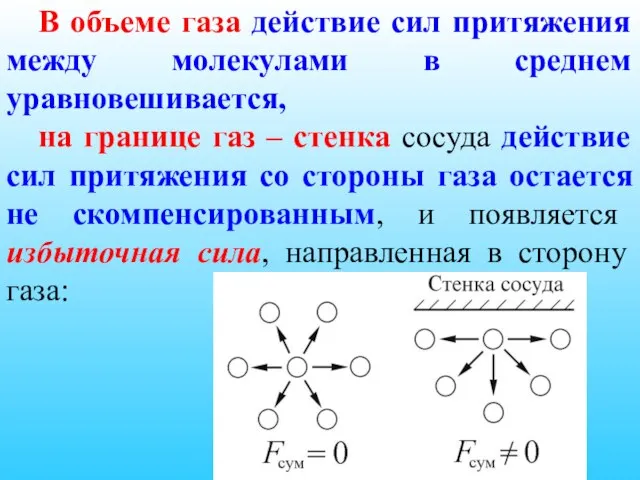
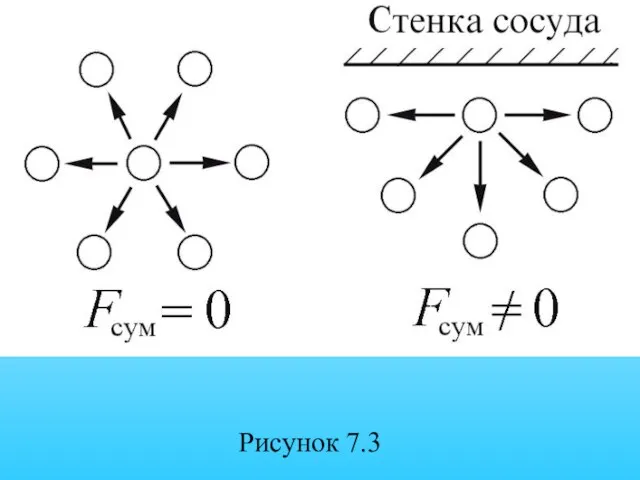
- 33. В объеме газа действие сил притяжения между молекулами в среднем уравновешивается, на границе газ – стенка
- 34. Рисунок 7.3
- 35. Дополнительное внутреннее давление пропорционально числу частиц, приходящихся на единицу площади границы nS и силе взаимодействия этих
- 36. Избыточное внутреннее давление Pi (i − intrinsic) будет пропорционально квадрату концентрации числа частиц Pi ~ nS
- 37. С учетом внутреннего давления уравнение состояния примет вид P + Pi = nkT, или (P +
- 38. Учитывая совместное действие сил притяжения и сил отталкивания и полученные поправки для объема и давления в
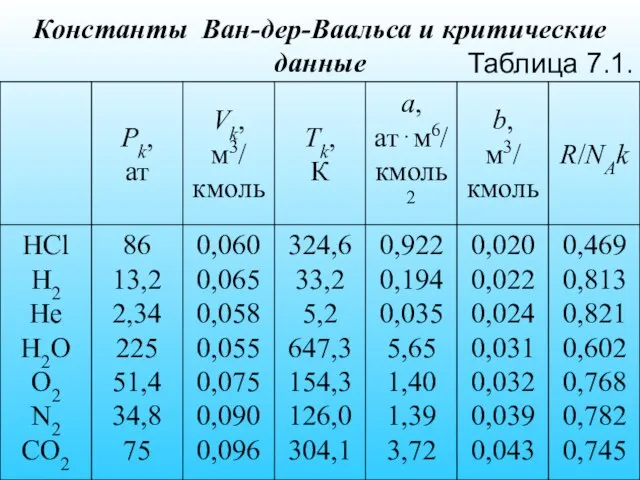
- 39. Константы Ван-дер-Ваальса и критические данные Таблица 7.1.
- 40. Примечание. Константы а и b выбраны таким образом, чтобы получить оптимальное согласование уравнения Ван-дер-Ваальса с измеренными
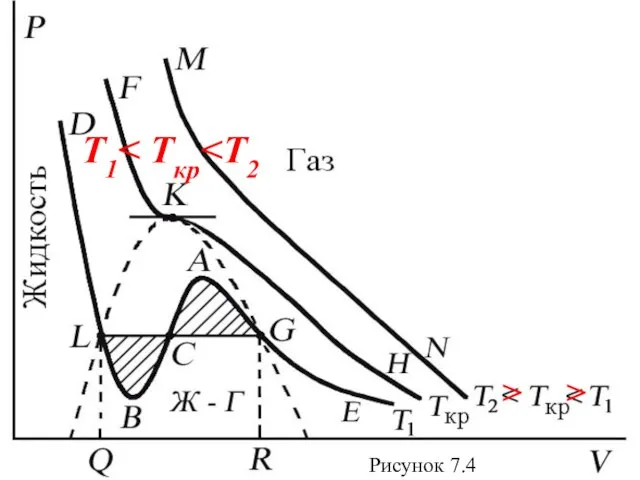
- 41. 7.3. Изотермы уравнения Ван-дер-Ваальса Проанализируем изотермы уравнения Ван-дер-Ваальса – зависимости Р от V для реального газа
- 42. Поскольку данное уравнение имеет третью степень относительно V, а коэффициенты при V действительны, то оно имеет
- 43. T1 > > Рисунок 7.4
- 44. Изотерма при Ткр, которая разделяет немонотонные T Tкр изотермы, соответствует изотерме при критической температуре. При температуре
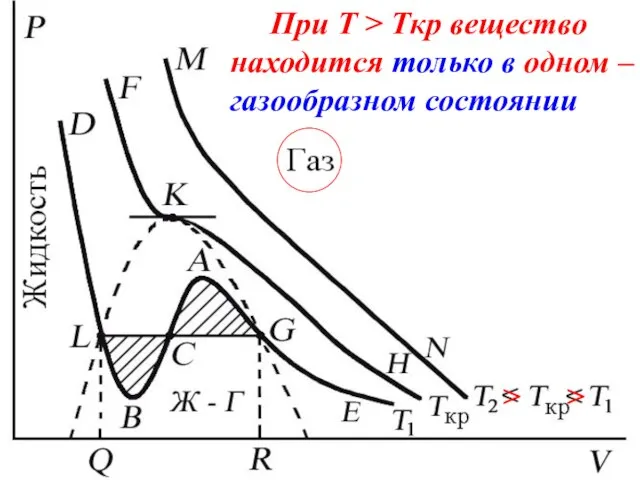
- 45. При T > Tкр вещество находится только в одном – газообразном состоянии > >
- 46. При температуре газа ниже критической есть возможность перехода вещества из газообразного в жидкое и наоборот. На
- 47. При температуре газа ниже критической есть возможность перехода вещества из газообразного в жидкое и наоборот. >
- 48. Поэтому область ВСА не может устойчиво существовать. В областях DLB и AGE давление падает с увеличением
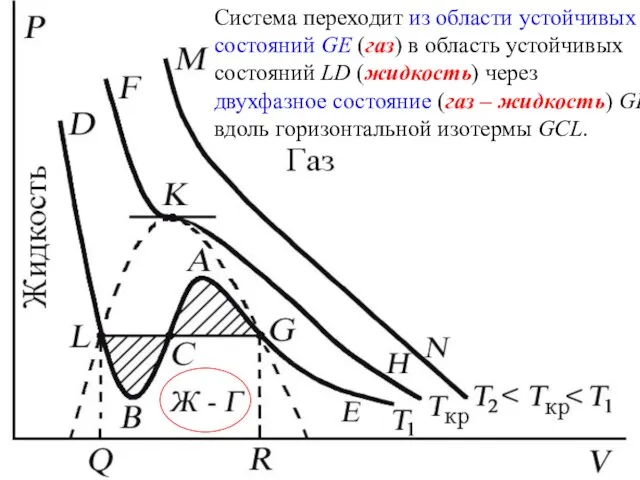
- 49. Система переходит из области устойчивых состояний GE (газ) в область устойчивых состояний LD (жидкость) через двухфазное
- 50. При квазистатическом сжатии, начиная с точки G, система распадается на 2 фазы – жидкость и газ,
- 51. Наличие критической точки на изотерме Ван-дер-Ваальса означает, что для каждой жидкости существует такая температура, выше которой
- 52. Такую температуру Менделеев назвал температурой абсолютного кипения. Выше этой температуры, согласно Менделееву, газ не может быть
- 53. Критическая точка K - точка перегиба критической изотермы, в которой касательная к изотерме горизонтальна (рисунок 7.5).
- 54. Ее можно определить также как точку, в которую в пределе переходят горизонтальные участки изотерм при повышении
- 55. На этом основан способ определения критических параметров Pk, Vk, Тk, (способ Эндрюса).
- 56. Строится система изотерм при различных температурах. Предельная изотерма, у которой горизонтальный участок LG переходит в точку,
- 57. 7.4. Внутренняя энергия газа Ван-дер-Ваальса Энергия одного моля газа Ван-дер-Ваальса слагается из: внутренней энергии молекул газа;
- 58. Потенциальная энергия притяжения молекул равна работе, необходимой для разведения молекул на бесконечное расстояние друг от друга.
- 59. Дополнительное давление газа Ван-дер-Ваальса за счет взаимного притяжения молекул равно a/Vm2, тогда потенциальная энергия взаимодействия равна
- 60. Полная энергия одного моля газа Ван-дер-Ваальса : Если СV не зависит от температуры, то полная энергия
- 61. Принципиальное значение уравнения Ван-дер-Ваальса определяется следующими обстоятельствами: 1) Уравнение было получено из модельных представлений о свойствах
- 62. 2) Уравнение долго рассматривалось как некоторый общий вид уравнения состояния реальных газов, на основе которого было
- 63. Причиной недостаточной точности уравнения Ван-дер-Ваальс считал ассоциацию молекул в газовой фазе, которую не удается описать, учитывая
- 64. Две модификации уравнения предложил Клаузиус, и обе они связаны с усложнением вида постоянной b. Больцман получил
- 65. Выяснилось, что ни одно из уравнений состояния, содержащих менее 5 индивидуальных постоянных, не оказалось достаточно точным
- 66. Если идеальный газ адиабатно расширяется и совершает при этом работу, то он охлаждается, так как работа
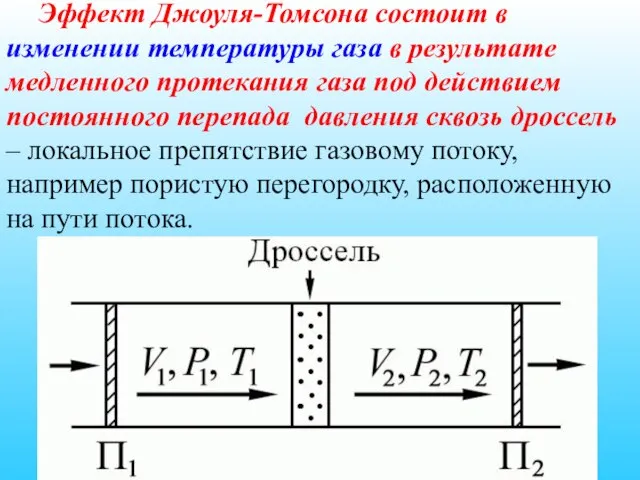
- 67. Эффект Джоуля-Томсона состоит в изменении температуры газа в результате медленного протекания газа под действием постоянного перепада
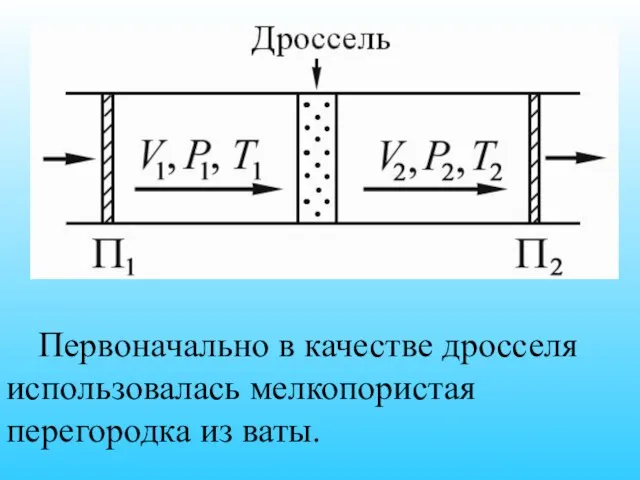
- 68. Первоначально в качестве дросселя использовалась мелкопористая перегородка из ваты.
- 69. Эффект Джоуля-Томсона свидетельствует о наличии в газе сил межмолекулярного взаимодействия. Газ совершает внешнюю работу – последующие
- 70. Совершенная над газом результирующая внешняя работа равна В адиабатических внешних условиях эта работа идет на изменение
- 71. Таким образом, в опыте Джоуля-Томсона сохраняется (остается неизменной) величина Она является функцией состояния и называется энтальпией.
- 72. Эффект Джоуля-Томсона принято называть положительным, если газ в процессе дросселирования охлаждается и отрицательным, если газ нагревается
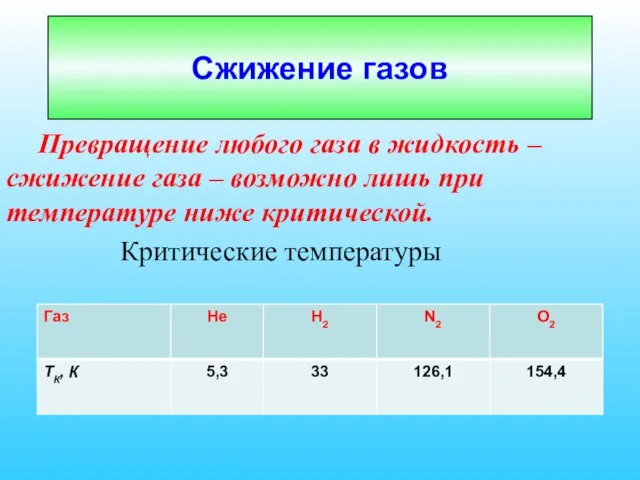
- 73. Превращение любого газа в жидкость – сжижение газа – возможно лишь при температуре ниже критической. Критические
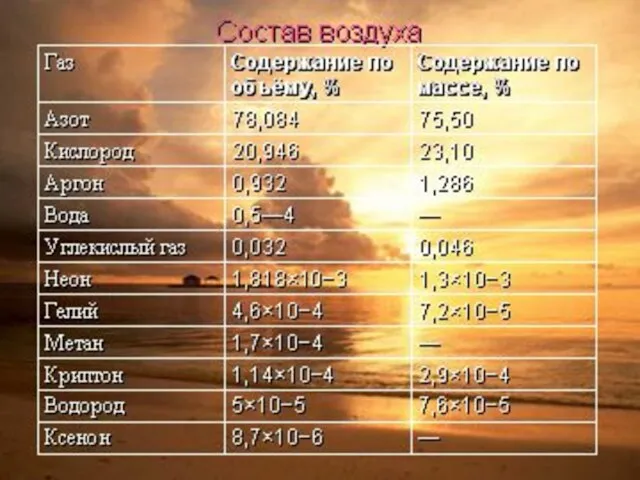
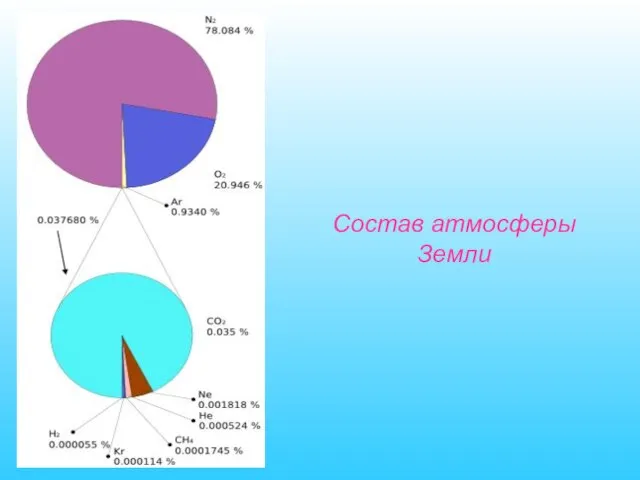
- 75. Состав атмосферы Земли
- 76. Схема установки для сжижения газов, в которой используется эффект Джоуля-Томсона – машина Линде. Воздух в компрессоре
- 77. Второй метод сжижения газов основан на охлаждении газа при совершении им работы. Сжатый газ, поступая в
- 78. Температуры до –261° С (12 К) и ниже можно также получать и поддерживать при помощи механических
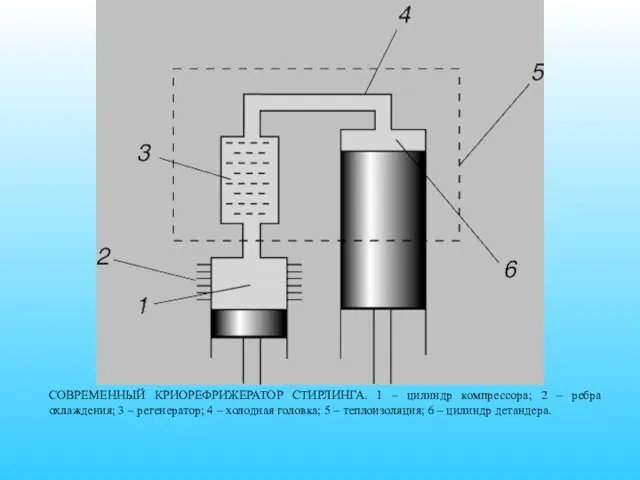
- 79. СОВРЕМЕННЫЙ КРИОРЕФРИЖЕРАТОР СТИРЛИНГА. 1 – цилиндр компрессора; 2 – ребра охлаждения; 3 – регенератор; 4 –
- 81. Основные результаты Уравнение Ван-дер-Ваальса для произвольного количества вещества ν реального газа учитывает конечный объем молекул νb
- 85. Скачать презентацию


































































 Кристаллические и аморфные тела
Кристаллические и аморфные тела Энергия движущейся воды и ветра
Энергия движущейся воды и ветра Тема: Приборы по физике своими руками и простые опыты с ними. Работу выполнил: ученик 9 класса- Давыдов Рома Руководитель: учит
Тема: Приборы по физике своими руками и простые опыты с ними. Работу выполнил: ученик 9 класса- Давыдов Рома Руководитель: учит Роботу виконала учениця 11-А класу Мельніченко Юлія
Роботу виконала учениця 11-А класу Мельніченко Юлія  Задания из ЕГЭ по физике за 2006 год
Задания из ЕГЭ по физике за 2006 год Второй закон Ньютона.
Второй закон Ньютона.  Лекционный курс «физические основы измерений и эталоны». Охлаждение при расширении газов. Эффект джоуля-томсона
Лекционный курс «физические основы измерений и эталоны». Охлаждение при расширении газов. Эффект джоуля-томсона Електричний струм в газах Підготувала Учениця 11-Б класу Криворізькоі гімназіі №49 Махіна Марія
Електричний струм в газах Підготувала Учениця 11-Б класу Криворізькоі гімназіі №49 Махіна Марія  Molecular-kinetic theory of ideal gases
Molecular-kinetic theory of ideal gases Никола Тесла (1856-1943)
Никола Тесла (1856-1943) Интерференция света. Пространственно-временная когерентность. Лекция 15(1)
Интерференция света. Пространственно-временная когерентность. Лекция 15(1) Атомы во внешнем магнитном поле. Магнитный момент атома. Спин электрона. Векторная модель атома
Атомы во внешнем магнитном поле. Магнитный момент атома. Спин электрона. Векторная модель атома Проверка формул по физике. 7 класс
Проверка формул по физике. 7 класс Бегом по радуге. Игра-состязание по физике среди 8 классов
Бегом по радуге. Игра-состязание по физике среди 8 классов Продолжение молекулярной физики
Продолжение молекулярной физики Курение, с точки зрения физики
Курение, с точки зрения физики Корпускулярные свойства рентгеновского излучения
Корпускулярные свойства рентгеновского излучения Экспериментальные факты, лежащие в основе теории магнетизма
Экспериментальные факты, лежащие в основе теории магнетизма Лампы накаливания
Лампы накаливания Уравнения теории упругости. Закон Гука для изотропного тела. Упругие постоянные. Объемная деформация. (Лекция 4)
Уравнения теории упругости. Закон Гука для изотропного тела. Упругие постоянные. Объемная деформация. (Лекция 4) Закон сохранения и превращения энергии.
Закон сохранения и превращения энергии. Плотность веществ
Плотность веществ Электрический ток в полупроводниках
Электрический ток в полупроводниках Робота електричного струму
Робота електричного струму Заттың агрегаттық күйлерінің өзгеруі. 8 сынып
Заттың агрегаттық күйлерінің өзгеруі. 8 сынып Механическая работа. Единицы работы. Мощность. Единицы мощности
Механическая работа. Единицы работы. Мощность. Единицы мощности Application of Variational Integrators in Modeling the Dynamics of Mechanical. Systems
Application of Variational Integrators in Modeling the Dynamics of Mechanical. Systems Энергия подводных морских и океанических течений
Энергия подводных морских и океанических течений