Содержание
- 2. Предмет биоорганической химии. Строение и изомерия органических соединений. Химическая связь и взаимовлияние атомов в органических соединениях.
- 3. Биоорганическая химия изучает строение и свойства веществ, участвующих в процессах жизнедеятельности, в связи с познанием их
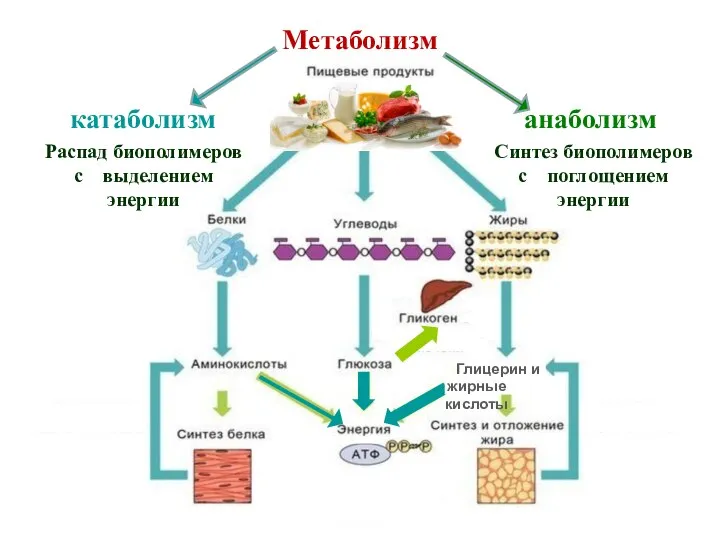
- 4. Совокупность химических реакций, протекающих в организме, называют обменом веществ, или метаболизмом. Вещества, образующиеся в клетках, тканях
- 5. Метаболизм
- 6. Основные положения теории строения органических соединений А.М. Бутлерова 1. Атомы в молекуле располагаются в определенной последовательности
- 7. Г о м о л о г и ч е с к и й р я
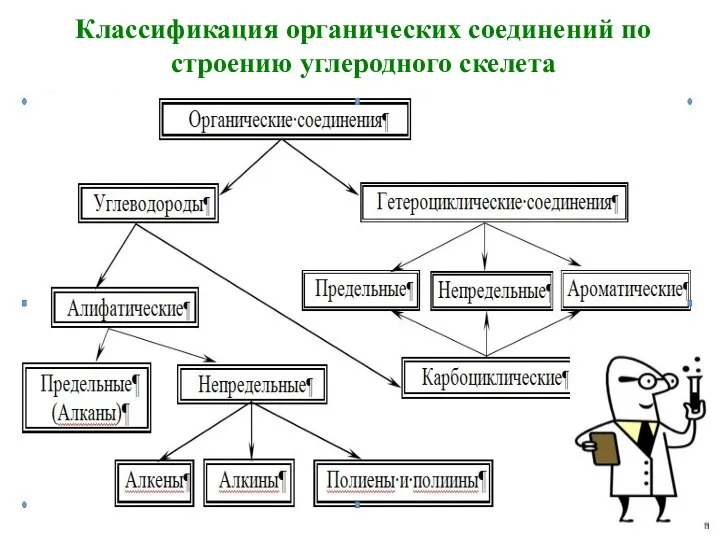
- 8. Классификация органических соединений по строению углеродного скелета
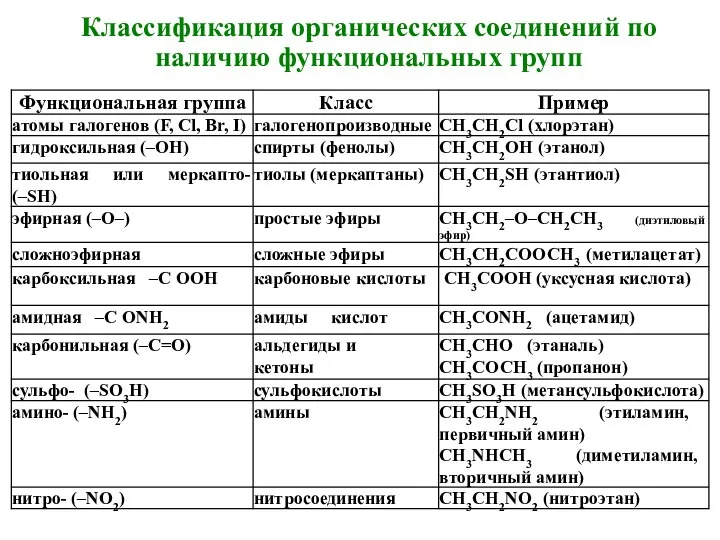
- 9. Классификация органических соединений по наличию функциональных групп
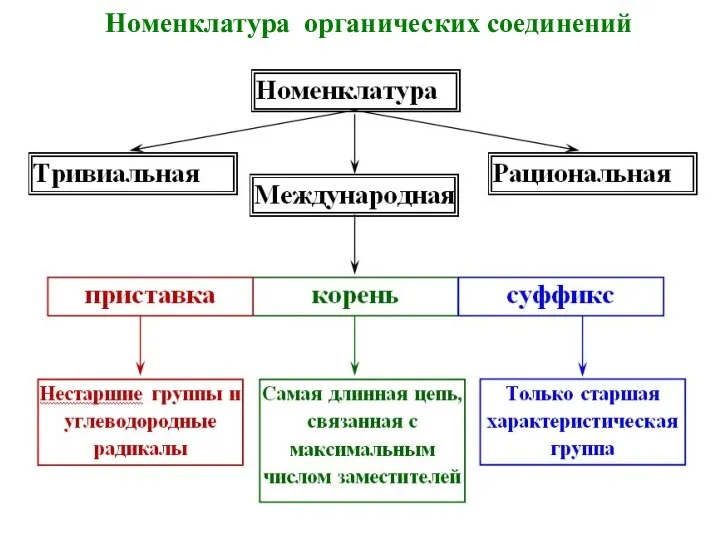
- 10. Номенклатура органических соединений
- 11. Изомерия органических соединений Если два или больше индивидуальных веществ имеют одинаковый количественный состав (молекулярную формулу), но
- 13. Вот такая геометрическая изомерия
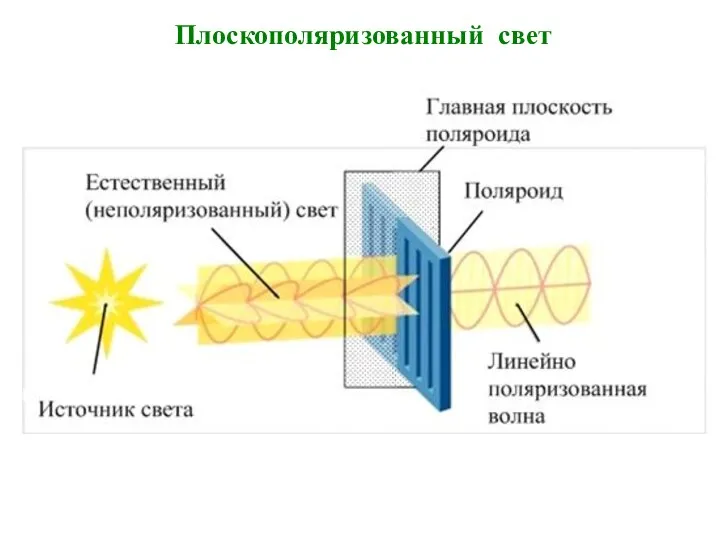
- 14. Плоскополяризованный свет
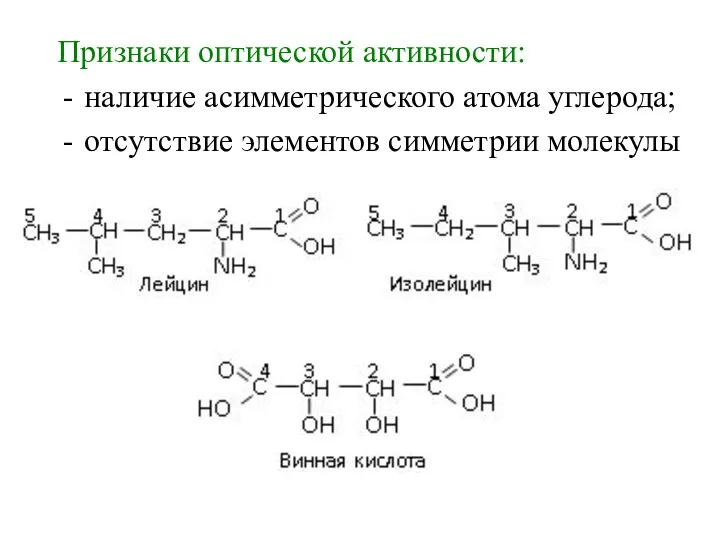
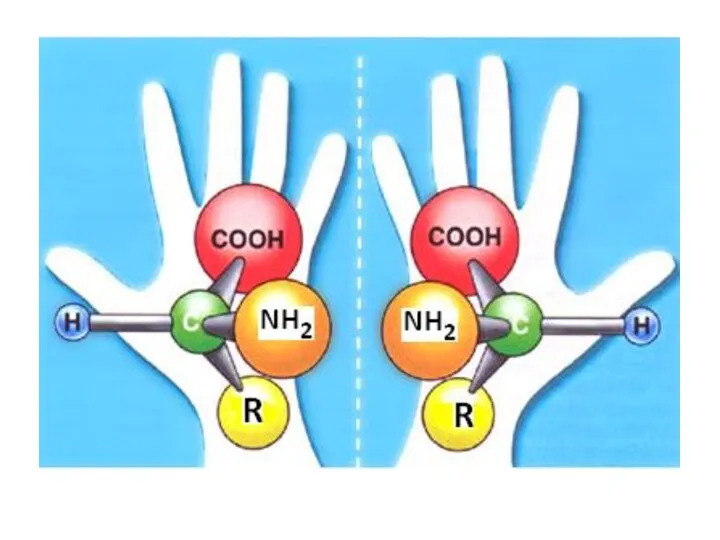
- 15. Признаки оптической активности: наличие асимметрического атома углерода; отсутствие элементов симметрии молекулы
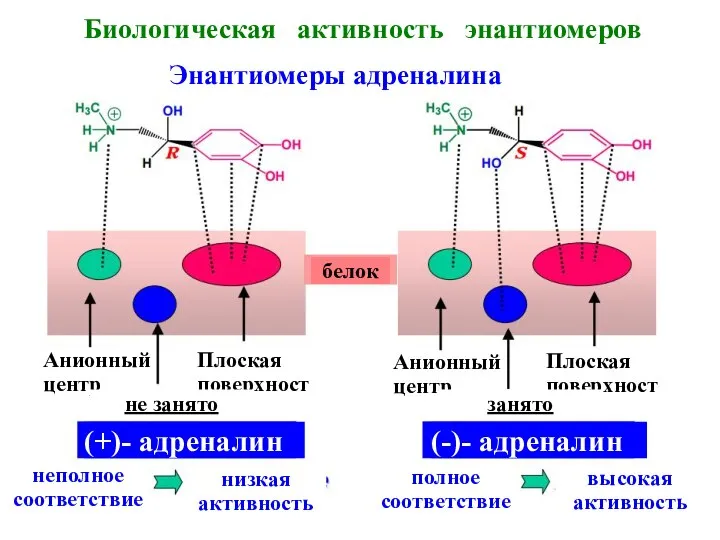
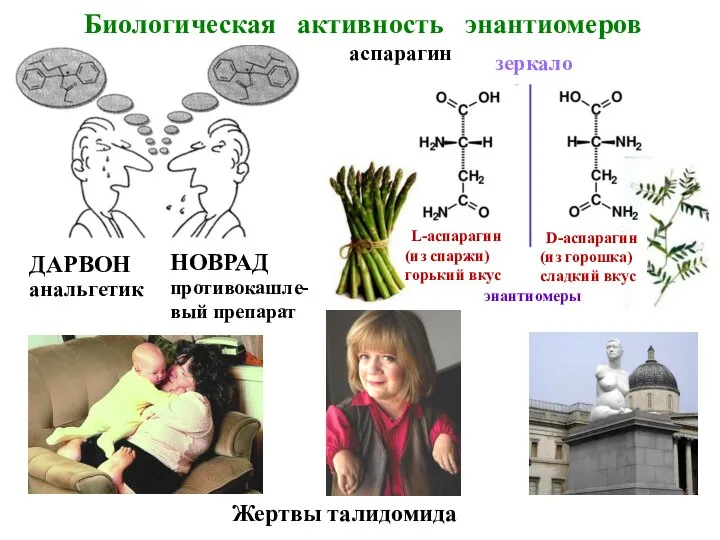
- 17. Биологическая активность энантиомеров
- 18. Жертвы талидомида Биологическая активность энантиомеров ДАРВОН анальгетик НОВРАД противокашле-вый препарат аспарагин зеркало L-аспарагин (из спаржи) горький
- 19. Кислотность и основность органических соединений Кислоты Бренстеда (протонные кислоты) — нейтральные молекулы или ионы, способные отдавать
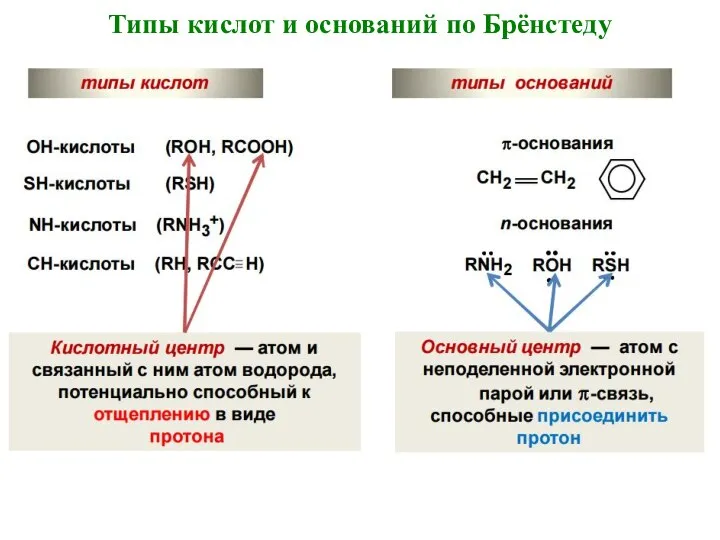
- 20. Типы кислот и оснований по Брёнстеду
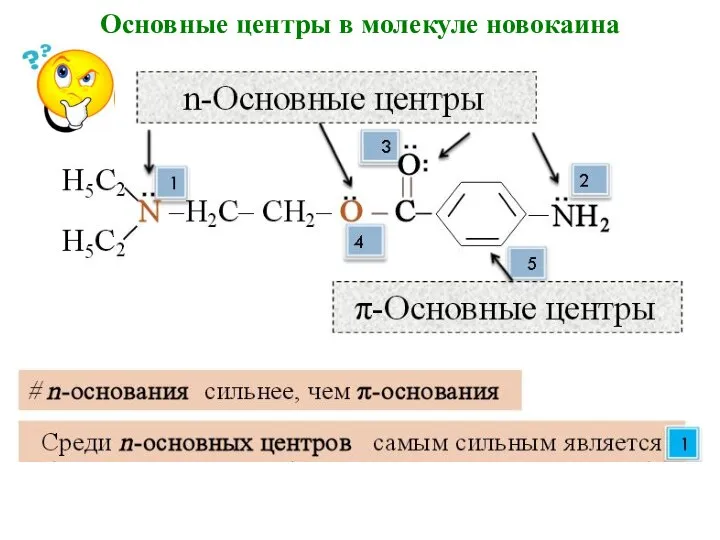
- 21. Основные центры в молекуле новокаина
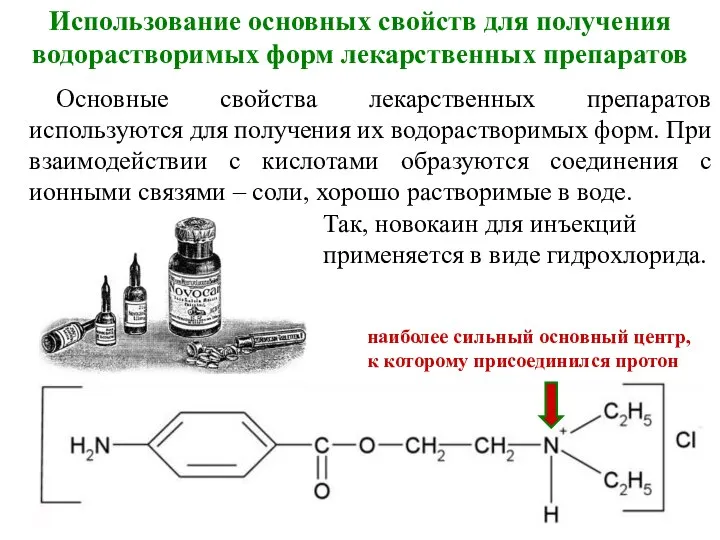
- 22. Использование основных свойств для получения водорастворимых форм лекарственных препаратов Основные свойства лекарственных препаратов используются для получения
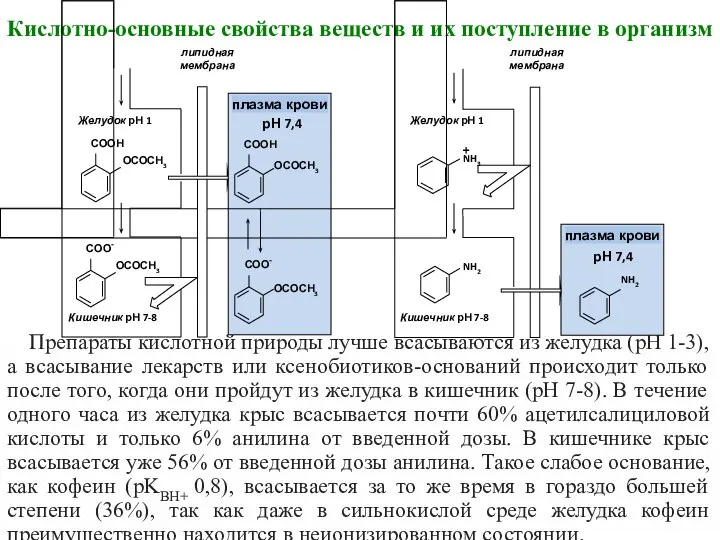
- 23. Кислотно-основные свойства веществ и их поступление в организм Препараты кислотной природы лучше всасываются из желудка (pH
- 24. Типы реакций в органической химии Органические реакции классифицируют по следующим признакам: 1. По электронной природе реагентов.
- 25. В зависимости от электронной природы реагентов различают реакции: нуклеофильные, электрофильные и свободнорадикальные Свободные радикалы – это
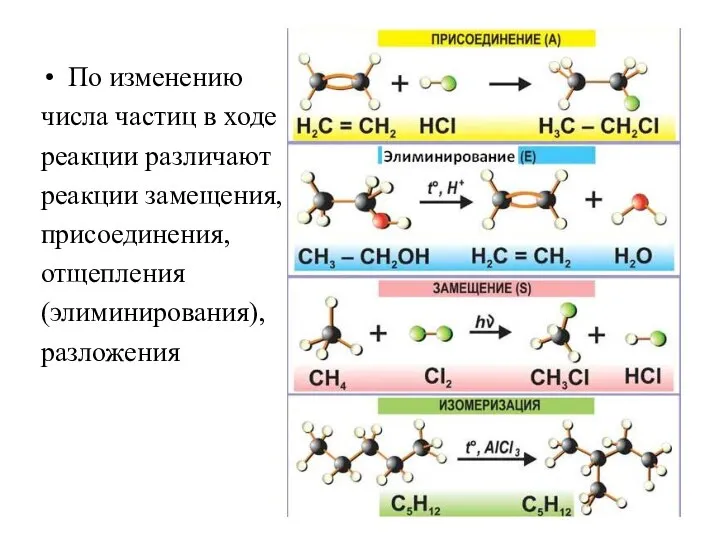
- 26. По изменению числа частиц в ходе реакции различают реакции замещения, присоединения, отщепления (элиминирования), разложения
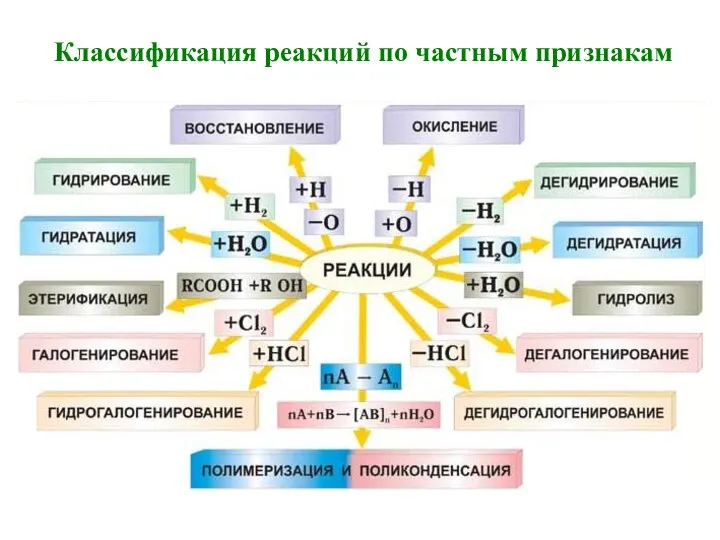
- 27. Классификация реакций по частным признакам
- 28. Селективность реакций в органической химии Реакционная способность всегда рассматривается только по отношению к реакционному партнеру. В
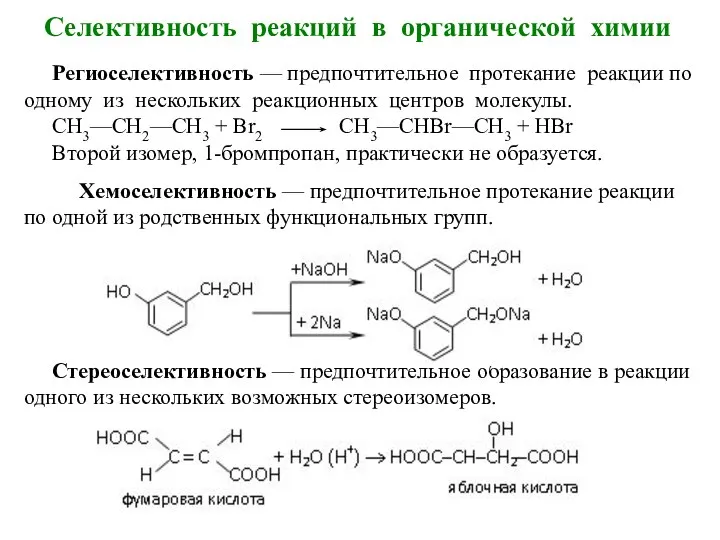
- 29. Селективность реакций в органической химии Региоселективность — предпочтительное протекание реакции по одному из нескольких реакционных центров
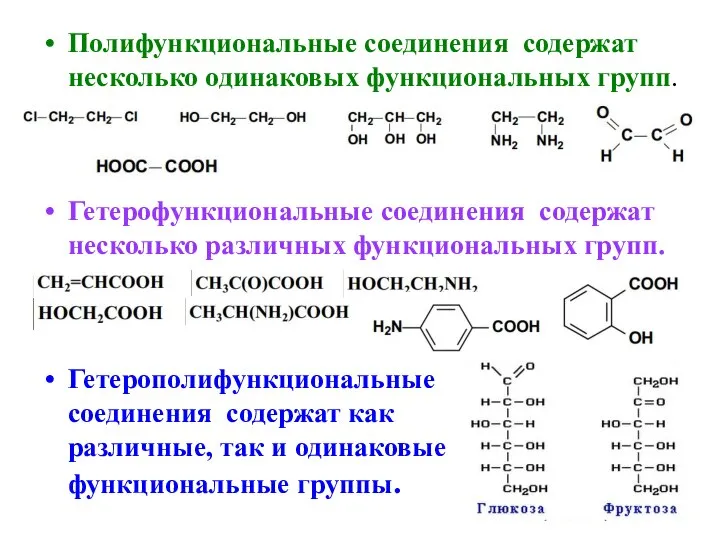
- 30. Полифункциональные соединения содержат несколько одинаковых функциональных групп. Гетерофункциональные соединения содержат несколько различных функциональных групп. Гетерополифункциональные соединения
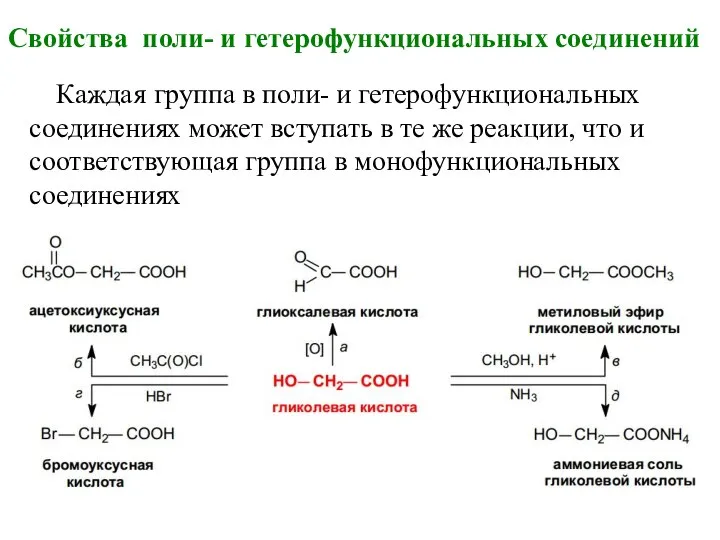
- 31. Свойства поли- и гетерофункциональных соединений Каждая группа в поли- и гетерофункциональных соединениях может вступать в те
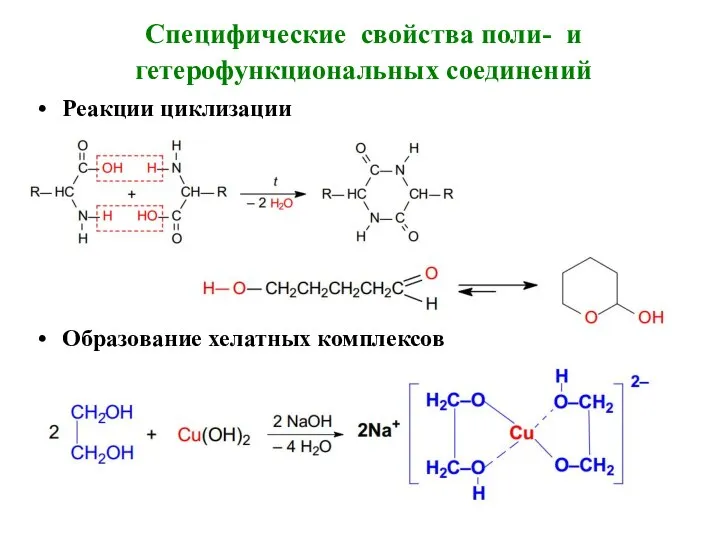
- 32. Специфические свойства поли- и гетерофункциональных соединений Реакции циклизации Образование хелатных комплексов
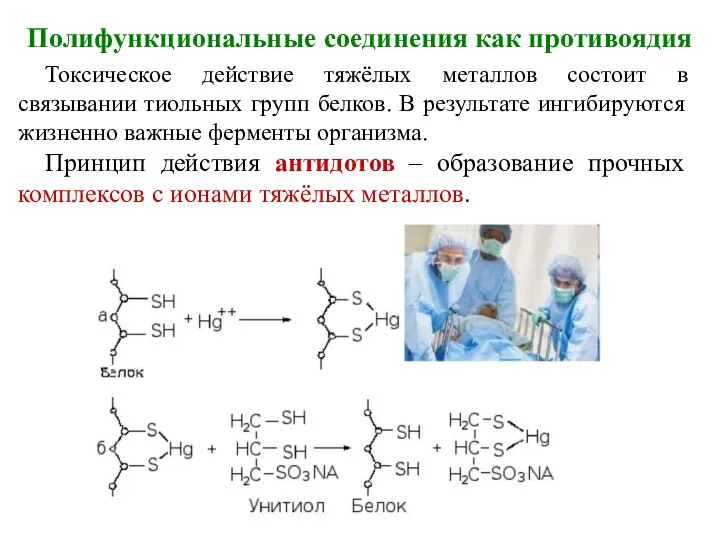
- 33. Полифункциональные соединения как противоядия Токсическое действие тяжёлых металлов состоит в связывании тиольных групп белков. В результате
- 35. Скачать презентацию












 Катализ и катализаторы. (Лекция 10)
Катализ и катализаторы. (Лекция 10) Слайд-шоу. Коррозия металлов и сплавов
Слайд-шоу. Коррозия металлов и сплавов Кислоты. Классификация кислот
Кислоты. Классификация кислот ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров
ВКР: Организация проведения товароведной экспертизы пищевкусовых товаров Методы защиты растений от вредителей
Методы защиты растений от вредителей Твердость минералов и их применение
Твердость минералов и их применение Современные представления о происхождении нефти и газа
Современные представления о происхождении нефти и газа Органические вещества 9 класс
Органические вещества 9 класс Элементы IV группы, побочной подгруппы периодической системы Менделеева
Элементы IV группы, побочной подгруппы периодической системы Менделеева Органические вещества
Органические вещества Молекулы. Свойства молекул
Молекулы. Свойства молекул Уравнения химической реакции 8 класс
Уравнения химической реакции 8 класс Оксид кремния
Оксид кремния Жуғыш заттар және жуғыш әсері. 1 Лекция
Жуғыш заттар және жуғыш әсері. 1 Лекция Чугуны. Структура и свойства. Классификация и применение
Чугуны. Структура и свойства. Классификация и применение Алканы. Хлороформ
Алканы. Хлороформ Экстракционные методы выделения продуктов микробиологического синтеза
Экстракционные методы выделения продуктов микробиологического синтеза Минералы. Классификация
Минералы. Классификация Строение атома кремния
Строение атома кремния Оксиды азота (II и IV). Азотная кислота. Строение молекулы
Оксиды азота (II и IV). Азотная кислота. Строение молекулы Презентация урока химии: «Металлы и их соединения» 9 класс. Учитель хим
Презентация урока химии: «Металлы и их соединения» 9 класс. Учитель хим Занимательные опыты по химии
Занимательные опыты по химии Enantioselective Total Synthesis
Enantioselective Total Synthesis Углерод. 9 класс
Углерод. 9 класс Спирты
Спирты Биополимеры: естественные и искусственные
Биополимеры: естественные и искусственные Коллигативные свойства растворов
Коллигативные свойства растворов Производство аммиака
Производство аммиака