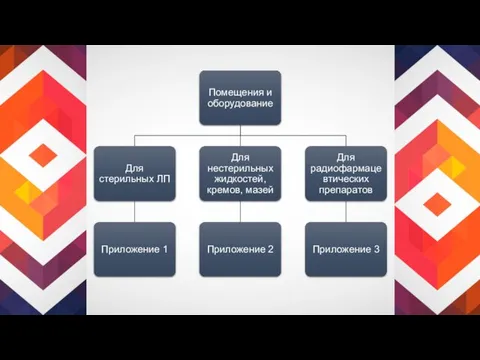
Требования к помещениям и оборудованию в рамках системы обеспечения качества при изготовлении лекарственных препаратов
- Главная
- Разное
- Требования к помещениям и оборудованию в рамках системы обеспечения качества при изготовлении лекарственных препаратов

Содержание
- 2. Основной документ: Руководство PIC/S по надлежащей практике изготовления лекарственных препаратов в в медицинских учреждениях, версия PE
- 3. Помещения и оборудование должны быть пригодны для планируемой деятельности и не должны представлять какой-либо опасности для
- 4. Помещения и оборудование: Общие требования 1. Помещения и оборудование должны быть надлежащим образом спроектированы и построены,
- 5. Помещения и оборудование: Производственные зоны 1. В производственных зонах должно обеспечиваться надлежащее разделение от других видов
- 6. Помещения и оборудование: Зоны хранения 1. Зоны хранения должны иметь достаточную вместимость для обеспечения организованного хранения
- 7. Помещения и оборудование: Зоны контроля качества Как правило, мероприятия по контролю качества должны проводиться в специализированной
- 8. 1. Оборудование для изготовления должно быть спроектировано, размещено и обслуживаться в соответствии с его целевым назначением.
- 10. Стерильное изготовление ЛП 13. Помещения должны располагаться в окружении, которое в совокупности с мерами по защите
- 11. Особые требования к изготовлению терминально стерилизуемых продуктов: 18. Изготовление компонентов и большинства продуктов должно производиться в
- 12. Особые требования к деятельности по стерильному изготовлению 19. После промывки компоненты следует обрабатывать в окружении класса
- 13. Особые требования к деятельности по стерильному изготовлению 20. Процесс изготовления под отрицательным давлением, защищающим оператора и
- 14. Особые требования к деятельности по стерильному изготовлению 22. Чтобы минимизировать риск перекрестного загрязнения, объекты должны быть
- 15. Изготовление нестерильных жидкостей, кремов, мазей 3. Для защиты продукта от загрязнения рекомендуется использовать закрытые системы обработки
- 16. j) Перед использованием проверьте контейнеры и крышки, чтобы убедиться, что они чистые и сухие. k) Контейнеры
- 17. Изготовление радиофармацевтических препаратов 11. Изготовление радиофармацевтических препаратов должно проходить на специализированных объектах. 12. Радиофармацевтические препараты для
- 18. Изготовление радиофармацевтических препаратов 17. Во всех возможных случаях продукты должны изготавливаться с использованием закрытого метода изготовления,
- 19. Изготовление радиофармацевтических препаратов 23. Генераторы должны размещаться в подходящей зоне или на рабочем месте, примыкающем к
- 20. Закрытые рабочие места определяются как изоляторы и горячие камеры, которые могут быть проверены на герметичность. Открытые
- 22. Скачать презентацию
Основной документ:
Руководство PIC/S по надлежащей практике изготовления лекарственных препаратов в в
Основной документ:
Руководство PIC/S по надлежащей практике изготовления лекарственных препаратов в в
Помещения и оборудование должны быть пригодны для планируемой деятельности и не
Помещения и оборудование должны быть пригодны для планируемой деятельности и не
Помещения и оборудование: Принципы
Помещения и оборудование: Общие требования
1. Помещения и оборудование должны быть надлежащим
Помещения и оборудование: Общие требования
1. Помещения и оборудование должны быть надлежащим
2. Для снижения риска загрязнения, например в результате перекрестного загрязнения или накопления пыли и грязи, следует использовать надлежащим образом спроектированные помещения и оборудование, а также тщательно продуманные и подходящие методы работы. Проектом должна быть предусмотрена возможность тщательной очистки. Особую осторожность следует проявлять при отборе проб или очистке оборудования, а также — в соответствующих случаях — его дезинфекции после ремонта или технического обслуживания.
3. Должны приниматься адекватные меры против проникновения насекомых и других животных (борьба с вредителями).
4. Деятельность по мытью и очистке сама по себе не должна быть источником загрязнения.
5. Зоны производства, хранения и контроля качества должны быть доступны только для уполномоченного персонала.
6. Окружающие условия (температура, влажность, освещение) во время производства, контроля качества и хранения (включая хранение в холодильниках) должны определяться и контролироваться и при необходимости регулироваться. Результаты контроля должны документироваться, оцениваться и сохраняться. Когда условия выходят за установленные пределы, должны приниматься соответствующие корректирующие меры.
7. Все помещения должны быть чистыми, опрятными и хорошо освещенными.
Помещения и оборудование: Производственные зоны
1. В производственных зонах должно обеспечиваться
Помещения и оборудование: Производственные зоны
1. В производственных зонах должно обеспечиваться
2. Следует рассмотреть вопрос о разделении зон для конкретных лекарственных форм (например, сухие и влажные производственные объекты). Если разделение зон для конкретных лекарственных форм не представляется возможным, необходимо провести документальную оценку риска и принять соответствующие меры, прежде чем работать с разными лекарственными формами одновременно.
3. Необходимо предусмотреть специализированные комнаты для опасных препаратов, например цитостатиков, пенициллинов, биопрепаратов, радиофармацевтических препаратов, препаратов крови. В исключительных случаях принцип работы в рамках производственных кампаний может быть приемлемым при условии принятия конкретных мер предосторожности и проведения всех необходимых оценок риска.
4. Материалы и продукты следует хранить и обрабатывать таким образом, чтобы риск перепутывания разных продуктов или их ингредиентов был минимальным, чтобы избежать перекрестного загрязнения и уменьшить риск пропуска или некорректного выполнения стадии обработки.
5. Зоны взвешивания и отбора проб должны быть в достаточной степени отделены от других зон изготовления, чтобы избежать перекрестного загрязнения.
Помещения и оборудование: Зоны хранения
1. Зоны хранения должны иметь достаточную
Помещения и оборудование: Зоны хранения
1. Зоны хранения должны иметь достаточную
2. Исходные и упаковочные материалы обычно хранятся вне зон изготовления, если только они не сегрегированы надлежащим образом.
3. Материалы и препараты, находящиеся в карантине, отклоненные, возвращенные или отозванные, должны храниться в изолированных зонах и должны быть четко помечены в качестве таковых.
4. Условия хранения (например, температура, относительная влажность), необходимые для того, чтобы не оказывать отрицательного воздействия на материал или качество препарата, должны быть определены и контролироваться. Контроль должен быть адекватным для поддержания всех частей соответствующей зоны хранения в соответствии с предписанными условиями. Зоны хранения должны быть оборудованы регистраторами или другими контрольными устройствами, которые показывали бы, когда установленные условия не поддерживались, чтобы можно было оценить ситуации, не удовлетворяющие техническим условиям, и принять соответствующие меры.
Помещения и оборудование: Зоны контроля качества
Как правило, мероприятия по контролю
Помещения и оборудование: Зоны контроля качества
Как правило, мероприятия по контролю
1. Комнаты для отдыха и приема пищи должны быть отделены от других помещений.
2. Туалеты, помещения для переодевания и умывания должны быть легко доступны и соответствовать числу пользователей. Туалеты не должны иметь непосредственного доступа из производственных или складских помещений
Помещения и оборудование: Дополнительные зоны
1. Оборудование для изготовления должно быть спроектировано, размещено и обслуживаться в
1. Оборудование для изготовления должно быть спроектировано, размещено и обслуживаться в
2. Оборудование должно быть сконструировано таким образом, чтобы его можно было легко и тщательно очистить. Оно должно содержаться в чистом и сухом состоянии.
3. Измерительное, взвешивающее и контрольное оборудование должно иметь требуемую прецизионность: оно должно калиброваться, а также проверяться на корректность работы и повторно калиброваться через соответствующие промежутки времени.
4. Неисправное оборудование подлежит выведению из зон производства и контроля качества или хотя бы иметь четкую маркировку «неисправно».
Помещения и оборудование: оборудование
Стерильное изготовление ЛП
13. Помещения должны располагаться в окружении, которое в совокупности
Стерильное изготовление ЛП
13. Помещения должны располагаться в окружении, которое в совокупности
14. Стерильные изготовления должны осуществляться в чистых специализированных зонах, имеющих воздушные шлюзы для доступа персонала, материалов и оборудования. Раздевалки должны быть выполнены в виде воздушных шлюзов.
15. Расположение и использование моек следует тщательно продумать с учетом их потенциальной способности вызывать микробиологическое загрязнение. Раковины или мойки рук не должны быть доступны в рабочих комнатах или вблизи выхода из раздевалок. Если раздевалка находится в прилежащих зонах, то ее следует регулярно контролировать и дезинфицировать.
16. Для всего оборудования, используемого для обработки, должны быть составлены и внедрены стандартные операционные процедуры.
17. Если оправданно, оборудование следует регулярно калибровать и проверять правильность приборов измерения объема.
Особые требования к изготовлению терминально стерилизуемых продуктов:
18. Изготовление компонентов и
Особые требования к изготовлению терминально стерилизуемых продуктов:
18. Изготовление компонентов и
Наполнение продуктов для терминальной стерилизации должно производиться в окружении класса не ниже С. В тех случаях, когда продукт подвергается необычному риску загрязнения из окружающей среды, например из-за низкой скорости проведения операции наполнения или из-за того, что контейнеры имеют широкое горлышко или обязательно выдерживаются в течение нескольких секунд перед укупориванием, наполнение должно производиться в зоне класса А с прилегающей зоной класса не ниже С.
Изготовление и наполнение мазей, кремов, суспензий и эмульсий обычно следует проводить в окружении класса С перед терминальной стерилизацией.
Особые требования к деятельности по стерильному изготовлению
19. После промывки компоненты следует
Особые требования к деятельности по стерильному изготовлению
19. После промывки компоненты следует
Изготовление растворов, подвергаемых стерильной фильтрации во время процесса, следует производить в окружении класса С; если они не фильтруются, то изготовление материалов и продуктов следует производить в окружении класса А.
Обработка и наполнение асептически изготовляемых продуктов (открытые и закрытые процедуры) должны выполняться в окружении класса А в шкафу с ламинарным потоком воздуха (LFC) или фармацевтическом изоляторе положительного давления. Комната должна иметь положительное давление (в идеале 10-15 Паскалей) и поток воздуха относительно окружающих зон более низкого класса, чтобы защитить продукт от загрязнения.
Примеры операций для асептически изготовляемых препаратов, которые должны выполняться в помещениях различного класса:
Особые требования к деятельности по стерильному изготовлению
20. Процесс изготовления под отрицательным
Особые требования к деятельности по стерильному изготовлению
20. Процесс изготовления под отрицательным
21. Поскольку терминальная стерилизация асептически изготовляемых продуктов не проводится, микробиологическое окружение, в котором их изготавливают, имеет первостепенное значение. В связи с этим необходимо контролировать окружающие условия и допускать в них только уполномоченных лиц. Если нет надлежащего обоснования, прилежащее окружение для LFC и BSC должно соответствовать требованиям к помещениям класса В, а для фармацевтических изоляторов — класса D.
Любое обоснование для прилежащего окружения более низкого класса должно основываться на документально подтвержденной оценке риска, которую следует проводить с большой тщательностью. Возможные факторы, которые могут быть учтены при такой оценке риска, включают:
• Время между изготовлением и применением
• Использование закрытой системы
• Природа и состав продукта
Особые требования к деятельности по стерильному изготовлению
22. Чтобы минимизировать риск перекрестного
Особые требования к деятельности по стерильному изготовлению
22. Чтобы минимизировать риск перекрестного
Изготовление нестерильных жидкостей, кремов, мазей
3. Для защиты продукта от загрязнения рекомендуется
Изготовление нестерильных жидкостей, кремов, мазей
3. Для защиты продукта от загрязнения рекомендуется
4. Производственные помещения не должны использоваться для других видов деятельности.
5. Должны приниматься меры по снижению риска загрязнения, которые включают:
a) Использование спецодежды и шапочек для покрытия волос.
b) Если используются открытые процедуры, рекомендуются местная фильтрация воздуха и ношение перчаток.
c) Оперативная чистка используемого оборудования.
d) Ополаскивание оборудования, которое контактирует с препаратом водой соответствующего класса после промывки (могут быть пригодны очищенная вода или бутилированная вода для инъекций либо орошение, если они используются в течение 24 часов после вскрытия).
e) Убедитесь, что удалены остатки чистящих и дезинфицирующих средств (например, гипохлориты).
f) Перед хранением убедитесь, что оборудование чистое и сухое. g) Бережное хранение очищенного оборудования.
h) Все материалы, поступающие в производственную зону, должны быть чистыми.
i) Дезинфекция спиртом критических поверхностей перед использованием.
j) Перед использованием проверьте контейнеры и крышки, чтобы убедиться, что они
j) Перед использованием проверьте контейнеры и крышки, чтобы убедиться, что они
k) Контейнеры с конечным продуктом не подлежат повторному использованию.
l) Швабры и тряпки не должны оставлять волокна, их следует дезинфицировать каждый день, если они используются повторно, и не следует использовать для очистки других помещений.
m) Если в производственной зоне одновременно осуществляется более одного вида деятельности, то должно быть обеспечено надлежащее разделение для предотвращения перекрестного загрязнения и перепутывания. Должна проводиться оценка риска.
n) Рекомендуется использовать специализированное оборудование в случае сильнодействующих веществ, пенициллинов, цефалоспоринов, сенсибилизаторов, цитотоксических средств, эктопаразитицидов и других веществ, которые очень опасны или трудно поддаются очистке. Эти материалы должны быть идентифицированы, и должна быть проведена оценка риска.
6. Резервуары, контейнеры, трубопроводы и насосы должны быть спроектированы и установлены таким образом, чтобы их можно было легко чистить и при необходимости дезинфицировать. В частности, конструкция оборудования должна включать минимум тупиковых или застойных участков, где могут скапливаться остатки, способствуя размножению микробов.
7. По возможности следует избегать использования стеклянных приборов. Высококачественная нержавеющая сталь часто является материалом выбора для деталей, вступающих в контакт с продуктом. Стеклянное оборудование, если оно используется, необходимо проверять на наличие повреждений до и после использования.
Изготовление нестерильных жидкостей, кремов, мазей
Изготовление радиофармацевтических препаратов
11. Изготовление радиофармацевтических препаратов должно проходить на специализированных объектах.
Изготовление радиофармацевтических препаратов
11. Изготовление радиофармацевтических препаратов должно проходить на специализированных объектах.
12. Радиофармацевтические препараты для инъекций следует изготавливать в окружении, защищающем продукт от микробного загрязнения. В то же время окружающая среда также должна быть защищена от ионизирующего излучения.
13. Если исследовательская деятельность и изготовление выполняются в одном и том же месте, необходимо обеспечить их физическое или организационное разделение, чтобы избежать влияния исследовательского персонала на задачи GMP.
14. Должно быть предусмотрено соответствующее оборудование для обнаружения радиации и мониторинга персонала на предмет радиационного облучения.
15. В связи с требованиями охраны труда и техники безопасности, чтобы обеспечить оперативное удаление загрязнений для персонала, может потребоваться разместить подходящие средства, например мойки и (или) душевые кабины, ближе к чистым комнатам, чем в случае обычных асептических операций (в зависимости от национальных требований к безопасности). Следует предусмотреть надлежащие средства контроля за проектированием и техническим обслуживанием моек и (или) душевых кабин. Могут быть использованы и другие методы обеззараживания в соответствии с местными требованиями.
16. Маркирование клеток крови необходимо производить в отдельной комнате, в которой не проводятся операции по изготовлению. Риск использования общих раздевалок для этих двух видов деятельности должен быть оценен и задокументирован.
Изготовление радиофармацевтических препаратов
17. Во всех возможных случаях продукты должны изготавливаться с
Изготовление радиофармацевтических препаратов
17. Во всех возможных случаях продукты должны изготавливаться с
19. Следует проводить осмотр перчаток для изоляторов и рукавов манипулятора горячих камер перед использованием. Испытания на герметичность горячих камер, если возможно, и изоляторов должны проводиться с интервалами, определенными в дополнении 1.
20. Ожидается, что любой открытый способ изготовления и обработки асептических продуктов будет осуществляться в окружении класса А. В случае закрытого способа изготовления, используемого для наполнения окончательного продукта в один контейнер для немедленного использования, для проведения операции наполнения может подойти зона класса С на основании оценки риска.
21. В случае продуктов, которые могут быть подвергнуты терминальной стерилизации, наполнение необходимо проводить в окружении класса С. В случае стадий до наполнения, например радиохимического синтеза, следует использовать окружение класса С или обосновать выбор окружения другого класса посредством оценки риска.
22. Материалы должны передаваться на рабочее место через передаточные люки, которые блокируются в соответствующих случаях
Изготовление радиофармацевтических препаратов
23. Генераторы должны размещаться в подходящей зоне или на
Изготовление радиофармацевтических препаратов
23. Генераторы должны размещаться в подходящей зоне или на
24. Если для изготовления радиофармацевтических препаратов используется изолятор, воздух из изолятора, как правило, не должен циркулировать в замкнутом цикле.
25. Класс, необходимый для окружающей комнаты, будет зависеть от различных факторов, которые должны оцениваться в рамках документированной оценки риска с учетом типа системы защиты рабочего места и метода изготовления продукта. В таблице ниже приведены минимальные ожидаемые стандарты для ряда видов деятельности.
Закрытые рабочие места определяются как изоляторы и горячие камеры, которые могут
Закрытые рабочие места определяются как изоляторы и горячие камеры, которые могут
Если асептически изготовляемый радиоактивный лекарственный препарат в открытом флаконе при любых обстоятельствах во время производства находится за пределами рабочего места, комната должна соответствовать классу В.
* Примечание: в случае немедленного введения допускается использовать зону класса C при условии оценки риска.
26. Радиоактивные материалы должны храниться в экранированной внешней упаковке, такой как свинцово-вольфрамовые сосуды или эквивалентные контейнеры для радиационной защиты.
27. В зависимости от микробного риска для продукта изготовление капсул и других нестерильных продуктов должно осуществляться в контролируемой среде с соответствующей радиационной защитой.
Изготовление радиофармацевтических препаратов


















 клуб бардовской песни
клуб бардовской песни 20110527_Interaktivnyy_plakat_Sinkveyn
20110527_Interaktivnyy_plakat_Sinkveyn Гарнизонная церковь в честь Покрова Богородицы в г. Орле
Гарнизонная церковь в честь Покрова Богородицы в г. Орле Предприятие по добыче, обогащению и переработке руд Тырныаузского вольфрамо-молибденового месторождения. Гидрометаллургический
Предприятие по добыче, обогащению и переработке руд Тырныаузского вольфрамо-молибденового месторождения. Гидрометаллургический Бейджики 1-Б
Бейджики 1-Б Сервис буровых растворов
Сервис буровых растворов 2 Kap2
2 Kap2 outlook
outlook Проектирование изделий из тканей, содержащих искусственные волокна, из искусственных кож, замши, тканей с пленочным покрытием
Проектирование изделий из тканей, содержащих искусственные волокна, из искусственных кож, замши, тканей с пленочным покрытием Программируемые логические контроллеры
Программируемые логические контроллеры 20140123_agressiya_1_u_detey_kak_sledstvie_uvlecheniya_kompyuternymi_-_kopiya_0
20140123_agressiya_1_u_detey_kak_sledstvie_uvlecheniya_kompyuternymi_-_kopiya_0 БОШКА
БОШКА Работа с фрагментами в Paint
Работа с фрагментами в Paint Общий прием сложения с переходом через десяток
Общий прием сложения с переходом через десяток kiber
kiber Портфолио Арсенұлы Әлнұр Арсен
Портфолио Арсенұлы Әлнұр Арсен Асинхронные машины. Конструкция и принцип действия
Асинхронные машины. Конструкция и принцип действия педсовет авг 20
педсовет авг 20 ФГОС ОО формирование компетенций ср-ми ДО
ФГОС ОО формирование компетенций ср-ми ДО Резюме2 (2)
Резюме2 (2) Угловые соединения
Угловые соединения Смена владельца сим-карты, МТС
Смена владельца сим-карты, МТС 28 листы рекомендаций
28 листы рекомендаций Ребенок с ограниченными возможностями здоровья в современном российском обществе
Ребенок с ограниченными возможностями здоровья в современном российском обществе Переробка та утилізація відходів нафтопереробної галузі
Переробка та утилізація відходів нафтопереробної галузі Очистные сооружения хозяйственно-бытовых стоков
Очистные сооружения хозяйственно-бытовых стоков Результаты работы с механизированным фондом скважин ЦДНГ №8 за 1 кв. 2015 г
Результаты работы с механизированным фондом скважин ЦДНГ №8 за 1 кв. 2015 г Мультимедийное оборудование в профессиональной деятельности
Мультимедийное оборудование в профессиональной деятельности