Содержание
- 2. Промышленное получение аммиака Фриц Габер, Карл Бош – Нобелевская премия 1918 и 1931 за создание технологии
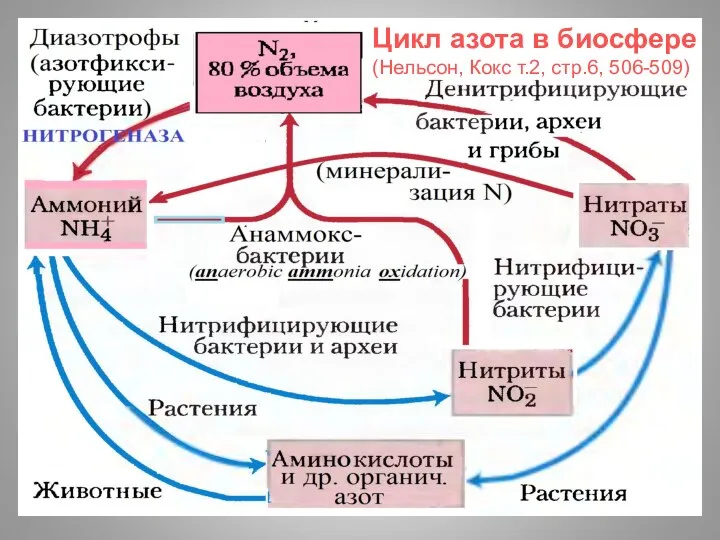
- 3. Цикл азота в биосфере (Нельсон, Кокс т.2, стр.6, 506-509)
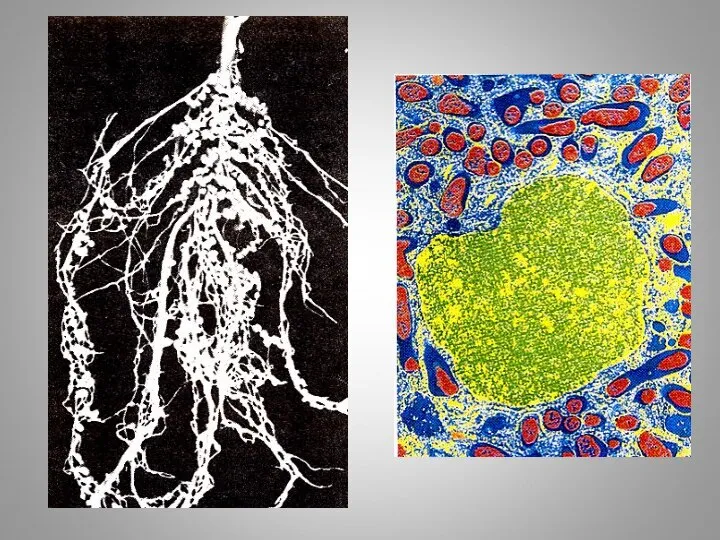
- 4. Биологическая фиксация молекулярного азота воздуха
- 5. Азотофиксирующие организмы НИТРОГЕНАЗА БАКТЕРИИ - диазотрофы: - свободноживущие (рр. Azotobacter, Clostridium, все фотосинтезирующие, ряд АРХЕЙ…) -
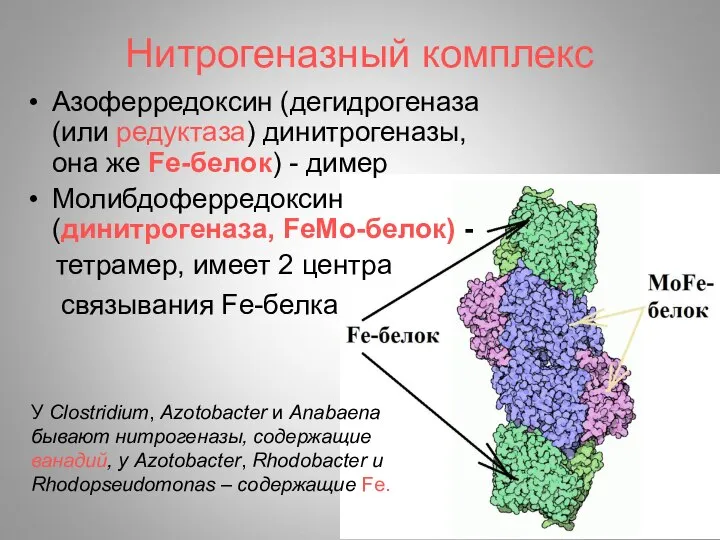
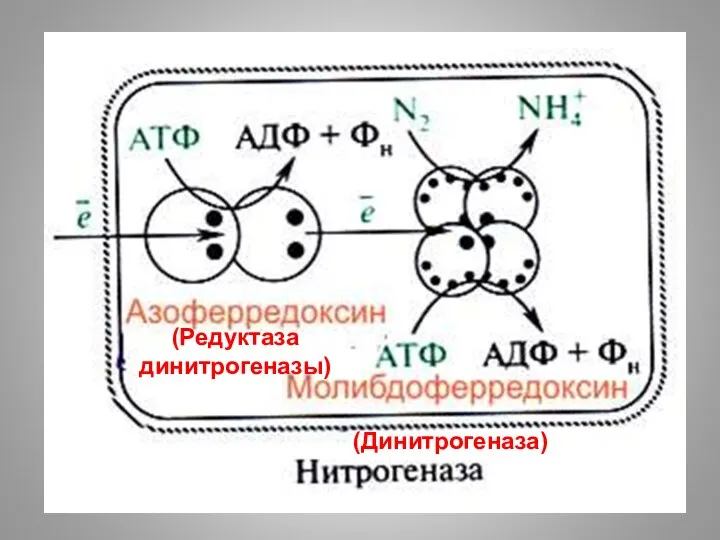
- 7. Нитрогеназный комплекс Азоферредоксин (дегидрогеназа (или редуктаза) динитрогеназы, она же Fe-белок) - димер Молибдоферредоксин (динитрогеназа, FeMo-белок) -
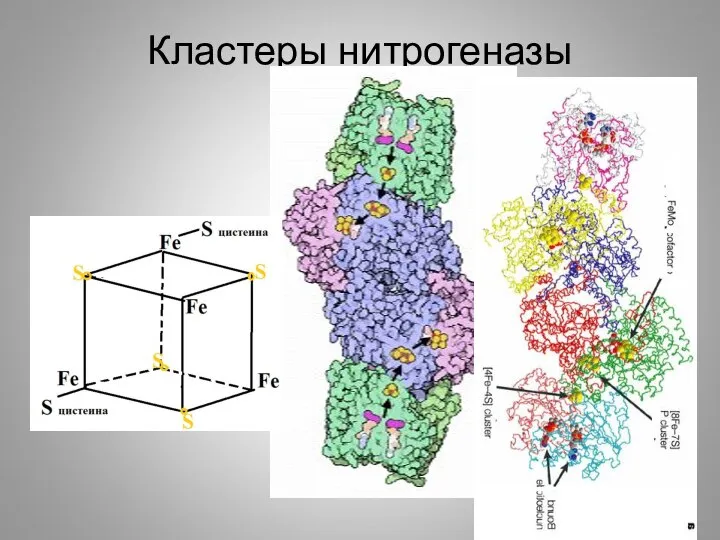
- 8. Кластеры нитрогеназы
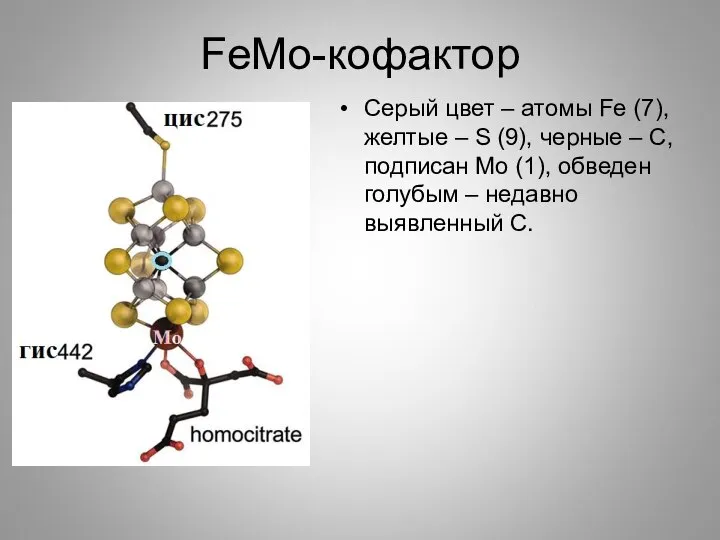
- 10. FeMo-кофактор Серый цвет – атомы Fe (7), желтые – S (9), черные – С, подписан Мо
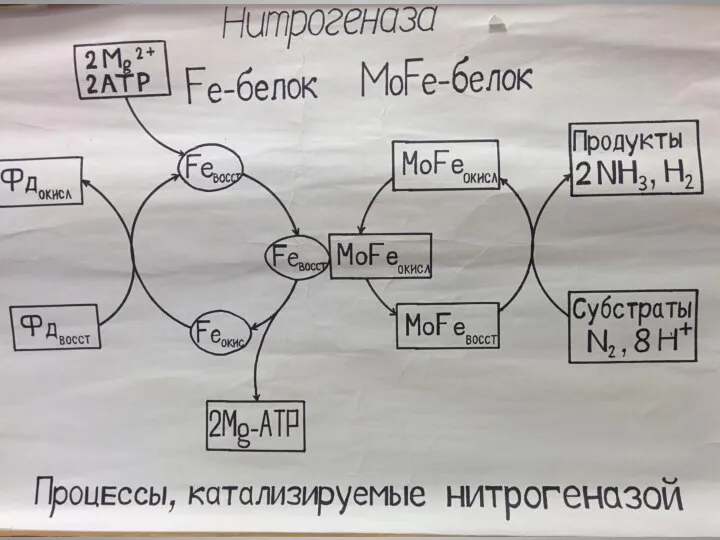
- 11. Работа нитрогеназы У Rhizobium для восстановления 1N2 может идти от 12 до 35 АТФ Побочная реакция
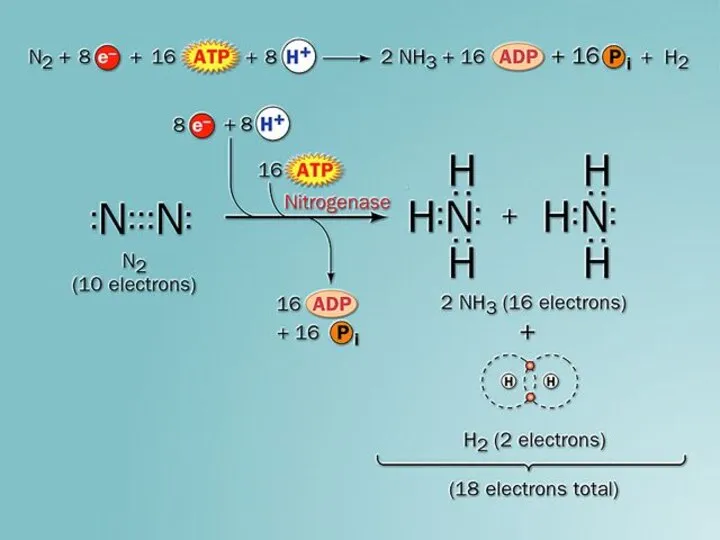
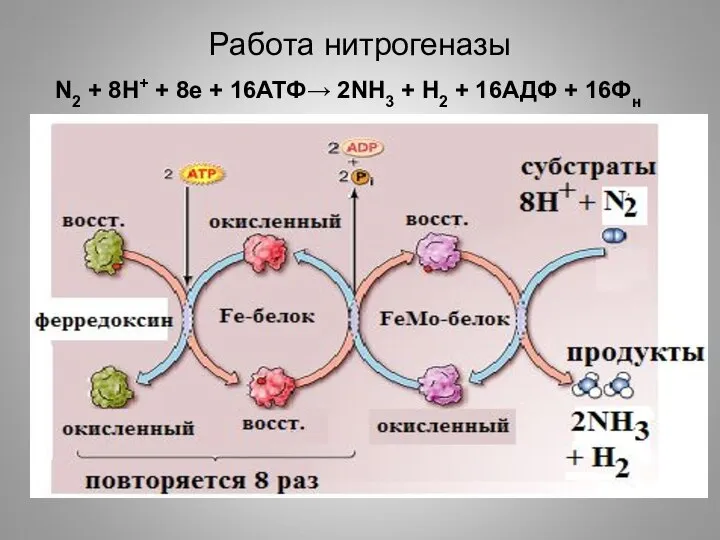
- 14. Работа нитрогеназы N2 + 8H+ + 8e + 16АТФ→ 2NH3 + H2 + 16АДФ + 16Фн
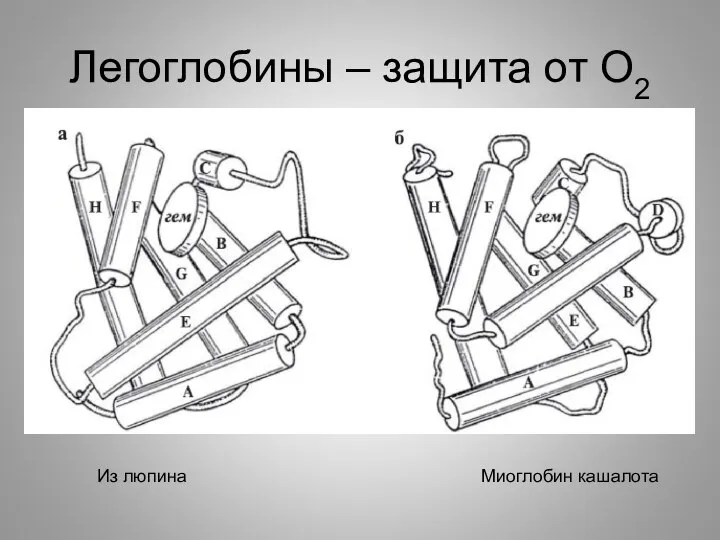
- 16. Легоглобины – защита от О2 Из люпина Миоглобин кашалота
- 17. РАСТЕНИЕ: поглощение и переработка NH4+ из почвы (или от симбионтов) 2 типа транспортных систем: если аммония
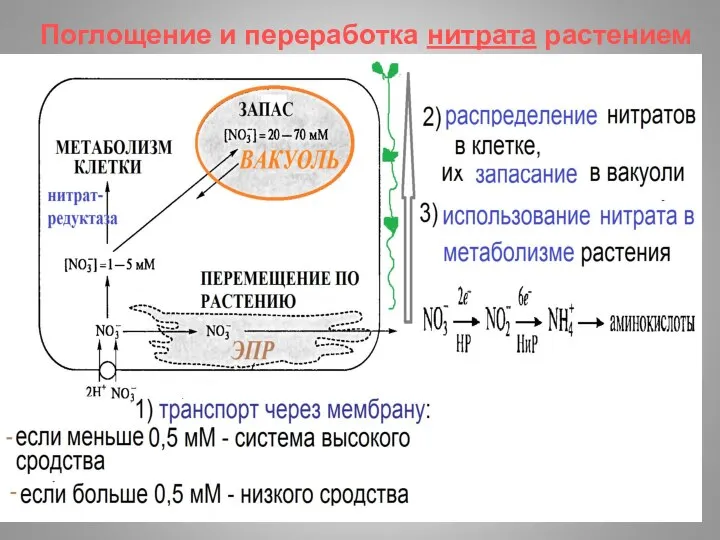
- 18. Поглощение и переработка нитрата растением
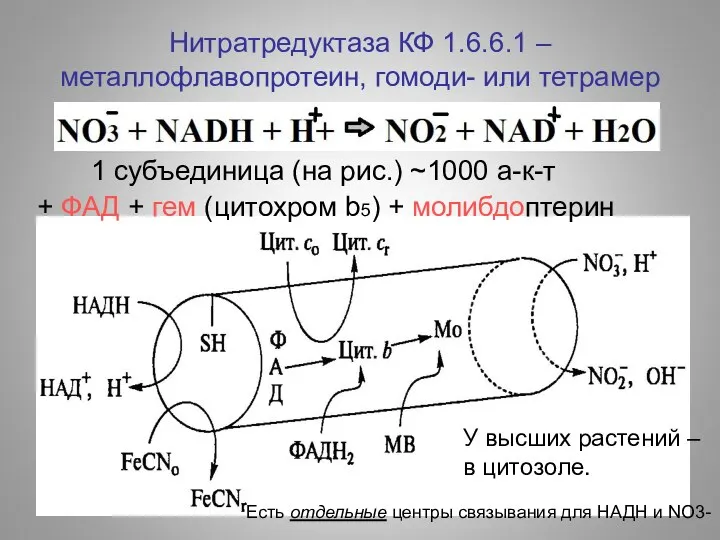
- 19. Нитратредуктаза КФ 1.6.6.1 – металлофлавопротеин, гомоди- или тетрамер + ФАД + гем (цитохром b5) + молибдоптерин
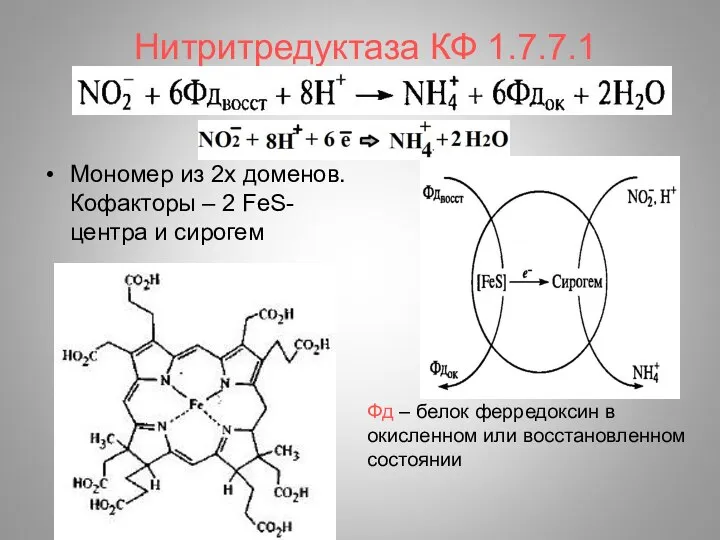
- 20. Нитритредуктаза КФ 1.7.7.1 Мономер из 2х доменов. Кофакторы – 2 FeS-центра и сирогем Фд – белок
- 21. нитраты и нитриты Рекомендации ВОЗ - в сутки не более 3,7 мг нитратов на 1 кг
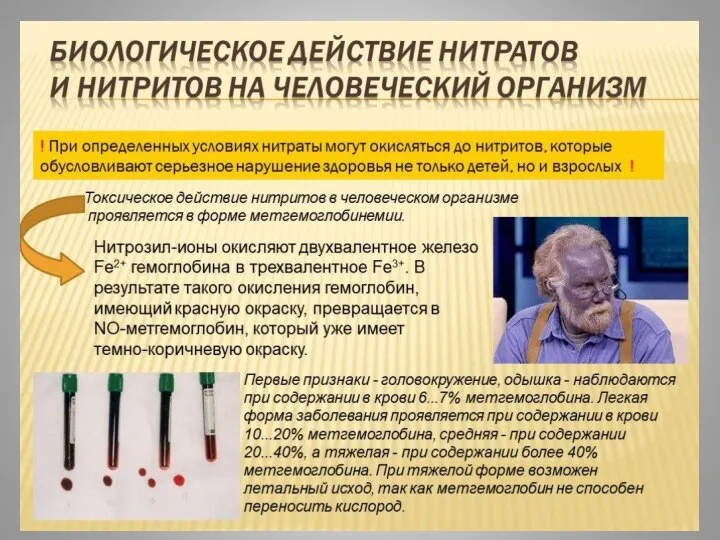
- 22. Типы токсического воздействия на организм человека ТОКСИЧНОСТЬ Первичная - самого нитрат-иона; Вторичная - нитрит-иона, Третичная –
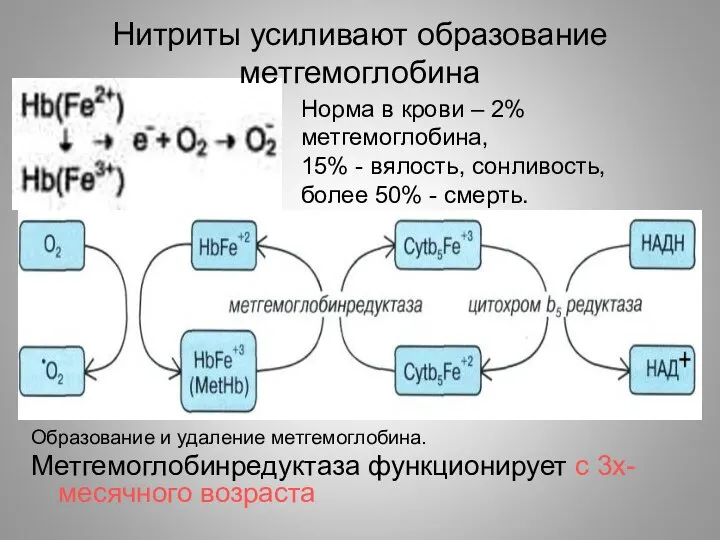
- 25. Нитриты усиливают образование метгемоглобина Образование и удаление метгемоглобина. Метгемоглобинредуктаза функционирует с 3х-месячного возраста Норма в крови
- 26. Нитрозамины и их образование Нитрозамины – это соединения с группировкой =N-N=O Например, нитрит-ион в водной среде
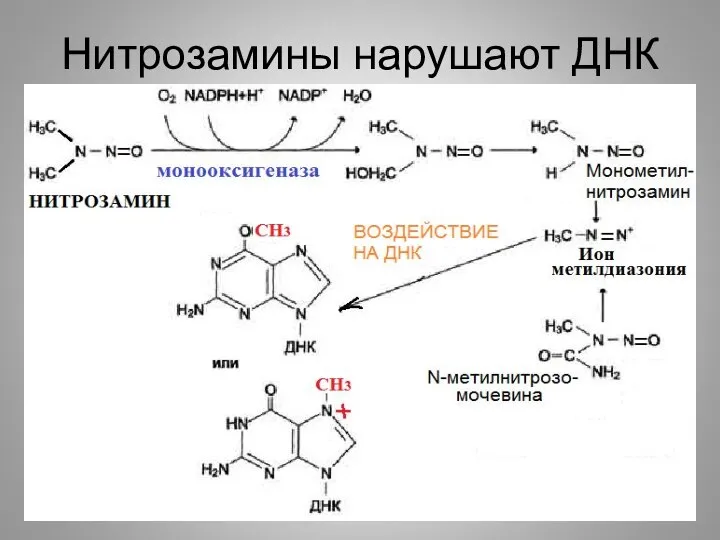
- 27. Нитрозамины нарушают ДНК
- 29. Проблема нитратов в пище Управление Роспотребнадзора по Нижегородской области, 2018: превышение по нитратам из 2000 взятых
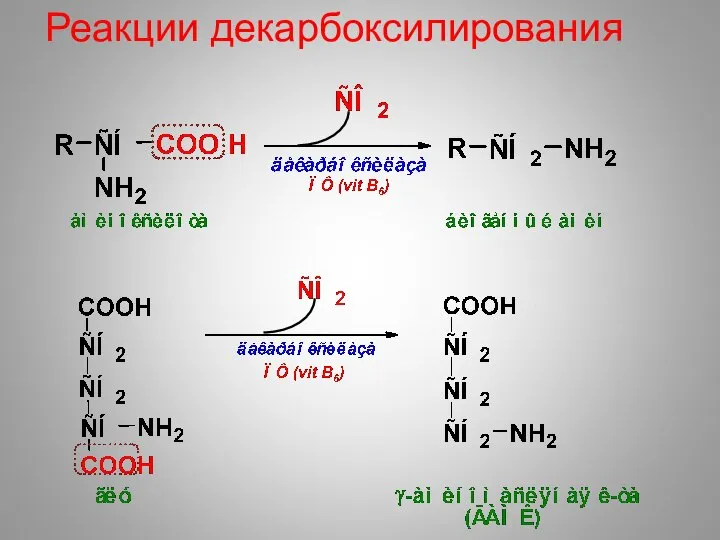
- 31. Пути синтеза белковых аминокислот 1) прямое восстановительное аминирование 1а) – образование амидов 2) переаминирование 3) ферментативные
- 32. Семейства белковых аминокислот по путям синтеза 1) Семейства 1 – 4 (на основе α-кетоглутаровой к-ты, ПВК,
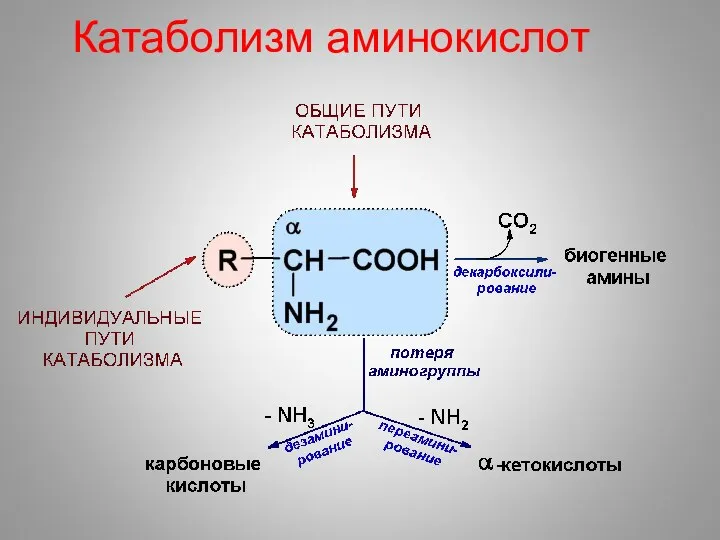
- 33. Катаболизм аминокислот
- 34. Катаболизм аминокислот
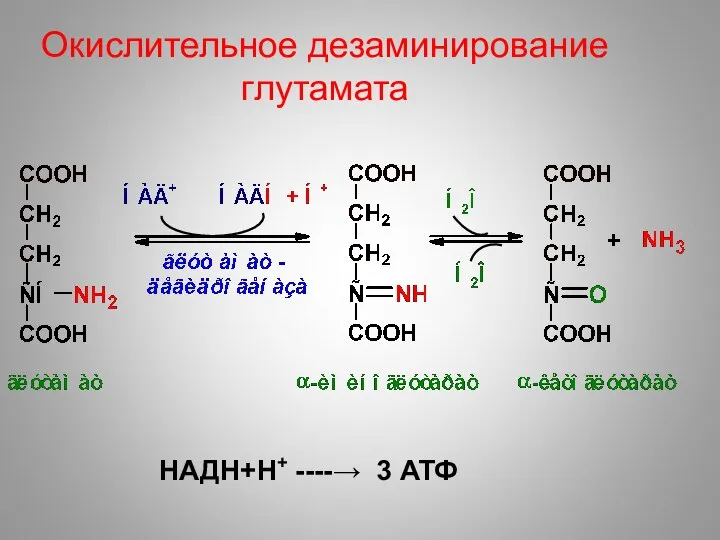
- 35. Окислительное дезаминирование глутамата НАДН+Н+ ----→ 3 АТФ
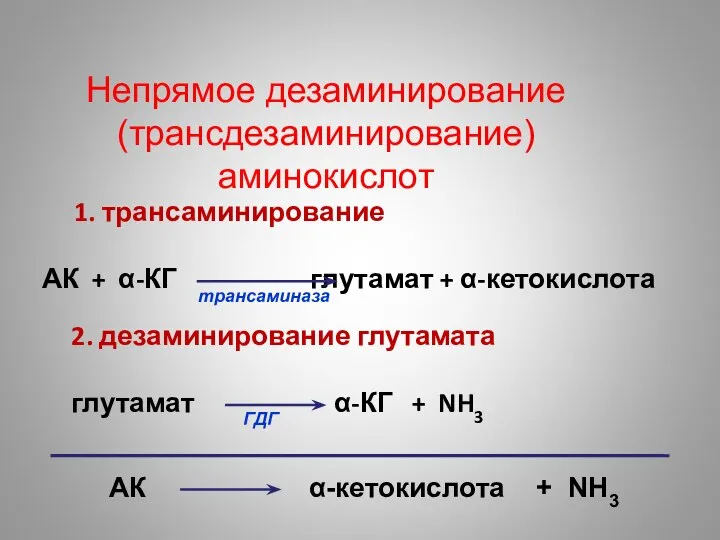
- 36. Непрямое дезаминирование (трансдезаминирование) аминокислот АК α-кетокислота + NH3 1. трансаминирование АК + α-КГ глутамат + α-кетокислота
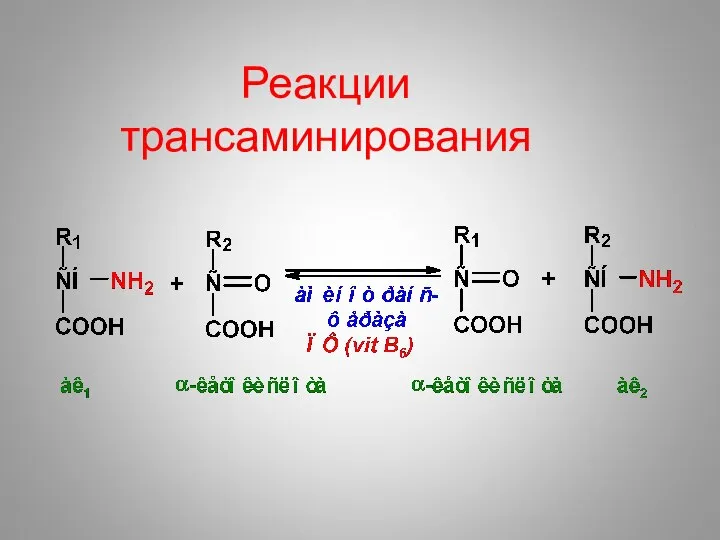
- 37. Реакции трансаминирования
- 38. Реакции декарбоксилирования
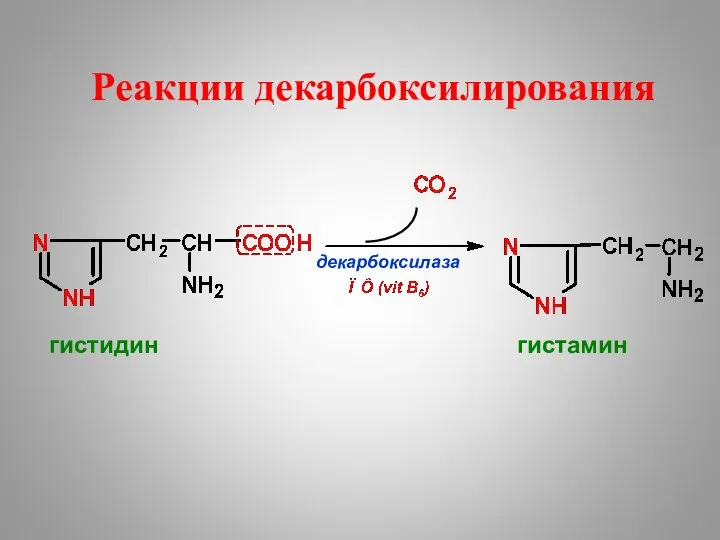
- 39. Реакции декарбоксилирования декарбоксилаза гистидин гистамин
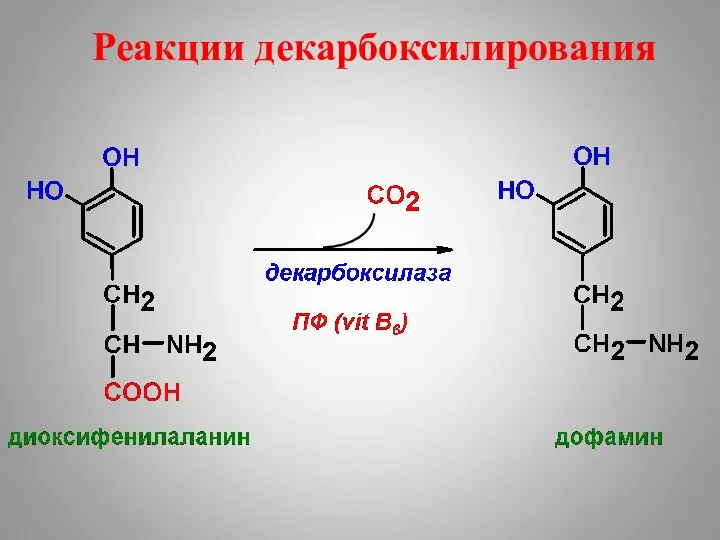
- 40. Реакции декарбоксилирования
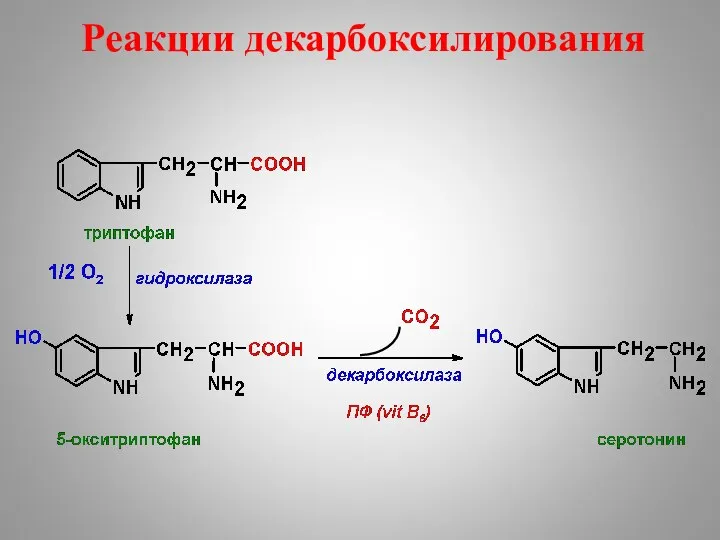
- 41. Реакции декарбоксилирования
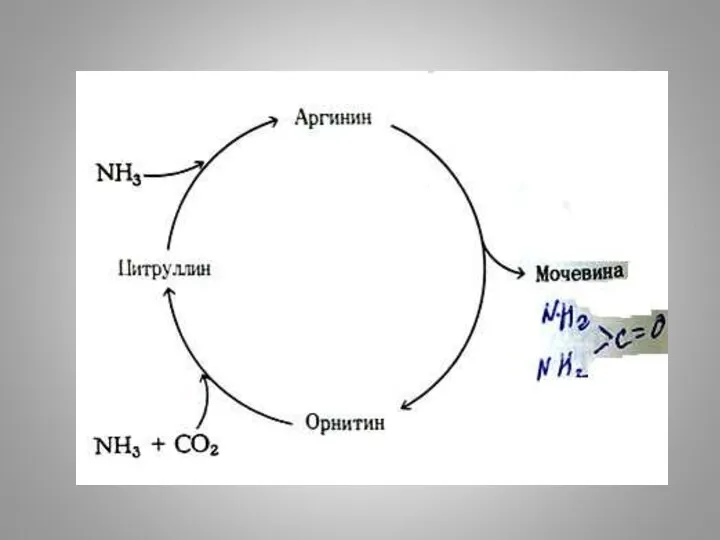
- 42. Выведение аммиака
- 43. Пути выведения аммиака в зависимости от систематического положения и экологических условий обитания организмов
- 48. Скачать презентацию




















 Презентация "Математика и искусство" - скачать презентации по МХК
Презентация "Математика и искусство" - скачать презентации по МХК Стартер
Стартер Введение в WCF. WCF-службы. Windows Communication Foundation
Введение в WCF. WCF-службы. Windows Communication Foundation Тензоры диэлектрической и магнитной проницаемости вещества
Тензоры диэлектрической и магнитной проницаемости вещества Динамические характеристики и точность информационных радио- и оптикоэлектронных систем и устройств
Динамические характеристики и точность информационных радио- и оптикоэлектронных систем и устройств История и место C++. Процесс построения программы
История и место C++. Процесс построения программы Презентация на тему "Болезни органов дыхания 1" - скачать презентации по Медицине
Презентация на тему "Болезни органов дыхания 1" - скачать презентации по Медицине Die innovative Lichttechnik des neuen BMW 7er
Die innovative Lichttechnik des neuen BMW 7er Презентация Сахар
Презентация Сахар Кутузовская медаль - презентация для начальной школы
Кутузовская медаль - презентация для начальной школы Смерч
Смерч  Разработка программ управления компьютером
Разработка программ управления компьютером Велимир Хлебников
Велимир Хлебников 围巾里的秘密
围巾里的秘密 С днем студента
С днем студента Символика Общероссийской общественной организации «Российский Союз Молодёжи»
Символика Общероссийской общественной организации «Российский Союз Молодёжи» День белорусской письменности. Викторина
День белорусской письменности. Викторина Маркетинг онлайн (тренды 2009) Евгений Шевченко Интернет-агентство UaMaster «THE MARKETING JAZZ FEST 2009»
Маркетинг онлайн (тренды 2009) Евгений Шевченко Интернет-агентство UaMaster «THE MARKETING JAZZ FEST 2009» Фотоэлектрические модули. (Лекция 5)
Фотоэлектрические модули. (Лекция 5)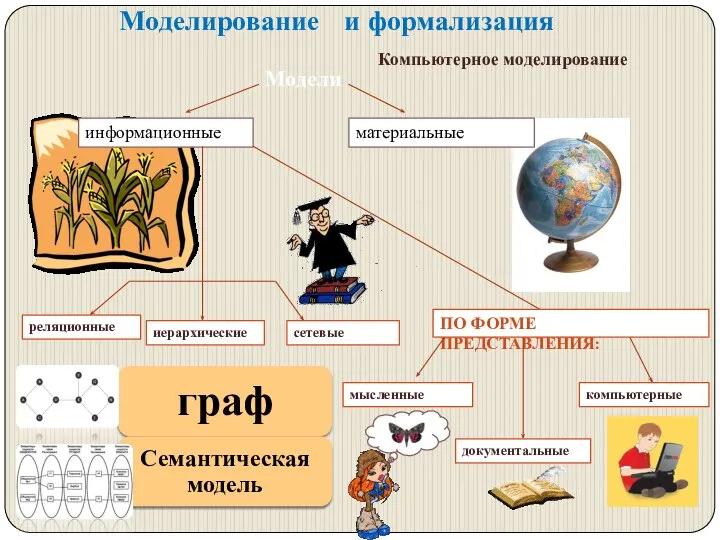 моделтрование - презентация по Алгебре
моделтрование - презентация по Алгебре Проектная работа на тему "Умный дом"
Проектная работа на тему "Умный дом" facts Основные тиристорные устройства
facts Основные тиристорные устройства весенние цветы - презентация для начальной школы
весенние цветы - презентация для начальной школы Свет и освещение
Свет и освещение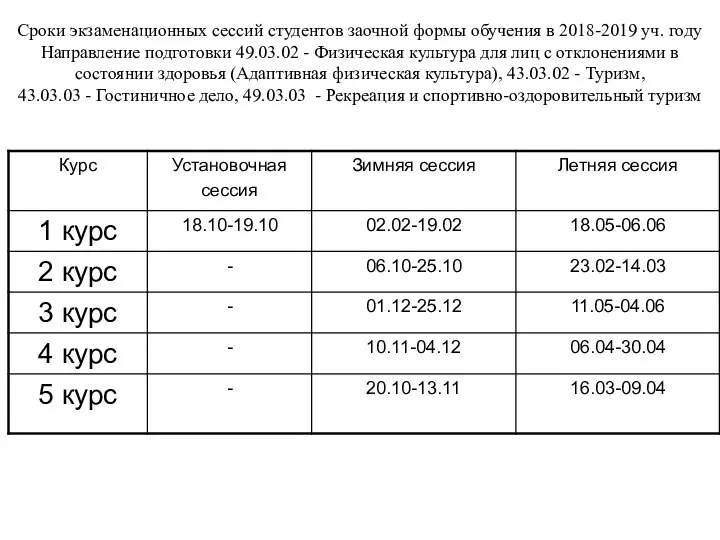 Сроки экзаменационных сессий студентов заочной формы обучения в 2018-2019 уч. году
Сроки экзаменационных сессий студентов заочной формы обучения в 2018-2019 уч. году Урок по математике 6 класс « Разложение на простые множители»
Урок по математике 6 класс « Разложение на простые множители»  Тема 1.1 Понятие и значение экономического анализа Выполнил: Тимофеев И.А.
Тема 1.1 Понятие и значение экономического анализа Выполнил: Тимофеев И.А. Кровная месть в современных обществах
Кровная месть в современных обществах