Содержание
- 2. План лекции Строение и функции печени Обмен веществ в печени Обмен веществ абсобтивный и постабсобтивний периоды
- 3. Печень – самый крупный орган в организме человека, состоит примерно из 300 млрд клеток, 80% из
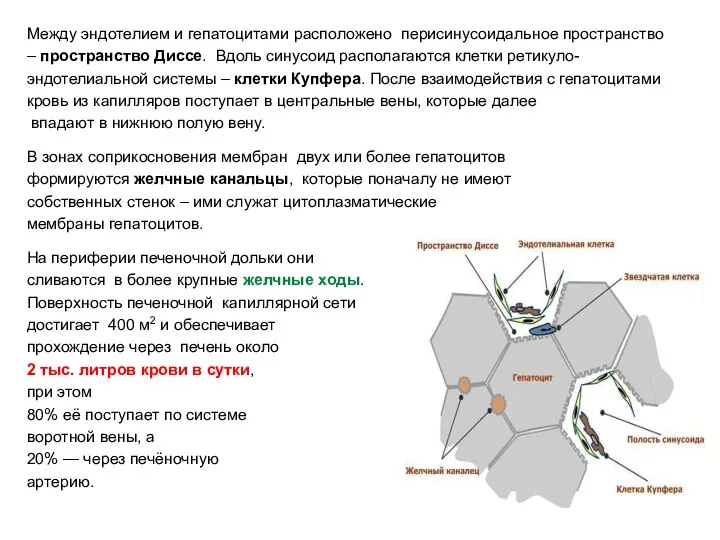
- 4. Между эндотелием и гепатоцитами расположено перисинусоидальное пространство – пространство Диссе. Вдоль синусоид располагаются клетки ретикуло- эндотелиальной
- 5. Печень перекрещивает метаболизм углеводов, липидов и белков Печень, являясь центральным органом метаболизма, участвует в поддержании метаболического
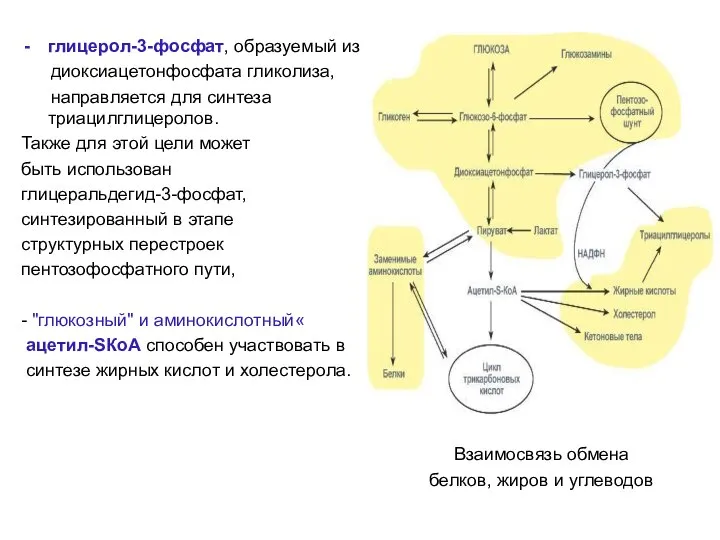
- 6. глицерол-3-фосфат, образуемый из диоксиацетонфосфата гликолиза, направляется для синтеза триацилглицеролов. Также для этой цели может быть использован
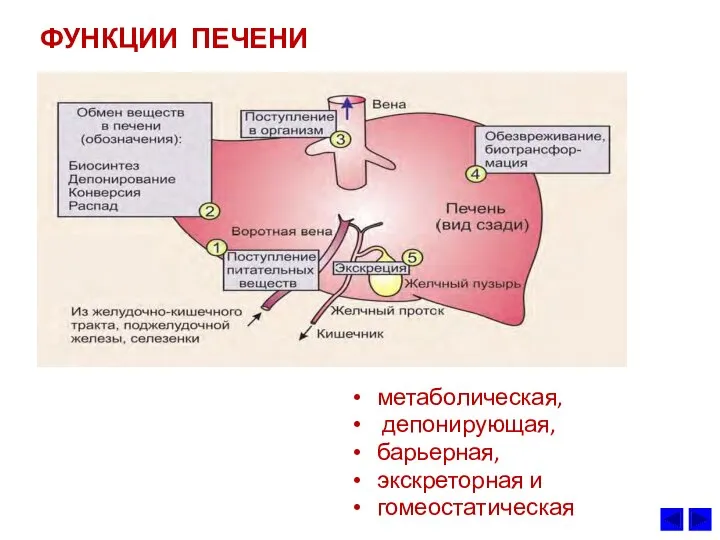
- 7. ФУНКЦИИ ПЕЧЕНИ метаболическая, депонирующая, барьерная, экскреторная и гомеостатическая
- 8. ФУНКЦИИ ПЕЧЕНИ Метаболическая. Продукты расщепления питательных веществ поступают в печень из пищеварительного тракта через воротную вену.
- 9. Обмен веществ в печени Печень принимает участие в метаболизме почти всех классов веществ
- 10. КОМПЕНСАТОРНЫЕ функции печени Ткани высших организмов нуждаются в постоянном притоке богатых энергией веществ и предшественников для
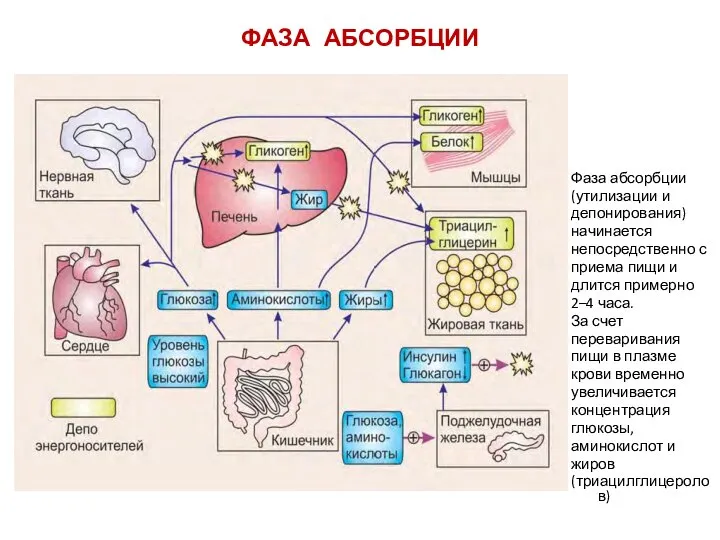
- 11. ФАЗА АБСОРБЦИИ Фаза абсорбции (утилизации и депонирования) начинается непосредственно с приема пищи и длится примерно 2–4
- 12. Поджелудочная железа отвечает на это изменением выброса гормонов: увеличением секреции инсулина и уменьшением секреции глюкагона. Увеличение
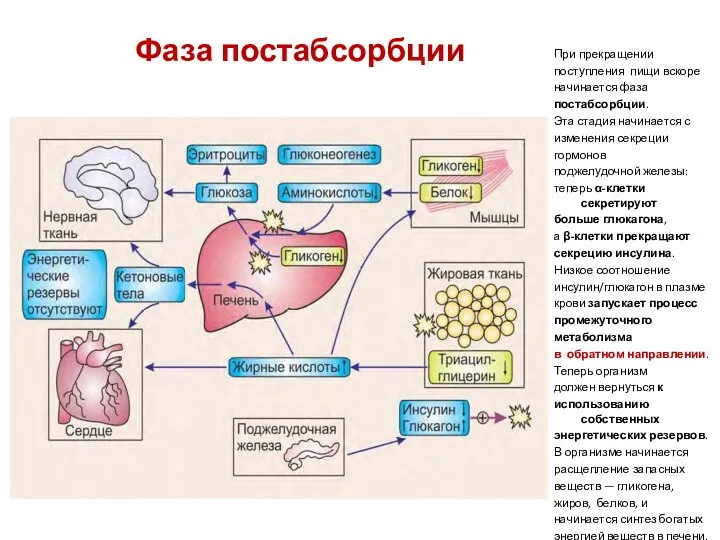
- 13. Фаза постабсорбции При прекращении поступления пищи вскоре начинается фаза постабсорбции. Эта стадия начинается с изменения секреции
- 14. В печени происходит мобилизация гликогена (гликогенолиз). Полученная глюкоза используется для обеспечения других тканей, прежде всего мозга,
- 15. Метаболизм углеводов Глюкоза наряду с жирными кислотами и кетоновыми телами является важнейшим источником энергии. Уровень глюкозы
- 16. Метаболизм липидов Если во время приема пищи в печень поступает избыток глюкозы, который не используется для
- 17. Белковый обмен Больше половины синтезируемого за сутки в организме белка приходится на печень. Скорость обновления всех
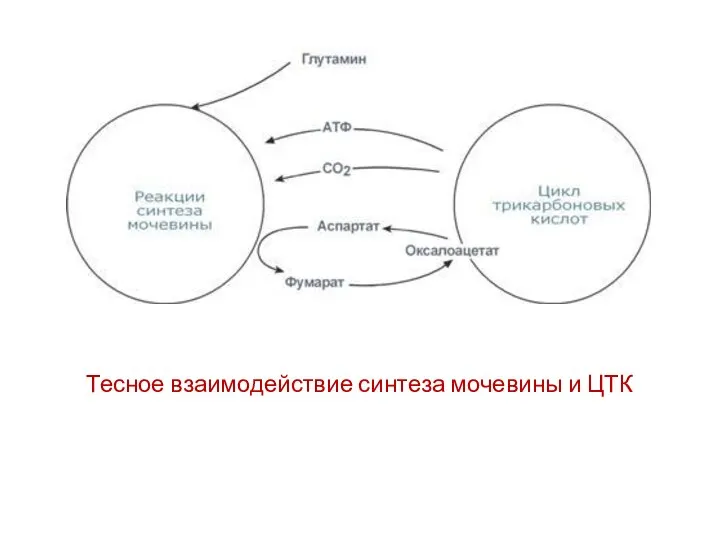
- 18. Тесное взаимодействие синтеза мочевины и ЦТК
- 19. Пигментный обмен Участие печени в пигментном обмене заключается в превращении гидрофобного билирубина в гидрофильную форму и
- 20. Оценка метаболической функции В клинической практике существуют приемы оценки той или иной функции: Участие в углеводном
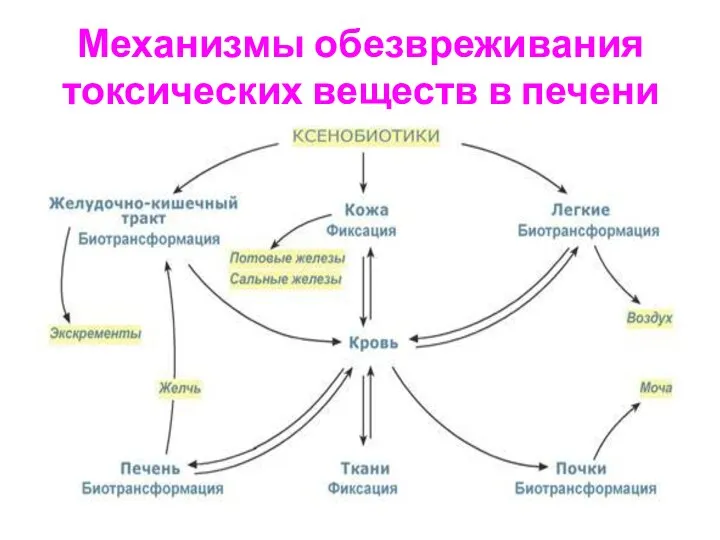
- 21. Механизмы обезвреживания токсических веществ в печени
- 22. Механизмы обезвреживания токсических веществ в печени
- 23. Инактивация чужеродных веществ в организме Чужеродные вещества, попадающие в организм из ЖКТ, через кожу и лёгкие
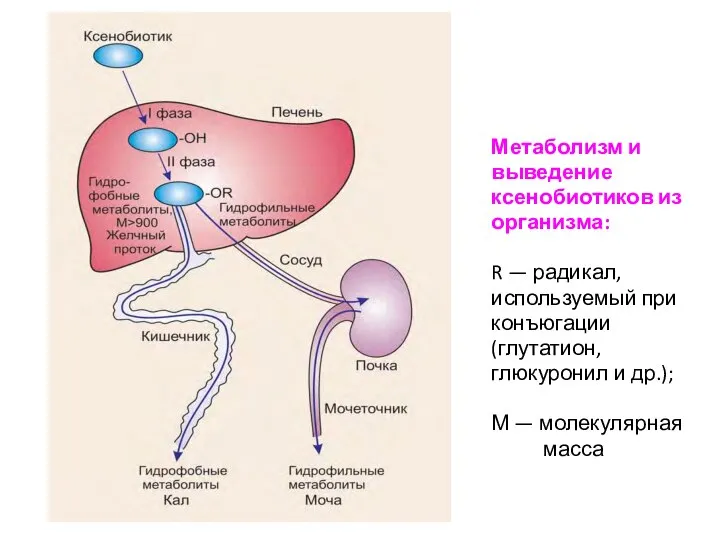
- 24. Метаболизм и выведение ксенобиотиков из организма: R — радикал, используемый при конъюгации (глутатион, глюкуронил и др.);
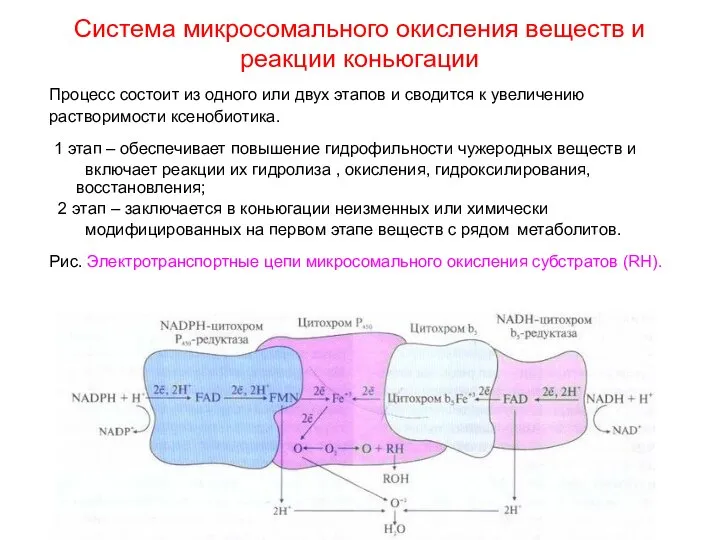
- 25. В мембранах эндоплазматического ретикулума (ЭР) практически всех тканей локализована система микросомального (монооксигеназного) окисления (МСО), отвечающая за
- 26. Система микросомального окисления веществ и реакции коньюгации Процесс состоит из одного или двух этапов и сводится
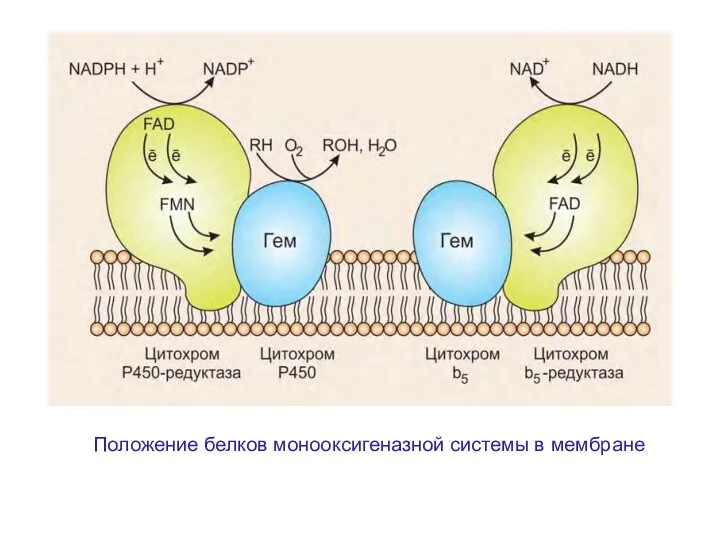
- 27. Положение белков монооксигеназной системы в мембране
- 28. В результате 1этапа - гидроксилирования возможны: повышение растворимости гидрофобного соединения, потеря молекулой ее биологической активности или
- 29. 2 этап инактивации – реакция коньюгации модифицированных на 1 этапе или содержащих полярные группы веществ. Они
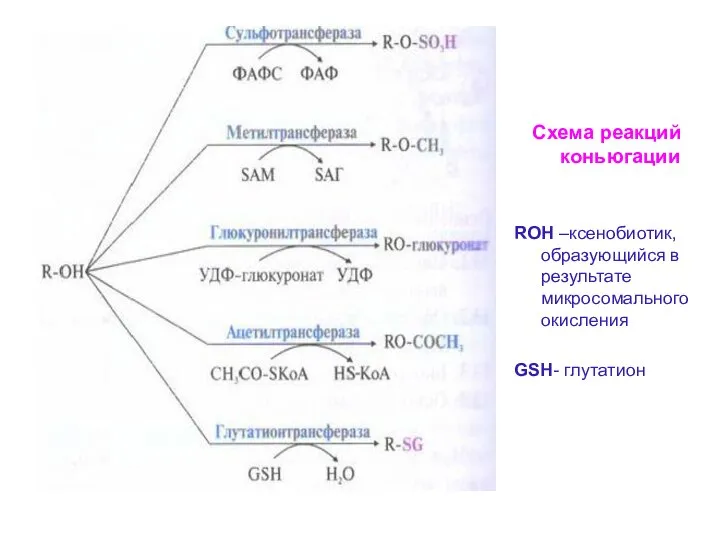
- 30. Схема реакций коньюгации RОН –ксенобиотик, образующийся в результате микросомального окисления GSН- глутатион
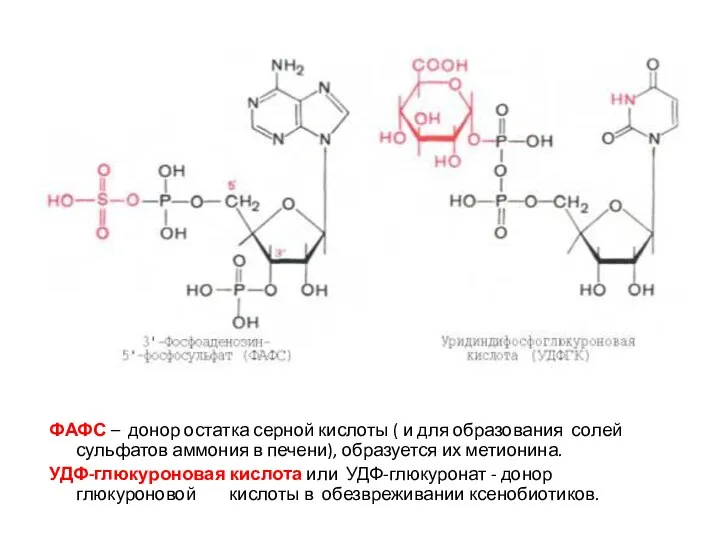
- 31. ФАФС – донор остатка серной кислоты ( и для образования солей сульфатов аммония в печени), образуется
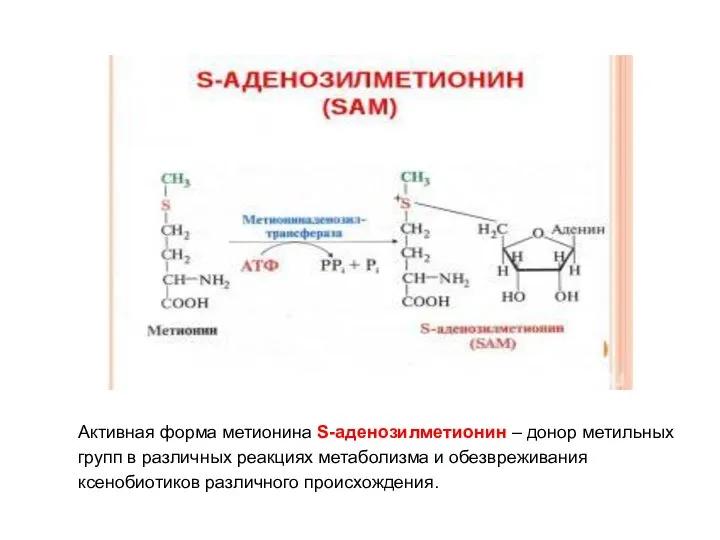
- 32. Активная форма метионина S-аденозилметионин – донор метильных групп в различных реакциях метаболизма и обезвреживания ксенобиотиков различного
- 33. Особое место среди ферментов, участвующих в обезвреживании ксенобиотиков, нормальных метаболитов и лекарств, занимают глутатионтрансферазы. Известно множество
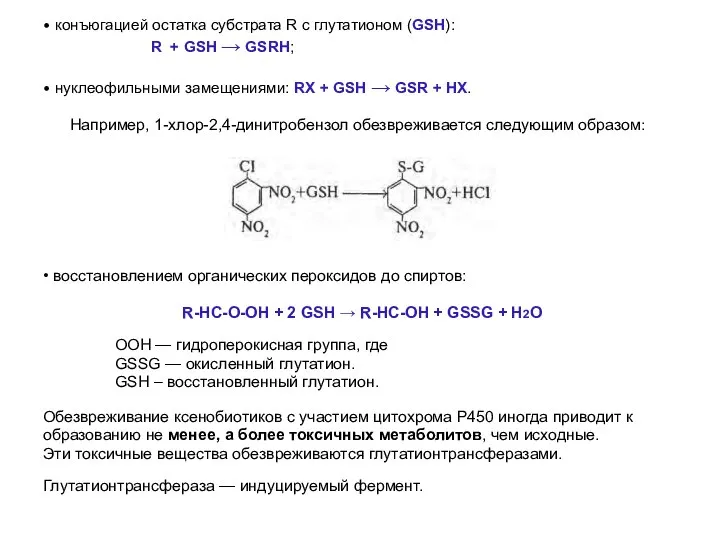
- 34. • конъюгацией остатка субстрата R с глутатионом (GSH): R + GSH → GSRH; • нуклеофильными замещениями:
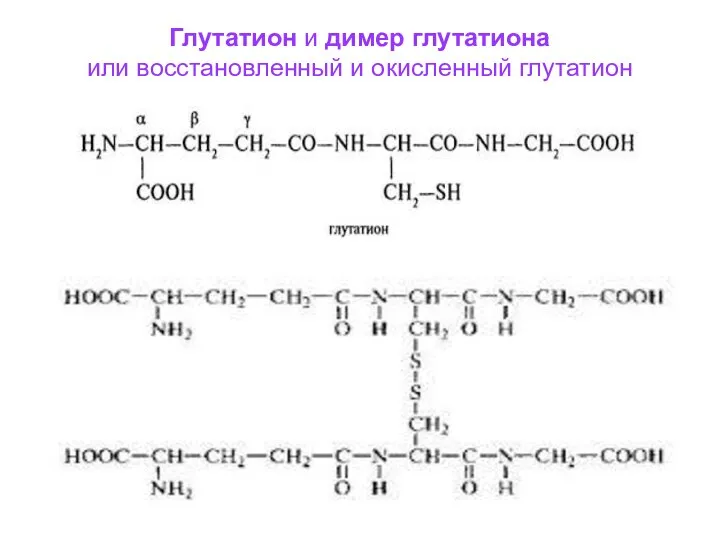
- 35. Глутатион и димер глутатиона или восстановленный и окисленный глутатион
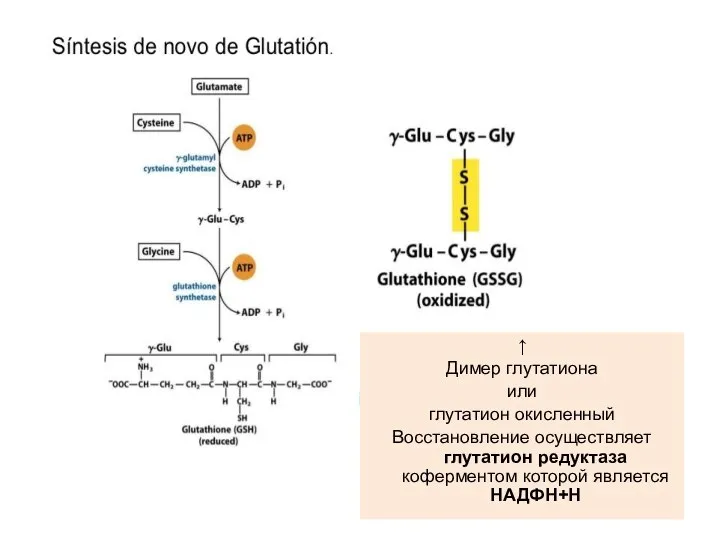
- 36. ↑ Димер глутатиона или глутатион окисленный Восстановление осуществляет глутатион редуктаза коферментом которой является НАДФН+Н
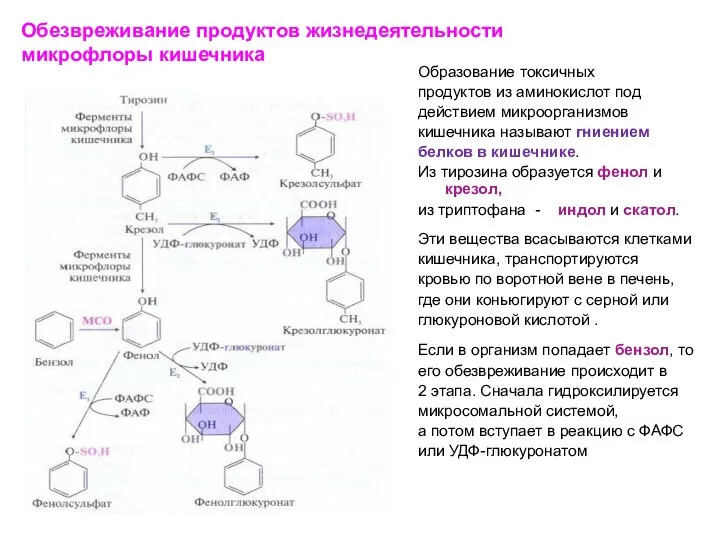
- 37. Обезвреживание продуктов жизнедеятельности микрофлоры кишечника Образование токсичных продуктов из аминокислот под действием микроорганизмов кишечника называют гниением
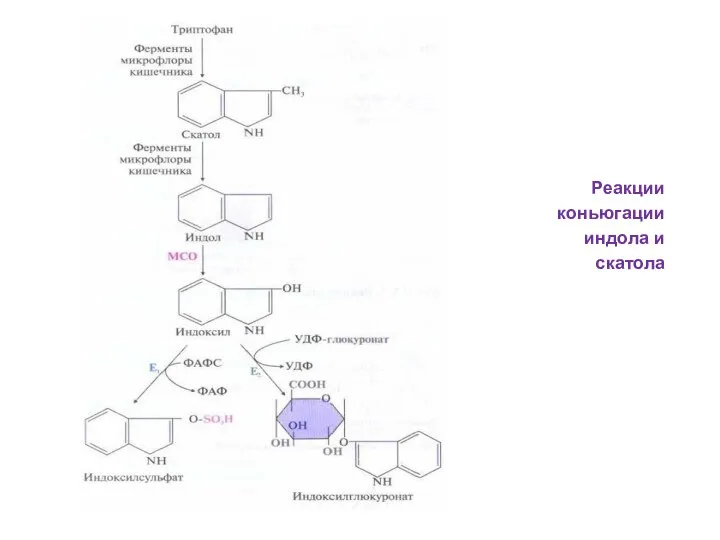
- 38. Реакции коньюгации индола и скатола
- 39. Биотрансформация лекарств печени Лекарства выводятся из организма в неизменном виде или подвергаются химической модификации. Последняя может
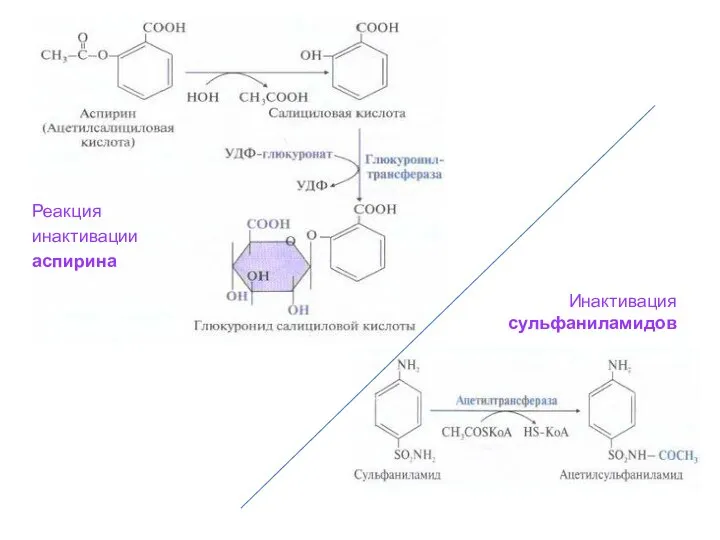
- 40. Реакция инактивации аспирина Инактивация сульфаниламидов
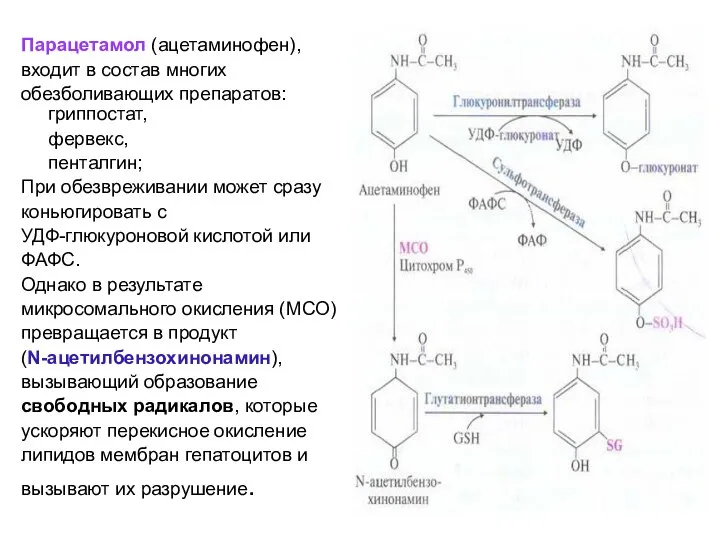
- 41. Парацетамол (ацетаминофен), входит в состав многих обезболивающих препаратов: гриппостат, фервекс, пенталгин, может сразу коньюгировать с УДФ-глюкуроновой
- 42. Парацетамол (ацетаминофен), входит в состав многих обезболивающих препаратов: гриппостат, фервекс, пенталгин; При обезвреживании может сразу коньюгировать
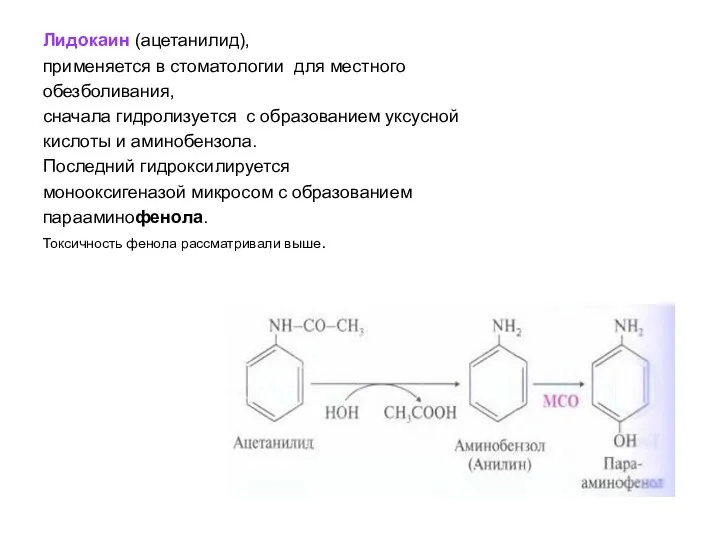
- 43. Лидокаин (ацетанилид), применяется в стоматологии для местного обезболивания, сначала гидролизуется с образованием уксусной кислоты и аминобензола.
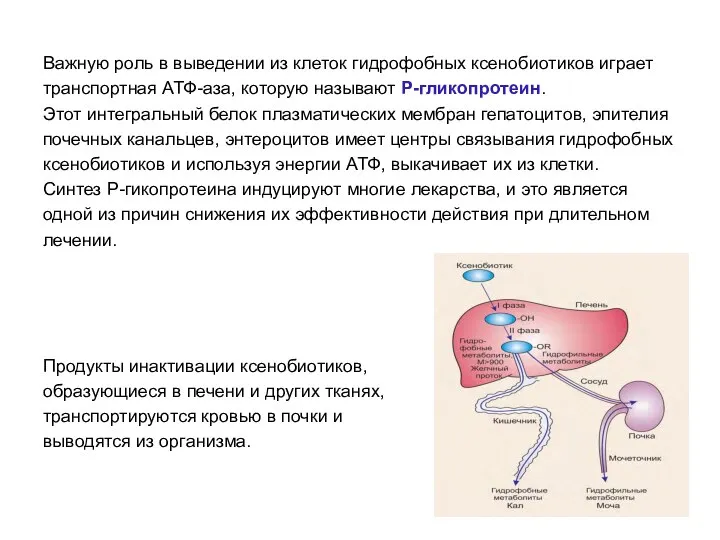
- 44. Важную роль в выведении из клеток гидрофобных ксенобиотиков играет транспортная АТФ-аза, которую называют Р-гликопротеин. Этот интегральный
- 45. Опять кровь
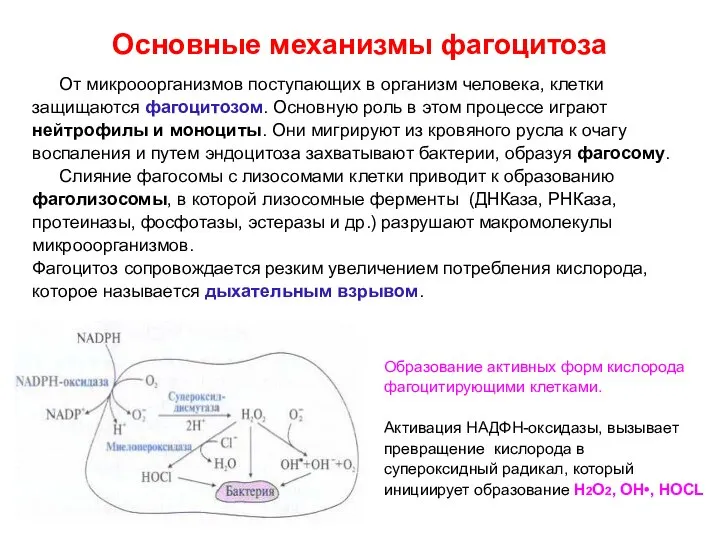
- 46. Основные механизмы фагоцитоза От микрооорганизмов поступающих в организм человека, клетки защищаются фагоцитозом. Основную роль в этом
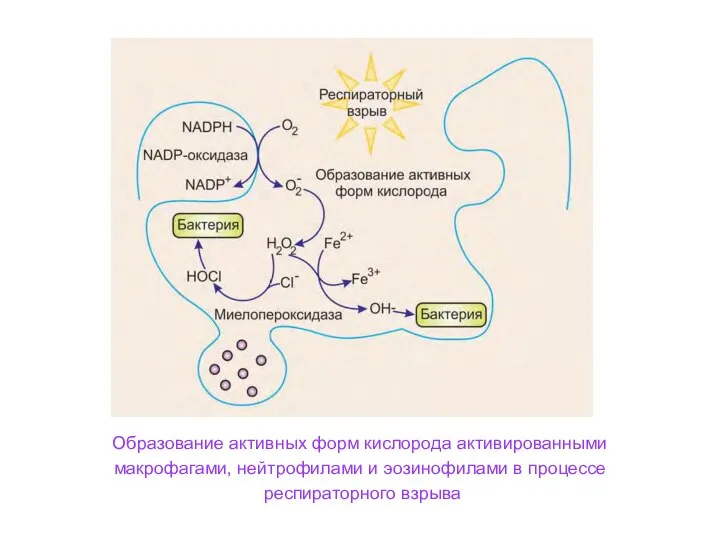
- 47. Образование активных форм кислорода активированными макрофагами, нейтрофилами и эозинофилами в процессе респираторного взрыва
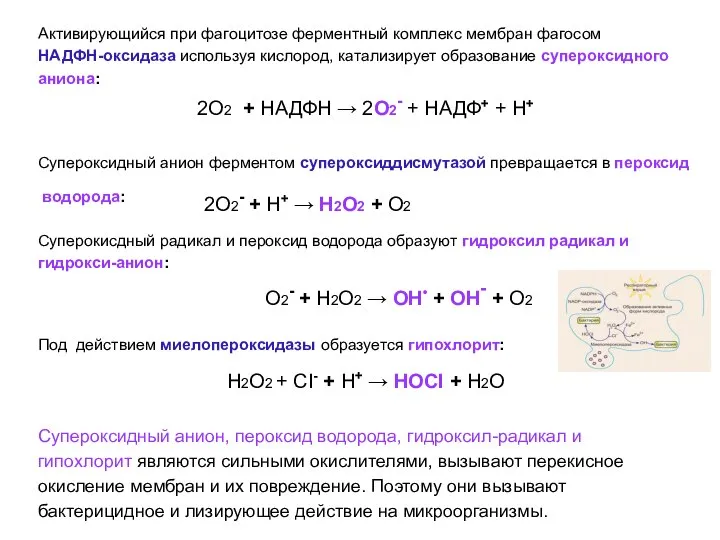
- 48. Активирующийся при фагоцитозе ферментный комплекс мембран фагосом НАДФН-оксидаза используя кислород, катализирует образование супероксидного аниона: 2О2 +
- 49. Благодарю за внимание
- 51. Скачать презентацию























 Бақытты сәм
Бақытты сәм Қазақтың ұлттық ойындары
Қазақтың ұлттық ойындары Презентация "Ненецкая кукла – нгухуко" - скачать презентации по МХК
Презентация "Ненецкая кукла – нгухуко" - скачать презентации по МХК Banya. A russian tradition
Banya. A russian tradition Основы применения языка SFC в CoDeSys. Реализация многозадачности
Основы применения языка SFC в CoDeSys. Реализация многозадачности Північна Корея
Північна Корея Форма государства. Форма правления. Монархия и республика
Форма государства. Форма правления. Монархия и республика Клеедощатые балки
Клеедощатые балки Функции финансового менеджмента в процессе осуществления ликвидационных процедур при банкротстве
Функции финансового менеджмента в процессе осуществления ликвидационных процедур при банкротстве Главное политическое событие декабря 1991 года - распад СССР
Главное политическое событие декабря 1991 года - распад СССР Технологический процесс изготовления детали «Соединительная втулка»
Технологический процесс изготовления детали «Соединительная втулка» Управление рисками
Управление рисками Государственное регулирование предпринимательской деятельности
Государственное регулирование предпринимательской деятельности Участие в разработке ИС. Создание WEB-сайта «Магазин канцелярских товаров»
Участие в разработке ИС. Создание WEB-сайта «Магазин канцелярских товаров» Футбольная команда «Рассвет»
Футбольная команда «Рассвет» Тоталітарна політична культура
Тоталітарна політична культура Кредит и кредитная система
Кредит и кредитная система Что проверяет инспектор в кадровых документах. Бесплатный онлайн-курс
Что проверяет инспектор в кадровых документах. Бесплатный онлайн-курс Технология строительного производства. Оборудование строительных площадок
Технология строительного производства. Оборудование строительных площадок История куклы Барби
История куклы Барби Антигены. Антитела. Реакции агглютинации и преципитации.
Антигены. Антитела. Реакции агглютинации и преципитации. Жители саванны - презентация для начальной школы_
Жители саванны - презентация для начальной школы_ Накшатры и брак
Накшатры и брак Творческий проект Тема: «ЛОГАРИФМЫ В АСТРОНОМИИ»
Творческий проект Тема: «ЛОГАРИФМЫ В АСТРОНОМИИ»  История изобретения турбин
История изобретения турбин Презентация по предмету: «Региональная экономика и управление» на тему: «Основные угрозы экономической безопасности.» 2011
Презентация по предмету: «Региональная экономика и управление» на тему: «Основные угрозы экономической безопасности.» 2011 Klikounova Publisher представляет
Klikounova Publisher представляет ИГРОВЫЕ ТЕХНОЛОГИИ В ОБУЧЕНИИ иностранному языку
ИГРОВЫЕ ТЕХНОЛОГИИ В ОБУЧЕНИИ иностранному языку