Содержание
- 2. План лекции Понятие о ферментах. Сущность явлений ферментативного катализа Структурная организация ферментов Механизм действия ферментов Специфичность
- 4. Практически все реакции в живом организме протекают с участием природных биокатализаторов, называемых ферментами, или энзимами. Слово
- 5. Известно, что для осуществления химической реакции необходимо, чтобы реагирующие вещества имели суммарную энергию выше чем величина
- 6. Сущность действия ферментов, так же как неорганических катализаторов заключается: в активации молекул реагирующих веществ, в разбиении
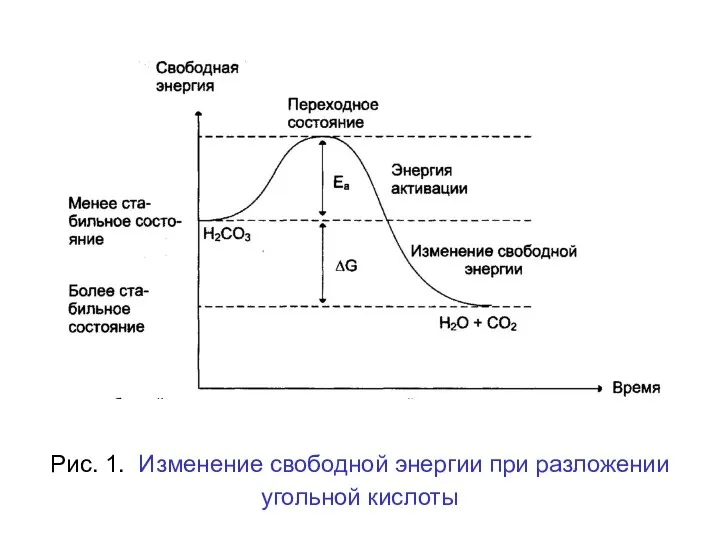
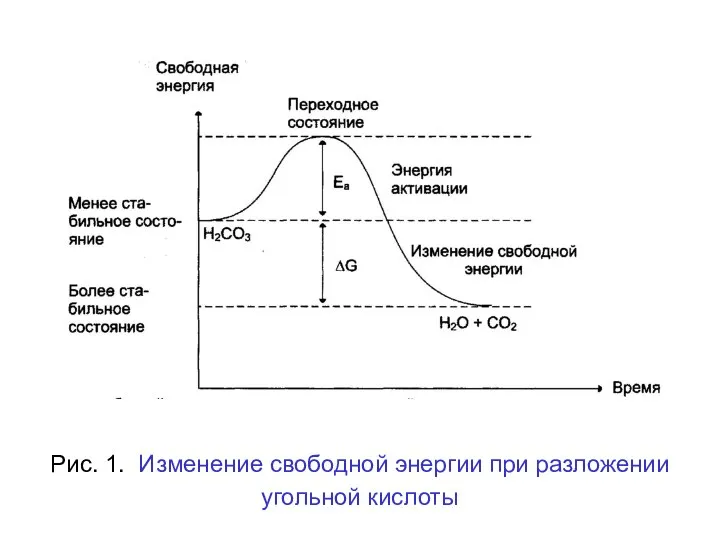
- 8. Рассмотрим реакцию разложения угольной кислоты (не ферментативной реакцией): Н2СО3 → Н2О + СО2 Угольная кислота слабая;
- 9. Рис. 1. Изменение свободной энергии при разложении угольной кислоты
- 10. При достижении этого энергетического барьера в молекуле происходят изменения, вызывающие перераспределение химических связей и образование новых
- 11. 1) катализируют только энергетически возможные реакции, т. е. те реакции, которые могут протекать и без них;
- 12. 1) Скорость ферментативных реакций намного выше; 2) Высокая специфичность; 3) Мягкие условия работы (внутриклеточные); 4) Возможность
- 13. Этапы ферментативного катализа В ферментативной реакции можно выделить следующие этапы: Присоединение субстрата (S) к ферменту (E)
- 14. Механизмы ферментативного катализа Кислотно-основной катализ – в активном центре фермента находятся группы специфичных аминокислотных остатков (радикалов
- 15. 2. Ковалентный катализ – ферменты реагируют со своими субстратами, образуя при помощи ковалентных связей очень нестабильные
- 16. Строение ферментов
- 17. Общая характеристика Ферменты имеют белковую природу и обладают всеми свойствами, характерными для белков: При гидролизе ферменты
- 18. Простые ферменты состоят только из аминокислот – например, пепсин, трипсин, лизоцим. Сложные ферменты (холоферменты) имеют в
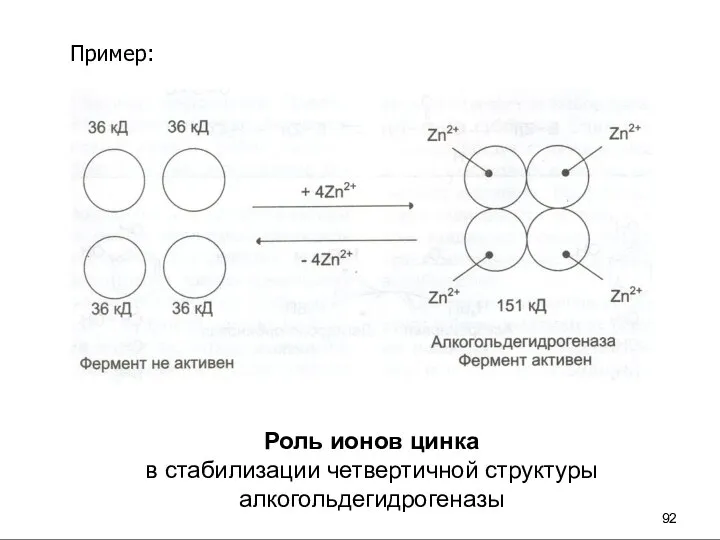
- 19. Схема формирования сложного фермента Кофактор + апофермент = холофермент holo – весь, целый
- 20. У сложных ферментов в активном центре обязательно расположены функциональные группы кофактора. Кофактор участвует в связывании субстрата
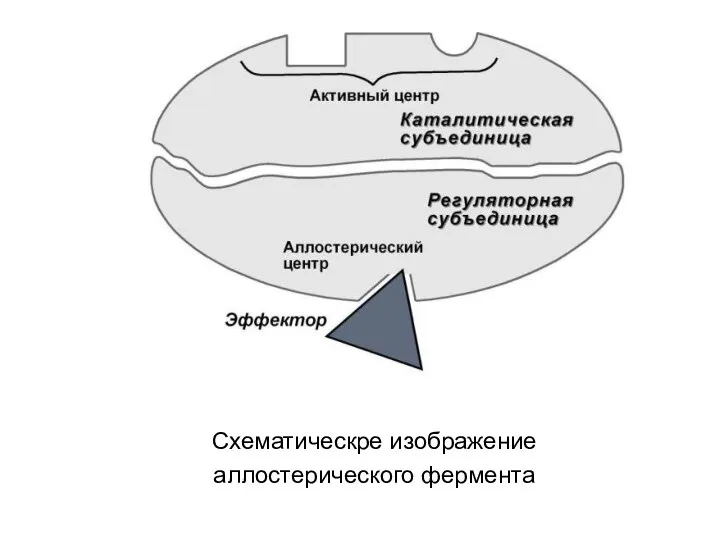
- 21. 2. Аллостерический центр (allos – чужой) – центр регуляции активности фермента, который пространственно отделен от активного
- 22. Схематическре изображение аллостерического фермента
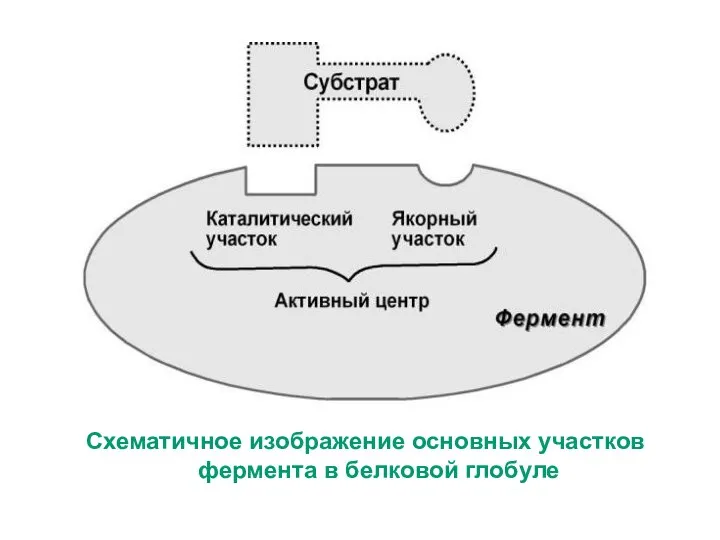
- 23. Структурно-функциональная организация ферментов или как ферменты работают. В составе фермента выделяют области, выполняющие различную функцию: Активный
- 24. Биологическая функция фермента, как и любого белка обусловлена наличием в его структуре активного центра. Лиганд, взаимодействующий
- 25. Схематичное изображение основных участков фермента в белковой глобуле
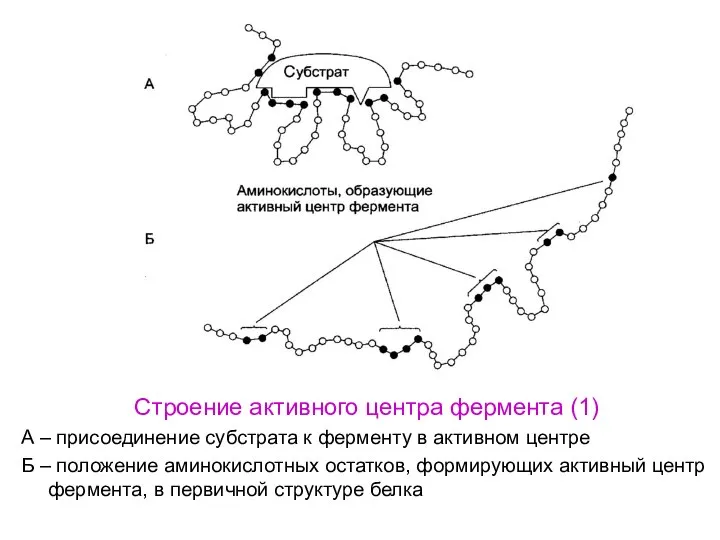
- 26. Строение активного центра фермента (1) А – присоединение субстрата к ферменту в активном центре Б –
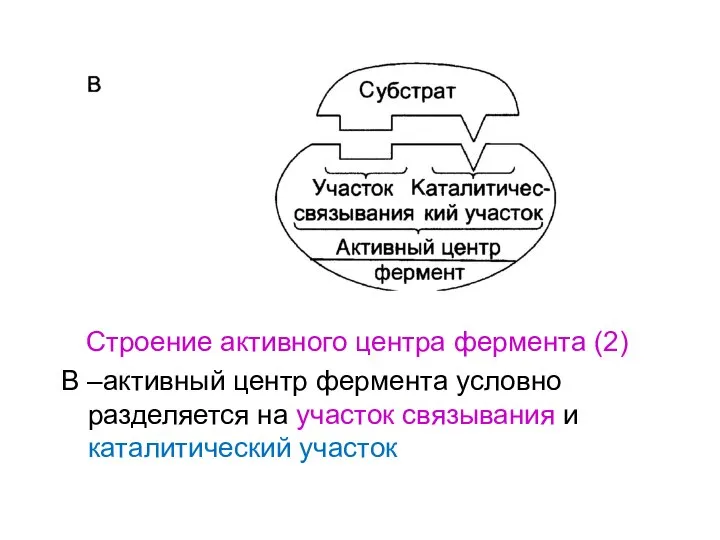
- 27. Строение активного центра фермента (2) В –активный центр фермента условно разделяется на участок связывания и каталитический
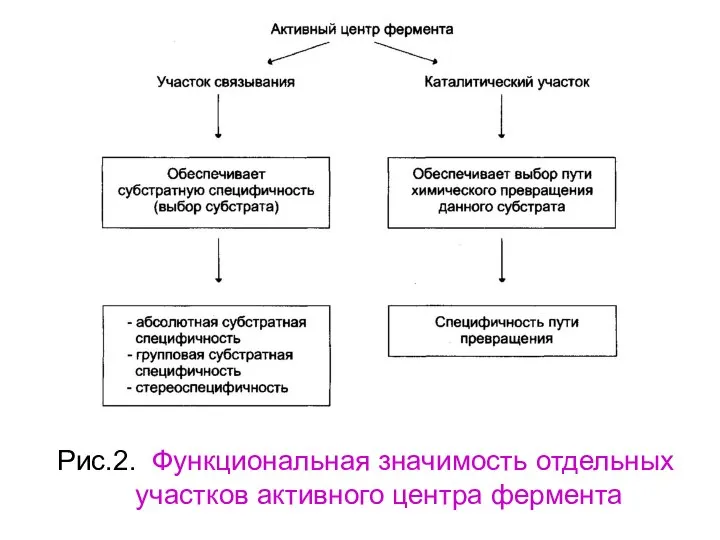
- 28. Рис.2. Функциональная значимость отдельных участков активного центра фермента
- 29. Что означает выражение «активность фермента»? При сравнении в характеристике ферментов и их изоформ есть понятия: активный
- 30. Активность фермента подразумевает результат реакции, а именно убыль субстрата или накопление продукта. Естественно при этом нельзя
- 31. 1. Активность фермента выражается в скорости накопления продукта или скорости убыли субстрата в пересчете на количество
- 32. Таким образом, активность фермента может выражаться, например, в ммоль / с × л, г / час
- 33. 2. Создание стандартных условий, чтобы можно было сравнивать результаты, полученные в разных лабораториях - оптимальная рН,
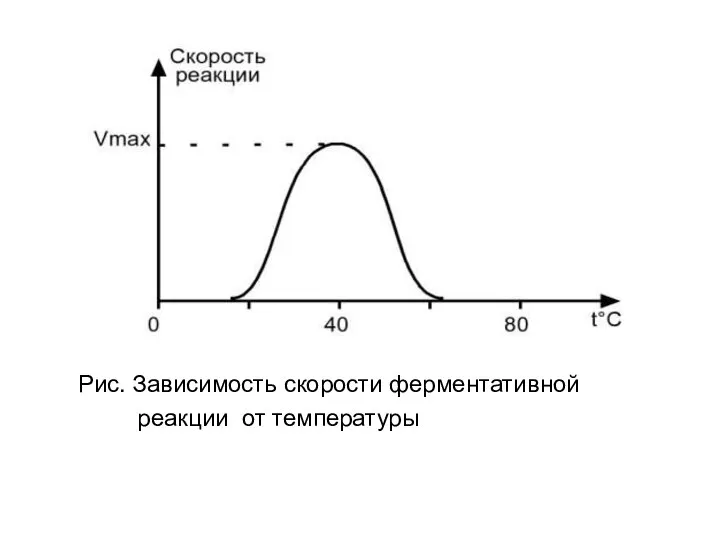
- 34. От чего зависит активность ферментов? Свойства ферментов Активность ферментов зависит от: - температуры, - рН, -
- 35. Рис. Зависимость скорости ферментативной реакции от температуры
- 36. Рис. Зависимость скорости реакции от рН
- 37. Зависимость скорости реакции от концентрации субстрата Зависимость скорости реакции от концентрации фермента
- 38. Ферменты избирательны в своём действии
- 39. Ферменты избирательны в своём действии Специфичность, т.е. высокая избирательность действия ферментов, основана на комплементарности структуры субстрата
- 40. 1 Стереоспецифичность При наличии у субстрата нескольких стереоизомеров фермент проявляет абсолютную специфичность к одному из них.
- 41. пример: Стереоспецифичность к цис-транс-изомерам Фермент фумараза оказывает действие только на фумарат. Малеинат (цис-изомер фумарата) не является
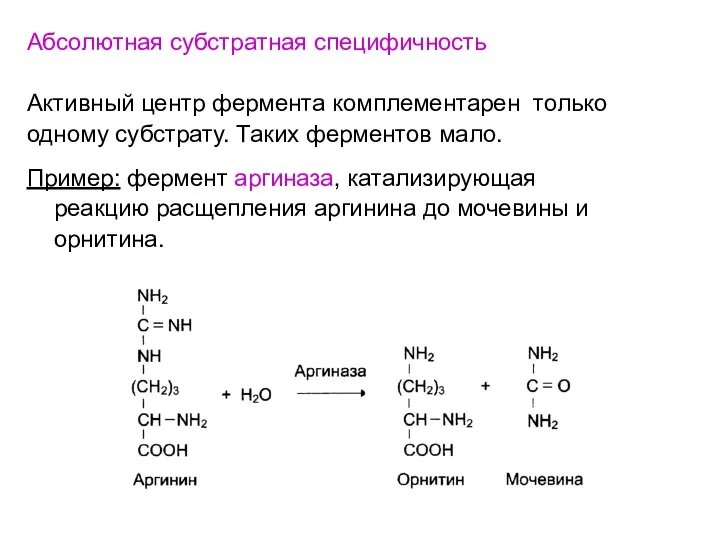
- 42. Абсолютная субстратная специфичность Активный центр фермента комплементарен только одному субстрату. Таких ферментов мало. Пример: фермент аргиназа,
- 43. Другой пример фермента с абсолютной субстратной специфичностью уреаза, катализирующая гидролиз мочевины до диоксида углерода и аммиака
- 44. Групповая субстратная специфичность Большинство ферментов катализируют однотипные реакции с небольшим количеством (группой) структурно похожих субстратов. Примеры:
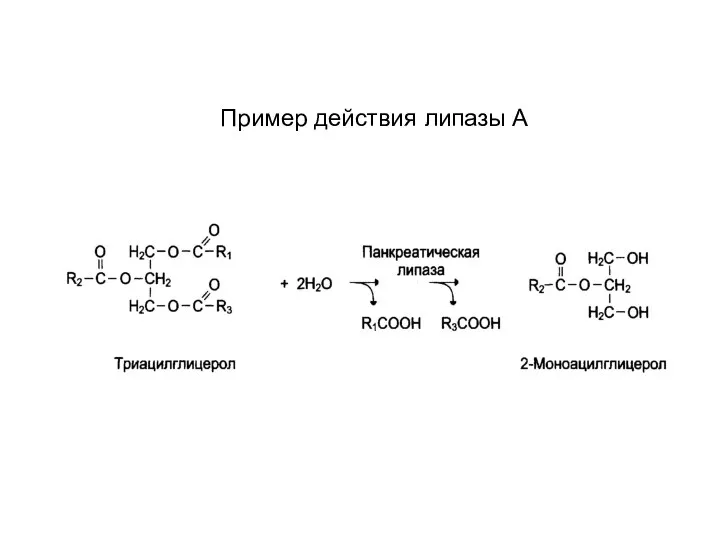
- 45. Пример действия липазы А
- 46. Относительная специфичность – превращение субстратов с некоторыми общими признаками. Например, цитохром Р450 окисляет только гидрофобные вещества,
- 47. МЕХАНИЗМЫ СПЕЦИФИЧНОСТИ В общем виде все сводится к комплементарному взаимодействию фермента и субстрата. При этом функциональные
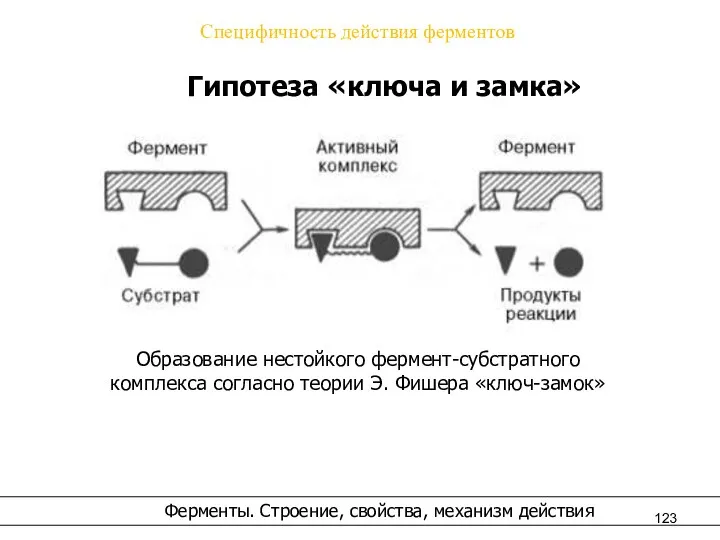
- 48. Гипотеза Фишера (модель "жесткой матрицы", "ключ-замок") – активный центр фермента строго соответствует конфигурации субстрата и не
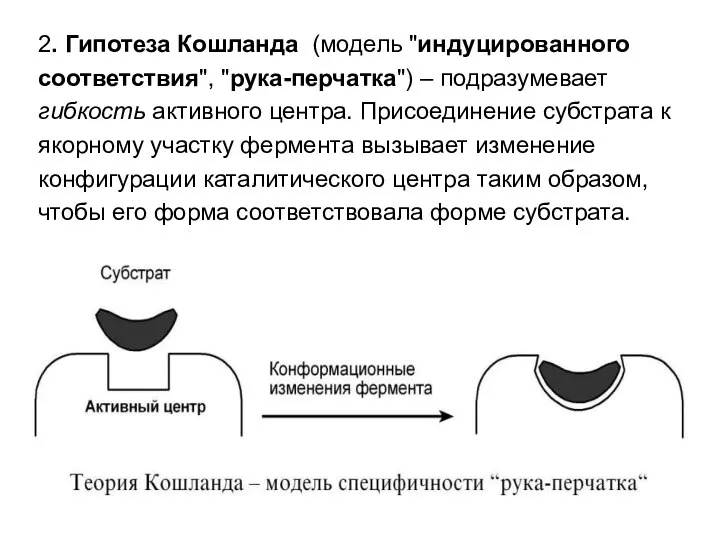
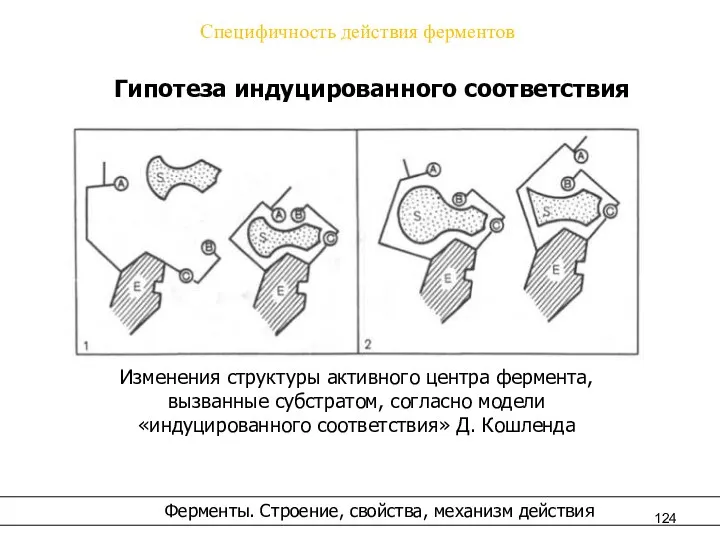
- 49. 2. Гипотеза Кошланда (модель "индуцированного соответствия", "рука-перчатка") – подразумевает гибкость активного центра. Присоединение субстрата к якорному
- 50. РЕГУЛЯЦИЯ АКТИВНОСТИ ФЕРМЕНТОВ IN VIVO Активность ферментов в клетке непостоянна во времени. Она чутко реагирует на
- 51. 1. Компартментализация, 2. Доступность субстрата или кофермента, 3. Изменение количества фермента, 4. Ограниченный частичный протеолиз проферментов,
- 52. Компартментализация. Компартментализация – это сосредоточение ферментов и их субстратов в одном компартменте (одной органелле) – в
- 53. 2. Доступность субстрата или кофермента. Здесь работает закон действия масс – фундаментальный закон химической кинетики: при
- 55. 3. Изменение количества фермента. Изменение количества фермента может происходить в результате увеличения или снижения его синтеза.
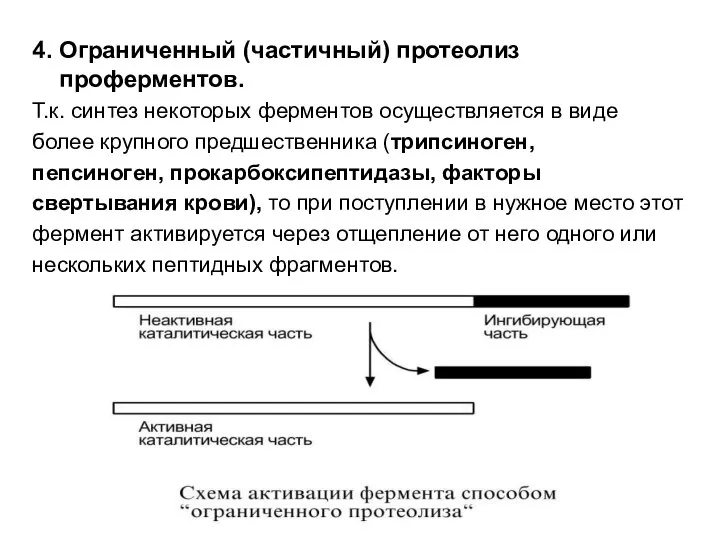
- 56. 4. Ограниченный (частичный) протеолиз проферментов. Т.к. синтез некоторых ферментов осуществляется в виде более крупного предшественника (трипсиноген,
- 57. 5. Аллостерическая регуляция. Аллостерические ферменты построены из двух и более субъединиц: одни субъединицы содержат каталитический центр,
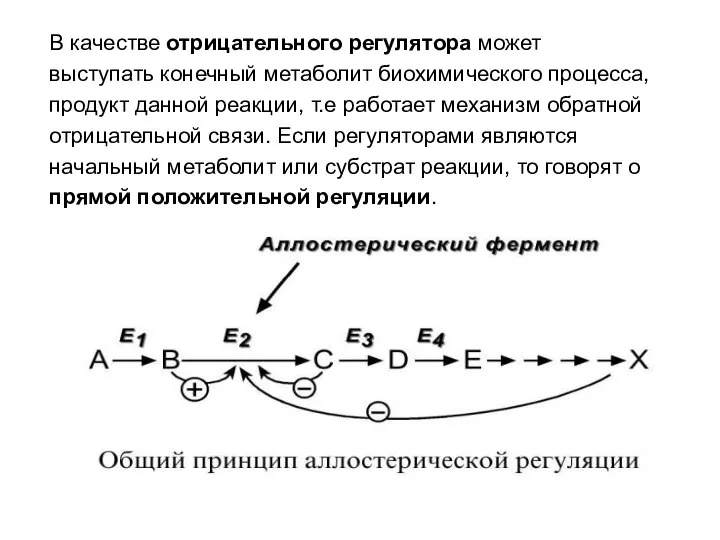
- 58. В качестве отрицательного регулятора может выступать конечный метаболит биохимического процесса, продукт данной реакции, т.е работает механизм
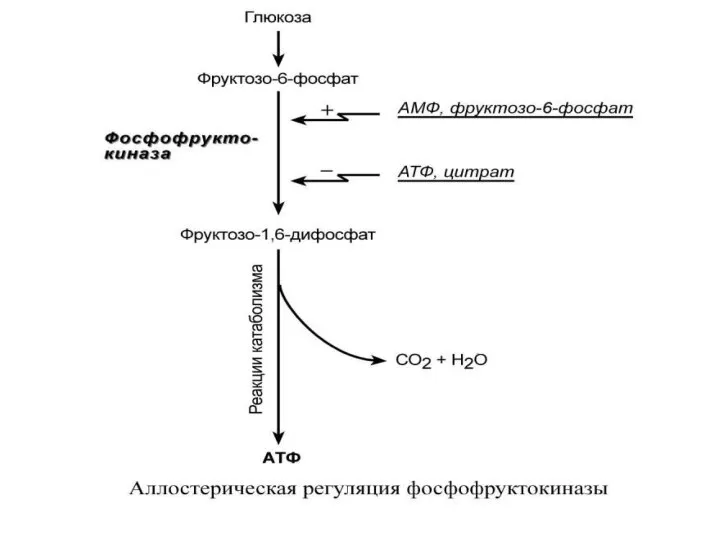
- 59. Например, фермент энергетического распада глюкозы, фосфофруктокиназа, регулируется промежуточными И конечными продуктами этого распада. При этом АТФ,
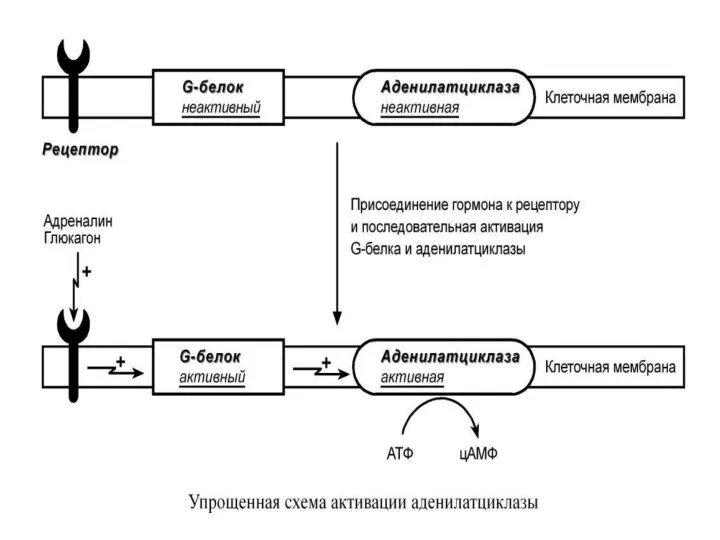
- 61. 6. Белок-белковое взаимодействие. Термин белок-белковое взаимодействие обозначает ситуацию, когда в качестве регулятора выступают не метаболиты биохимических
- 63. Другим примером белок-белкового взаимодействия может быть регуляция активности протеинкиназы А. Протеинкиназа А является тетрамерным ферментом, состоящим
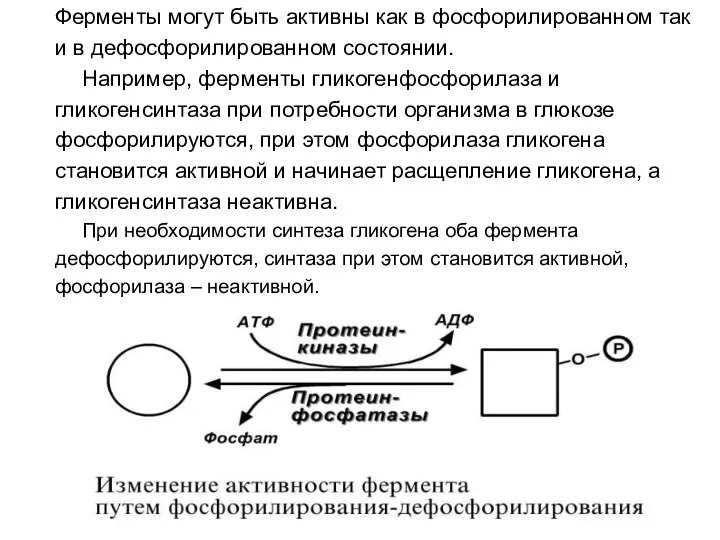
- 65. 7. Ковалентная (химическая) модификация. Ковалентная модификация заключается в обратимом присоединении или отщеплении определенной группы, благодаря чему
- 66. Ферменты могут быть активны как в фосфорилированном так и в дефосфорилированном состоянии. Например, ферменты гликогенфосфорилаза и
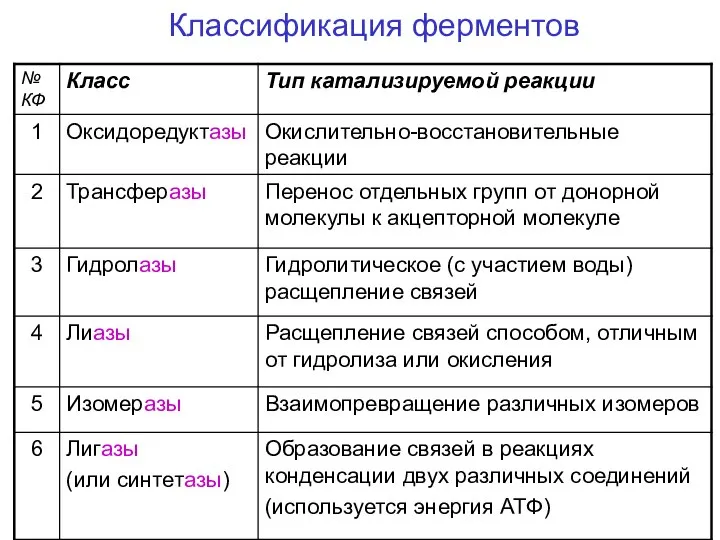
- 67. II классификация и номенклатура ферментов Каждый фермент имеет 2 названия. Первое короткое, так называемое рабочее. Второе
- 68. II классификация и номенклатура ферментов В 1961 г в Москве V Международный биохимический союз принял современную
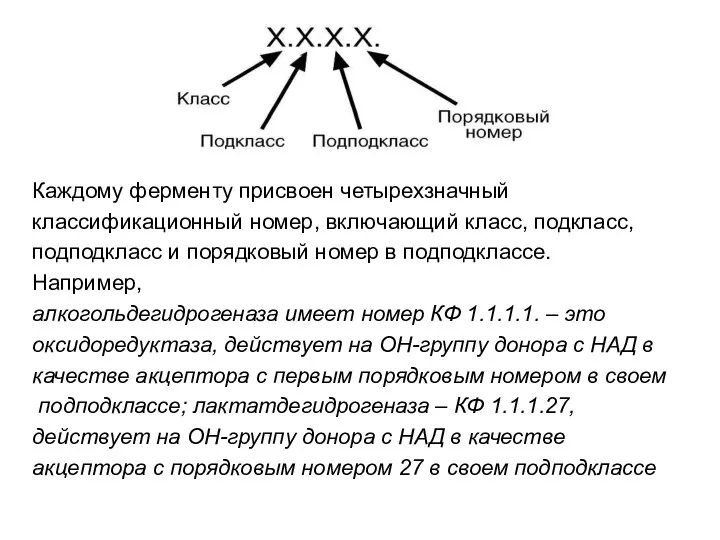
- 69. Каждому ферменту присвоен четырехзначный классификационный номер, включающий класс, подкласс, подподкласс и порядковый номер в подподклассе. Например,
- 70. Номенклатера ферментов Тривиальное название – название, сложившееся исторически. Например, пепсин, трипсин. Для некоторых ферментов к названию
- 71. Классификация ферментов
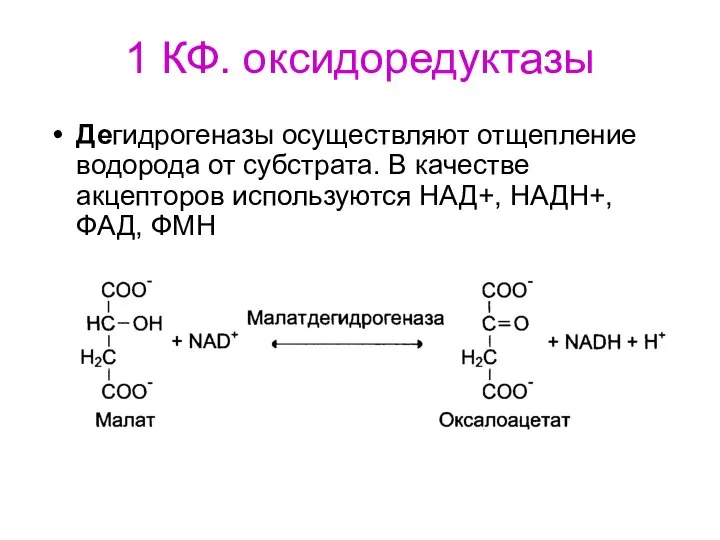
- 72. 1 КФ. оксидоредуктазы Дегидрогеназы осуществляют отщепление водорода от субстрата. В качестве акцепторов используются НАД+, НАДH+, ФАД,
- 73. 1 КФ. оксидоредуктазы Другой пример: У оксидоредуктаз, акцептором электрона(ов) служит молекулярный кислород.
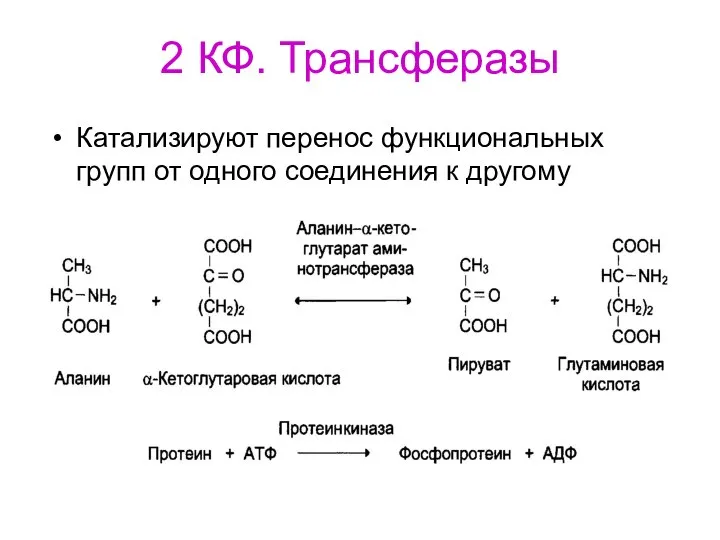
- 74. 2 КФ. Трансферазы Катализируют перенос функциональных групп от одного соединения к другому
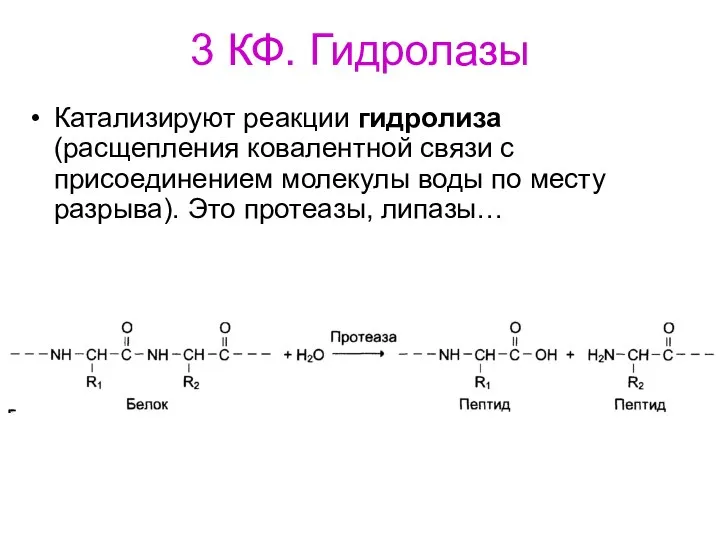
- 75. 3 КФ. Гидролазы Катализируют реакции гидролиза (расщепления ковалентной связи с присоединением молекулы воды по месту разрыва).
- 76. 4 КФ. Лиазы К лиазам относят ферменты, отщепляющие от субстрата негидролитическим путём определённую группу (при этом
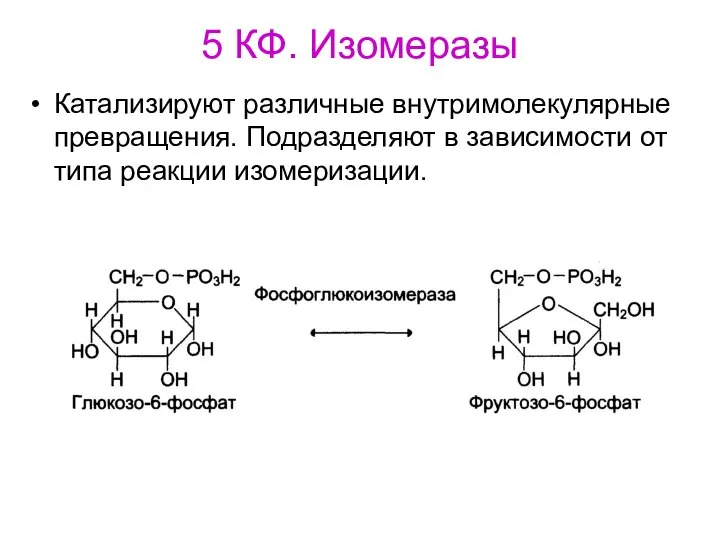
- 77. 5 КФ. Изомеразы Катализируют различные внутримолекулярные превращения. Подразделяют в зависимости от типа реакции изомеризации.
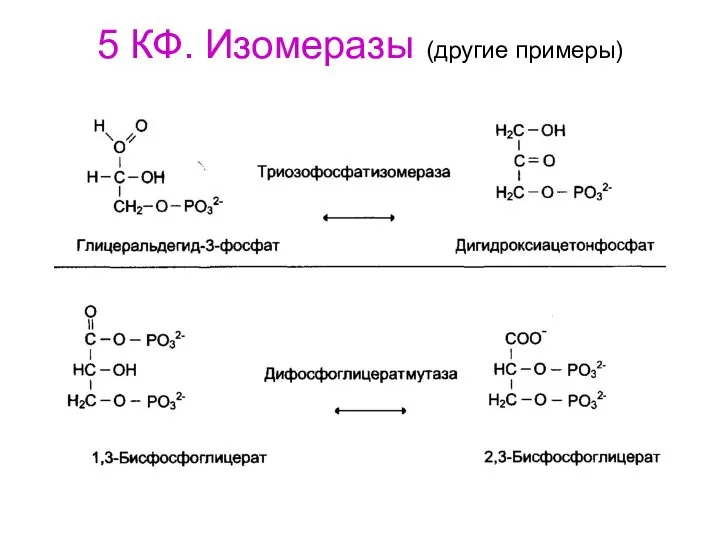
- 78. 5 КФ. Изомеразы (другие примеры)
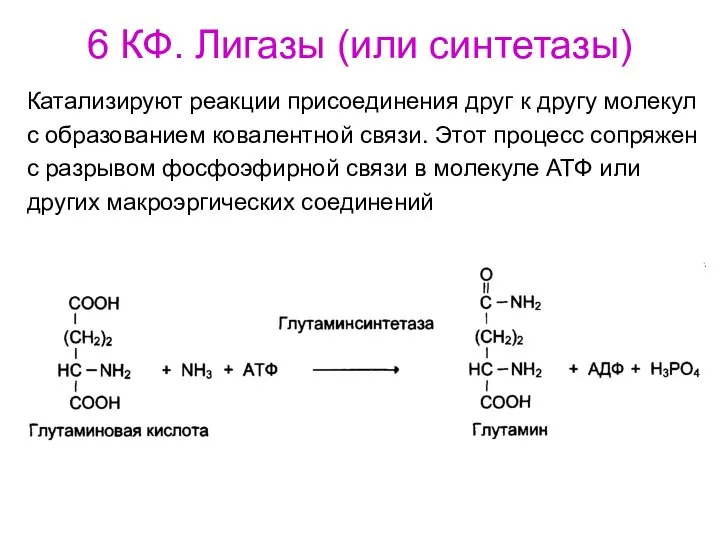
- 79. 6 КФ. Лигазы (или синтетазы) Катализируют реакции присоединения друг к другу молекул с образованием ковалентной связи.
- 82. III. Кофакторы и коферменты Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой
- 83. Большинство ферментов состоит из термолабильной белковой части и термостабильного небелкового фактора – кофермента. Белковую часть называют
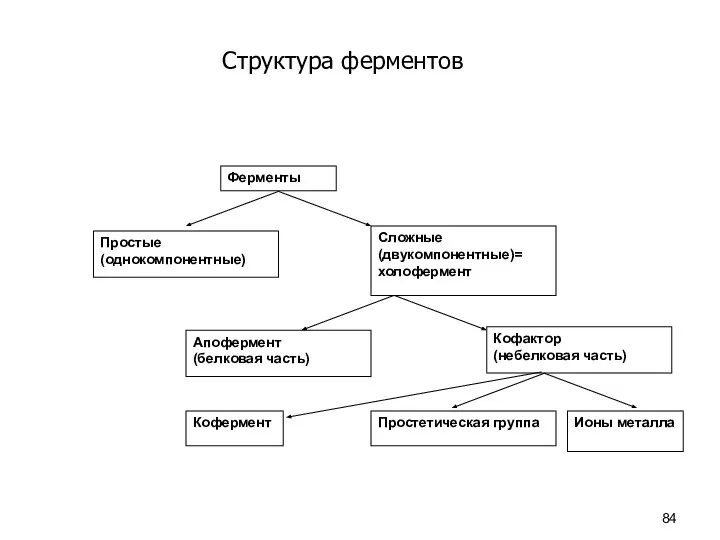
- 84. Структура ферментов Ферменты Простые (однокомпонентные) Сложные (двукомпонентные)= холофермент Апофермент (белковая часть) Кофактор (небелковая часть) Ионы металла
- 85. Структурная организация ферментов Структура ферментов Согласно одной из классификаций все коферменты делят на 2 группы: –
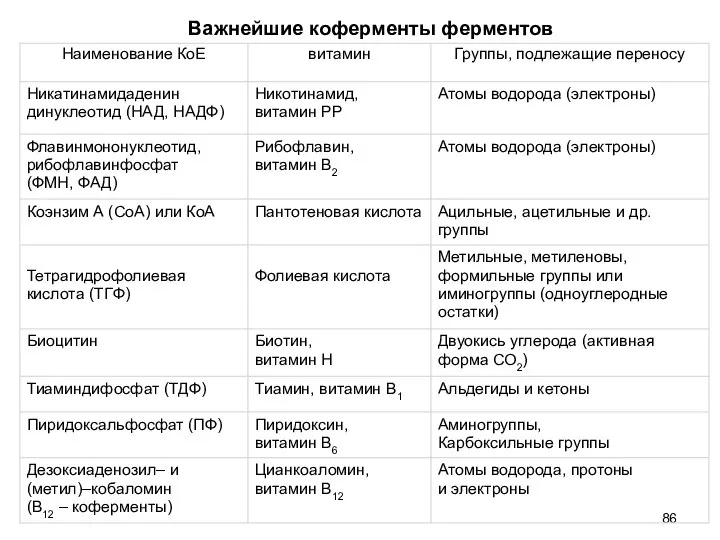
- 86. Важнейшие коферменты ферментов
- 87. Невитаминные кофакторы К невитаминным кофакторам относят следующие соединения: – НS-глутатион, – АТФ, – липоевая кислота, –
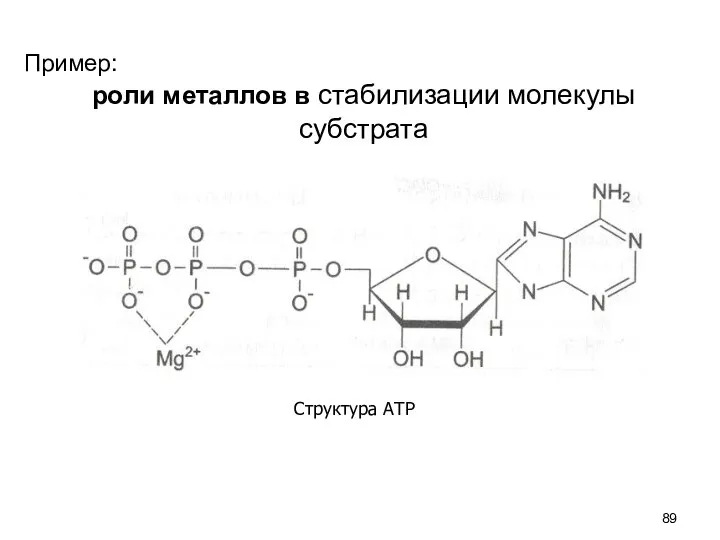
- 88. Роль металлов в функционировании ферментов 1. Ионы металла выполняют функцию стабилизаторов молекулы субстрата, активного центра фермента
- 89. Пример: роли металлов в стабилизации молекулы субстрата Структура АТР
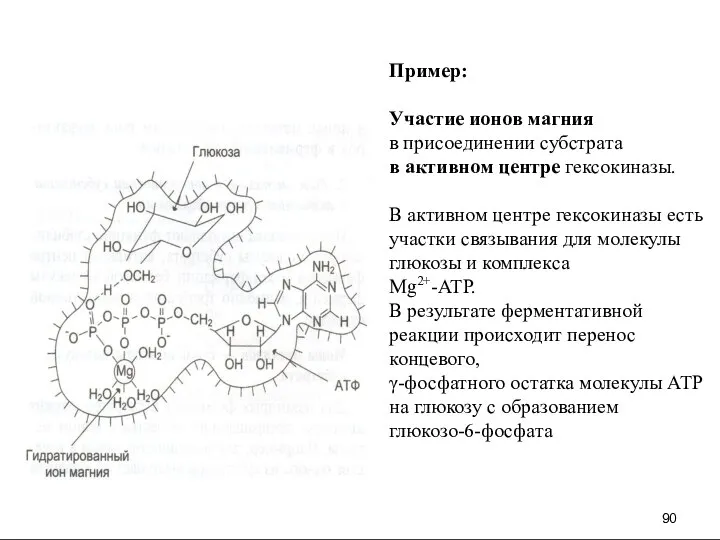
- 91. Пример:
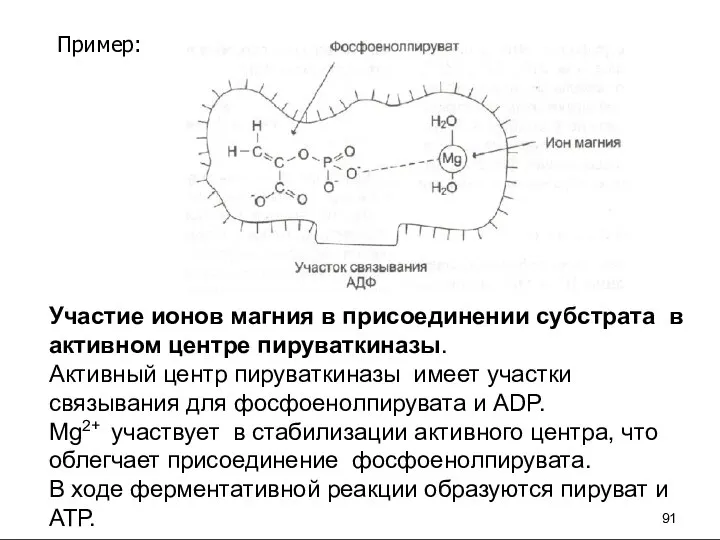
- 92. Пример:
- 93. Активные и аллостерические центры, их характеристика Аллостерический центр (или центры) (от греч. allos– другой, иной и
- 94. IV Механизм действия ферментов Механизм действия ферментов может быть рассмотрен с 2-х позиций: С точки зрения
- 95. А. Энергетические изменения при химических реакциях Любые химические реакции протекают подчиняясь двум основным законам термодинамики: Закону
- 96. Рассмотрим реакцию разложения угольной кислоты (не ферментативной реакцией): Н2СО3 → Н2О + СО2 Угольная кислота слабая;
- 97. Рис. 1. Изменение свободной энергии при разложении угольной кислоты
- 98. При достижении этого энергетического барьера в молекуле происходят изменения, вызывающие перераспределение химических связей и образование новых
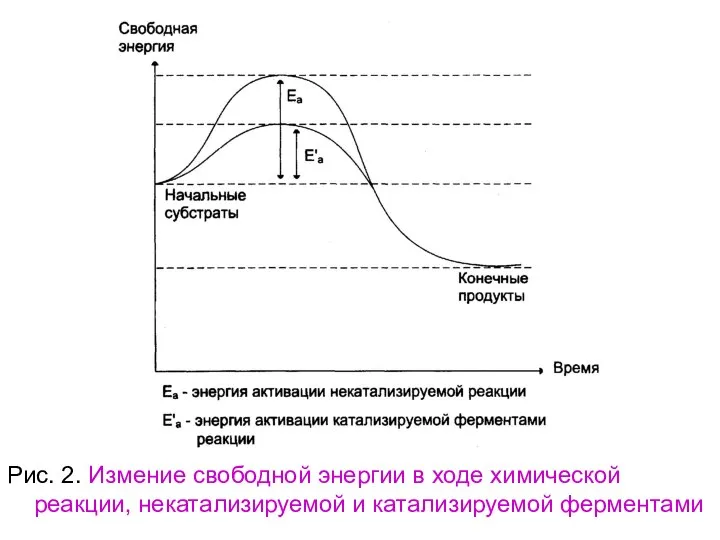
- 99. Чем больше молекул обладают энергией, превышающей уровень Еа, тем выше скорость химической реакции. Повысить скорость химической
- 100. Таким образом, ферменты снижают высоту энергетического барьера, в результате возрастает количество реакционно-способных молекул, следовательно, увеличивается скорость
- 101. Рис. 2. Измение свободной энергии в ходе химической реакции, некатализируемой и катализируемой ферментами
- 102. Таким образом, биологические катализаторы (ферменты) не изменяют свободную энергию субстратов и поэтому не меняют равновесие реакции
- 103. Фермент, выполняя функцию катализатора химической реакции, подчиняется общим законам катализа и обладает всеми свойствами, характерными для
- 104. Сходство ферментов с небиологическими катализаторами: фермент катализирует энергетически возможные реакции; энергия химической системы остается постоянной; в
- 105. Отличие ферментов от небиологических катализаторов: скорость ферментативных реакций выше, чем реакций катализируемых небелковыми катализаторами; ферменты обладают
- 106. Б. Кинетика ферментативного катализа См стр. 94 Ученые Михаэлис и Ментен разработали теорию взаимодействия фермента и
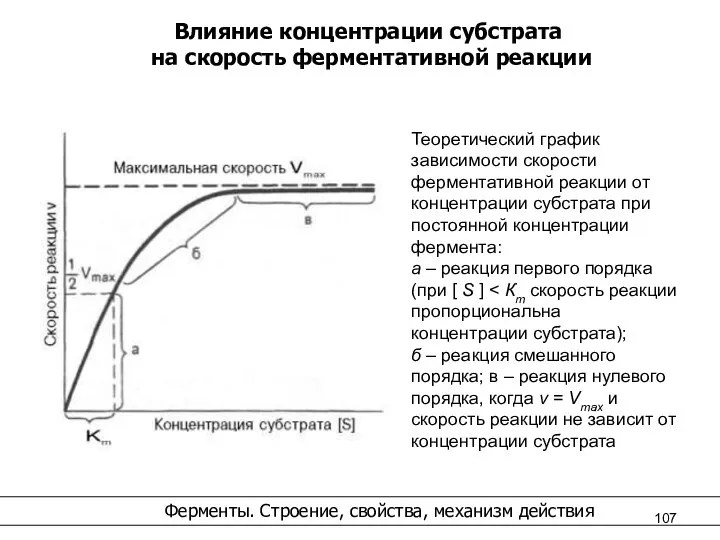
- 107. Влияние концентрации субстрата на скорость ферментативной реакции Ферменты. Строение, свойства, механизм действия
- 108. E+S→ES* → ES** → EP → E+P Диффузия субстрата(S) к ферменту(E) и стерическое связывание его с
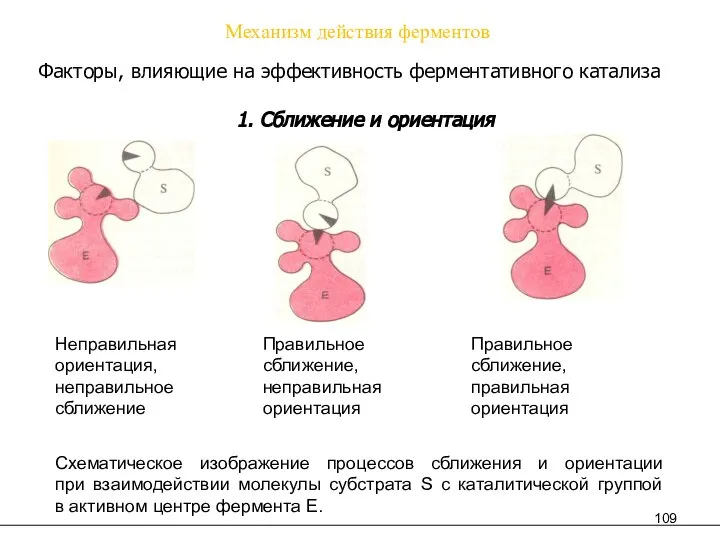
- 109. Механизм действия ферментов Факторы, влияющие на эффективность ферментативного катализа 1. Сближение и ориентация
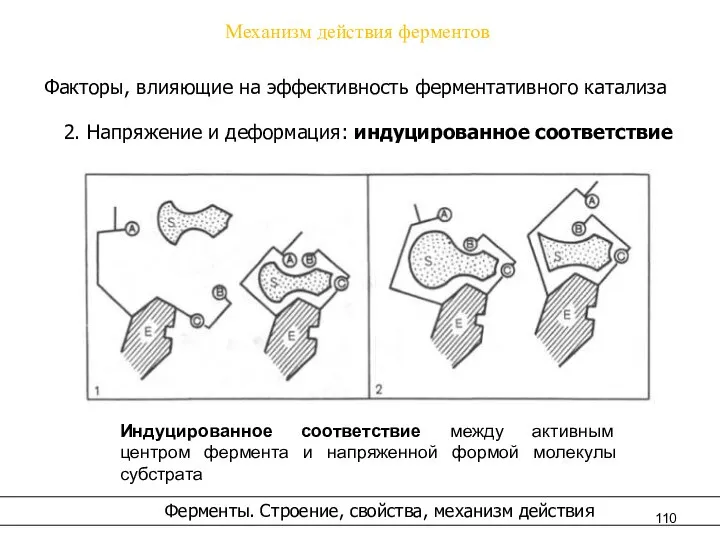
- 110. Механизм действия ферментов Факторы, влияющие на эффективность ферментативного катализа 2. Напряжение и деформация: индуцированное соответствие Ферменты.
- 111. Молекулярные механизмы ферментативного катализа Механизмы ферментативного катализа определяются ролью функциональных групп активного центра фермента в химической
- 112. Сложно…..
- 113. Кислотно-основной катализ Концепция кислотно-основного катализа объясняет ферментативную активность участием в химической реакции кислотных групп (доноры протонов)
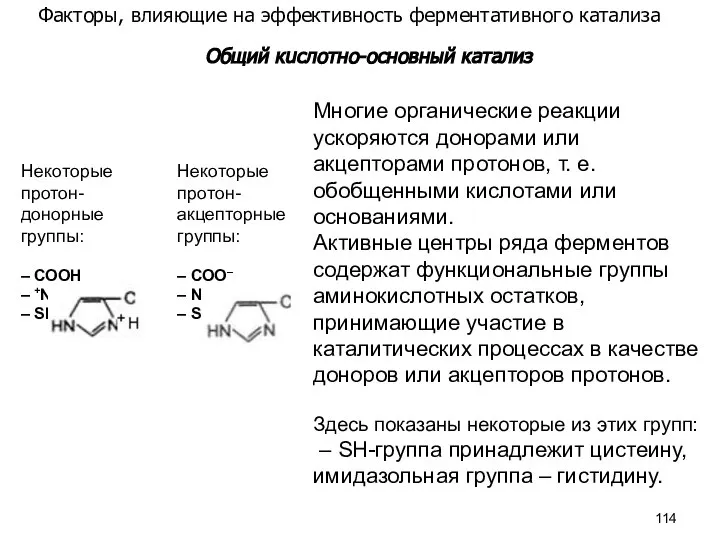
- 114. Факторы, влияющие на эффективность ферментативного катализа Общий кuслотно-основный катализ
- 115. К аминокислотам, участвующим в кислотно-основном катализе, в первую очередь относят цистеин, тирозин, серин, лизин, глутаминовую и
- 116. Примером кислотно-основного катализа ,в котором кофакторами являются ионы Zn2+, а в качестве кофермента используется молекула NAD+,
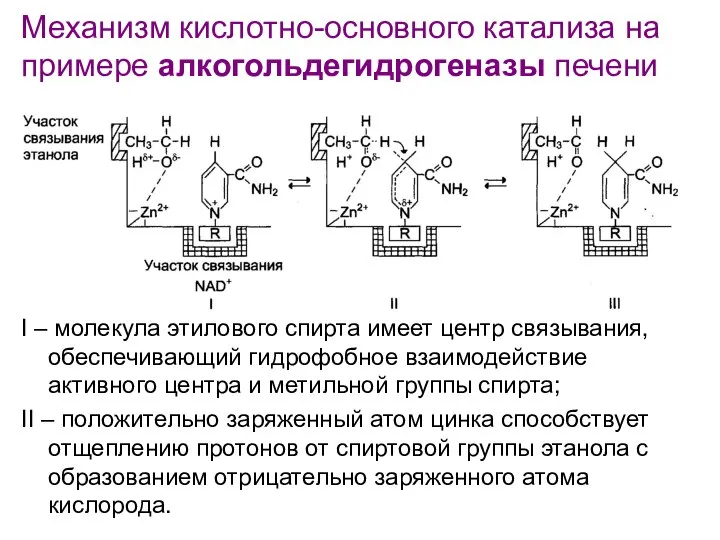
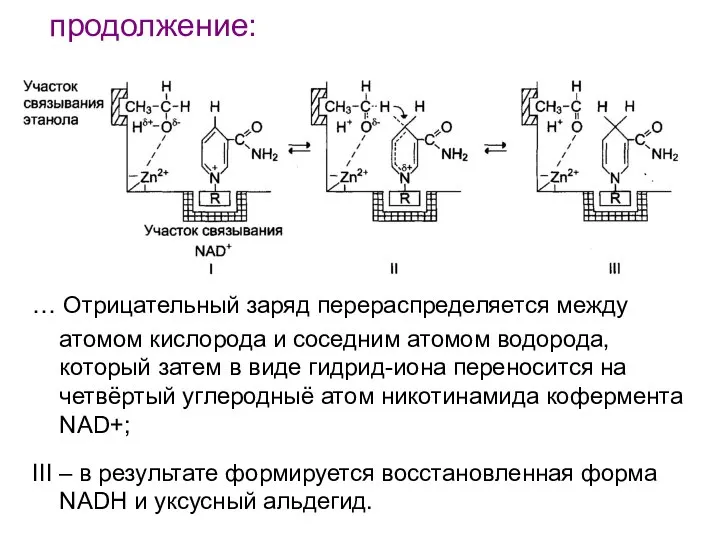
- 117. Механизм кислотно-основного катализа на примере алкогольдегидрогеназы печени I – молекула этилового спирта имеет центр связывания, обеспечивающий
- 118. продолжение: … Отрицательный заряд перераспределяется между атомом кислорода и соседним атомом водорода, который затем в виде
- 119. 2. Ковалентный катализ Ковалентный катализ основан на атаке нуклеофильных (отрицательно заряженных) или электрофильных (положительно заряженных) групп
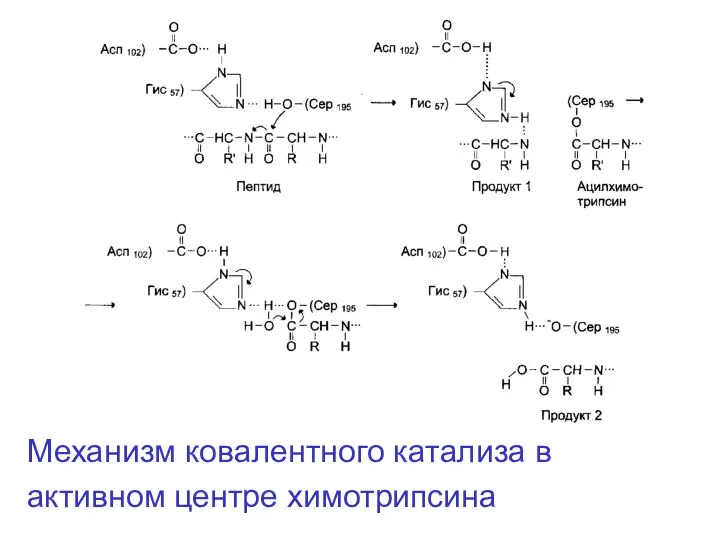
- 120. Действие «сериновых протеаз», таких как трипсин, химитрипсин и тромбин, пример механизма ковалентного катализа когда ковалентная связь
- 121. Механизм ковалентного катализа в активном центре химотрипсина
- 122. Механизм действия ферментов Факторы, влияющие на эффективность ферментативного катализа Ковалентный катализ Одна из моделей ковалентного катализа.
- 123. Специфичность действия ферментов Гипотеза «ключа и замка» Ферменты. Строение, свойства, механизм действия Образование нестойкого фермент-субстратного комплекса
- 124. Специфичность действия ферментов Гипотеза индуцированного соответствия Изменения структуры активного центра фермента, вызванные субстратом, согласно модели «индуцированного
- 125. Объяснить: Методы определения скорости ферментативных реакция По убыли субстрата, По нарастанию концентрации продуктов реакции …синтетические цветные
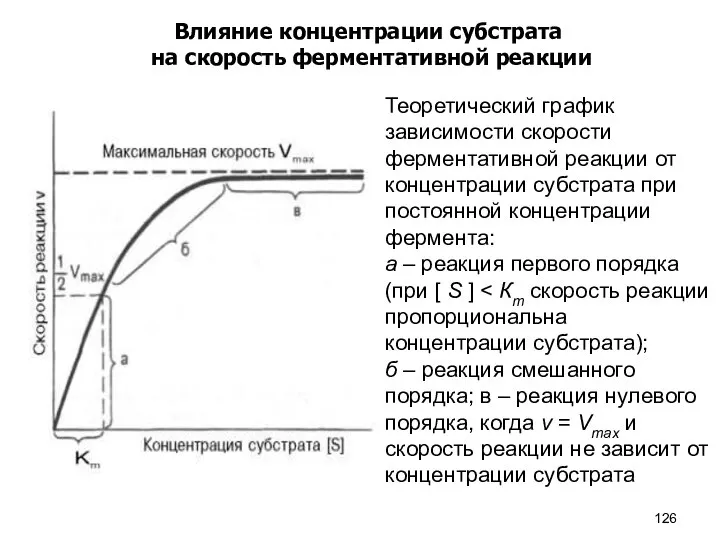
- 126. Влияние концентрации субстрата на скорость ферментативной реакции
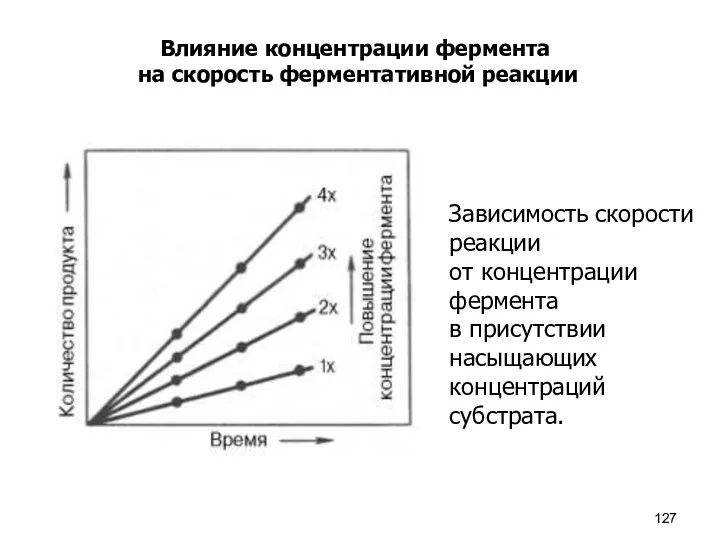
- 127. Влияние концентрации фермента на скорость ферментативной реакции Зависимость скорости реакции от концентрации фермента в присутствии насыщающих
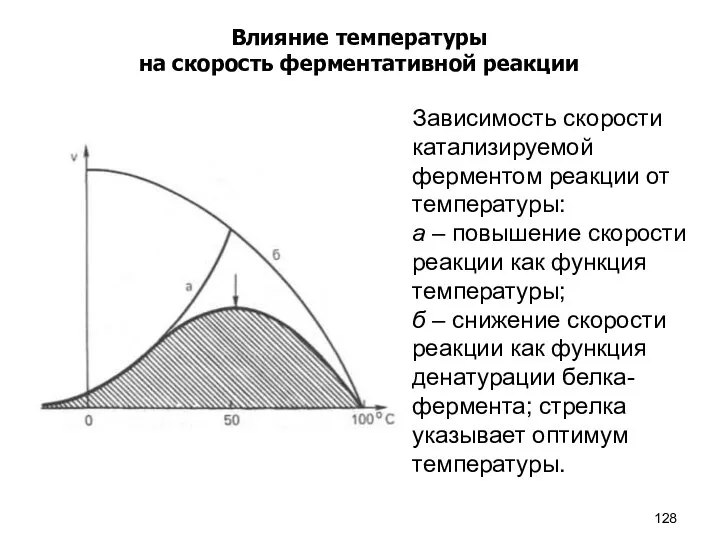
- 128. Влияние температуры на скорость ферментативной реакции Зависимость скорости катализируемой ферментом реакции от температуры: а – повышение
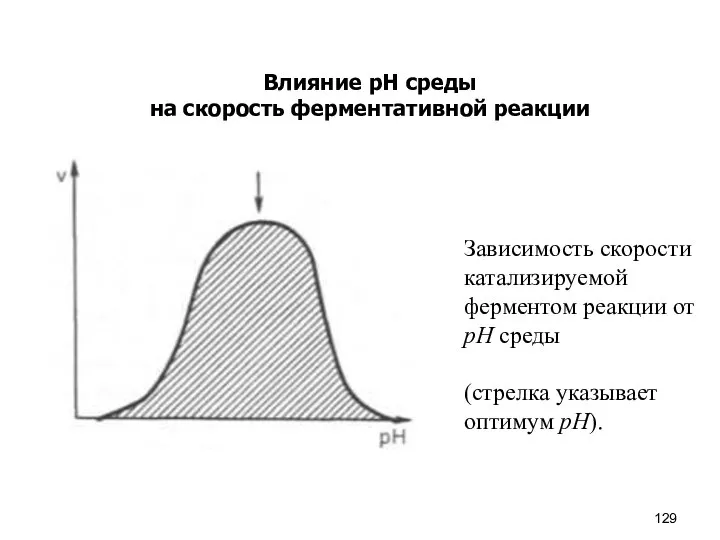
- 129. Влияние рН среды на скорость ферментативной реакции
- 130. Лекция Регуляция ферментативной активности. Классификация ферментов
- 131. План лекции Активаторы ферментов Ингибиторы ферментов Регуляция активности ферментов Классификация и номенклатура ферментов
- 132. Активаторы ферментов Регуляция ферментативной активности. Классификация ферментов Примеры активаторов Активирующее влияние на скорость ферментативной реакции оказывают
- 133. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Необратимое ингибирование Если ингибитор вызывает стойкие изменения пространственной третичной
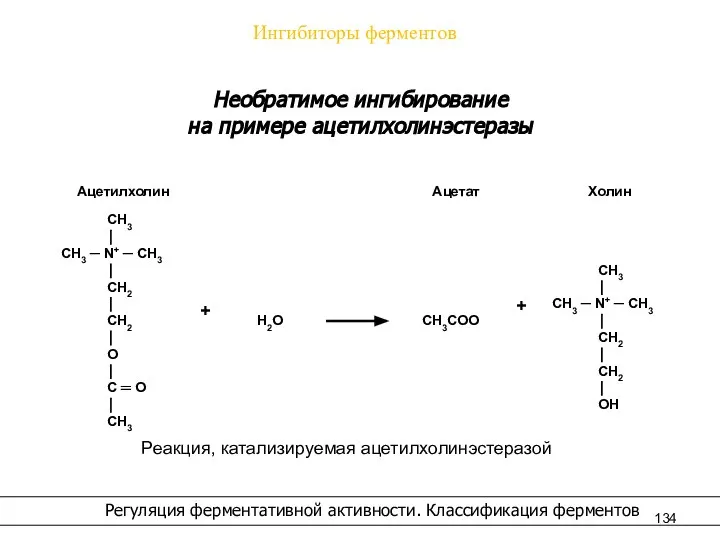
- 134. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Необратимое ингибирование на примере ацетилхолинэстеразы Реакция, катализируемая ацетилхолинэстеразой
- 135. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Необратимое ингибирование на примере ацетилхолинэстеразы Е Необратимое ингибирование ацетилхолинэстеразы
- 136. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Обратимое ингибирование В случае обратимого действия ингибитор образует с
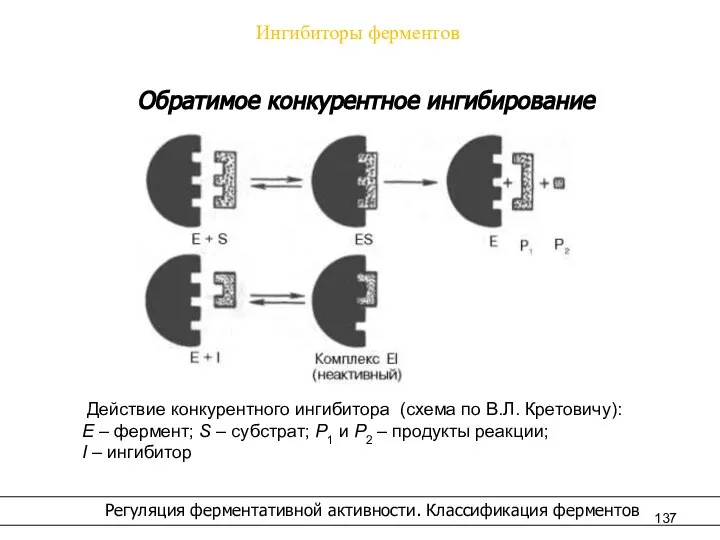
- 137. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Обратимое конкурентное ингибирование
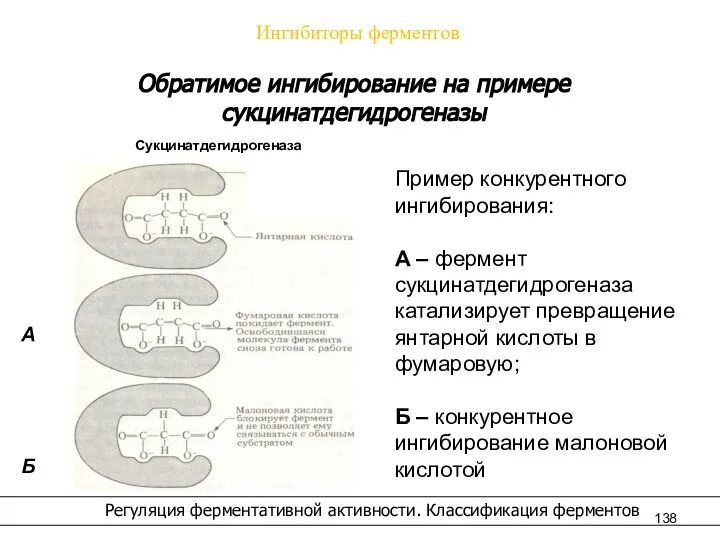
- 138. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Обратимое ингибирование на примере сукцинатдегидрогеназы
- 139. Объяснить Обратимое ингибирование «снимается» (ликвидируется) высокой концентрацией субстрата
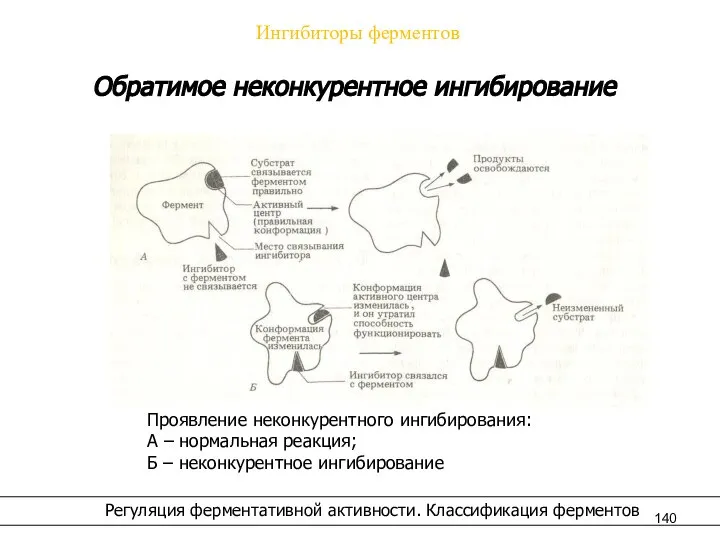
- 140. Ингибиторы ферментов Регуляция ферментативной активности. Классификация ферментов Обратимое неконкурентное ингибирование Проявление неконкурентного ингибирования: А – нормальная
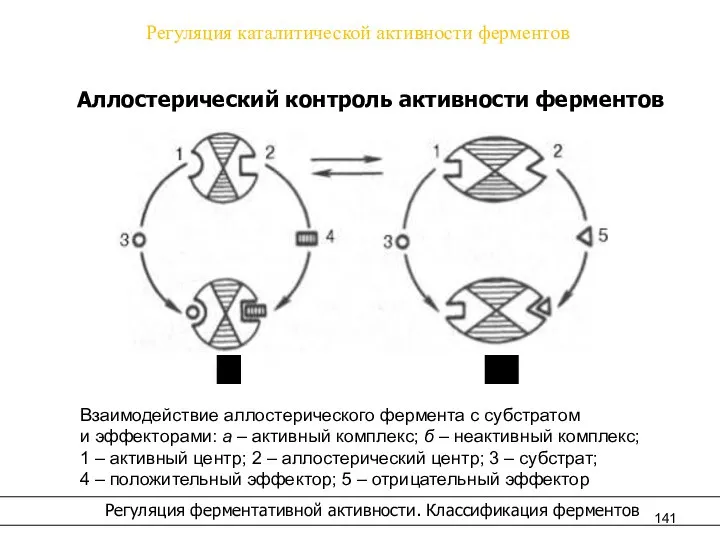
- 141. Регуляция каталитической активности ферментов Регуляция ферментативной активности. Классификация ферментов Аллостерический контроль активности ферментов а б
- 142. Объяснить Строение клетки органеллы компартменты компартментализация клетки
- 144. Скачать презентацию




























































































 Презентация "Математика и искусство" - скачать презентации по МХК
Презентация "Математика и искусство" - скачать презентации по МХК Стартер
Стартер Введение в WCF. WCF-службы. Windows Communication Foundation
Введение в WCF. WCF-службы. Windows Communication Foundation Тензоры диэлектрической и магнитной проницаемости вещества
Тензоры диэлектрической и магнитной проницаемости вещества Динамические характеристики и точность информационных радио- и оптикоэлектронных систем и устройств
Динамические характеристики и точность информационных радио- и оптикоэлектронных систем и устройств История и место C++. Процесс построения программы
История и место C++. Процесс построения программы Презентация на тему "Болезни органов дыхания 1" - скачать презентации по Медицине
Презентация на тему "Болезни органов дыхания 1" - скачать презентации по Медицине Die innovative Lichttechnik des neuen BMW 7er
Die innovative Lichttechnik des neuen BMW 7er Презентация Сахар
Презентация Сахар Кутузовская медаль - презентация для начальной школы
Кутузовская медаль - презентация для начальной школы Смерч
Смерч  Разработка программ управления компьютером
Разработка программ управления компьютером Велимир Хлебников
Велимир Хлебников 围巾里的秘密
围巾里的秘密 С днем студента
С днем студента Символика Общероссийской общественной организации «Российский Союз Молодёжи»
Символика Общероссийской общественной организации «Российский Союз Молодёжи» День белорусской письменности. Викторина
День белорусской письменности. Викторина Маркетинг онлайн (тренды 2009) Евгений Шевченко Интернет-агентство UaMaster «THE MARKETING JAZZ FEST 2009»
Маркетинг онлайн (тренды 2009) Евгений Шевченко Интернет-агентство UaMaster «THE MARKETING JAZZ FEST 2009» Фотоэлектрические модули. (Лекция 5)
Фотоэлектрические модули. (Лекция 5) моделтрование - презентация по Алгебре
моделтрование - презентация по Алгебре Проектная работа на тему "Умный дом"
Проектная работа на тему "Умный дом" facts Основные тиристорные устройства
facts Основные тиристорные устройства весенние цветы - презентация для начальной школы
весенние цветы - презентация для начальной школы Свет и освещение
Свет и освещение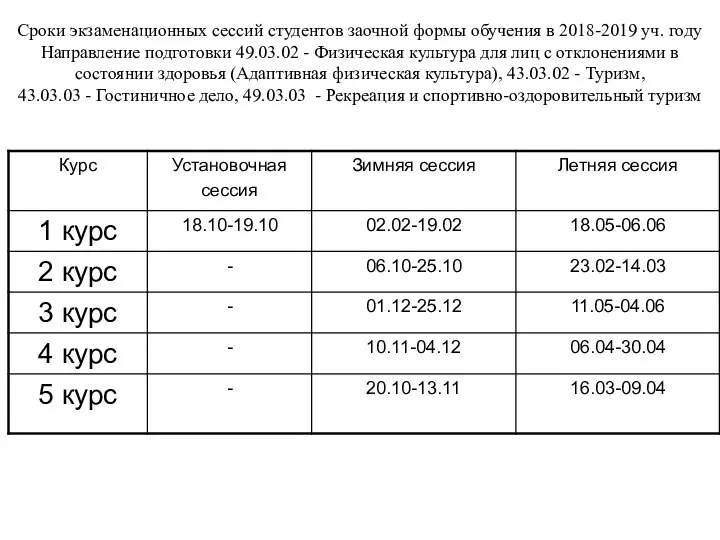 Сроки экзаменационных сессий студентов заочной формы обучения в 2018-2019 уч. году
Сроки экзаменационных сессий студентов заочной формы обучения в 2018-2019 уч. году Урок по математике 6 класс « Разложение на простые множители»
Урок по математике 6 класс « Разложение на простые множители»  Тема 1.1 Понятие и значение экономического анализа Выполнил: Тимофеев И.А.
Тема 1.1 Понятие и значение экономического анализа Выполнил: Тимофеев И.А. Кровная месть в современных обществах
Кровная месть в современных обществах