Содержание
- 2. В настоящее время в эпоху глобального роста резистентности госпитальной микрофлоры к АМП проблема нозокомиальной инфекции, особенно,
- 3. Несовершенство современных медицинских технологий и практики АМТ стало причиной появления и распространения АБ-устойчивых нозокомиальных инфекций. Одной
- 4. Учитывая тяжесть состояния больных и невозможность на практике достаточно быстро получать лабораторные данные по этиологии инфекционного
- 5. В течение длительного времени основу такой терапии составляли комбинации цефалоспоринов III поколения и аминогликозидов. Однако появление
- 6. В качестве альтернативы комбинациям цефалоспоринов III поколения и аминогликозидов используют фторхинолоны и карбапенемы. Однако и эти
- 7. Первый из карбапенемных антибиотиков – ИМИПЕНЕМ используется в медицинской практике уже более 30 лет, тем не
- 8. 20 лет назад в России зарегистрирован карбапенемный антибиотик МЕРОПЕНЕМ, обладающий некоторыми отличиями и преимуществами в сравнении
- 9. Итогом многих исследований по антибиотикорезистентности явились следующие выводы: карбапенемные антибиотики, в частности, МЕРОПЕНЕМ, по спектру действия
- 10. однако это не исключает необходимости микробиологической диагностики инфекций, так как существуют микроорганизмы, обладающие к ним природной
- 11. Устойчивость клинически значимых микроорганизмов к антимикробным препаратам требует проведения мониторинга внебольничной и нозокомиальной флоры. Чрезвычайно важны
- 12. Основным критерием роста резистентности микрофлоры, как это не странно для клиницистов, считаются не клинические данные, а
- 13. Идеальная доза антибиотика должна обеспечивать наиболее высокую вероятность киллинга бактерий. Следовательно, положительный клинический и бактериологический эффект
- 14. МЕРОПЕНЕМ даже в высоких дозах (6 г/сут ≈ 90 мг/кг) у больных с инфекциями нервной системы
- 15. В исследованиях in vitro и in vivo показано, что клиническая эффективность β-лактамных антибиотиков при концентрациях в
- 16. Рис. 1. %Т>МПК - отношение длительности периода превышения МПК к интервалу дозирования (в %) при введении
- 17. Таким образом, изменение режимов дозирования препаратов позволяет добиваться максимального подавления флоры и снижения количества бактерий, способных
- 18. Максимальное значение %Т>МПК может быть достигнуто путем уменьшения интервала дозирования (более частое введение) или увеличения продолжительности
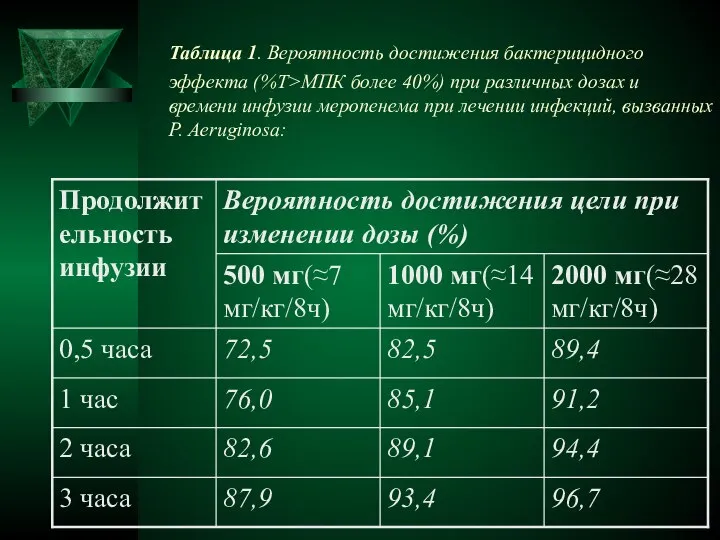
- 19. Таблица 1. Вероятность достижения бактерицидного эффекта (%Т>МПК более 40%) при различных дозах и времени инфузии меропенема
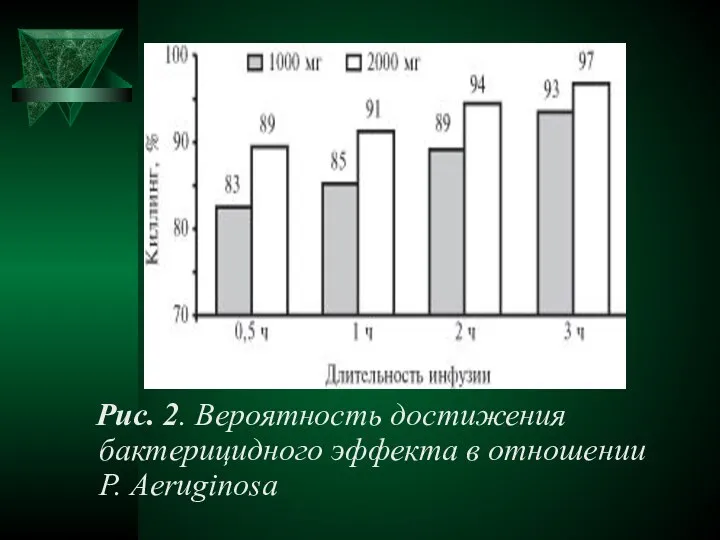
- 20. Рис. 2. Вероятность достижения бактерицидного эффекта в отношении P. Аeruginosa
- 21. Постоянная инфузия бета-лактамных антибиотиков применяется в сложных клинических ситуациях, например, у больных ОАРИТ, у пациентов с
- 22. Этот метод экономичен, быстро обеспечивает терапевтические уровни препарата в крови. Однако могут возникать проблемы со стабильностью
- 23. При наличии наиболее резистентных возбудителей может потребоваться комбинированное применение карбапенемов с аминогликозидами, по крайней мере, в
- 24. Непременным условием успешного долговременного использования АБТ является разумное его применение. С этой целью важным является правильное
- 25. МЕРОПЕНЕМ эффективен в режиме монотерапии при лечении госпитальных инфекций различной локализации: пневмония, осложненные инфекции мочевыводящих путей,
- 26. В большинстве случаев препарат используется как резервное средство в случае неэффективности начальной терапии. Однако необходимо особо
- 27. 1. При эмпирической терапии: инфекции у больных в критическом состоянии поздняя (свыше 5 сут) ВАП инфекционные
- 28. 2. При этиотропной терапии: тяжелые инфекции, вызванные P.Аeruginosa, Acinetobacter, Burkholderia cepacia, выделение штаммов Enterobacteriaceae продуцирующих БЛРС
- 29. Дозирование МЕРОПЕНЕМА: в большинстве случаев адекватной является доза 1,5 г ≈ 20 мг/кг/сутки (0,5 г ≈
- 30. В отделении недоношенных детей НИИ педиатрии РАМН накоплен опыт по клиническому применению МЕРОПЕНЕМА (МЕРОНЕМ – "Астра-Зенека"//
- 31. Препарат вводился парентерально из расчета 15-20 мг/кг массы тела в сутки в 3 приема. У детей
- 32. Показаниями к назначению МЕРОПЕНЕМА были: генерализованный инфекционный процесс (сепсис); локализованные формы инфекционно-воспалительных заболеваний (пневмония, менингит, перитонит,
- 33. При проведении бактериологического мониторинга различных биологических образцов, полученных от новорожденных детей, основными возбудителями инфекционного процесса были
- 34. Клинический эффект при использовании МЕРОПЕНЕМА оценивался как «удовлетворительный» и «неудовлетворительный». Фактически, во всех случаях он признан
- 35. Ни в гемограмме, ни в биохимических критериях гепатотоксичности при динамическом контроле на фоне использования МЕРОПЕНЕМА, кроме
- 36. Помимо вышеуказанного, велся пролонгированный мониторинг за пациентами и наблюдение за ними в катамнезе до 6-месячного возраста
- 37. Ни в одном случае не было отмечено явлений дисбактериоза кишечника, что, безусловно, является положительным моментом при
- 38. Таким образом, использование меропенема в неонатологической практике позволяет отказаться от комбинированного антибактериального лечения и перейти на
- 39. В настоящее время актуальным является фармакоэкономический анализ предлагаемых стандартов действий и средств. В бюджете многопрофильного ЛПУ
- 40. В одном из ретроспективных фармакоэкономических исследований сравнивались две схемы АБТ нозокомиальной инфекции у пациентов в ОРИТ:
- 41. Сравнение проводилось методом «затраты–эффективность». Показателем клинической эффективности был процент выздоровления больных. В группе, получавшей МЕРОНЕМ, выздоровление
- 42. Общие затраты складывались из стоимости основной АБТ, дополнительной АБТ, которая назначалась при неэффективности основной, и стоимости
- 43. Хотя стоимость курса основной АБТ в группе МЕРОНЕМА была на 80% выше, чем в стандарте, общие
- 44. стоимость дополнительной АБТ в группе стандартной АБТ в сумме с основной АБТ на 15% превысила таковую
- 45. превышение затрат на пребывание пациентов в ОРИТ в группе стандартной терапии (из-за менее эффективного лечения) составило
- 46. Таким образом, в группе, получавшей МЕРОНЕМ, итоговые затраты оказались на 30% ниже, чем в группе стандартной
- 47. Рис. 3. Структура затрат в группе пациентов, получавших Меронем, и в группе, получавшей стандартную АБ терапию
- 48. Рис. 4. Соотношение «затраты–эффективность» при проведении стандартной терапии и с использованием Меронема
- 49. Антибиотикорезистентность — неизбежное биологическое явление, предотвратить ее практически невозможно. Действие АМП приводит к гибели чувствительных микробов,
- 50. Растущая резистентность связана не только и не столько с увеличением применения АМП. Главная причина роста резистентности
- 51. Фармакоэпидемиологические исследования показали, что для России характерен невысокий уровень общего использования АМП и необычный по сравнению
- 52. Это заключается в существенно более высоком удельном весе относительно дешевых, нередко устаревших препаратов с неблагоприятным профилем
- 53. Почему АМП используют нерационально? Проблема, прежде всего, в недостатке знаний, неправильных представлениях и ошибочных выводах.
- 54. Возможным путём решения проблемы резистентности может быть разработка новых АМП. Но в последние годы отмечается дефицит
- 55. Антимикробные препараты — невосстановимые ресурсы. Если человечество не сможет защитить это величайшее достижение медицинской науки, оно
- 57. Скачать презентацию




















































 Таланты Богородска © Истрина Татьяна Валерьевна
Таланты Богородска © Истрина Татьяна Валерьевна Формы поведения
Формы поведения  БЖД - введение
БЖД - введение  Ближний Восток
Ближний Восток Технологическое обслуживание, ремонт, сборка и диагностика щитка приборов и датчиков на участке диагностики
Технологическое обслуживание, ремонт, сборка и диагностика щитка приборов и датчиков на участке диагностики Архангельский государственны й музей деревянного зодчества и народного искусства «Малые Корелы»
Архангельский государственны й музей деревянного зодчества и народного искусства «Малые Корелы» АКУСТИЧЕСКОЕ ПРОЕКТИРОВАНИЕ ПРОВОСЛАВНЫХ ХРАМОВ
АКУСТИЧЕСКОЕ ПРОЕКТИРОВАНИЕ ПРОВОСЛАВНЫХ ХРАМОВ Написання програм
Написання програм Биогенные стимуляторы
Биогенные стимуляторы Электронная подпись
Электронная подпись Recording studio and Bedroom interior design
Recording studio and Bedroom interior design Природно-климатические условия местности в архитектурном проектировании
Природно-климатические условия местности в архитектурном проектировании Создание систем бизнес-аналитики планирования деятельности BPM
Создание систем бизнес-аналитики планирования деятельности BPM Оценки степени созревания органического вещества осадков
Оценки степени созревания органического вещества осадков Особенности эмоциональной сферы личности младших школьников, обучающихся в коррекционных классах Психологические нарушения в э
Особенности эмоциональной сферы личности младших школьников, обучающихся в коррекционных классах Психологические нарушения в э Методы лазерной дифракции в исследовании наноматериалов и наноструктур
Методы лазерной дифракции в исследовании наноматериалов и наноструктур  Знакомство с системой компьютерной математики
Знакомство с системой компьютерной математики Япония на рубеже XIX и 20 веков
Япония на рубеже XIX и 20 веков  Правила корректности дедуктивных умозаключений
Правила корректности дедуктивных умозаключений Вебинары : новый инструмент коммуникаций 1. - презентация
Вебинары : новый инструмент коммуникаций 1. - презентация Массив. Индекс элемента массива. Сортировка массива. Алгоритмы сортировки
Массив. Индекс элемента массива. Сортировка массива. Алгоритмы сортировки Модели и моделирование
Модели и моделирование Літо. Місяць липень
Літо. Місяць липень Методи аналізу ризику та надійності атомних електричних станцій
Методи аналізу ризику та надійності атомних електричних станцій Демократия
Демократия Позиционные задачи. Метод конкурирующих точек (Лекция 3)
Позиционные задачи. Метод конкурирующих точек (Лекция 3) Посвящение в первоклассники - презентация для начальной школы__________________________________________________________________________________________________________________
Посвящение в первоклассники - презентация для начальной школы__________________________________________________________________________________________________________________ Уход при ангине
Уход при ангине