Содержание
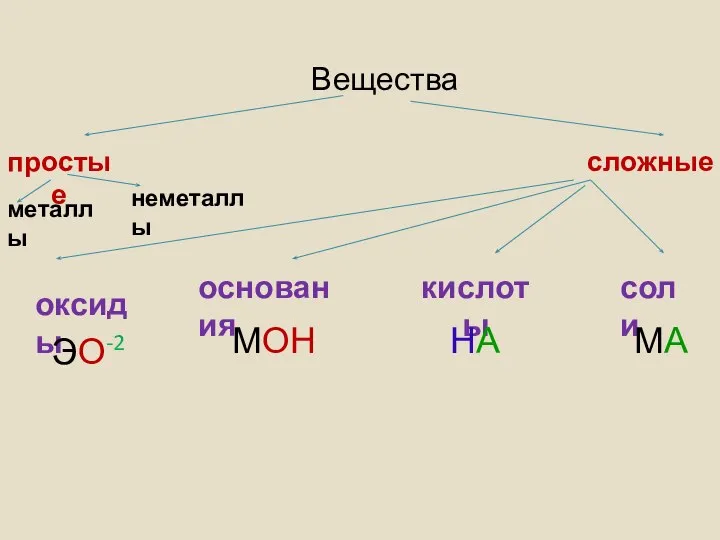
- 2. кислоты Вещества простые сложные оксиды основания соли ЭО-2 МОН НА МА
- 3. Оксиды- бинарные соединения, в которых кислород стоит на втором месте и имеет степень окисления (-2) ЭО
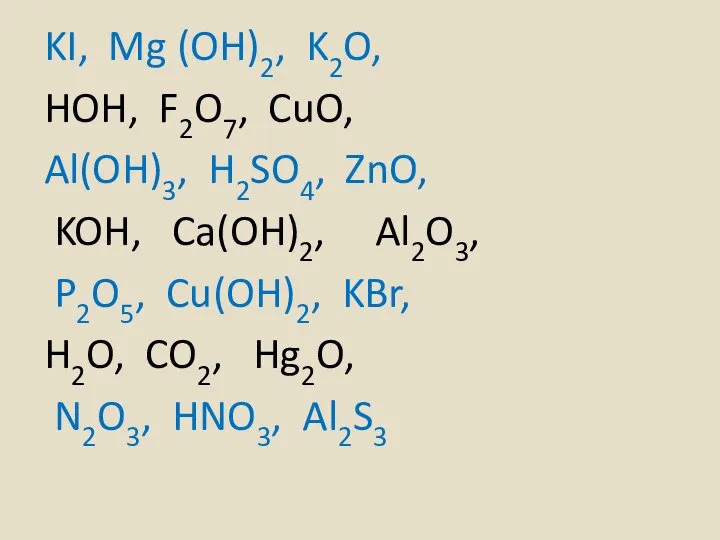
- 4. Начертите таблицу на страницу Выпишите формулы оксидов в левый столбик
- 5. KI, Mg (OH)2, K2O, HOH, F2O7, CuO, Al(OH)3, H2SO4, ZnO, KOH, Ca(OH)2, Al2O3, P2O5, Cu(OH)2, KBr,
- 6. Оксиды Основные: Э-металл (главные подгруппы I и II групп) или (побочная подгруппа с валентностью I или
- 7. K2O F2O7 CuO ZnO Al2O3 P2O5 H2O CO2 Hg2O N2O3
- 8. Номенклатура оксидов “Оксид” + ”элемента” + “переменная валентность” K2O –оксид калия P2O3 –оксид фосфора (III)
- 9. Составьте формулы оксидов Оксид марганца (II) Оксид марганца (IV) Оксид марганца (VII) Оксид хрома (III) Оксид
- 10. Основания -сложные соединения металлов с гидроксогруппой (ОН-). Число гидрокогрупп равно валентности металла. М(ОН)n
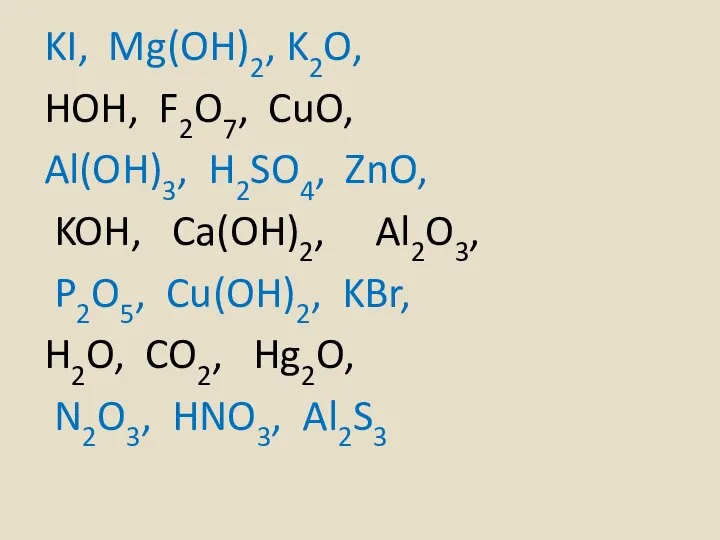
- 11. Продолжите таблицу Выпишите формулы оснований в левый столбик
- 12. KI, Mg(OH)2, K2O, HOH, F2O7, CuO, Al(OH)3, H2SO4, ZnO, KOH, Ca(OH)2, Al2O3, P2O5, Cu(OH)2, KBr, H2O,
- 13. Основания Щелочи- растворимые в воде основания. Гидроксиды (⭣) –нерастворимые в воде основания.
- 14. Mg(OH)2 KOН Al(OH)3 Ca(OH)2 Cu(OH)2
- 15. Номенклатура оснований “гидроксид” + название металла + переменная валентность металла Fe(ОН)3- гидроксид железа (III)
- 16. 1. Составьте формулы оснований Гидроксид хрома (III) Гидроксид цинка Гидроксид железа (II) Гидроксид лития 2. Определите
- 18. Кислоты (НА) Н- водород А- кислотный остаток Н2SO4 –серная кислота Валентность кислотного остатка равна числу атомов
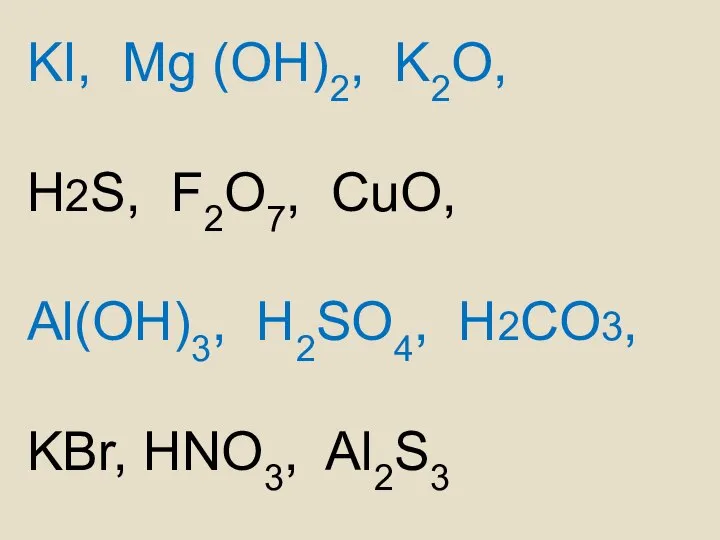
- 19. Кислоты (НА) Валентность кислотного остатка равна числу атомов водорода Выпишите формулы кислот в столбик. Назовите их.
- 20. KI, Mg (OH)2, K2O, H2S, F2O7, CuO, Al(OH)3, H2SO4, H2CO3, KBr, HNO3, Al2S3
- 21. H2S H2SO4 H2CO3 HNO3
- 22. Соли- это сложные вещества, состоящие из ионов металлов и кислотных остатков. МА
- 23. KI KBr Al2S3
- 24. номенклатура Название кислотного остатка + название металла + переменная валентность металла FeCL3- хлорид железа (III)
- 26. Скачать презентацию



















 Организация лечебно-эвакуационного обеспечения населения при ликвидации последствий нападения противника
Организация лечебно-эвакуационного обеспечения населения при ликвидации последствий нападения противника Успенский храм
Успенский храм Особенности юридической техники: Мальта, Кипр, Гибралтар
Особенности юридической техники: Мальта, Кипр, Гибралтар С днём рожденья
С днём рожденья «Российский архитектор итальянского происхождения ампир» Карл Иванович Росси
«Российский архитектор итальянского происхождения ампир» Карл Иванович Росси Александр Николаевич Островский Мой дом - театр
Александр Николаевич Островский Мой дом - театр Компания «Петро-Композит». Проект «Зеленый город»
Компания «Петро-Композит». Проект «Зеленый город» ООО «Завод-Новатор как логистическая система Выполнили: Епифанова, Шунайлова, Шалтаева
ООО «Завод-Новатор как логистическая система Выполнили: Епифанова, Шунайлова, Шалтаева История Европейского союза
История Европейского союза  Оформление КГД
Оформление КГД Типы рыночных структур Проект по экономике для студентов 1 курса Авторы: Мельник Анастасия, Корякина Любовь
Типы рыночных структур Проект по экономике для студентов 1 курса Авторы: Мельник Анастасия, Корякина Любовь Болезни легких
Болезни легких  Маршрутизация
Маршрутизация Софийский собор
Софийский собор Коррозия и защита полимерных строительных материалов
Коррозия и защита полимерных строительных материалов Биология Новокуйбышевск
Биология Новокуйбышевск Конфликт Грузии и Абхазии
Конфликт Грузии и Абхазии Презентация "Всемирный банк в Казахстане" - скачать презентации по Экономике
Презентация "Всемирный банк в Казахстане" - скачать презентации по Экономике Технологии программирования (первый семестр)
Технологии программирования (первый семестр) Аттестационная работа. Создание творческого проекта «Кукла-мотанка»
Аттестационная работа. Создание творческого проекта «Кукла-мотанка» Повышение организации труда на предприятии «Фотон»
Повышение организации труда на предприятии «Фотон» Іскерлік қатынастың этикасы
Іскерлік қатынастың этикасы Kim jestem w perspektywie Bożego planu?
Kim jestem w perspektywie Bożego planu? Писанкарство
Писанкарство Контрольно-измерительные приборы
Контрольно-измерительные приборы Виды зубчатых передач
Виды зубчатых передач Презентация "А.С.Пушкин на портретах художников О.Кипренского и В.Тропинина" - скачать презентации по МХК
Презентация "А.С.Пушкин на портретах художников О.Кипренского и В.Тропинина" - скачать презентации по МХК Қазан төңкерісіне дейінгі Қазақстандағы музейлер және оны ұйымдастырушылар
Қазан төңкерісіне дейінгі Қазақстандағы музейлер және оны ұйымдастырушылар