Содержание
- 2. ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ РАЗВИТИЮ Государственное образовательное учреждение высшего профессионального образования «ПЯТИГОРСКАЯ ГОСУДАРСТВЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ
- 3. ГОСТ Р 52249-2004 УТВЕРЖДЕН Постановлением Госстандарта России от 10 марта 2004 г. N 160-ст Дата введения
- 4. Сведения о стандарте 1. Подготовлен Ассоциацией инженеров по контролю микрозагрязнений (АСИНКОМ) по собственному аутентичному переводу, указанному
- 5. ВВЕДЕНИЕ В мировой практике одним из важнейших документов, определяющим требования к производству и контролю качества лекарственных
- 6. ВВЕДЕНИЕ "Правила производства лекарственных средств" - "Good Manufacturing Practice for Medicinal Products (GMP). Направлены на: обеспечение
- 7. ВВЕДЕНИЕ Правила GMP устанавливают требования к: системе управления качеством контролю качества персоналу помещениям и оборудованию документации
- 8. ОБЛАСТЬ ПРИМЕНЕНИЯ Настоящий стандарт устанавливает требования к производству и контролю качества лекарственных средств для человека и
- 9. ОСНОВНЫЕ ТРЕБОВАНИЯ ФУП
- 10. Управление качеством Принципы Производитель лекарственных средств должен организовать их производство так, чтобы лекарственные средства гарантированно соответствовали
- 11. Основные требования I. Все производственные процессы должны быть четко регламентированы и периодически пересматриваться с учетом накопленного
- 12. III. Следует обеспечить все необходимые условия для выполнения требований настоящего стандарта, в т.ч. включая наличие: a)
- 14. VI. В процессе производства следует составлять протоколы (заполняемые в рукописной форме и/или с использованием технических средств),
- 15. VIII. Порядок реализации (оптовой продажи) продукции должен сводить к минимуму любой риск для ее качества. IX.
- 16. 2. Персонал Предприятие должно быть укомплектовано персоналом необходимой численности и квалификации. Должностные обязанности каждого сотрудника должны
- 17. Руководящие работники 2.3. Руководители производства, руководитель службы (отдела) контроля качества и Уполномоченное лицо (лица) должны быть
- 18. Обязанности Уполномоченных лиц: a) для лекарственных средств, выпущенных в Российской Федерации, Уполномоченное лицо должно гарантировать, что
- 19. Основные обязанности руководителя производства I. Организация производства и хранения продукции в соответствии с документацией с целью
- 20. V. Контроль за проведением работ по аттестации (валидации). VI. Организация первичного и последующего обучения производственного персонала.
- 21. Основные обязанности руководителя службы контроля качества I. Утверждение или отклонение исходных и упаковочных материалов, промежуточной, нерасфасованной
- 22. VI. Контроль работы подведомственного отдела, обслуживания его помещений и оборудования. VII. Контроль проведения аттестации (валидации). VIII.
- 23. Гигиена персонала 2.13. На предприятии должны быть разработаны правила личной гигиены персонала с учетом особенностей конкретного
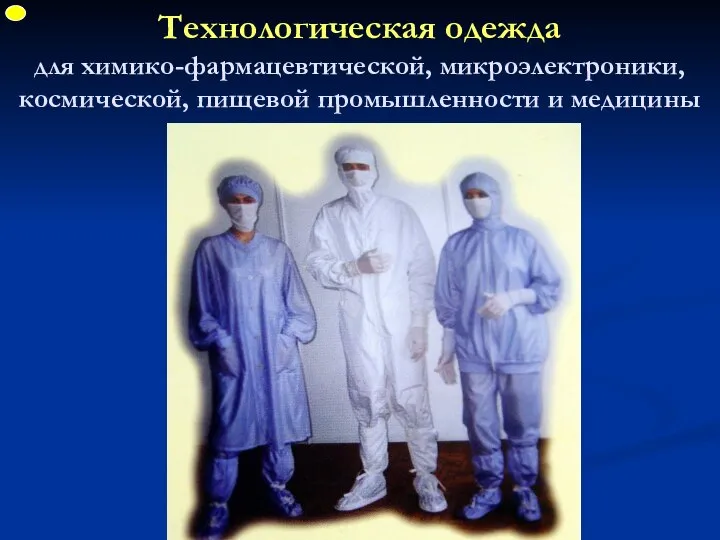
- 24. Технологическая одежда для химико-фармацевтической, микроэлектроники, космической, пищевой промышленности и медицины ФУП
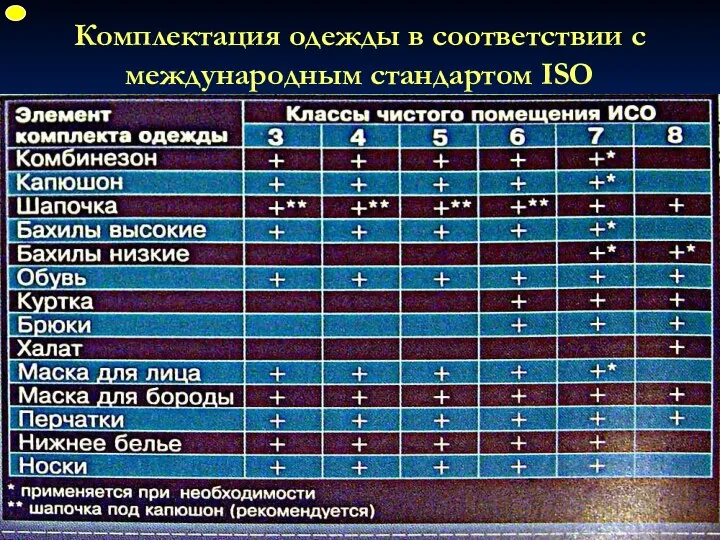
- 25. Комплектация одежды в соответствии с международным стандартом ISO ФУП
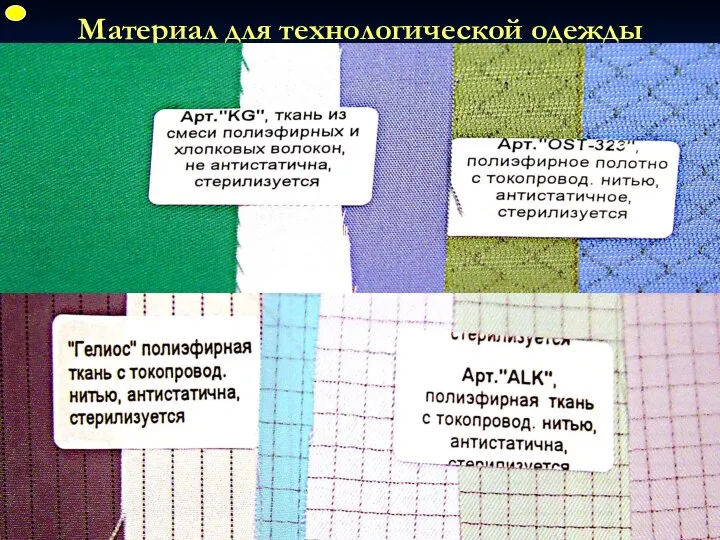
- 26. Материал для технологической одежды ФУП
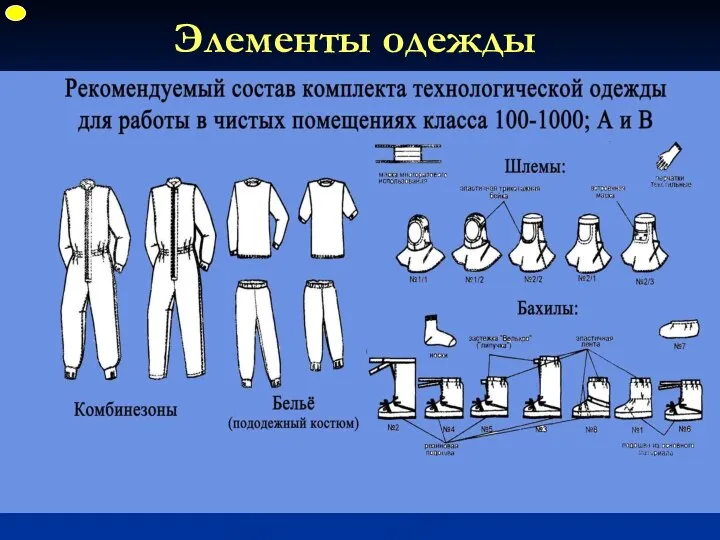
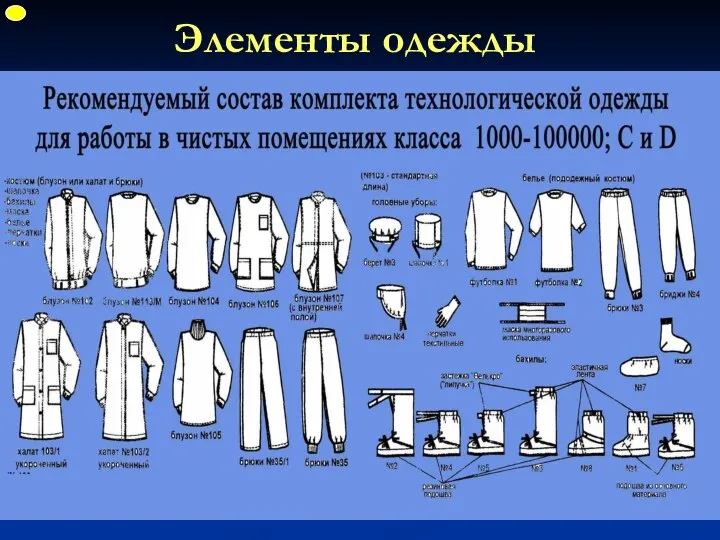
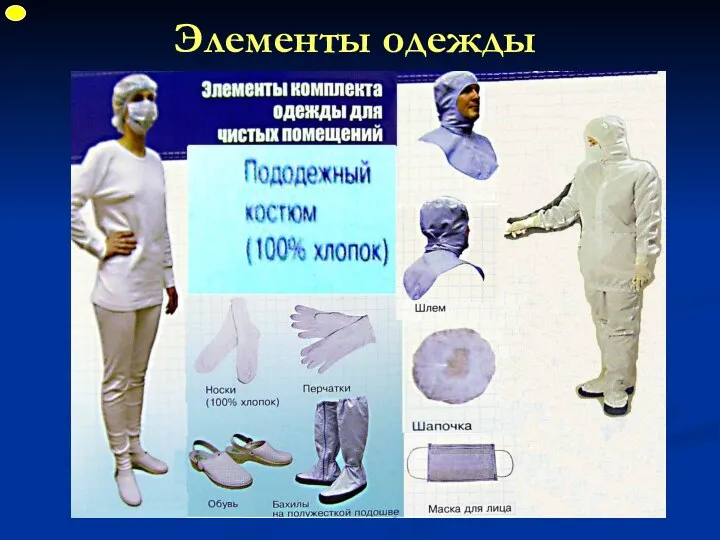
- 27. Элементы одежды ФУП
- 28. Элементы одежды ФУП
- 29. Элементы одежды ФУП
- 30. ФУП
- 31. 3. Помещения и оборудование Принципы Место расположения, проект, строительство, монтаж, оснащение и обслуживание помещений и оборудования
- 32. Оборудование 3.34. Конструкция, монтаж и порядок технического обслуживания оборудования должны соответствовать его назначению. 3.35. Работы по
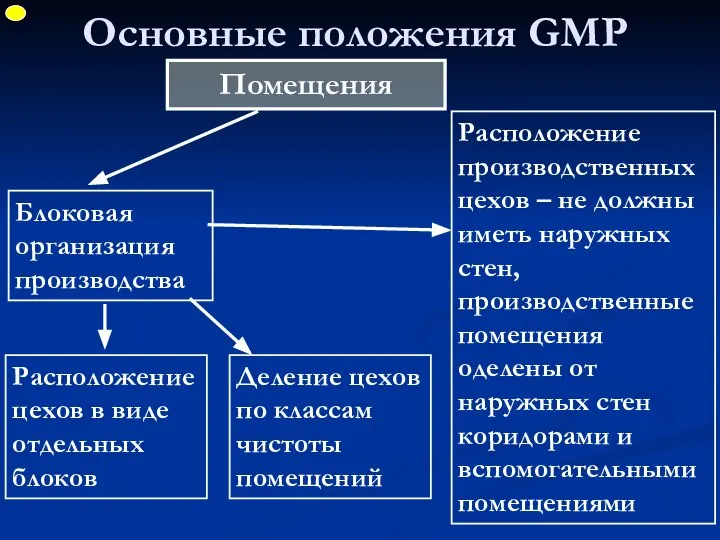
- 33. Основные положения GMP Помещения Блоковая организация производства Расположение цехов в виде отдельных блоков Деление цехов по
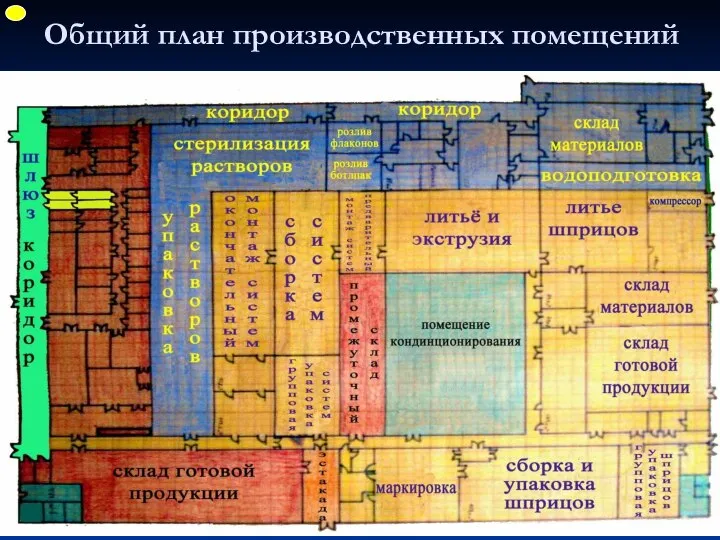
- 35. Общий план производственных помещений ФУП
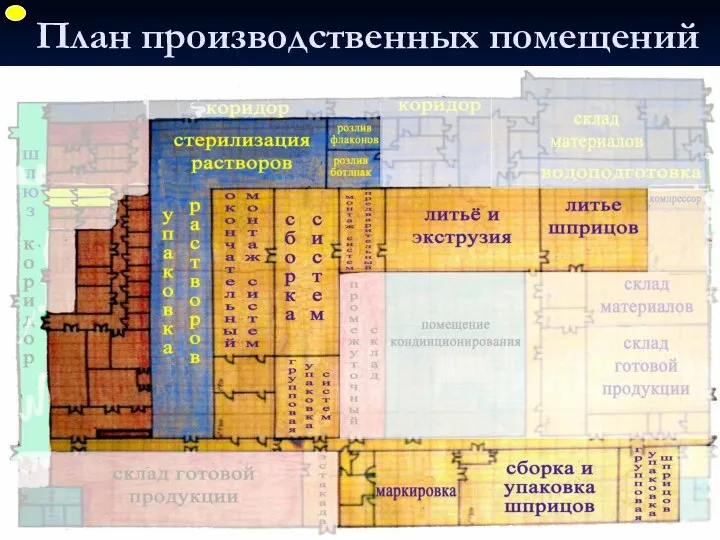
- 36. План производственных помещений ФУП
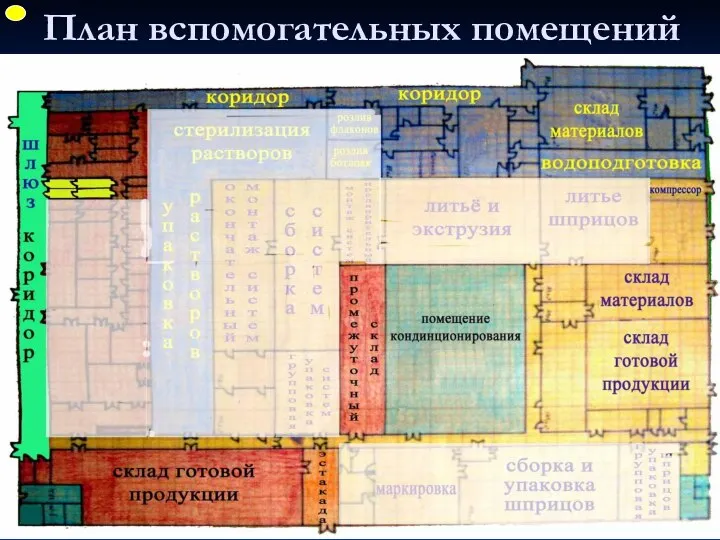
- 37. План вспомогательных помещений ФУП
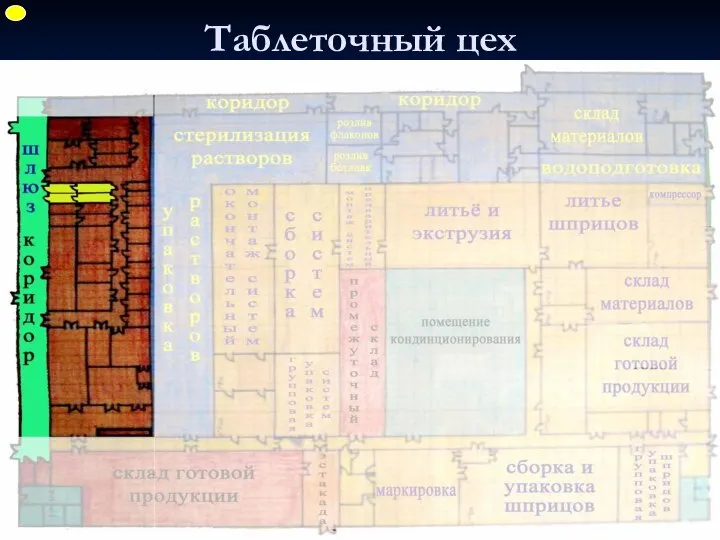
- 38. Таблеточный цех ФУП
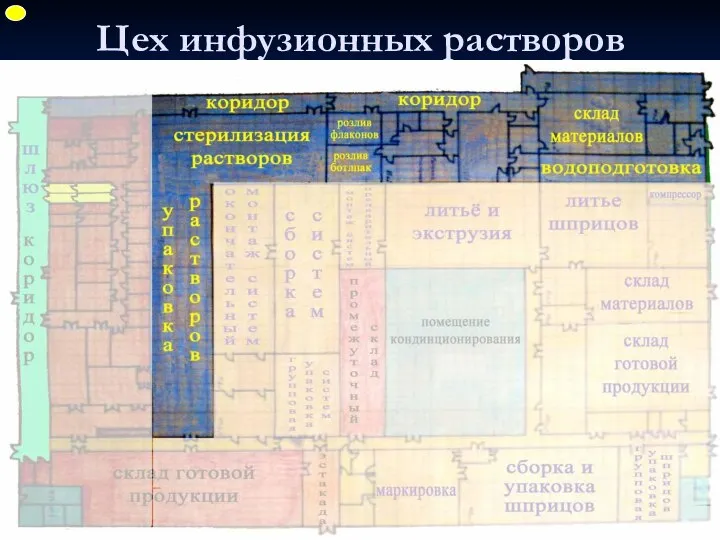
- 39. Цех инфузионных растворов ФУП
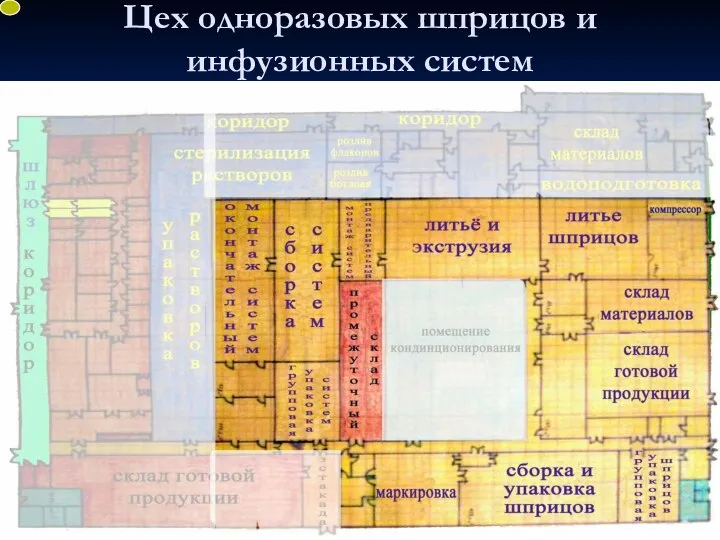
- 40. Цех одноразовых шприцов и инфузионных систем
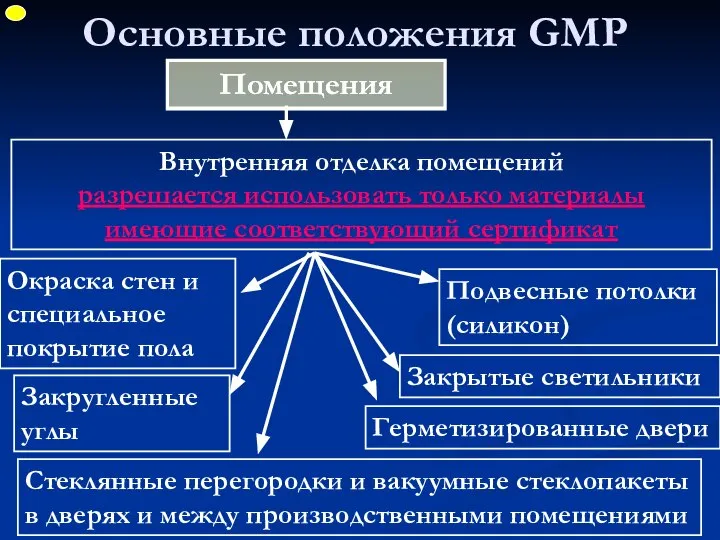
- 41. Основные положения GMP Помещения Закругленные углы Окраска стен и специальное покрытие пола Внутренняя отделка помещений разрешается
- 42. Наружные окна Вакуумные стеклопакеты Светозащитная пленка Внутренняя отделка помещений ФУП
- 43. Отделка стен Внутренняя отделка помещений Многослойное покрытие пола полимерными материалами ФУП
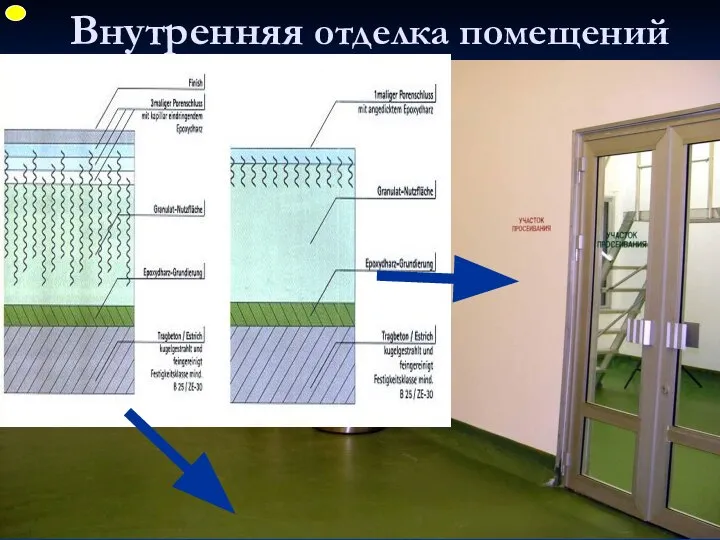
- 44. Внутренняя отделка помещений ФУП
- 45. Закругленные углы Внутренняя отделка помещений ФУП
- 46. Внутренняя отделка помещений Прозрачные двери и стеклянные перегородки между помещениями ФУП
- 47. Подвесные «силиконовые» потолки Внутренняя отделка помещений Закрытые осветительные приборы ФУП
- 48. Двери Автоматическая и ручная блокировка Внутренняя отделка помещений ФУП
- 49. Двери Герметизация Внутренняя отделка помещений ФУП
- 50. ФУП
- 51. ФУП
- 52. Разделение помещений по классам чистоты прозрачными перегородками с технологическими люками (окнами) ФУП
- 53. ФУП
- 54. Система очистки и кондиционирования воздуха ФУП
- 55. Система очистки и кондиционирования воздуха Датчик разницы давления воздуха между помещениями Жалюзи с автоматической регулировкой подачи
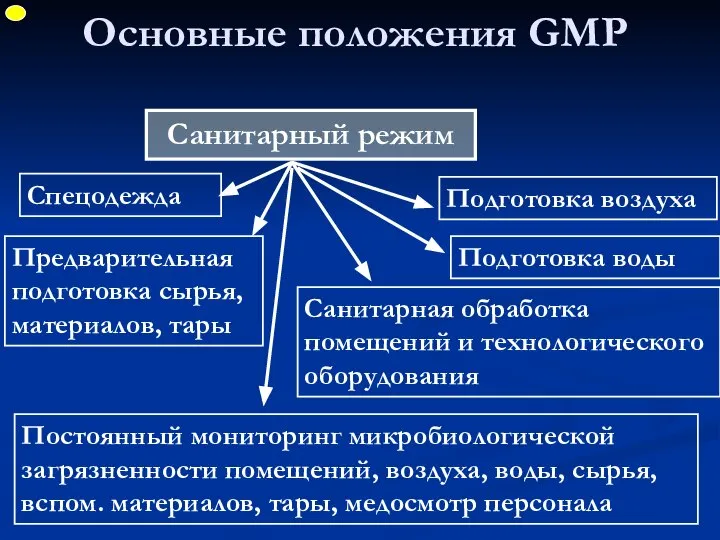
- 58. Основные положения GMP Предварительная подготовка сырья, материалов, тары Спецодежда Подготовка воздуха Подготовка воды Санитарная обработка помещений
- 59. Санитарный режим Шлюз для персонала М Шлюз для персонала Ж Вход в производственные помещения через шлюз
- 60. Устройство шлюза для персонала Входная дверь в шлюз из коридора ФУП
- 61. Устройство шлюза для персонала Комната предварительной подготовки
- 62. Раздевалка (шлюз) (вид со стороны коридора) Раздевалка (шлюз) (вид со стороны производства) Вешалки для технологической одежды
- 63. Выход из шлюза в производственные помещения Коврик пропитанный дезинфицирующим раствором Герметичная стеклянная дверь ФУП
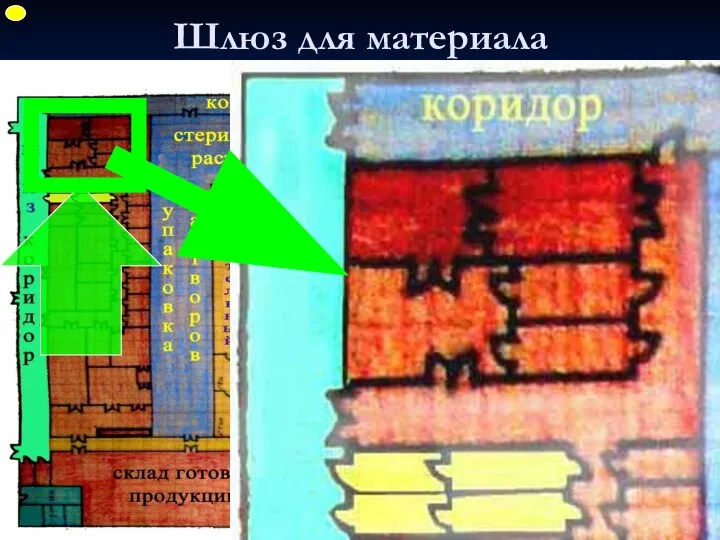
- 65. Шлюз для материала ФУП
- 66. Склад сырья и материалов (промежуточный) ФУП
- 67. 4. Документация Принципы Правильно составленная документация является важной частью системы обеспечения качества. Четкое оформление документации позволяет
- 68. 4.1. Виды документов: спецификация (specification) промышленный регламент, технологическая инструкция и инструкция по упаковке (manufacturing formulae, processing
- 69. спецификация (specification) документ, содержащий требования к материалам и продуктам, используемым или получаемым при производстве, являющийся основой
- 70. промышленный регламент, технологическая инструкция и инструкция по упаковке документы, определяющие все используемые исходные материалы и операции
- 71. 4.15. Технологические инструкции включают в себя: a) данные о месте нахождения производства и основном оборудовании; b)
- 72. инструкция, методика, процедура (procedure) документ, содержащий указания по выполнению отдельных видов операций (например, по очистке, переодеванию,
- 73. протокол на серию (record) документ, отражающий ход производства каждой серии продукции, в т.ч. разрешение на ее
- 74. 4.5. Документы следует регулярно пересматривать и актуализировать. При пересмотре документа необходимо исключить использование устаревшей версии. 4.6.
- 75. 5. Производство Принципы Для получения продукции требуемого качества технологические операции следует выполнять согласно промышленному регламенту и
- 76. 5.8. Для гарантии отсутствия отклонений за допустимые пределы следует обеспечить контроль выхода продукции и количественное сопоставление
- 79. 6. Контроль качества Принципы Контроль качества связан с отбором проб, проведением испытаний и проверок на соответствие
- 80. К документации по контролю качества относятся: - спецификации; - методики отбора проб; - методики и протоколы
- 81. Отбор проб Отбор проб должен проводиться в соответствии с утвержденными инструкциями, включающими в себя: - методику
- 82. Проведение испытаний Аналитические методики должны быть аттестованы (валидированы). Все испытания, приведенные в нормативной документации, должны быть
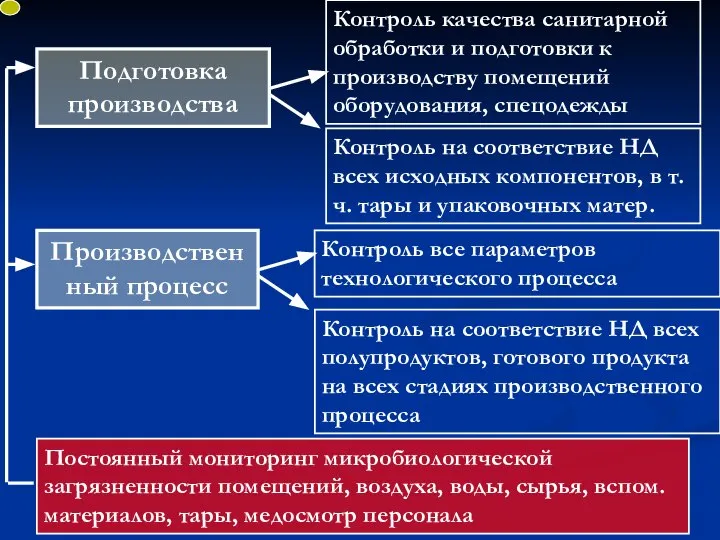
- 83. Контроль качества санитарной обработки и подготовки к производству помещений оборудования, спецодежды Постоянный мониторинг микробиологической загрязненности помещений,
- 84. Технологический контроль
- 85. Контроль инъекционных растворов перед стерилизацией
- 86. Контроль качества инъекционных растворов после стерилизации и упаковка во вторичную упаковку
- 88. 7. Работа по контрактам на производство продукции и проведение анализов Принципы Во избежание разночтений, способных привести
- 89. 8. Рекламации и отзыв продукции Принципы Все рекламации и информация, касающиеся продукции с предполагаемыми нарушениями качества,
- 90. 9. Самоинспекция Принципы Самоинспекция должна проводиться с целью проверки выполнения предприятием требований настоящего стандарта и принятия
- 91. Подготовка производственного оборудования и тары
- 92. Участок подготовки тары Участок грязной тары Обработка тары Участок чистой тары
- 93. Участок грязной тары
- 94. Участок чистой тары
- 96. Оборудование для подготовки помещений и оборудования к производственному процессу Промышленный пылесос типIFS-1/ZX-Ех Передвижной, механической очистки. Исполнение
- 97. Оборудование для подготовки помещений и оборудования к производственному процессу Промышленные установки для очистки помещений и оборудования
- 98. Оборудование для подготовки помещений и оборудования к производственному процессу Промышленные установки для очистки помещений и оборудования
- 99. Чистый раствор Грязный раствор Отжим швабры
- 101. Литература: Государственная фармакопея СССР/ М-во здравоохранения СССР.-11-е изд. - М.: Медицина, 1987.- Вып.1,2. ГОСТ Р ИСО
- 102. ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ РАЗВИТИЮ Государственное образовательное учреждение высшего профессионального образования «ПЯТИГОРСКАЯ ГОСУДАРСТВЕННАЯ ФАРМАЦЕВТИЧЕСКАЯ
- 103. Коллектив авторов выражает признательность за возможность использования в данном учебном пособии фото и видеоматериалов предприятиям:
- 105. Скачать презентацию




















































































 Фирма
Фирма Наиболее уязвимые места, с которых начинается разрушаться здания
Наиболее уязвимые места, с которых начинается разрушаться здания День Великомучениці Катерини
День Великомучениці Катерини Hobbys. Was machst du gern. Что ты любишь делать
Hobbys. Was machst du gern. Что ты любишь делать Презентация "Школа искусств" - скачать презентации по МХК
Презентация "Школа искусств" - скачать презентации по МХК من عجائب القرآن الكريم
من عجائب القرآن الكريم Театральная педагогика в школе
Театральная педагогика в школе  Презентация_____
Презентация_____ Экологические характеристики ДВС
Экологические характеристики ДВС  Организм человека как единая саморазвивающаяся биологическая система (Лекция 4)
Организм человека как единая саморазвивающаяся биологическая система (Лекция 4) Политика как общественное явление и научная теория
Политика как общественное явление и научная теория Река. Найди 10 отличий - презентация для начальной школы
Река. Найди 10 отличий - презентация для начальной школы Cервисная деятельность в годы великой отечественной войны
Cервисная деятельность в годы великой отечественной войны Производство по пересмотру вступивших в законную силу судебных актов по новым или вновь открывшимся обстоятельствам
Производство по пересмотру вступивших в законную силу судебных актов по новым или вновь открывшимся обстоятельствам Денежно-кредитная политика Цели, инструменты и методы
Денежно-кредитная политика Цели, инструменты и методы Дуополия Курно и Штакельберга
Дуополия Курно и Штакельберга Система органов государственной власти в Российской Федерации
Система органов государственной власти в Российской Федерации Туркеста́но-Сиби́рская магистра́ль
Туркеста́но-Сиби́рская магистра́ль МЕТОДЫ ПОИСКОВ МЕСТОРОЖДЕНИЙ ПОЛЕЗНЫХ ИСКОПАЕМЫХ
МЕТОДЫ ПОИСКОВ МЕСТОРОЖДЕНИЙ ПОЛЕЗНЫХ ИСКОПАЕМЫХ  СИСТЕМА КАЧЕСТВА В ТЕПЛОСНАБЖЕНИИ
СИСТЕМА КАЧЕСТВА В ТЕПЛОСНАБЖЕНИИ Анализ работы СтатГрад
Анализ работы СтатГрад Арабская лингвистическая традиция
Арабская лингвистическая традиция Сохранение и укрепление здоровья - важная часть подготовки юношей до 18 лет к военной службе и трудовой деятельности
Сохранение и укрепление здоровья - важная часть подготовки юношей до 18 лет к военной службе и трудовой деятельности Россельхозбанк
Россельхозбанк Живопись импрессионизма
Живопись импрессионизма  Нежилое помещение. Фото (3)
Нежилое помещение. Фото (3) Планирование ремонтно-строительного производства при реконструкции и капитальном ремонте
Планирование ремонтно-строительного производства при реконструкции и капитальном ремонте Закаливание организма
Закаливание организма