Поволжское управление министерства образования и науки Самарской области Анализ результатов ЕГЭ по химии 2010 (окружной семин
Содержание
- 2. Результаты ЕГЭ 2010 Граница минимального балла -33 тестовых балла (12 первичных баллов) Уровни оценивания: неудовлетворительный –
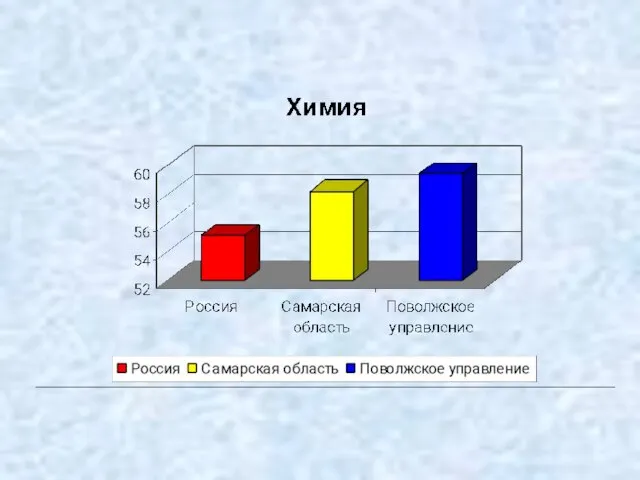
- 3. Самарская область Число учащихся - 1077 человек Средний балл -58,2 100 баллов – 8 учащихся 24
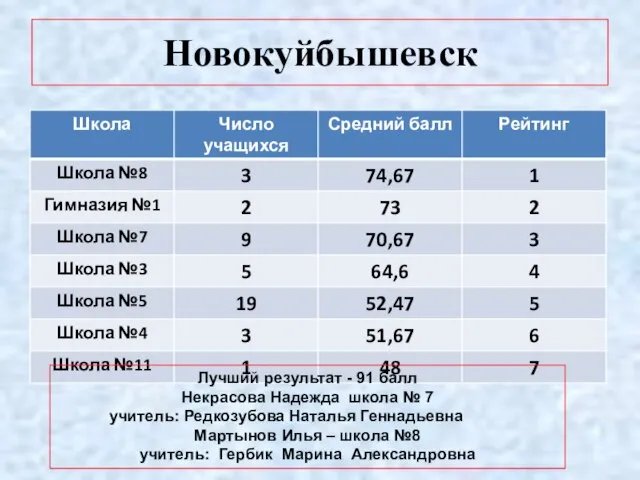
- 4. Новокуйбышевск Лучший результат - 91 балл Некрасова Надежда школа № 7 учитель: Редкозубова Наталья Геннадьевна Мартынов
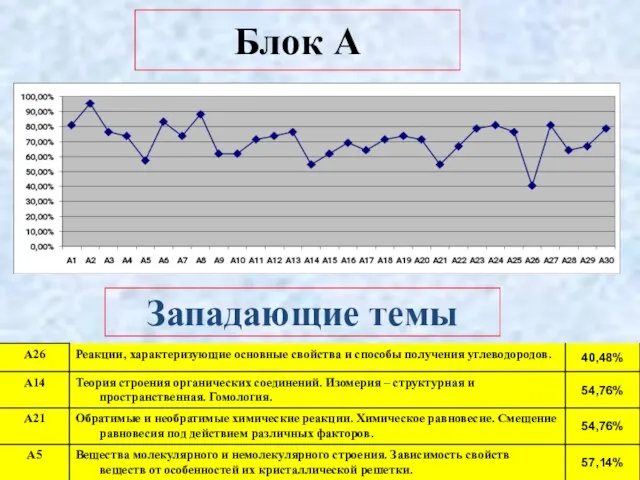
- 5. Блок А Западающие темы
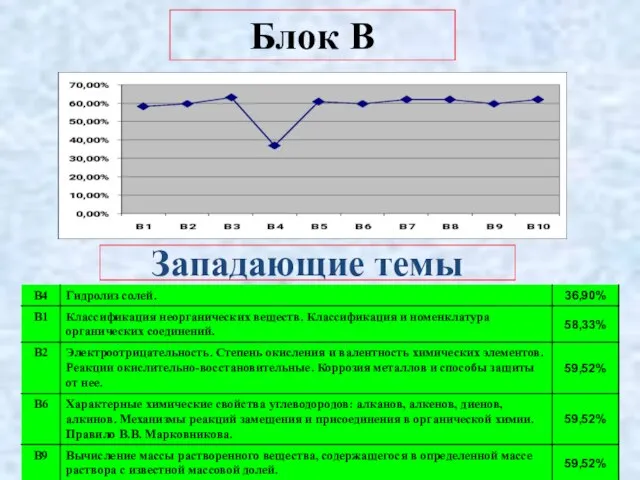
- 6. Блок В Западающие темы
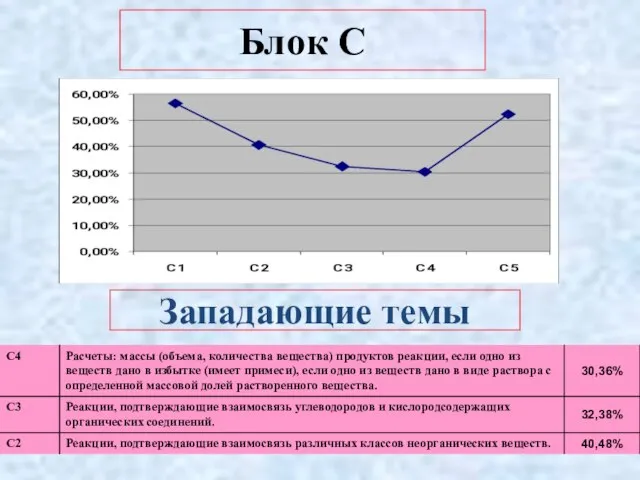
- 7. Блок С Западающие темы
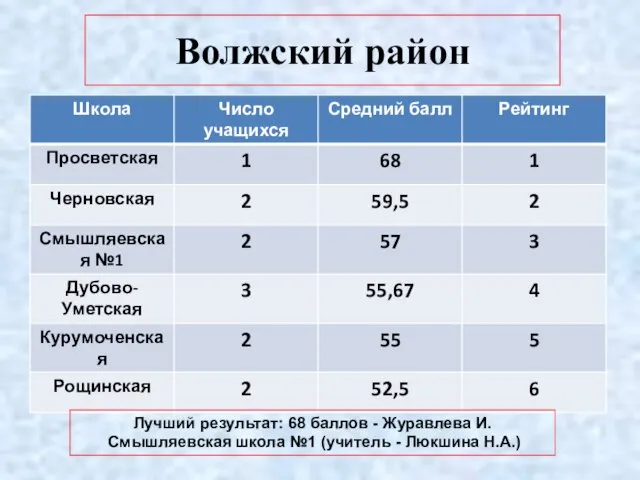
- 8. Волжский район Лучший результат: 68 баллов - Журавлева И. Смышляевская школа №1 (учитель - Люкшина Н.А.)
- 9. Блок А Западающие темы
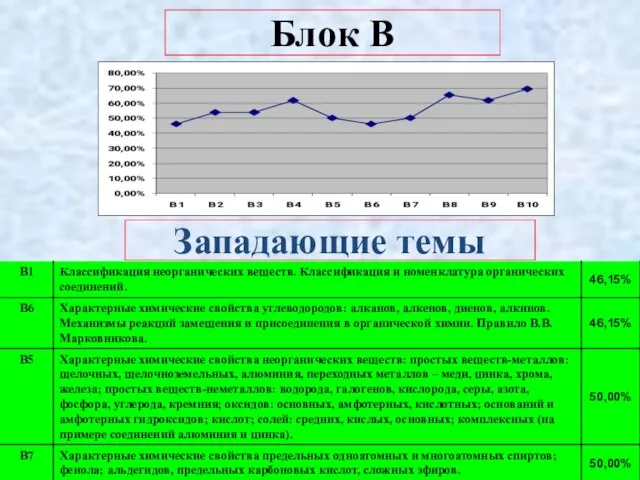
- 10. Блок В Западающие темы
- 11. Блок С Западающие темы
- 13. Западающие темы
- 14. Химическая связь (А 4) Ошибки: полярность связи; понятие о типах связи в органических веществах
- 15. Степень окисления (А 4, В 2) Ошибки: определение степени окисления в 4-х элементных соединениях; не учитывался
- 16. Кристаллические решетки (А 5) Ионную кристаллическую решетку имеет: 1)Хлор 2)хлорид цезия 3)хлорид фосфора (III) 4)оксид углерода
- 17. Свойства простых веществ и неорганических соединений (А 9) Ошибки: не используют ряд активности металлов; свойства амфотерных
- 18. Химические свойства неорганических веществ (А 12) Химическая реакция возможна между Zn и CuCl2 2) Fe и
- 19. Изомерия органических соединений (А 14) Изомером 2-метилпропанола-1 является 1)метилизопропиловый эфир 2) пропанол-1 3) 2-метилбутанол-1 4)пропандиол-1,2 Ошибки:
- 20. Химическое равновесие (А 21) Ошибки: незнание влияния концентрации реагирующих веществ на смещение равновесия
- 21. Общие химические свойства органических веществ (А 26) С бромной водой взаимодействует каждое из двух веществ: 1)этилен
- 22. Химические свойства органических веществ (А27) Альдегид получается при гидратации 1)этина 2) пропина 3) бутина-1 4) пентина-1
- 23. Свойства амфотерных гидроксидов (В 3) Ошибки: определение продуктов взаимодействия амфотерных гидроксидов со щелочами при сплавлении и
- 24. Гидролиз (В4) Ошибки: неправильное определение силы кислот и оснований как электролитов
- 25. Свойства угловодородов (В 6) Ошибки: не знают реакции альдегида со спиртами Ошибки: не знают отношение амина
- 26. Свойства кислородсодержащих органических веществ (В 7) В отличие от фенола метанол 1)взаимодействует с растворами щелочей 2)вступает
- 27. Свойства неорганических веществ (С 2) Даны вещества: йод, азотная кислота (конц.), сероводород и кислород. Написать 4
- 28. Комбинированная задача(С4) Ошибки: определение избытка вещества и расчет общей массы раствора с исключением выделившегося газа
- 30. Скачать презентацию




















 Силова електроніка
Силова електроніка C++ Classes How to Create and Use Them (Constructor, Destructor)
C++ Classes How to Create and Use Them (Constructor, Destructor) Молодежная мода в 2018 году
Молодежная мода в 2018 году Объекты авторского права
Объекты авторского права Один путь к Богу
Один путь к Богу Моя любимая профессия техник-механик
Моя любимая профессия техник-механик Встреча с медведем
Встреча с медведем Объект и предмет исследования. Гипотеза. Формулировка исходной гипотезы.
Объект и предмет исследования. Гипотеза. Формулировка исходной гипотезы. Партия «Единая Россия» г. Уфы
Партия «Единая Россия» г. Уфы 02.06 Сыр
02.06 Сыр Веселые щебеталочки или говорим на птичьем языке
Веселые щебеталочки или говорим на птичьем языке  Презентация "Герой и защитник Отечества" - скачать презентации по МХК
Презентация "Герой и защитник Отечества" - скачать презентации по МХК Программа Приток
Программа Приток Элитарная демократия и корпоративизм Выполнил: Бродовский М.А. Григоров Г.С. Т-082
Элитарная демократия и корпоративизм Выполнил: Бродовский М.А. Григоров Г.С. Т-082 Что такое ГТО
Что такое ГТО Методы синтеза и анализа цифровых фильтров. Метод окон для синтеза КИХ-фильтров
Методы синтеза и анализа цифровых фильтров. Метод окон для синтеза КИХ-фильтров Вертикальное слияние Выполнили: Минниахметова М. Сочнева А.
Вертикальное слияние Выполнили: Минниахметова М. Сочнева А. Техническая механика. Червячные передачи
Техническая механика. Червячные передачи Основные международные НПА, с требованием которых необходимо соотносить семейное право России
Основные международные НПА, с требованием которых необходимо соотносить семейное право России Награды современной России Автор: Преподаватель - организатор ОБЖ МОУ СОШ № 175 Советского района города Казани Е.А.Майсейков На
Награды современной России Автор: Преподаватель - организатор ОБЖ МОУ СОШ № 175 Советского района города Казани Е.А.Майсейков На Создание графических приложений
Создание графических приложений 09.08.11И. О. Орлов, СПФКС-91 The LHC: Citius, Altius, Fortius… James Gillies, Head, communication group, CERN 27 November 2006 Большой адронный коллайдер. - презентация
09.08.11И. О. Орлов, СПФКС-91 The LHC: Citius, Altius, Fortius… James Gillies, Head, communication group, CERN 27 November 2006 Большой адронный коллайдер. - презентация Бил Клинтън 42-ри президент на САЩ (1993-2001)
Бил Клинтън 42-ри президент на САЩ (1993-2001) ДОЛИ И ДРОБИ 4 класс - презентация для начальной школы_
ДОЛИ И ДРОБИ 4 класс - презентация для начальной школы_ Презентация Теории происхождения права
Презентация Теории происхождения права Виды Мышления
Виды Мышления Преподобный Тихон Калужский
Преподобный Тихон Калужский Николай Коперник. Теория действительности
Николай Коперник. Теория действительности