Содержание
- 2. Лигандом может быть как низкомолекулярное, так и высокомолекулярное (макромолекула) вещество, в том числе и другой белок.
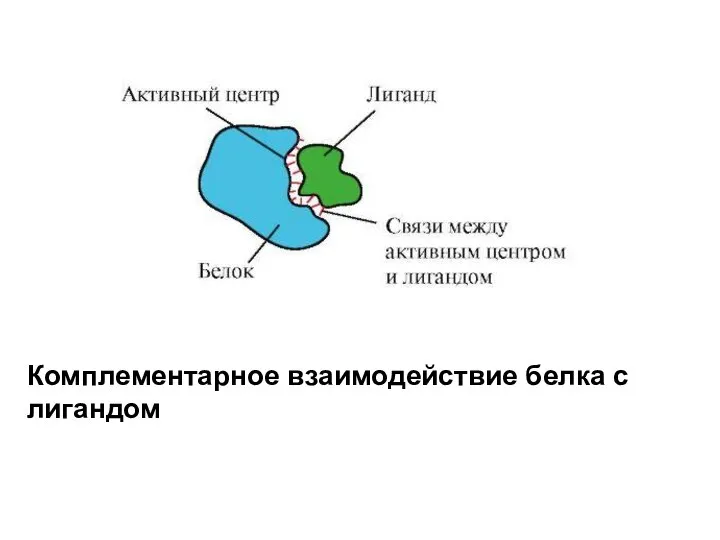
- 3. Высокая специфичность взаимодействия белка с лигандом обеспечивается комплементарностью структуры активного центра структуре лиганда.
- 4. Комплементарность - это пространственное и химическое соответствие взаимодействующих поверхностей. Активный центр должен не только пространственно соответствовать
- 5. Комплементарное взаимодействие белка с лигандом
- 8. КЛАССИФИКАЦИЯ БЕЛКОВ 1. Простые белки состоят только из аминокислот. 2. Сложные белки (холопротеины) содержат белковую часть
- 9. В качестве простетической группы могут выступать различные органические (липиды, углеводы) и неорганические (металлы) вещества. Связь между
- 10. Сложные белки - хромопротеины - нуклеопротеины - липопротеины - фосфопротеины - гликопротеины - металлопротеины
- 11. Металлопротеинам можно отнести холоферменты, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеинов есть белки, выполняющие депонирующие
- 12. Металлопротеины часто являются ферментами. Ионы металлов в этом случае: - участвуют в ориентации субстрата в активном
- 13. К ферментативным металлопротеинам относятся белки, содержащие например: - медь – цитохромоксидаза, в комплексе с другими ферментами
- 14. Ферритин
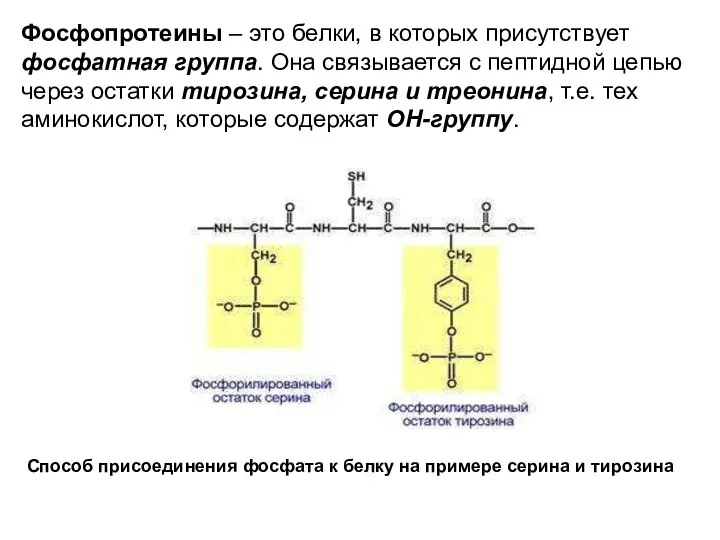
- 15. Фосфопротеины – это белки, в которых присутствует фосфатная группа. Она связывается с пептидной цепью через остатки
- 16. Фосфорная кислота может выполнять: - Структурную роль, придавая заряд, растворимость и изменяя свойства белка, например, в
- 17. Фосфорилирование — процесс переноса остатка фосфорной кислоты от фосфорилирующего агента-донора к субстрату, как правило, катализируемый ферментами
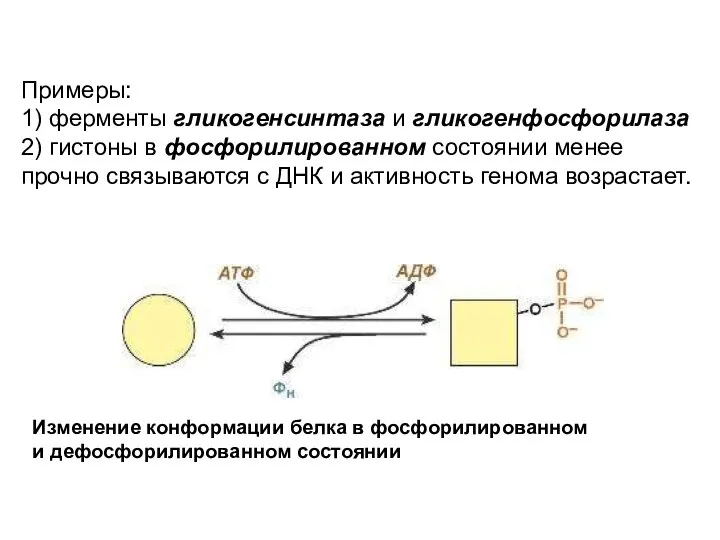
- 18. Примеры: 1) ферменты гликогенсинтаза и гликогенфосфорилаза 2) гистоны в фосфорилированном состоянии менее прочно связываются с ДНК
- 19. Липопротеины содержат в качестве простетической части нековалентно связанные липиды. Липиды, в частности жиры, холестерол и его
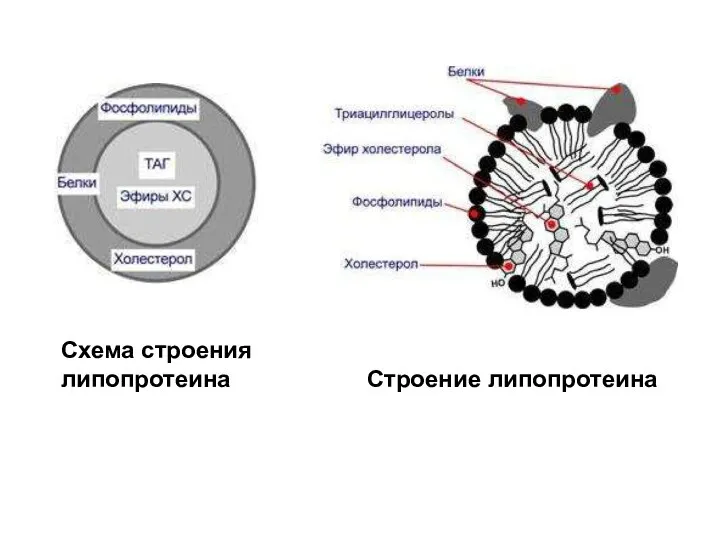
- 20. Все липопротеины имеют сходное строение: ядро состоит из гидрофобных молекул: триацилглицеролов, эфиров холестерола, а на поверхности
- 21. Схема строения липопротеина Строение липопротеина
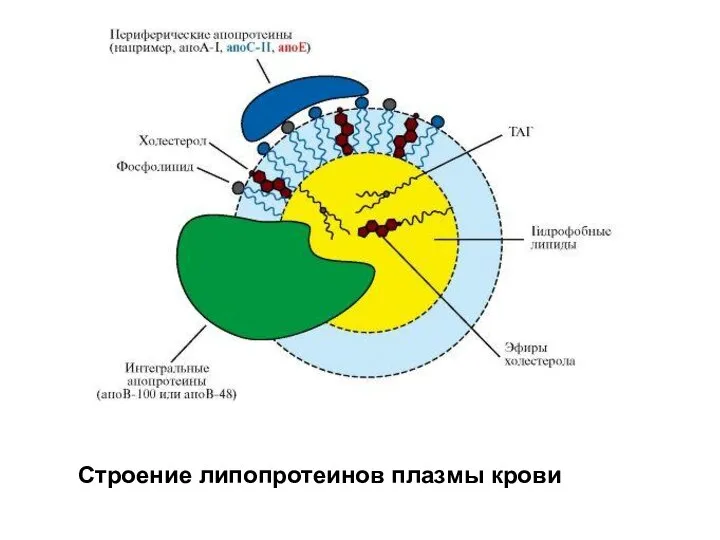
- 22. Строение липопротеинов плазмы крови
- 23. Выделяют четыре основных класса липопротеинов: -липопротеины высокой плотности (ЛПВП), -липопротеины низкой плотности (ЛПНП), -липопротеины очень низкой
- 25. Гликопротеины или, гликоконъюгаты – это белки, содержащие углеводный компонент, ковалентно присоединенный к полипептидной основе. Содержание углеводов
- 26. Гликопротеины ● доля углеводов ● углеводные цепи содержат не более 15 звеньев, ● углевод имеет нерегулярное
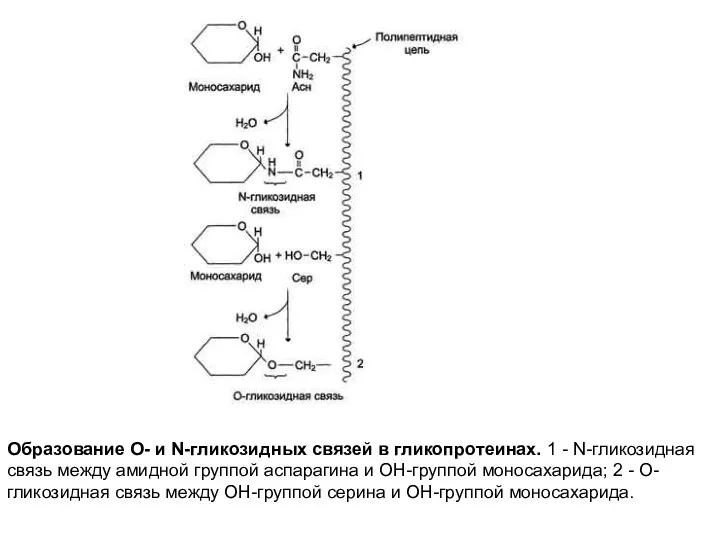
- 27. Для гликопротеинов характерно невысокое содержание углеводов, которые присоединены: - N-гликозидной связью к NН2-группе какого-нибудь аминокислотного остатка,
- 28. Образование О- и N-гликозидных связей в гликопротеинах. 1 - N-гликозидная связь между амидной группой аспарагина и
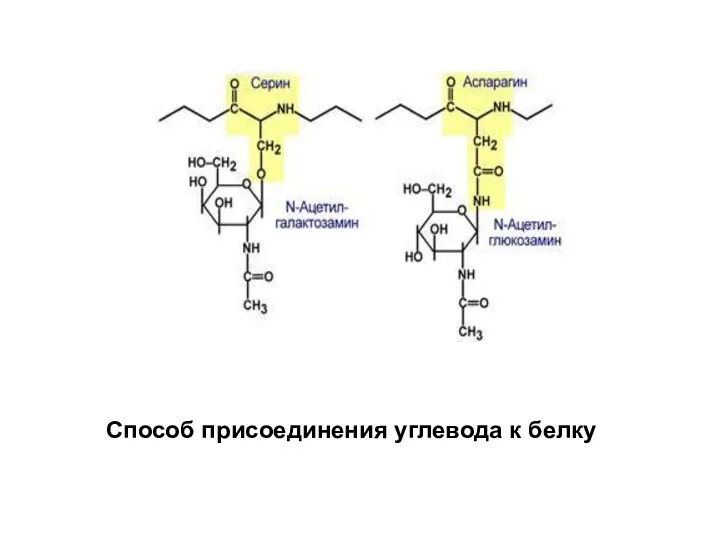
- 29. Способ присоединения углевода к белку
- 30. Функцией гликопротеинов являются: 1. Структурная – клеточная стенка бактерий, костный матрикс, например, коллаген, эластин. 2. Защитная
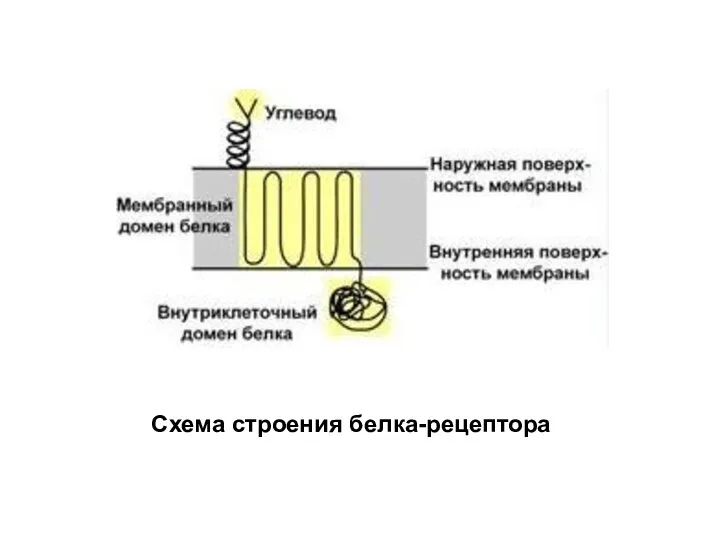
- 31. Схема строения белка-рецептора
- 32. Хромопротеины — собирательное название сложных белков с окрашенными простетическими группами различной химической природы. гемопротеины (содержат гем),
- 33. Флавопротеины - это ферменты окислительно-восстановительных реакций. Содержат производные витамина В2 флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Связываются
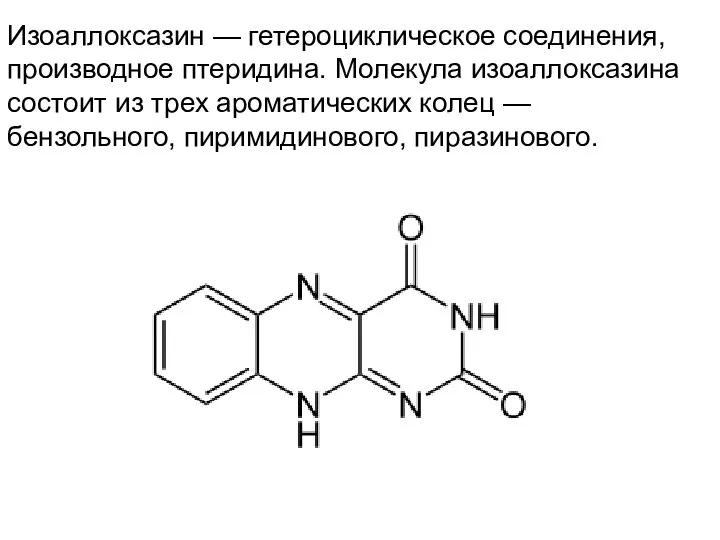
- 34. Изоаллоксазин — гетероциклическое соединения, производное птеридина. Молекула изоаллоксазина состоит из трех ароматических колец — бензольного, пиримидинового,
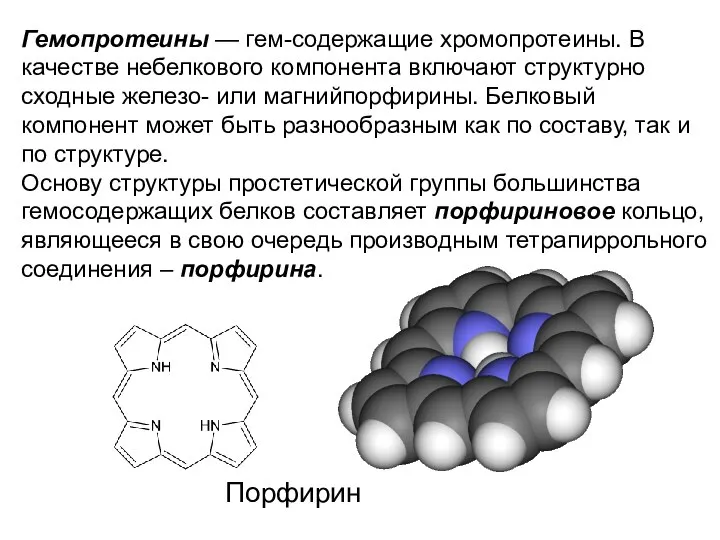
- 35. Гемопротеины — гем-содержащие хромопротеины. В качестве небелкового компонента включают структурно сходные железо- или магнийпорфирины. Белковый компонент
- 36. Порфириновое кольцо способно образовывать координационные соединения с различными ионами металлов. В результате комплексообразования формируются металлопорфирины: содержащие
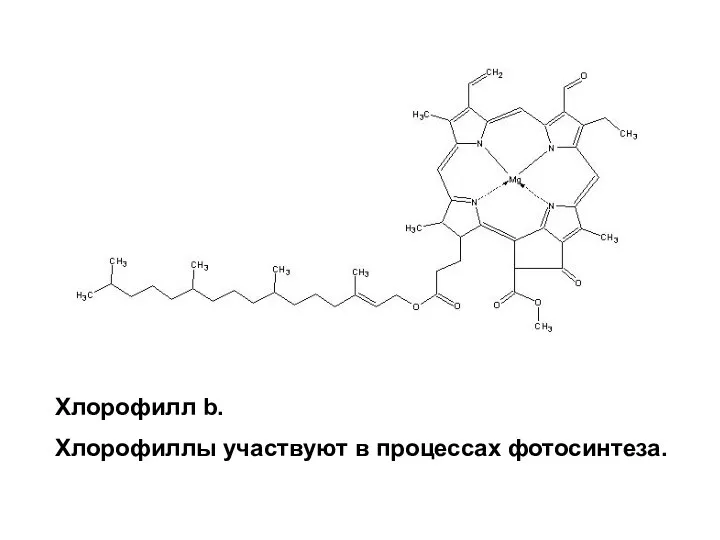
- 37. Хлорофилл b. Хлорофиллы участвуют в процессах фотосинтеза.
- 38. Цитохромы различаются аминокислотным составом пептидных цепей, числом цепей и разделяются на типы а, b, с, d.
- 39. Миоглобин (Мв) - белок, находящийся в красных мышцах, основная функция которого - создание запасов О2, необходимых
- 40. Формирование конформации Мв. В красных мышцах на рибосомах в ходе трансляции идет синтез первичной структуры Мв,
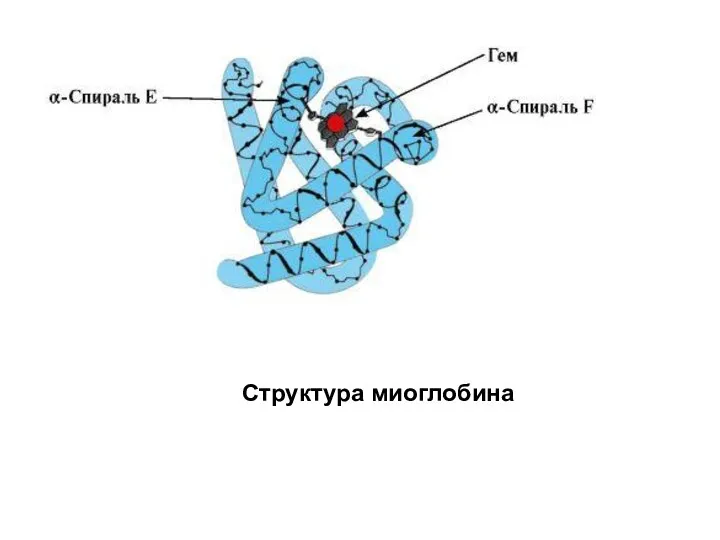
- 41. Структура миоглобина
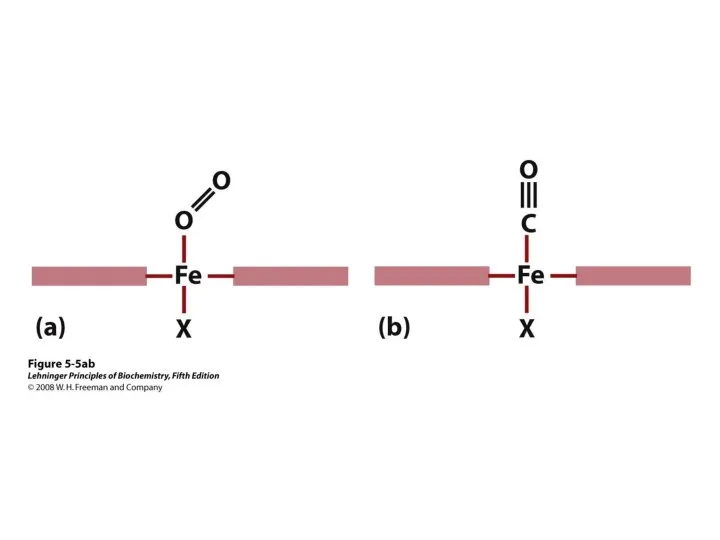
- 42. Особенности строения и функционирования активного центра Мв. Активный центр Мв сформирован преимущественно гидрофобными радикалами аминокислот, далеко
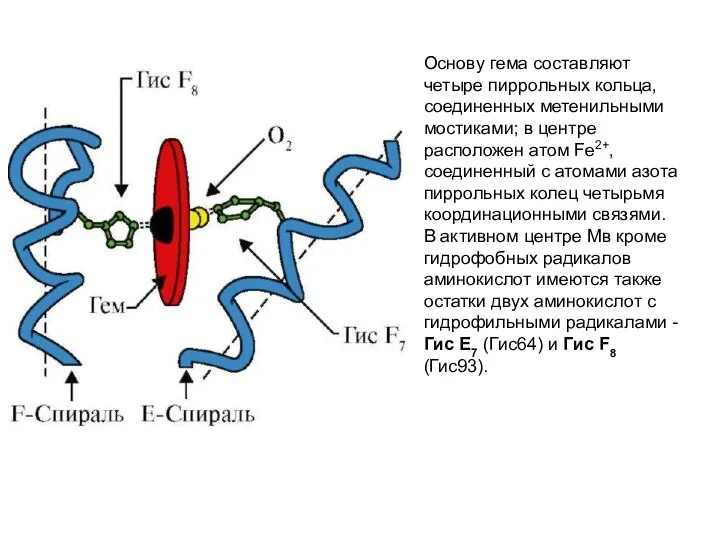
- 43. Основу гема составляют четыре пиррольных кольца, соединенных метенильными мостиками; в центре расположен атом Fe2+, соединенный с
- 44. Гис F8 образует координационную связь с Fe2+ и прочно фиксирует гем в активном центре. Гис Е7
- 45. Олигомерное строение Нв и регуляция сродства Нв к О2 лигандами. Гемоглобины человека - семейство белков, так
- 46. Нв А - белок, родственный миоглобину (Мв), содержится в эритроцитах взрослого человека. Строение его отдельных протомеров
- 47. Олигомерная структура гемоглобина
- 48. Каждый протомер Нв связан с небелковой частью - гемом и соседними протомерами. Соединение белковой части Нв
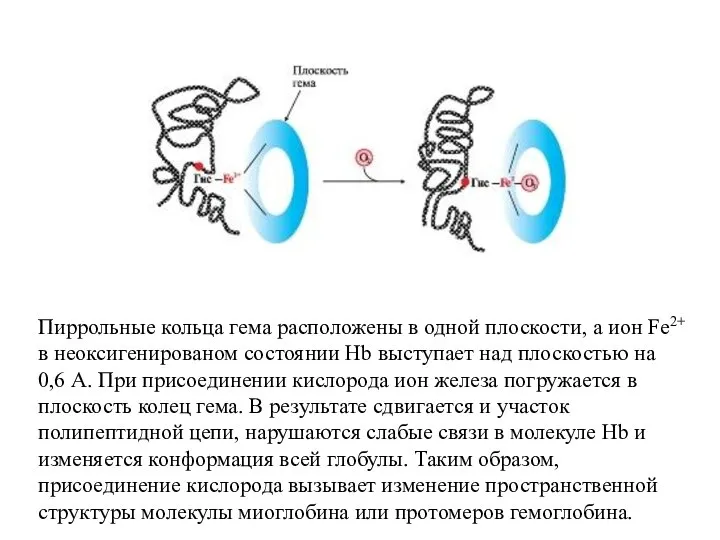
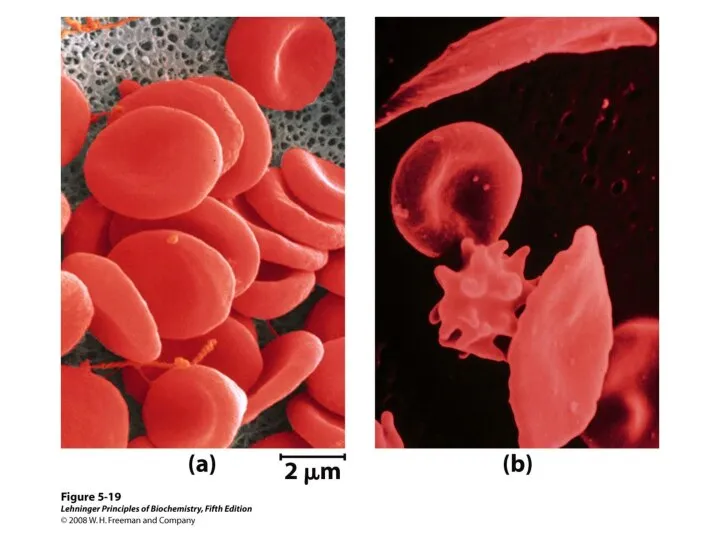
- 50. Пиррольные кольца гема расположены в одной плоскости, а ион Fe2+ в неоксигенированом состоянии Hb выступает над
- 51. Гемоглобин может существовать как в свободной (дезоксигемоглобин), так и в оксигенированной форме, присоединяя до 4 молекул
- 52. Кооперативные изменения конформации молекулы гемоглобина при взаимодействии с кислородом
- 53. В тканях, где содержание кислорода ниже, наоборот, отщепление каждой молекулы О2 облегчает освобождение последующих. Таким образом,
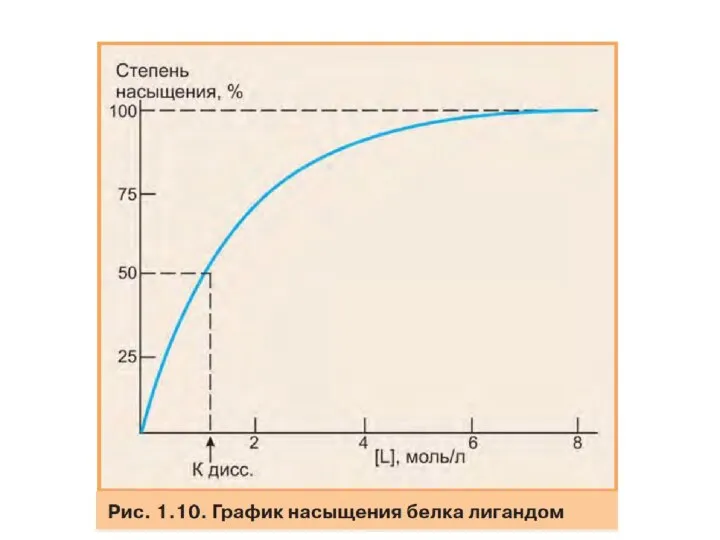
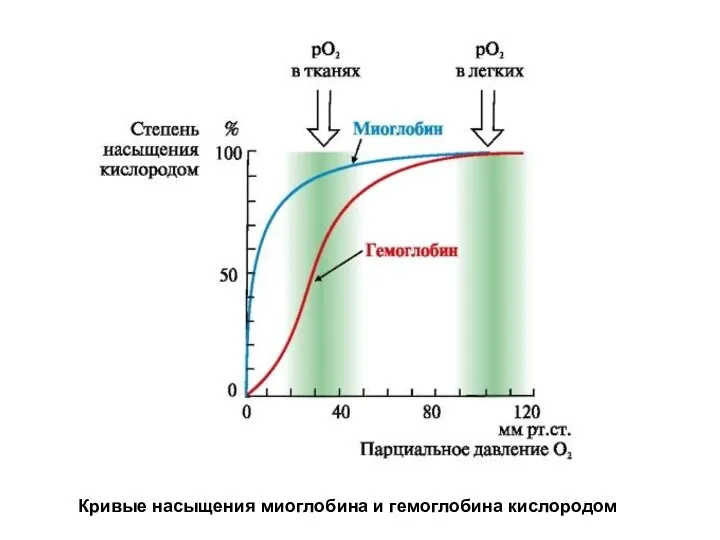
- 54. Взаимодействие обоих белков (Mb и Hb) с кислородом зависит от его парциального давления в тканях. Эта
- 55. Кривые насыщения миоглобина и гемоглобина кислородом
- 56. CO2 и Н+, образующиеся при катаболизме органических веществ, уменьшают сродство гемоглобина к О2 пропорционально их концентрации.
- 57. Ионы Н+ способны присоединятся к радикалам Гис146 в β-цепях гемоглобина, т.е. в участках, удаленных от гема.
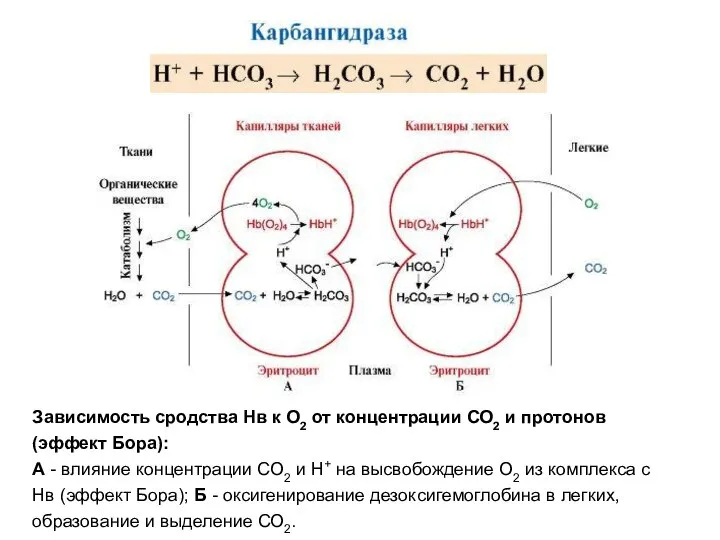
- 58. Зависимость сродства Нв к О2 от концентрации СО2 и протонов (эффект Бора): А - влияние концентрации
- 59. Образовавшийся СО2 поступает в альвеолярное пространство и удаляется с выдыхаемым воздухом. Таким образом, количество высвобождаемого гемоглобином
- 60. Изменение функциональной активности белка при взаимодействии с другими лигандами вследствие конформационных изменений называется аллостерической регуляцией, а
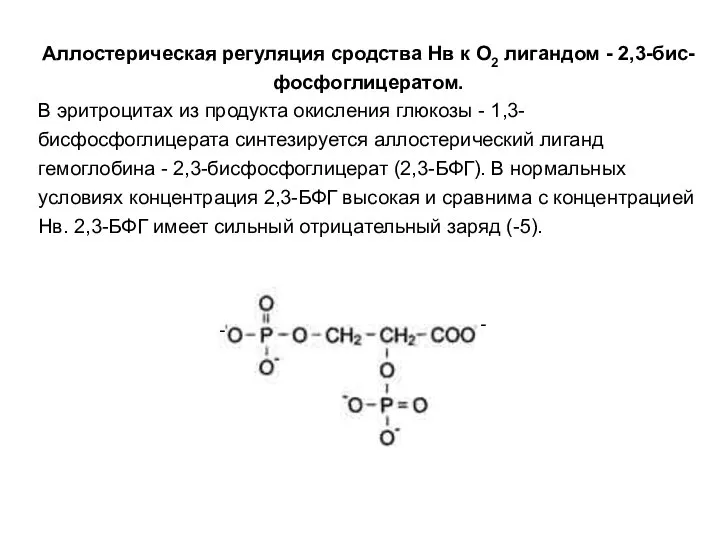
- 61. Аллостерическая регуляция сродства Нв к О2 лигандом - 2,3-бис-фосфоглицератом. В эритроцитах из продукта окисления глюкозы -
- 62. В центре тетрамерной молекулы гемоглобина находится полость. Ее образуют аминокислотные остатки всех четырех протомеров. В капиллярах
- 63. Центр связывания БФГ находится в положительно заряженной полости между 4 протомерами гемоглобина. Взаимодействие БФГ с центром
- 65. Таким образом, олигомерные белки обладают новыми по сравнению с мономерными белками свойствами. Присоединение лигандов на участках,
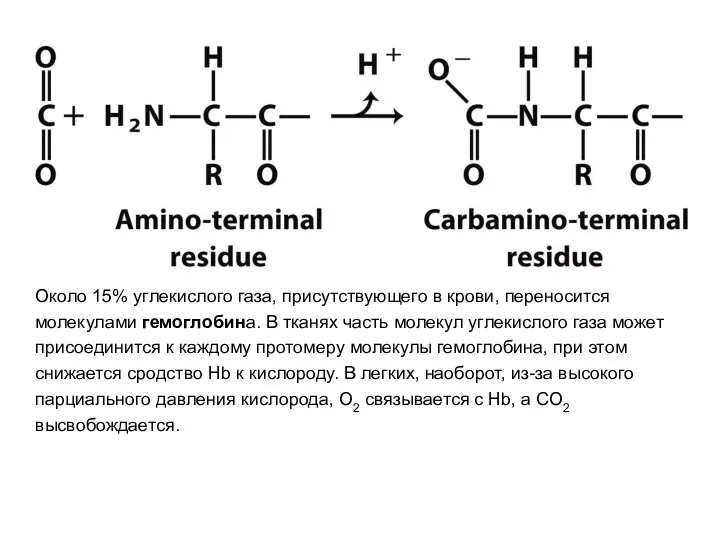
- 66. Около 15% углекислого газа, присутствующего в крови, переносится молекулами гемоглобина. В тканях часть молекул углекислого газа
- 69. Скачать презентацию













































 Функциональные блоки мозга
Функциональные блоки мозга Домашня аптечка
Домашня аптечка  Ученые – биологи, внесшие большой вклад в развитие современных наук о человеке
Ученые – биологи, внесшие большой вклад в развитие современных наук о человеке  Мал азықтық дақылдар. Еркекшөп
Мал азықтық дақылдар. Еркекшөп Презентация на тему Жилища животных
Презентация на тему Жилища животных  Ягуар
Ягуар Презентация на тему Влияние асоциальных факторов на экосистему человека
Презентация на тему Влияние асоциальных факторов на экосистему человека Мхи. Чем отличаются высшие растения от низших?
Мхи. Чем отличаются высшие растения от низших? Митоз и мейоз клетки
Митоз и мейоз клетки Выращивание рассады бархатцев
Выращивание рассады бархатцев Здоров'я людини та навколишнє середовище
Здоров'я людини та навколишнє середовище  Деревья и кустарники
Деревья и кустарники Эволюция человека
Эволюция человека Як бачать тварини?
Як бачать тварини? Красные и бурые водоросли
Красные и бурые водоросли Презентация на тему "Магнолия" - скачать бесплатно презентации по Биологии
Презентация на тему "Магнолия" - скачать бесплатно презентации по Биологии Ген. Хромосома
Ген. Хромосома Генетика человека и ее значение для медицины и здравоохранения (урок биологии в 11 классе)
Генетика человека и ее значение для медицины и здравоохранения (урок биологии в 11 классе) Arthropod parasites
Arthropod parasites Презентация на тему "Путешествие по пищеварительной системе" - скачать презентации по Биологии
Презентация на тему "Путешествие по пищеварительной системе" - скачать презентации по Биологии Коты. Кельтская кошка
Коты. Кельтская кошка Lepechin Ivan Ivanovich
Lepechin Ivan Ivanovich Понятие филэмбриогенезов. Практическая значимость для врача
Понятие филэмбриогенезов. Практическая значимость для врача Ткани человека
Ткани человека Соединения костей черепа, позвонков, ребер, грудины
Соединения костей черепа, позвонков, ребер, грудины Sex Dimorphism of C. aurantimaculata
Sex Dimorphism of C. aurantimaculata Презентация на тему "Богатыри" - скачать бесплатно презентации по Биологии
Презентация на тему "Богатыри" - скачать бесплатно презентации по Биологии ЭНДОКРИННАЯ СИСТЕМА. Тесты. Шильцова Наталья Петровна - учитель биологии МОУ СОШ№9, пос. Восточно-Горняцкий(Горняцкий) г Белая Кали
ЭНДОКРИННАЯ СИСТЕМА. Тесты. Шильцова Наталья Петровна - учитель биологии МОУ СОШ№9, пос. Восточно-Горняцкий(Горняцкий) г Белая Кали