Содержание
- 2. Ферменты, или энзимы, представляют собой высокоспециализированный класс веществ белковой природы, используемый живыми организмами для осуществления с
- 3. КЛАССИФИКАЦИЯ ФЕРМЕНТОВ И НОМЕНКЛАТУРА Первоначально ферментам давали названия, образуемые путем добавления окончания -аза к на- названию
- 4. Номенклатура, введенная Международным биохимическим союзом (IUB), на первый взгляд кажется сложной и громоздкой, но зато она
- 5. 1. Реакции и ферменты, которые их катализируют, подразделяются на шесть классов, в каждом из которых имеется
- 6. 4. Каждый фермент имеет кодовый номер по классификации ферментов (КФ): первая цифра характеризует класс реакции, вторая
- 7. 1.Оксидоредуктазы.Ферменты,катализирующие окислительно-восстановительные реакции с участием двух субстратов, S и S': S (восст)+S`(окисл) = S(окисл) + S`
- 8. 2. Трансферазы. Ферменты, катализирующие перенос группы G (отличной от атома водорода) с субстрата S на субстрат
- 9. 3. Гидролазы. Ферменты, катализирующие гидролиз эфирных, сложноэфирных, пептидных и гликозильных связей, кислотных ангидридов, связей С— С,
- 10. 4. Лиазы ферменты, отщепляющие группы от субстратов по негидролитическому механизму, с обра3ованием двойных связей. Ферменты, действующие
- 11. 5. Изомеразы. В этот класс включены все фер- менты, катализирующие взаимопревращения оптических, геометрических и позиционных изомеров.
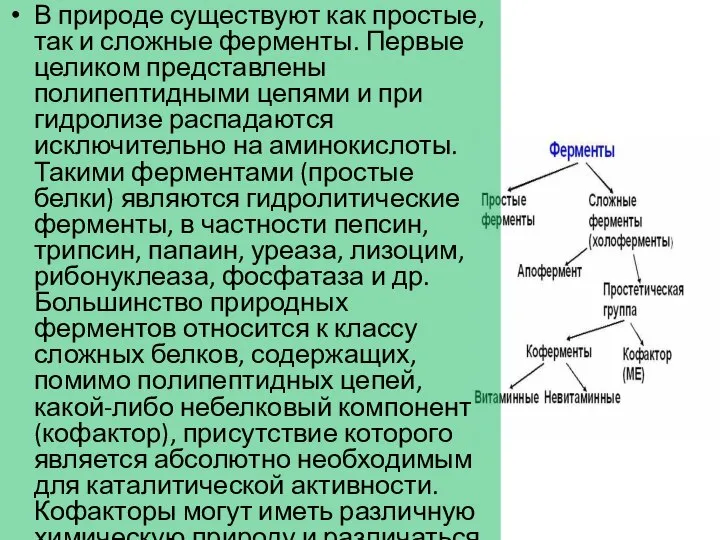
- 12. В природе существуют как простые, так и сложные ферменты. Первые целиком представлены полипептидными цепями и при
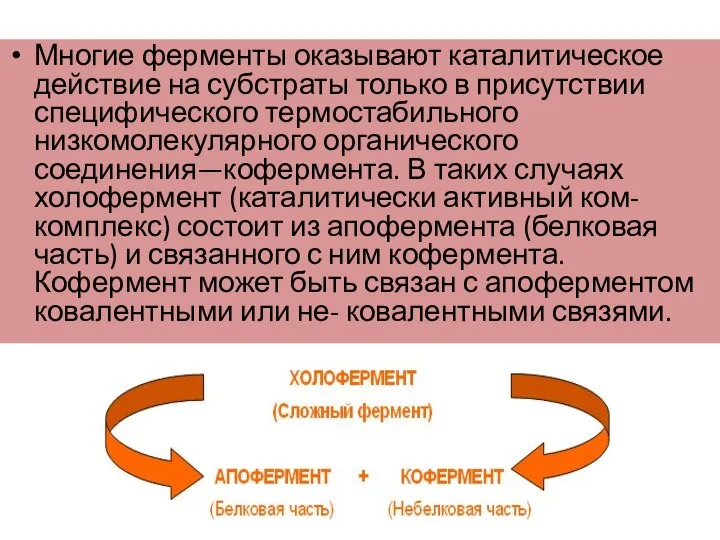
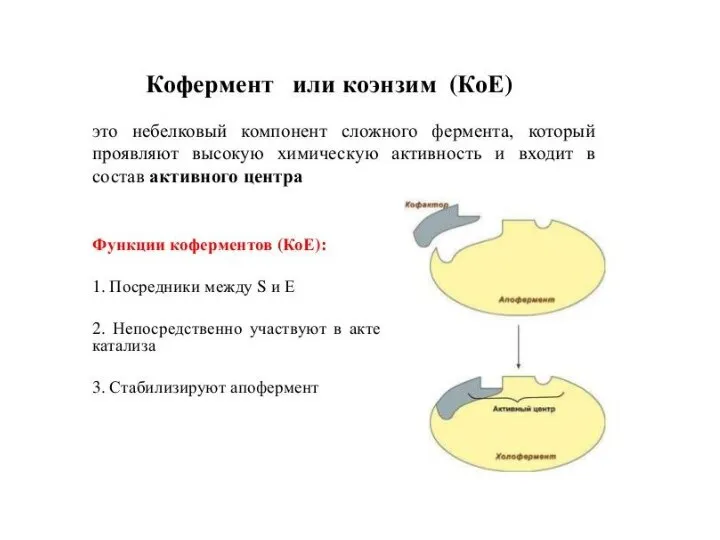
- 13. Многие ферменты оказывают каталитическое действие на субстраты только в присутствии специфического термостабильного низкомолекулярного органического соединения—кофермента. В
- 14. Коферменты, участвующие в переносе любых групп, кроме атомов водорода: Сахарофосфаты CoASH Тиаминпирофосфат Пиридоксальфосфат Фолиатные коферменты Биотин
- 16. Под активным центром подразумевают уникальную комбинацию аминокислотных остатков в молекуле фермента, обеспечивающую непосредственное связывание ее с
- 17. Изоферменты, или изоэнзимы,– это множественные формы фермента, катализирующие одну и ту же реакцию, но отличающиеся друг
- 18. Ферментативная активность зависит в основном от следующих факторов: концентрация фермента и субстрата, температура, рН, присутствие ингибиторов.
- 19. рН Умеренные изменения рН оказывают влияние на ионное состояние фермента, а зачастую и субстрата. Как показывают
- 20. Энзимодиагностика Энзимодиагностика – это исследование активности ферментов плазмы крови, мочи, слюны с целью диагностики тех или
- 21. При многих заболеваниях происходит повреждение клеток, и их содержимое, в том числе и ферменты, высвобождаются в
- 22. Ферментный анализ обычно основан на измерении каталитической активности фермента, а не концентрации самого ферментного белка. Поскольку
- 23. Ферменты, имеющие диагностическое значение
- 24. Щелочная фосфатаза (ЩФ) ЩФ присутствует в высоких концентрациях в печени, костях (остеобласты), плаценте и кишечном эпителии.
- 25. Концентрация фермента в плазме высока при рождении, но затем быстро падает. Тем не менее она остается
- 26. Концентрации ЩФ, превышающие верхний предел нормы в 10 раз, могут наблюдаться при тяжелой болезни Педжета, рахите
- 28. Кислая фосфатаза Этот фермент присутствует в высоких концентрациях в предстательной железе, и его повышенная концентрация в
- 29. Трансаминазы Два вида трансаминаз (точнее, аминотрансфераз) находят применение в диагностической энзимологии. Это аспартаттрансаминаза (АсАТ) и аланинтрансаминаза
- 30. Очень высокая активность АлАТ, иногда превышающая верхнюю границу нормы в 100 раз, наблюдается при тяжелых поражениях
- 31. При инфаркте миокарда активность АсАТ плазмы начинает повышаться примерно через 12 ч после инфаркта, достигая пика
- 32. Причины повышения активности трансаминаз плазмы Превышение верхней границы нормы более, чем в 10 раз: Острый гепатит
- 33. При большинстве заболеваний, связанных с повышением концентрации АсАТ, наблюдается одновременный, хотя и менее высокий, подъем концентрации
- 34. Только изредка встречаются концентрации, более чем в 20 раз превышающие верхний предел нормы, и наиболее вероятно
- 35. Y-Глутамилтрансфераза (ГГТ) Данный фермент присутствует в высоких концентрациях в печени, почках и поджелудочной железе. Его активность
- 36. Y-Глутамилтрансфераза (ГГТ) Активность ГГТ в плазме возрастает при отсутствии заболеваний печени у пациентов, принимающих антиконвульсанты, фенитоин
- 37. Активность ГГТ в плазме, как правило, очень высока у пациентов с алкогольным поражением печени, но эта
- 38. Некоторые причины повышения активности у-глутамилтрансферазы плазмы
- 39. Лактатдегидрогеназа (ЛДГ) Этот фермент существует в тканях организма в форме тетрамера: два мономера, Н и М,
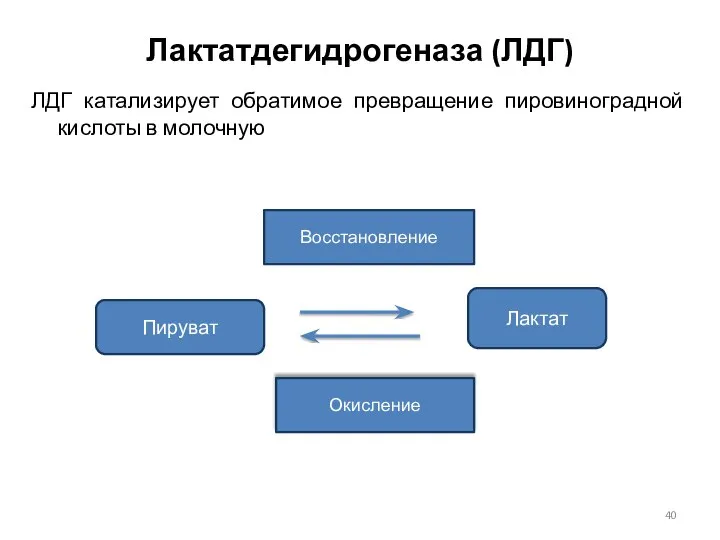
- 40. Лактатдегидрогеназа (ЛДГ) ЛДГ катализирует обратимое превращение пировиноградной кислоты в молочную Пируват Лактат Восстановление Окисление
- 41. Лактатдегидрогеназа (ЛДГ) В тканях с аэробным метаболизмом (сердце, почки и др.) преобладают изоферменты ЛДГ1, ЛДГ2. Эти
- 42. Лактатдегидрогеназа (ЛДГ) Повышение ЛДГ активности наблюдается при широком спектре патологических состояний: острое поражение печени, скелетных мышц
- 43. Определение активности изоферментов ЛДГ может быть результативным при подозрении на инфаркт миокарда и в диагностике гемолитического
- 44. ЛДГ1 имеет длительное время полусуществования в плазме; после инфаркта миокарда ее активность медленно повышается, достигая пика
- 45. Креатинкиназа Активная молекула КК представляет собой димер; два мономера, М и В, образуют три изофермента —
- 46. Креатинкиназа сердечной мышцы содержит значительно больше изофермента MB (примерно 30 %), чем скелетные мышцы (менее 1
- 47. Однако, если у больных с подозрением на инфаркт миокарда, который последовал за физической нагрузкой, травмой или
- 48. Причины повышения активности креатинкиназы плазмы
- 49. Амилаза Амилаза обнаружена в слюнных железах и экзокринной части поджелудочной железы, а ее тканеспецифические изоферменты можно
- 50. Внеабдоминальные причины редко вызывают повышение активности амилазы в плазме свыше 5-кратного превышения пределов нормы. Примером высокой
- 51. Мелкие молекулы амилазы фильтруются в почечных клубочках, но большинство ферментов, вероятно, удаляются клетками ретикулоэндотелиальной системы. Активность
- 53. Скачать презентацию














































 Презентация на тему Естественный отбор – направляющий фактор эволюции.
Презентация на тему Естественный отбор – направляющий фактор эволюции.  Зоология - наука о животных
Зоология - наука о животных Жизненный цикл клетки
Жизненный цикл клетки Каракал
Каракал Игра-путешествие Наши зелёные друзья
Игра-путешествие Наши зелёные друзья Перелетные и зимующие птицы. Конспект занятий в старшей группе
Перелетные и зимующие птицы. Конспект занятий в старшей группе Ткани человека
Ткани человека Қолдан сұрыптау
Қолдан сұрыптау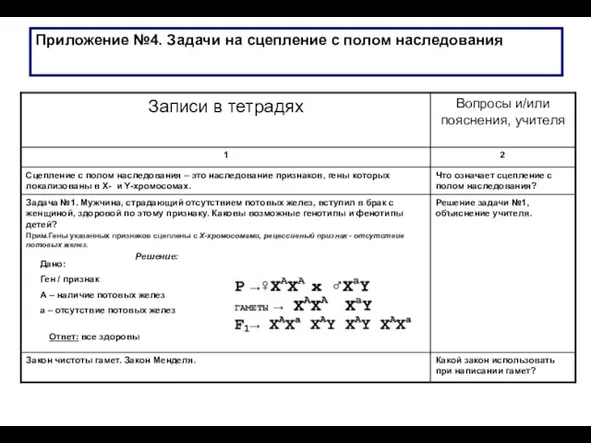 Задачи на сцепление с полом наследования. (Приложение 4)
Задачи на сцепление с полом наследования. (Приложение 4) Нәсілдердің қалыптасуы
Нәсілдердің қалыптасуы Человек
Человек Основные направления эволюции
Основные направления эволюции Плесневые грибы. Дрожжи
Плесневые грибы. Дрожжи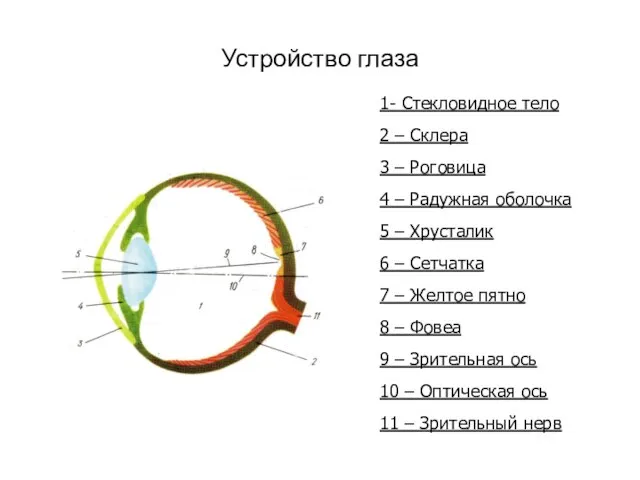 Устройство глаза
Устройство глаза Презентация на тему СТРУКТУРА И ФУНКЦИИ ХРОМОСОМ
Презентация на тему СТРУКТУРА И ФУНКЦИИ ХРОМОСОМ Общая вирусология. Бактериофаги
Общая вирусология. Бактериофаги Бесполое и половое размножение. Мужская и женская половые системы
Бесполое и половое размножение. Мужская и женская половые системы Электрофорез. Введение в теорию электрофореза
Электрофорез. Введение в теорию электрофореза Презентация на тему "Нарушения речи" - скачать бесплатно презентации по Биологии
Презентация на тему "Нарушения речи" - скачать бесплатно презентации по Биологии Презентация Природные ресурсы и охрана природы
Презентация Природные ресурсы и охрана природы Многоклеточные (Metazoa)
Многоклеточные (Metazoa) Викторина Зимушка-зима
Викторина Зимушка-зима Жидкое, а не вода, Белое, а не снег. Выполнила: Никулина Галина Ивановна Учитель начальных классов МОУ «СОШ №4» г.Энгельс
Жидкое, а не вода, Белое, а не снег. Выполнила: Никулина Галина Ивановна Учитель начальных классов МОУ «СОШ №4» г.Энгельс Ботаника. ОГЭ по биологии
Ботаника. ОГЭ по биологии Анатомо-физиологические особенности органа зрения у собак и кошек
Анатомо-физиологические особенности органа зрения у собак и кошек Стандартизация и оценка соответствия малины и ежевики
Стандартизация и оценка соответствия малины и ежевики Бронхи и лёгкие человека
Бронхи и лёгкие человека ГМО Генетически модифицированный организм
ГМО Генетически модифицированный организм