Содержание
- 2. План 1. Липиды. Классификация. Функции. Потребности организма в липидах. 2. Переваривание липидов: ферменты, роль желчных кислот,
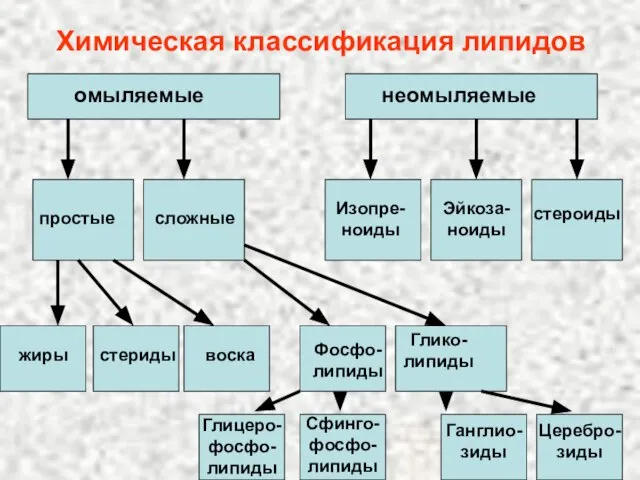
- 3. Химическая классификация липидов простые сложные Изопре-ноиды Эйкоза-ноиды стероиды омыляемые неомыляемые жиры стериды воска Фосфо-липиды Глико-липиды Глицеро-фосфо-липиды
- 4. Функции жиров Энергетическая: при окислении 1 г жира выделяется около 9,3 ккал энергии. 2. Резерв эндогенной
- 5. Функции липоидов Мембранная: обеспечивают избирательную проницаемость участвуют в активном транспорте необходимы для упорядочения ферментативных цепей необходимы
- 6. Функции липоидов Специфические функции: обеспечивают устойчивость эритроцитов ганглиозиды связывают токсины и яды 3. Энергетическая (не имеет
- 7. Функции биологически активных липидов Регуляторная стероидные гормоны (половые и гормоны надпочечников) гормоны, производные полиненасыщенных жирных кислот
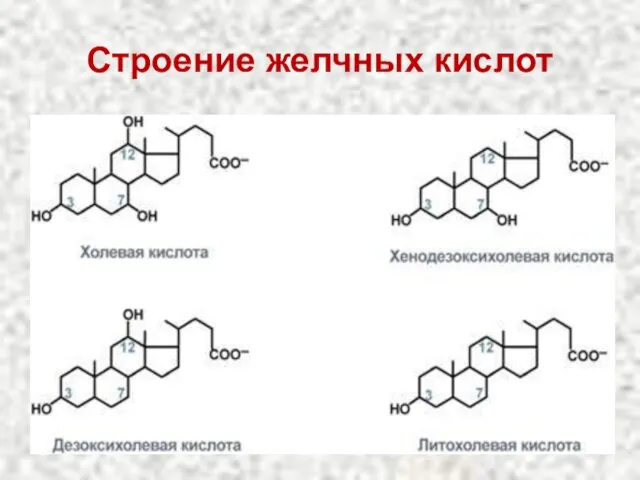
- 9. Строение желчных кислот
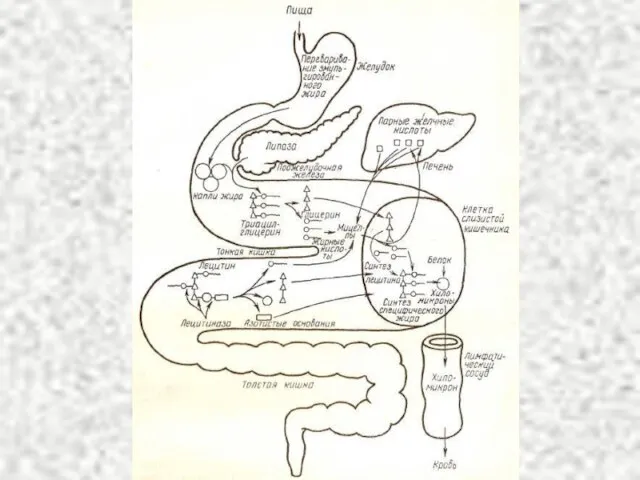
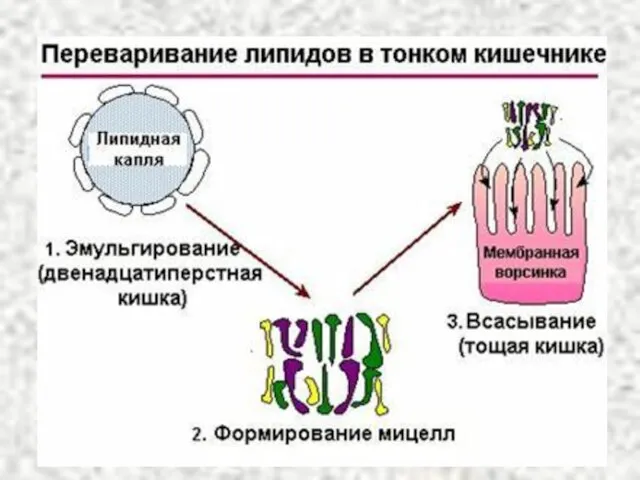
- 10. Роль желчных кислот в переваривании жира 1. Эмульгируют жир, располагаясь на поверхности капель жира и снижая
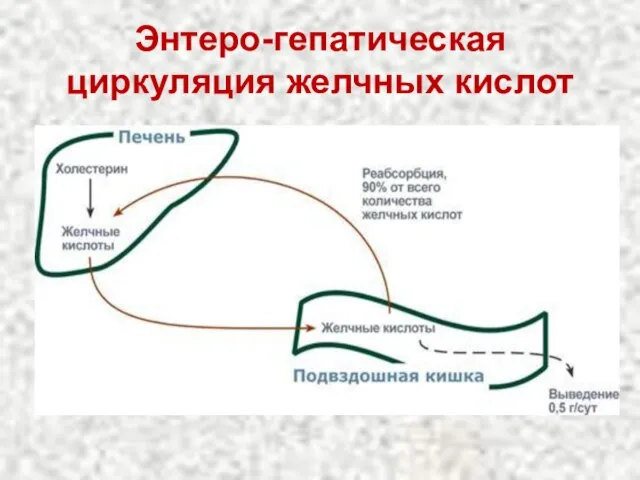
- 12. Энтеро-гепатическая циркуляция желчных кислот
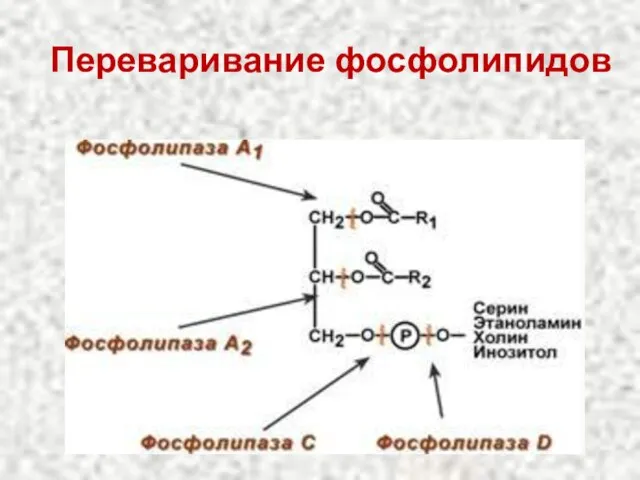
- 13. Переваривание фосфолипидов
- 15. Нарушение переваривания и всасывания жиров. Стеаторея. Нарушение переваривания и всасывания жиров приводит к увеличению количества жиров
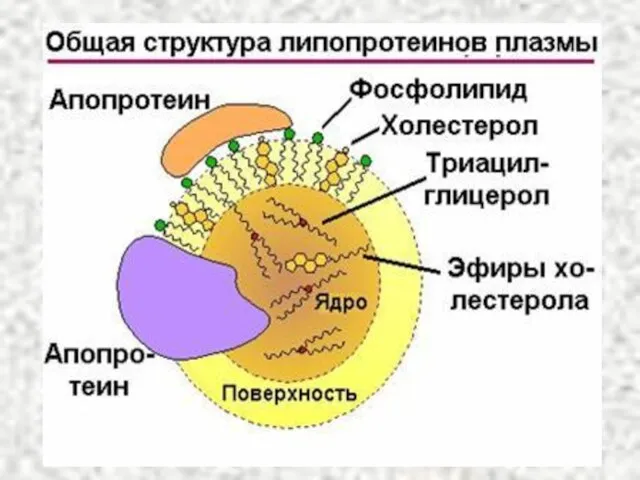
- 17. Функции апопротеинов: Формируют структуру ЛП. Взаимодействуют с рецепторами на поверхности клеток и т.о. определяют, какими тканями
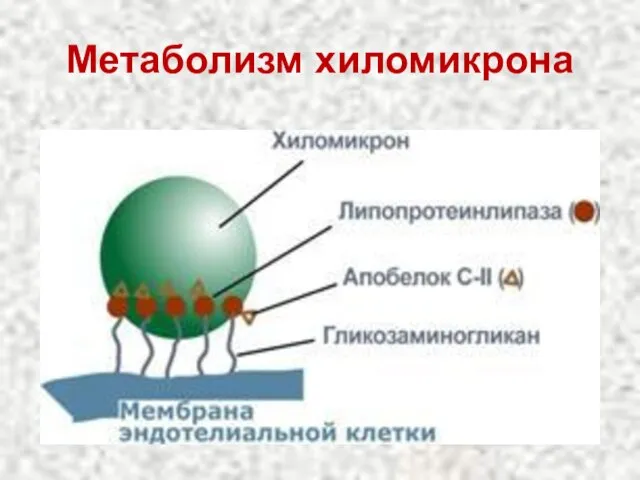
- 18. Метаболизм хиломикрона
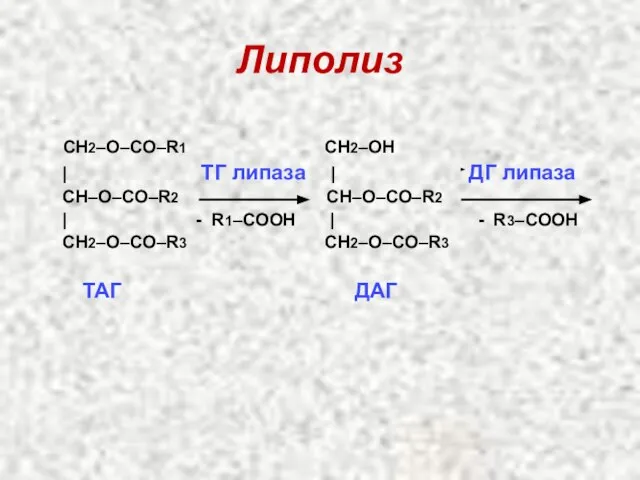
- 19. Липолиз Липолиз – это расщепление жира до глицерина и жирных кислот. Триглицеридлипаза является лимитирующим ферментом липолиза.
- 20. Липолиз СН2–О–СО–R1 СН2–ОН | ТГ липаза | ДГ липаза CН–О–СО–R2 CН–О–СО–R2 | - R1–CООН | -
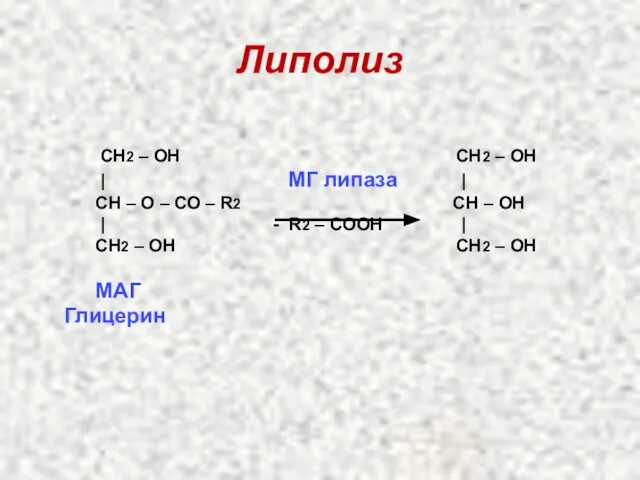
- 21. Липолиз CН2 – ОН CН2 – ОН | МГ липаза | CН – О – СО
- 22. Регуляция липолиза Активируют липолиз: КА, глюкагон, СТГ, АКТГ, тироксин, липотропин гипофиза, цАМФ Ингибирует: инсулин
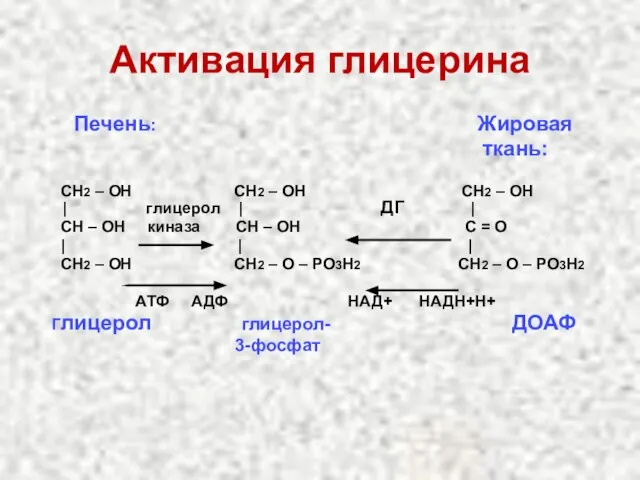
- 23. Активация глицерина Печень: Жировая ткань: СН2 – ОН СН2 – ОН СН2 – ОН | глицерол
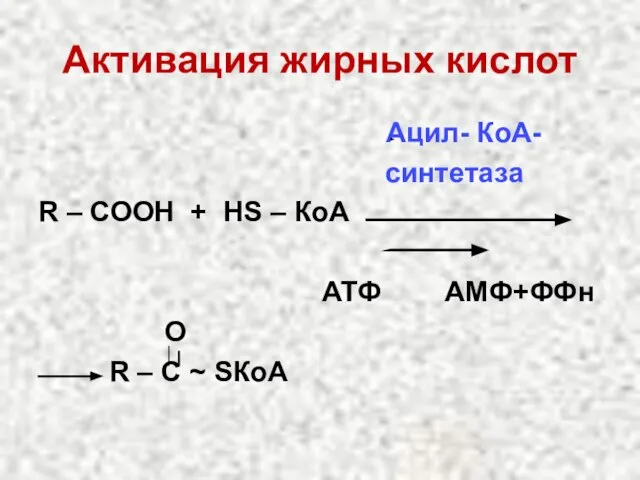
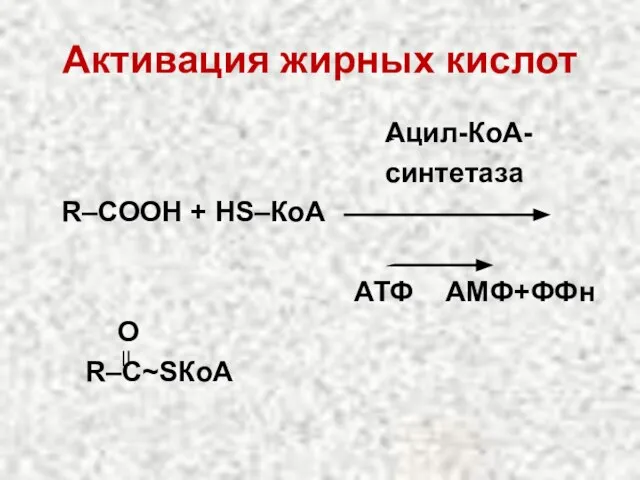
- 24. Активация жирных кислот Ацил- КоА- синтетаза R – СООН + НS – КоА АТФ АМФ+ФФн О
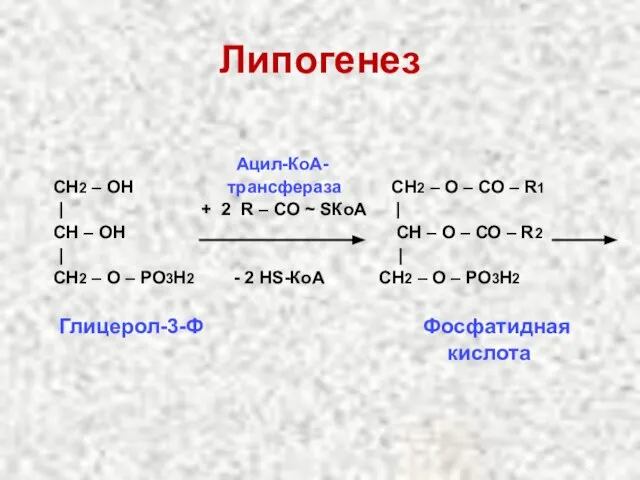
- 25. Липогенез Ацил-КоА- СН2 – ОН трансфераза СН2 – О – СО – R1 | + 2
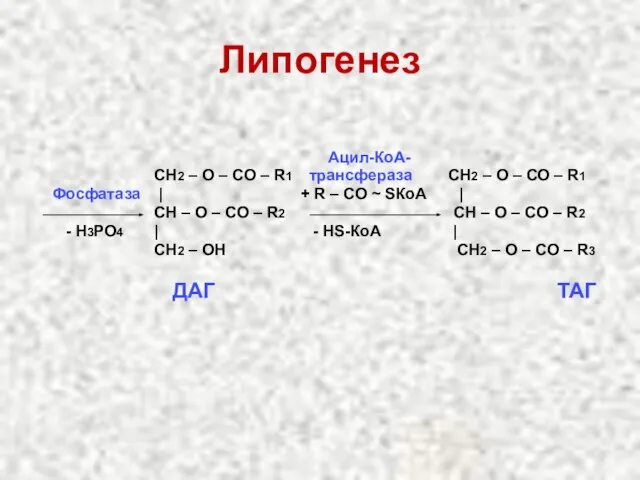
- 26. Липогенез Ацил-КоА- СН2 – О – СО – R1 трансфераза СН2 – О – СО –
- 27. Регуляция липогенеза Активируют: инсулин, эстрогены и АТФ Ингибируют: КА, СТГ, ЙТ, АКТГ, АДФ
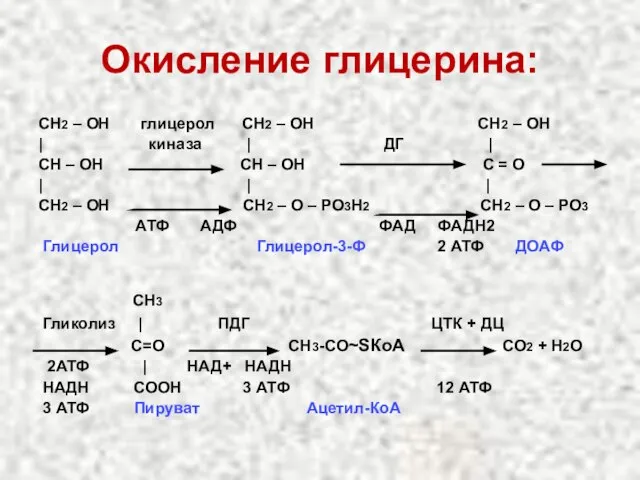
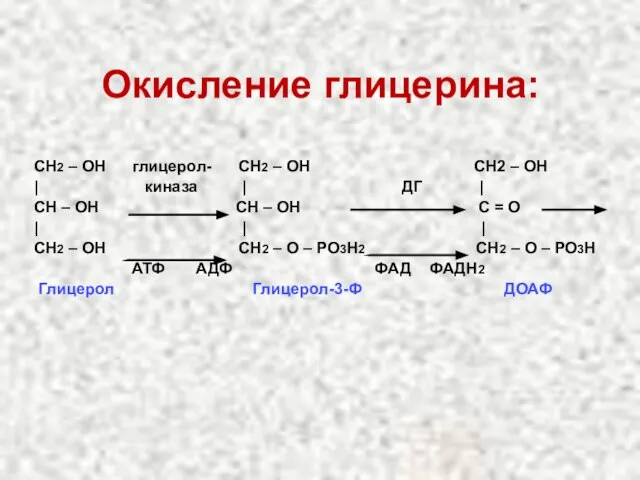
- 28. Окисление глицерина: СН2 – ОН глицерол СН2 – ОН СН2 – ОН | киназа | ДГ
- 29. Окисление глицерина: СН2 – ОН глицерол- СН2 – ОН СН2 – ОН | киназа | ДГ
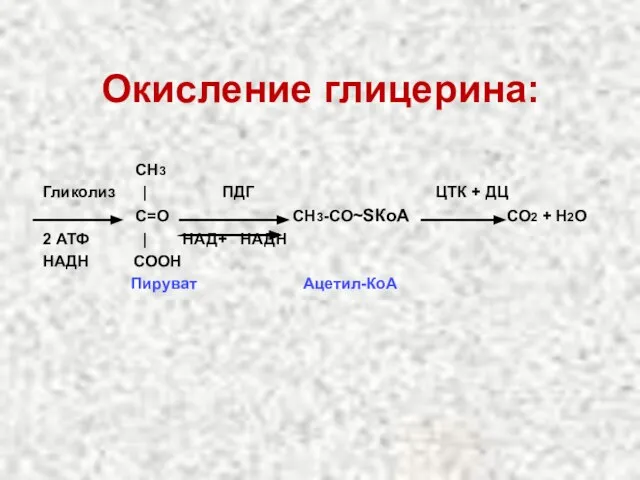
- 30. Окисление глицерина: СН3 Гликолиз | ПДГ ЦТК + ДЦ С=О СН3-СО~SКоА СО2 + Н2О 2 АТФ
- 31. Окисление жирных кислот Жирная + НS-КоА + АТФ Ацил-КоА + АМФ + ФФн кислота ацил-КоА-синтетаза 1.
- 32. Активация жирных кислот Ацил-КоА- синтетаза R–СООН + НS–КоА АТФ АМФ+ФФн О R–С~SКоА
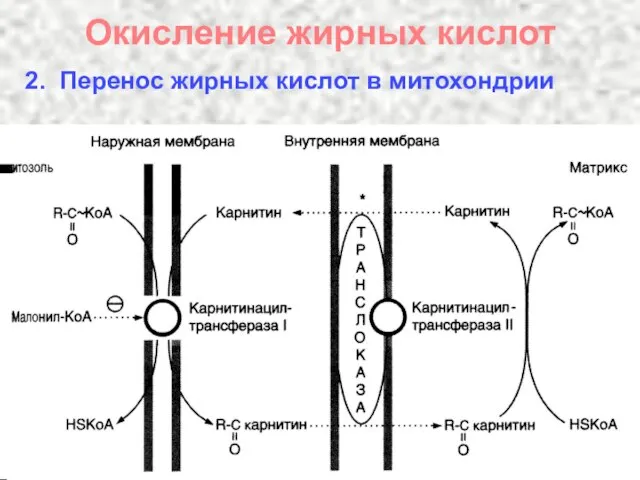
- 33. Окисление жирных кислот 2. Перенос жирных кислот в митохондрии
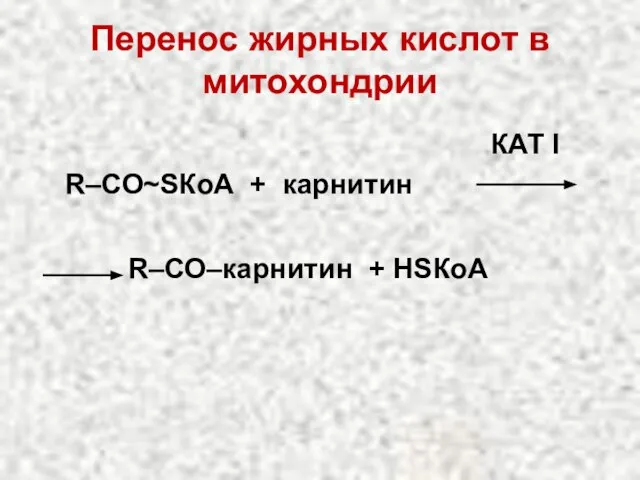
- 34. Перенос жирных кислот в митохондрии КАТ І R–СО~SКоА + карнитин R–СО–карнитин + НSКоА
- 35. Перенос жирных кислот в митохондрии КАТ II R–СО–карнитин + НSКоА R–СО~SКоА + карнитин
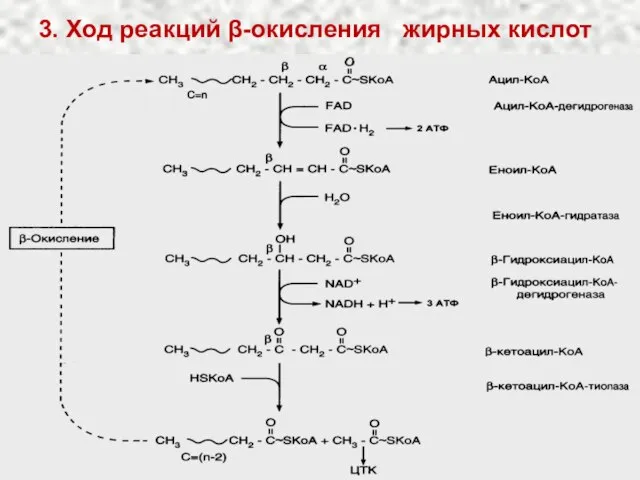
- 36. 3. Ход реакций β-окисления жирных кислот
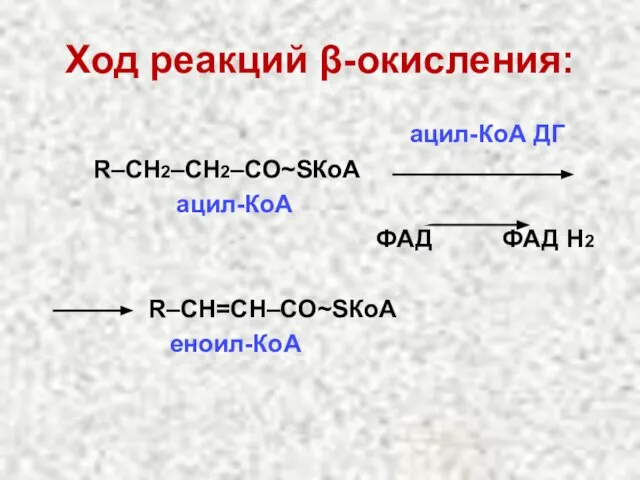
- 37. Ход реакций β-окисления: ацил-КоА ДГ R–СН2–СН2–СО~SКоА ацил-КоА ФАД ФАД Н2 R–СН=СН–СО~SКоА еноил-КоА
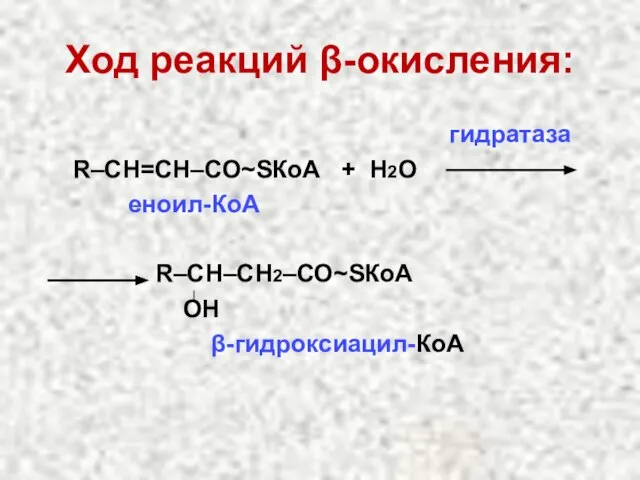
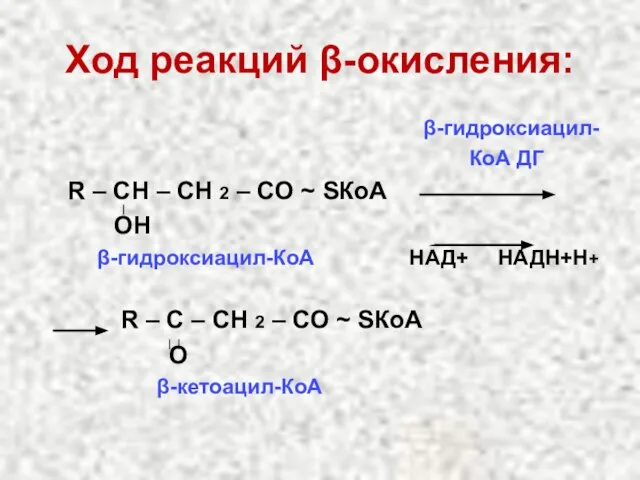
- 38. Ход реакций β-окисления: гидратаза R–СН=СН–СО~SКоА + Н2О еноил-КоА R–СН–СН2–СО~SКоА ОН β-гидроксиацил-КоА
- 39. Ход реакций β-окисления: β-гидроксиацил- КоА ДГ R – СН – СН 2 – СО ~ SКоА
- 40. Ход реакций β-окисления: тиолаза R–С–СН2–СО~SКоА + НS–КоА О β-кетоацил-КоА СН3–СО~SКоА + R–СО~SКоА ацетил-КоА ацил-КоА
- 41. Общее уравнение β-окисления пальмитиновой кислоты С15Н31СО~SКоА + 7 ФАД + 7 НАД+ + 7 НS–КоА 8
- 42. Регуляция β-окисления жирных кислот - Ключевым процессом является поступление жирных кислот в митохондрии - Карнитинацилтрансфераза I
- 43. Регуляция β-окисления жирных кислот активируют β-окисление: КА, СТГ, глюкагон тормозит: инсулин
- 44. Синтез жирных кислот Происходит главным образом в жировой ткани, молочной железе и печени. Местом синтеза жирных
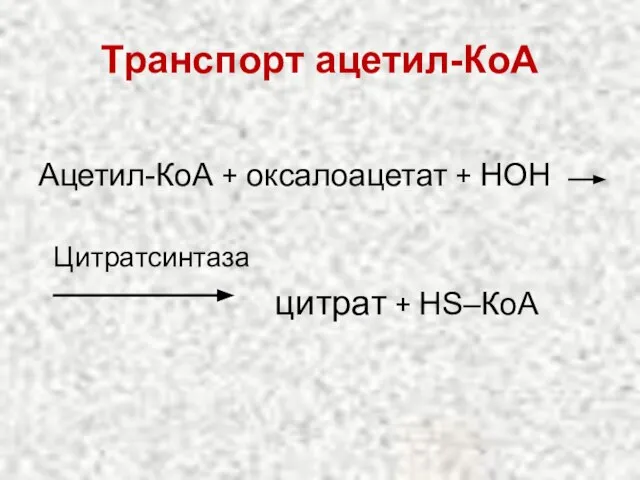
- 45. Транспорт ацетил-КоА Ацетил-КоА + оксалоацетат + НОН Цитратсинтаза цитрат + НS–КоА
- 46. Транспорт ацетил-КоА цитратлиаза Цитрат + НS–КоА + АТФ Ацетил-КоА + АДФ + Н3РО4 + + оксалоацетат
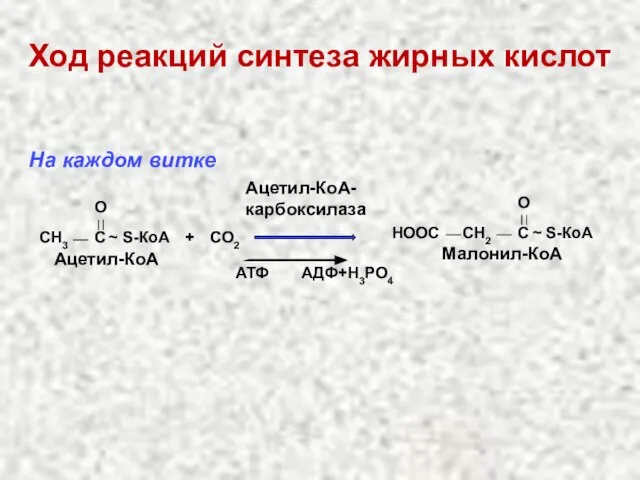
- 47. Ход реакций синтеза жирных кислот CH3 C O ~ S-КоА Ацетил-КоА + CO2 Ацетил-КоА-карбоксилаза АТФ АДФ+Н3РО4
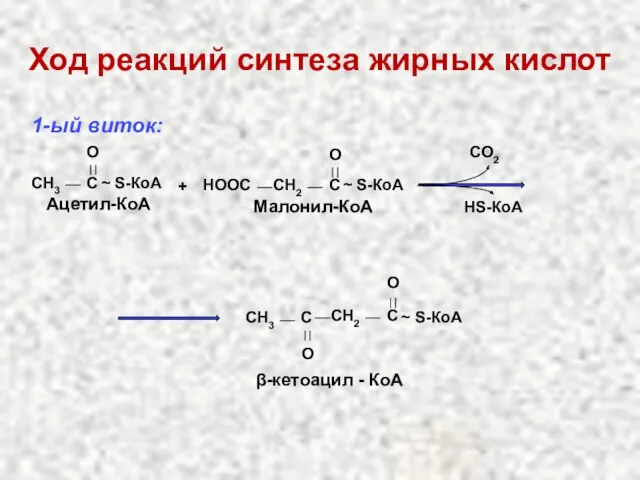
- 48. Ход реакций синтеза жирных кислот 1-ый виток: CH3 C O ~ S-КоА Ацетил-КоА CH2 C O
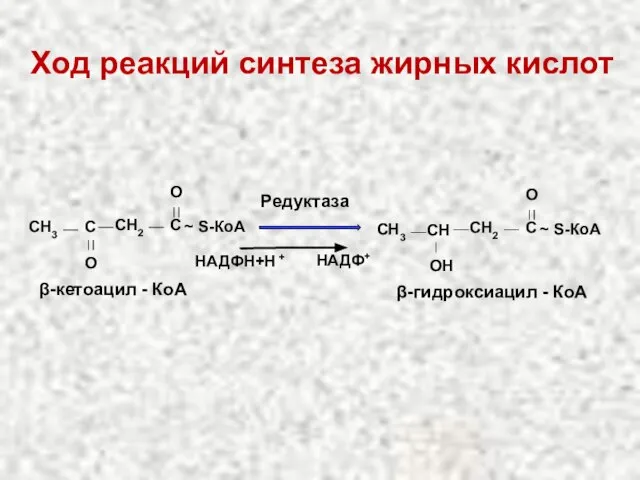
- 49. Ход реакций синтеза жирных кислот CH2 C O ~ S-КоА СН3 С O β-кетоацил - КоА
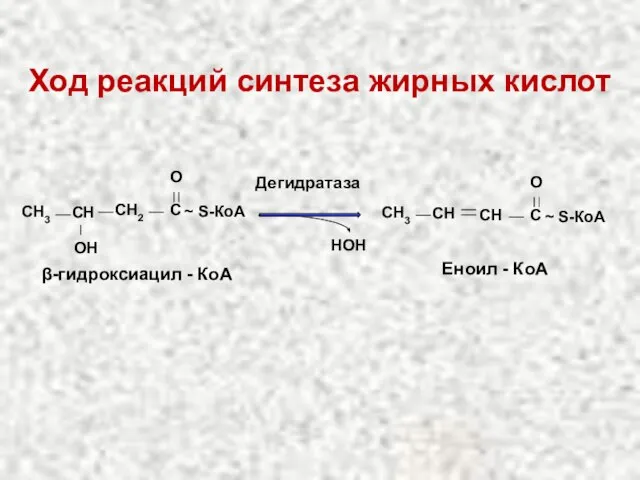
- 50. Ход реакций синтеза жирных кислот CH2 C O ~ S-КоА СН3 СН OН β-гидроксиацил - КоА
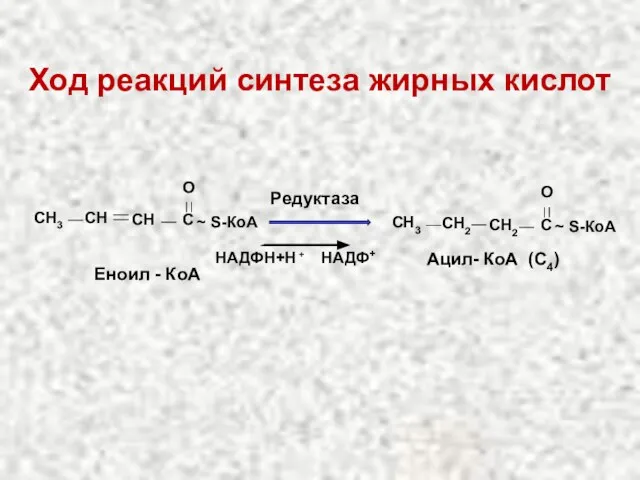
- 51. Ход реакций синтеза жирных кислот CH C O ~ S-КоА СН3 СН Еноил - КоА Редуктаза
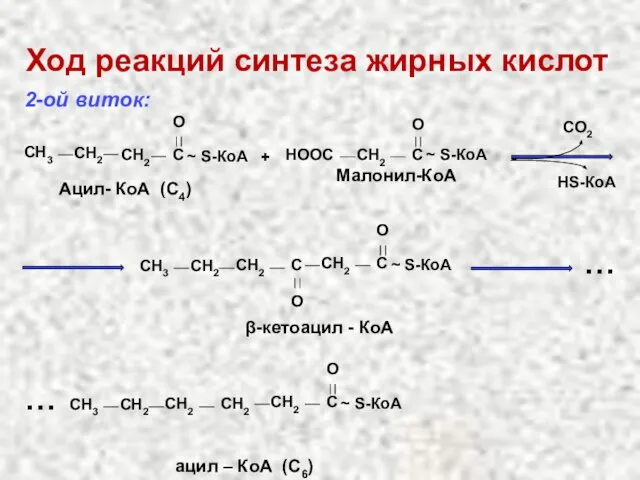
- 52. Ход реакций синтеза жирных кислот 2-ой виток: CH2 C O ~ S-КоА СН3 СН2 Ацил- КоА
- 53. Регуляция синтеза жирных кислот Лимитирующий фермент – Ацетил-КоА-карбоксилаза Аллостерические активаторы – АТФ и цитрат Ингибиторы –
- 54. Гормональная регуляция синтеза жирных кислот Активируют: Инсулин, эстрогены Ингибируют: КА и стресс
- 55. Пути образования ацетил-КоА 1. Из пирувата в ходе ПДГ-реакции Этот путь преобладает при кратковременной и напряженной
- 56. Пути использования ацетил-КоА Ацетил-КоА окисляется в цикле Кребса Используется в синтезе жирных кислот Используется на синтез
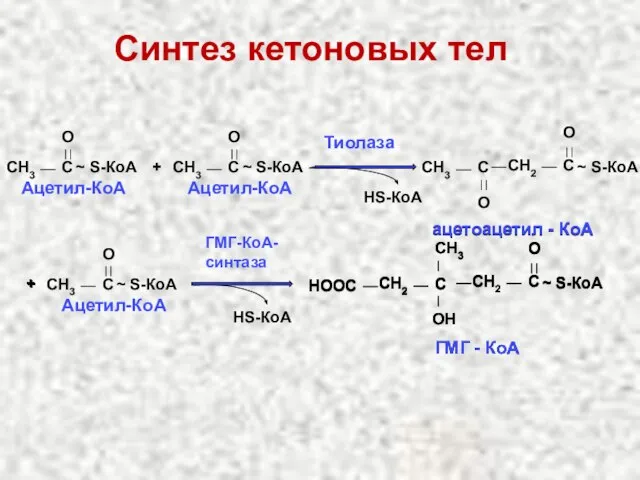
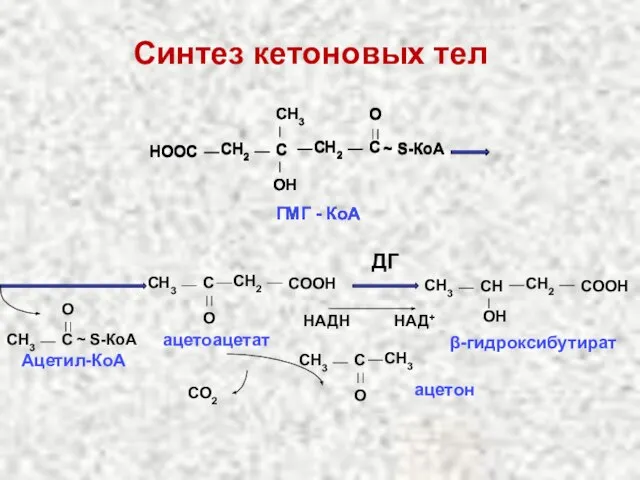
- 57. Кетоновые тела Под кетоновыми телами понимают три вещества: Ацетоацетат β-гидроксибутират Ацетон Кетоновые тела образуются в печени
- 58. Синтез кетоновых тел CH3 C O ~ S-КоА Ацетил-КоА + CH3 C O ~ S-КоА Ацетил-КоА
- 59. CH2 СН3 С O СООН ацетоацетат CH3 C O ~ S-КоА Ацетил-КоА CH2 СН3 СН OН
- 61. Функции кетоновых тел Энергетическая (скелетная и сердечная мышцы, головной мозг и другие внепеченочные ткани) 2. Кетоновые
- 62. Кетоз Кетоз – это накопление кетоновых тел в организме. Сопровождается кетонемией и кетонурией. Различают: 1. Физиологический
- 63. Регуляция синтеза кетоновых тел Ключевой фермент - ГМГ-КоА-синтаза Активируют: КА, глюкагон, СТГ Ингибирует: инсулин
- 64. Регуляция синтеза кетоновых тел Активность ГМГ-КоА-синтазы повышается при поступлении ЖК в гепатоциты печени. Синтез ГМГ-КоА-синтазы усиливается
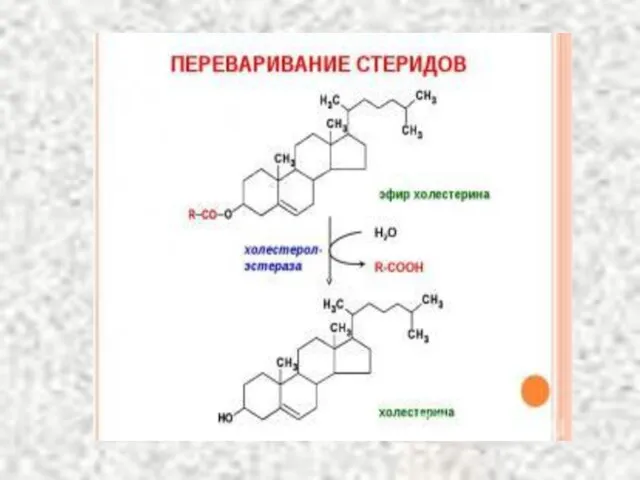
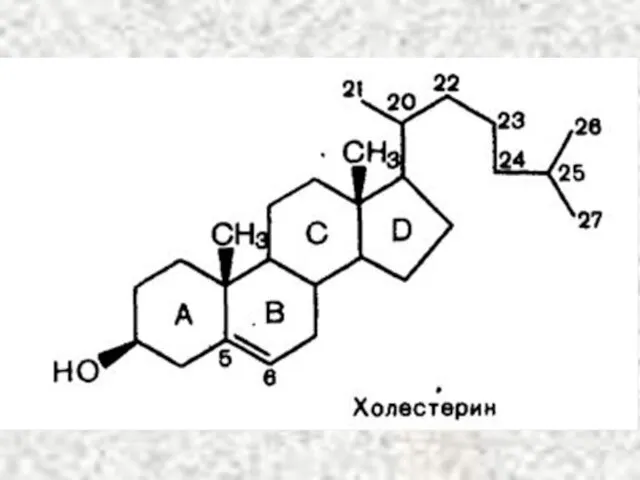
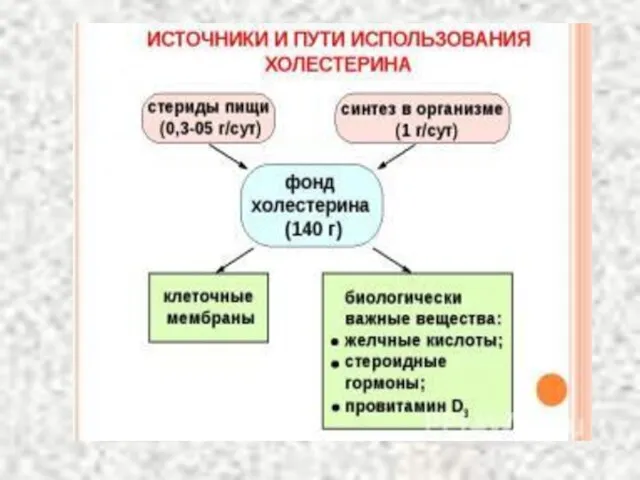
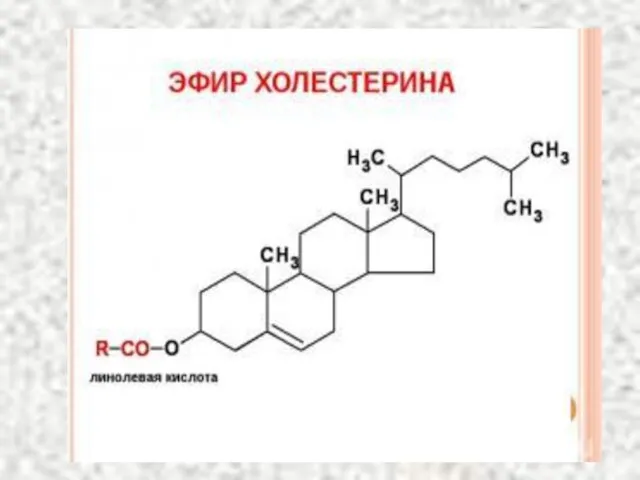
- 66. Источники холестерина 1. Пищевые продукты (желток куриного яйца, головной мозг, печень животных, сливочное масло и др.)
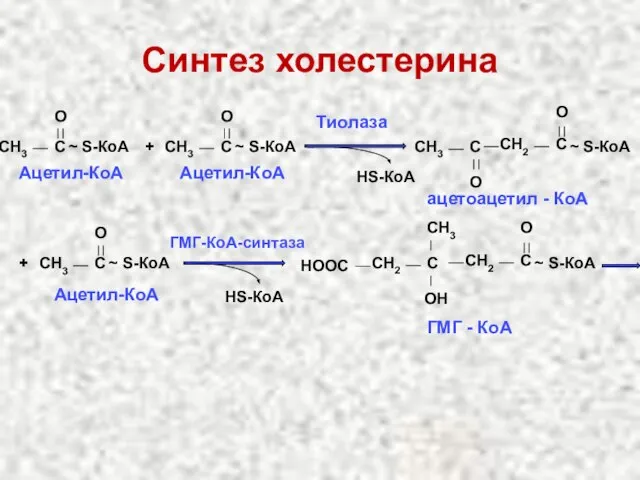
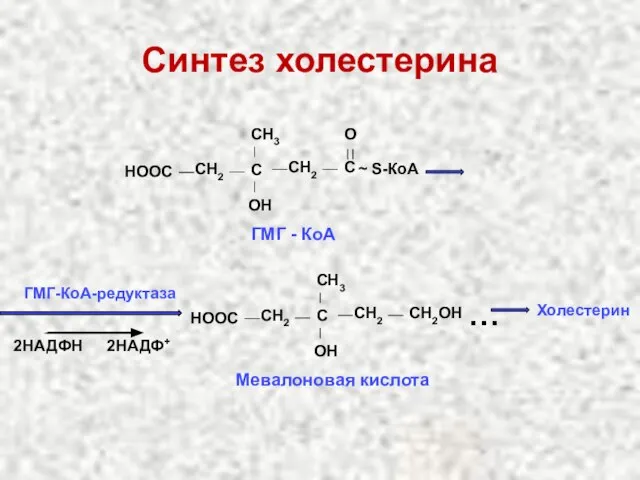
- 67. Синтез холестерина CH3 C O ~ S-КоА Ацетил-КоА + CH3 C O ~ S-КоА Ацетил-КоА Тиолаза
- 68. ГМГ-КоА-редуктаза 2НАДФН 2НАДФ+ CH2 CН2ОН СН2 С OН Мевалоновая кислота СН3 НООС … Холестерин Синтез холестерина
- 69. Регуляция синтеза холестерина Ключевой (лимитирующий) фермент ГМГ-КоА-редуктаза Активируют синтез: КА, СТГ, ГКС, андрогены насыщенные ЖК пища,
- 70. Регуляция синтеза холестерина Снижают синтез: инсулин, тироксин, эстрогены ненасыщенные ЖК холестерин (по принципу отрицательной обратной связи)
- 71. Роль холестерина в организме Входит в состав клеточных мембран и обеспечивает их текучесть Синтез желчных кислот
- 75. Липопротеины крови хиломикроны (ХМ) Содержат 1-2% белка и 98-99% липидов Самые гидрофобные ЛП, имеют наименьшую плотность,
- 76. Липопротеины пре β-липопротеины (или ЛПОНП) Содержат 10% белка, 90% липидов Образуются в печени и очень мало
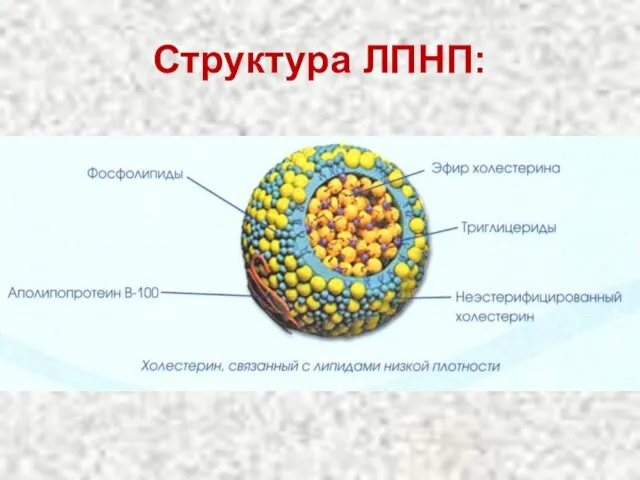
- 77. Структура ЛПНП:
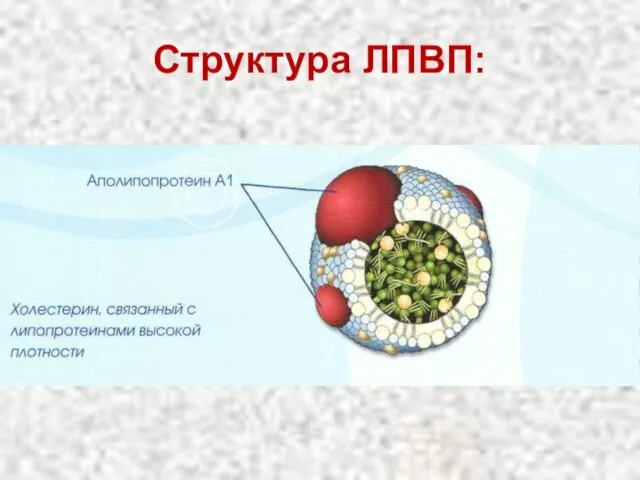
- 78. Структура ЛПВП:
- 79. Липопротеины крови β-липопротеины (ЛПНП) Содержат около 25% белка и 75% липидов. Главными компонентами являются холестерин (примерно
- 80. Липопротеины α-липопротеины (ЛПВП) Содержат 50% белков, 25% фосфолипидов, 20% эфиров холестерина и очень мало триацилглицеринов. Образуются
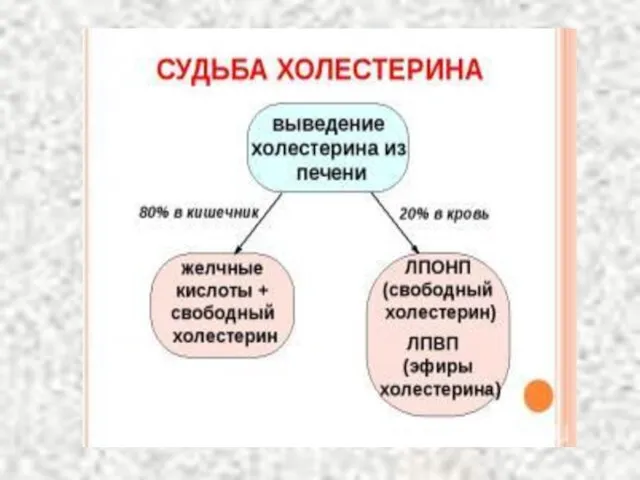
- 82. Липопротеины крови ЛПОНП и ЛПНП являются атерогенными, т. е. вызывающими атеросклероз. ЛПВП - антитиатерогенными.
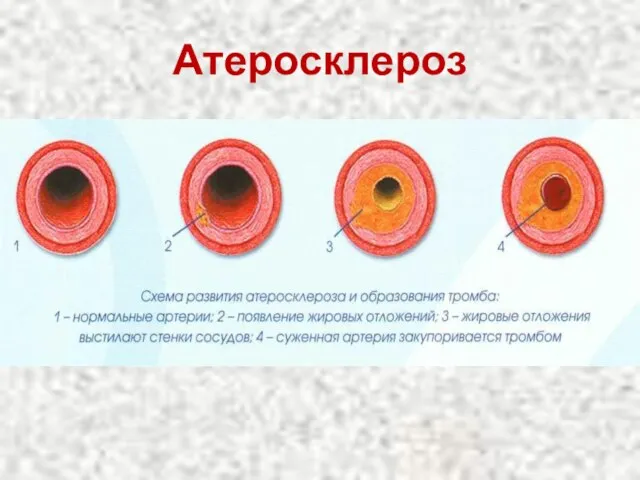
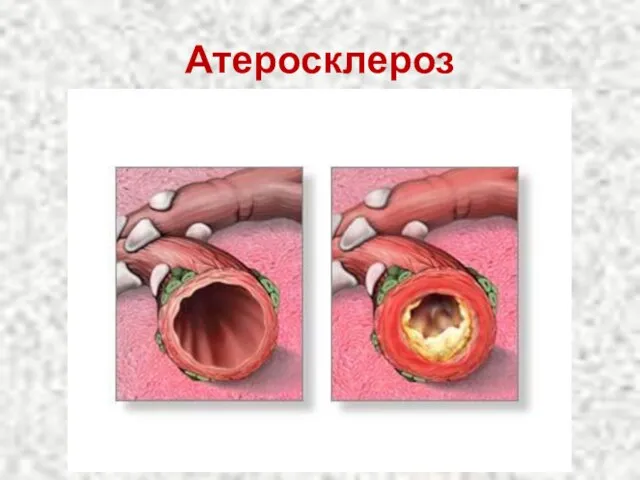
- 83. Атеросклероз
- 84. Атеросклероз
- 85. Механизмы защиты сосудов от атеросклероза Действие липопротеинлипазы в стенке сосуда Наличие ЛПВП
- 86. Биохимические причины атеросклероза Увеличение атерогенных липопротеинов (ЛПОНП и ЛПНП); Снижение антиатерогенных ЛПВП; Снижение активности липопротеинлипазы; Снижение
- 87. Факторы риска развития атеросклероза Курение Стресс Переедание (пища, богатая насыщенными ЖК и углеводами)
- 88. Факторы риска развития атеросклероза Эндокринные факторы: - гипотиреоз - сахарный диабет - андрогены - климакс -
- 89. Факторы риска развития атеросклероза Хронические гипоксии Гиподинамия Семейно-наследственные факторы
- 90. Коэффициент атерогенности Общий холестерин – холестерин ЛПВП холестерин ЛПВП У здоровых людей это соотношение не должно
- 91. Ожирение Ожирение – это состояние, когда масса тела превышает 20% от «идеальной» для данного человека. Причины
- 92. Ожирение Причины вторичного ожирения: Гипотиреоз Синдром Иценко-Кушинга Гипогонадизм другие эндокринные патологии
- 94. Желчнокаменная болезнь Желчнокаменная болезнь – это патология, при которой в желчном пузыре образуются камни, основу которых
- 95. Причины желчнокаменной болезни Пища, богатая холестерином Гиперкалорийное питание Застой желчи в желчном пузыре Нарушение синтеза желчных
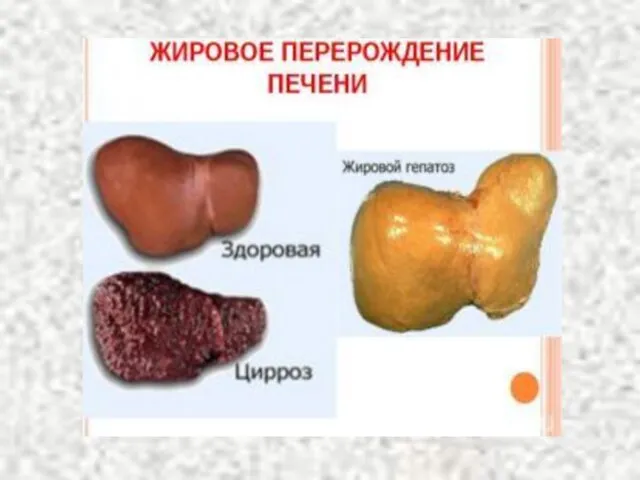
- 96. Липидозы Болезнь Тея-Сакса (ганглиозидоз) Накопление ганглиозидов в клетках мозга, меньше в других тканях. Болезнь Гоше (цереброзидоз)
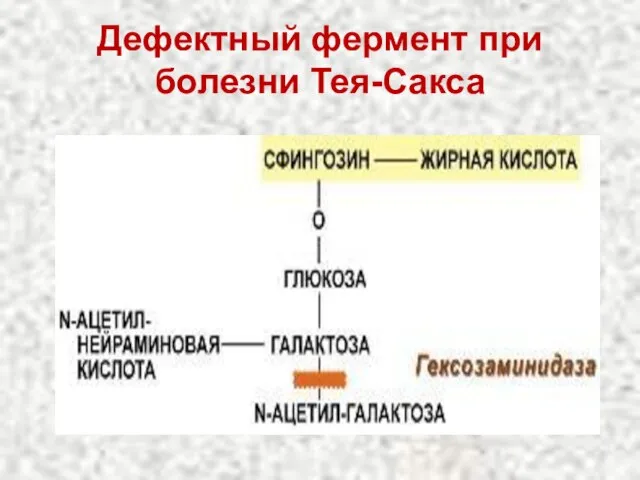
- 97. Дефектный фермент при болезни Тея-Сакса
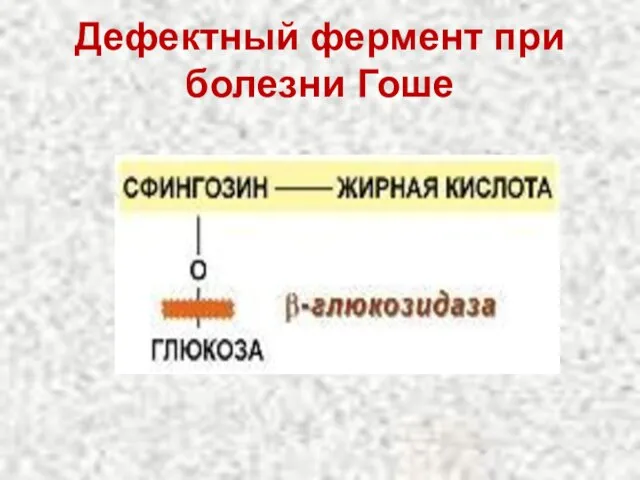
- 98. Дефектный фермент при болезни Гоше
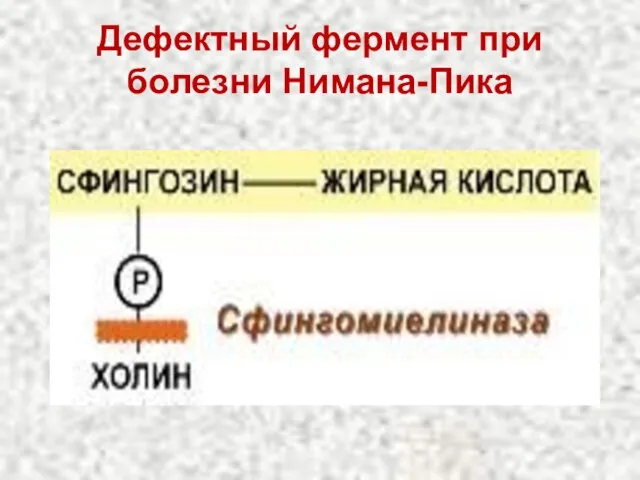
- 99. Дефектный фермент при болезни Нимана-Пика
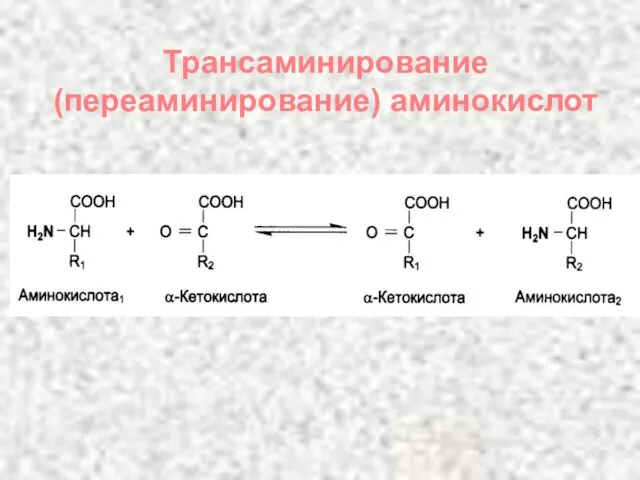
- 100. Трансаминирование (переаминирование) аминокислот
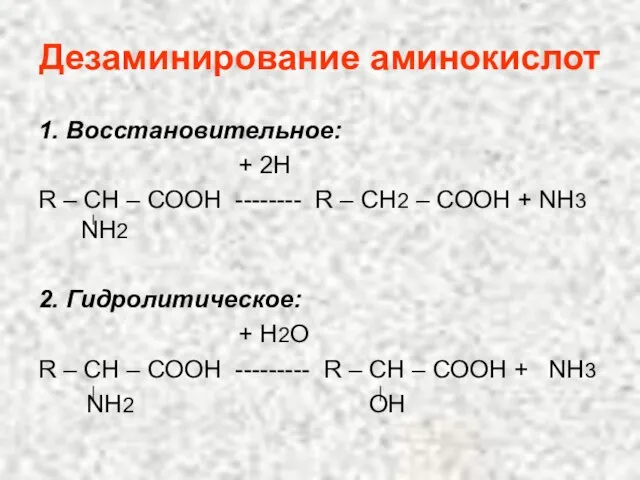
- 101. Дезаминирование аминокислот 1. Восстановительное: + 2Н R – СН – СООН -------- R – СН2 –
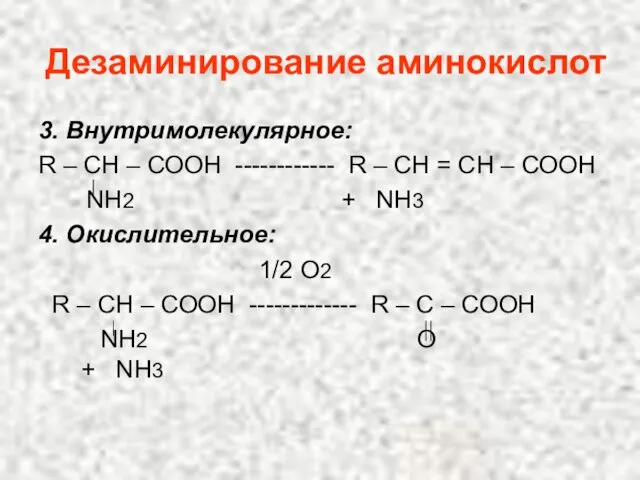
- 102. Дезаминирование аминокислот 3. Внутримолекулярное: R – СН – СООН ------------ R – СН = СН –
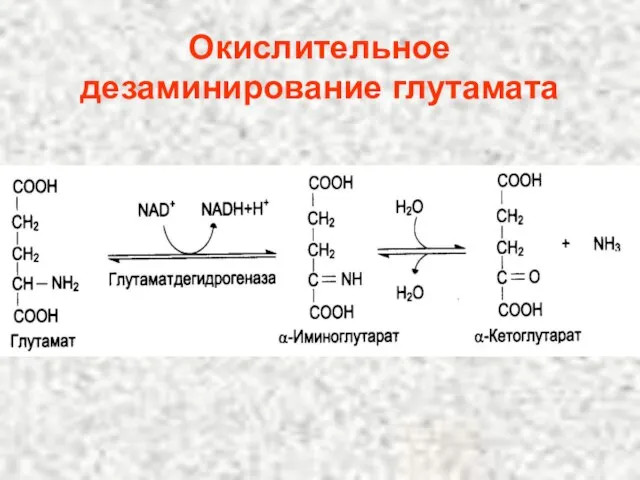
- 103. Окислительное дезаминирование глутамата .
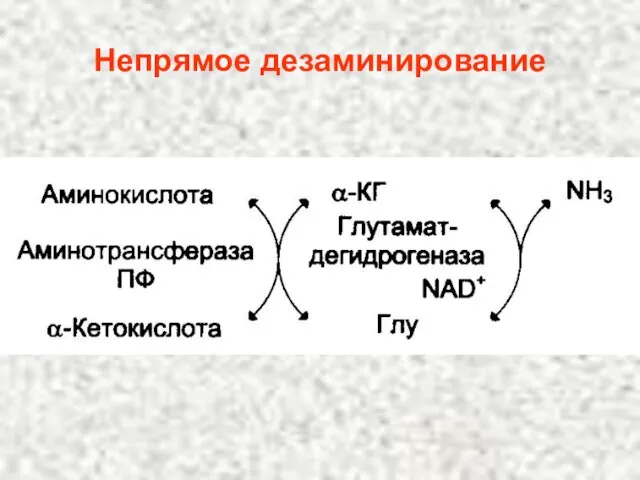
- 104. Непрямое дезаминирование
- 105. Продукты непрямого дезаминирования: α-кетокислота, которая может 1) окисляться в цикле Кребса 2) использоваться в ГНГ на
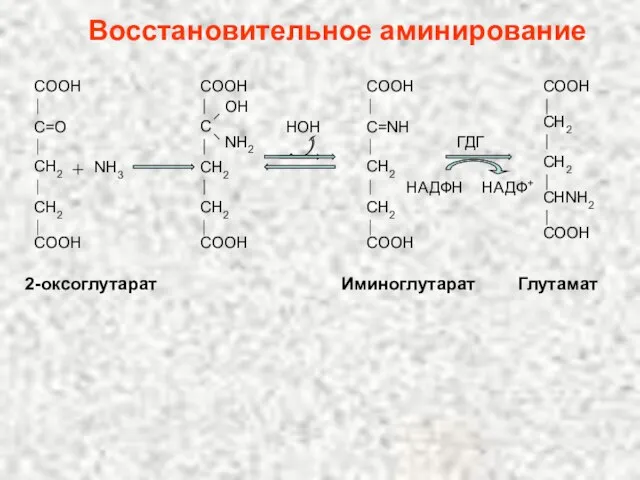
- 106. Восстановительное аминирование COOH C=O CH2 CH2 COOH NH3 COOH C OH NH2 CH2 CH2 COOH COOH
- 107. Значение восстановительного аминирования: глутамат является источником аминогрупп для синтеза заменимых аминокислот служит одним из способов связывания
- 108. Источники аммиака : Реакции дезаминирования аминокислот биогенных аминов (гистамина, серотонина, катехоламинов и др.) пуриновых и пиримидиновых
- 109. Причины токсичности аммиака 1) Легко проникает через клеточные мембраны 2) Связывается с 2-оксоглутаратом, что вызывает угнетение
- 110. Причины токсичности аммиака 4) Аммиак в крови и цитозоле образует ион NH4+, накопление которого нарушает трансмембранный
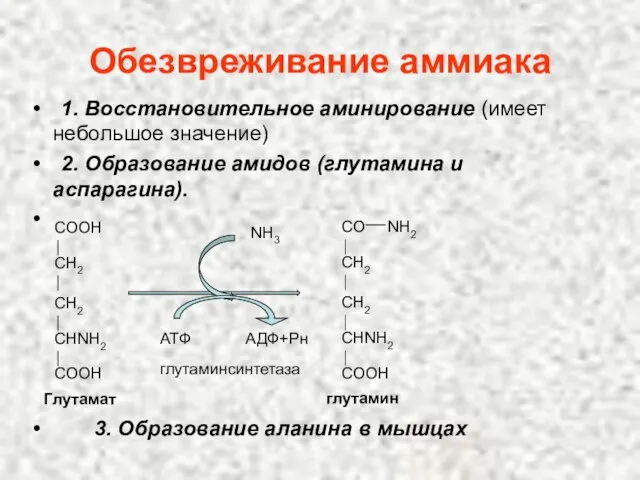
- 111. Обезвреживание аммиака COOH CH2 CH2 CHNH2 COOH Глутамат CO NH2 CH2 CH2 CHNH2 COOH NH3 АТФ
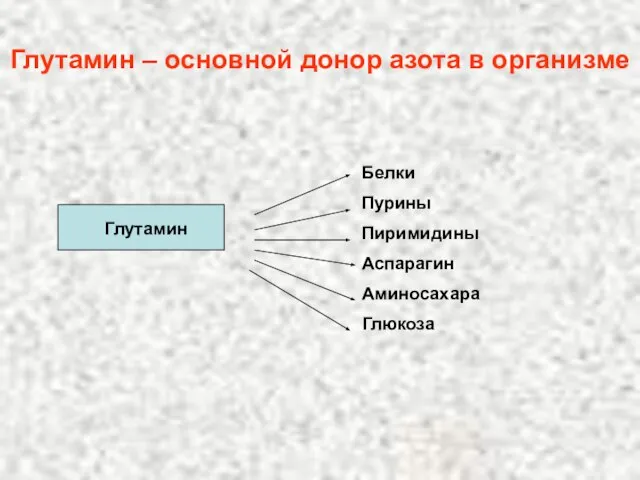
- 112. Глутамин – основной донор азота в организме Глутамин Белки Пурины Пиримидины Аспарагин Аминосахара Глюкоза
- 114. Скачать презентацию























































 Биосинтез заменимых аминокислот. Деградация нуклеиновых кислот. (Лекция 4)
Биосинтез заменимых аминокислот. Деградация нуклеиновых кислот. (Лекция 4) Строение углерода и его функции
Строение углерода и его функции Животный мир Арктики и Антарктики
Животный мир Арктики и Антарктики Презентация на тему "Половое размножение" - скачать бесплатно презентации по Биологии
Презентация на тему "Половое размножение" - скачать бесплатно презентации по Биологии Ботаническое ресурсоведение. Классификация биологических ресурсов
Ботаническое ресурсоведение. Классификация биологических ресурсов Нодулярный дерматит. Особенности клинического проявления
Нодулярный дерматит. Особенности клинического проявления Беспозвоночные. Круглые черви
Беспозвоночные. Круглые черви День защиты животных
День защиты животных Что такое микроскоп?
Что такое микроскоп? Презентация на тему Нейроцитология
Презентация на тему Нейроцитология  Окружающая среда Презентацию подготовил Ученик 11-А класса Средней школы №135 Саливончик Эдуард Сергеевич
Окружающая среда Презентацию подготовил Ученик 11-А класса Средней школы №135 Саливончик Эдуард Сергеевич Особенности организации представителей типа Ciliophora
Особенности организации представителей типа Ciliophora Презентация на тему "Фруктовые деревья" - скачать бесплатно презентации по Биологии
Презентация на тему "Фруктовые деревья" - скачать бесплатно презентации по Биологии Первичнополостные черви
Первичнополостные черви Орсодакниды
Орсодакниды Побег и почка
Побег и почка Вавилов Николай Иванович
Вавилов Николай Иванович Виды мышц
Виды мышц  Дача - июль. Часть 2
Дача - июль. Часть 2 Презентация на тему "Путешествие в страну насекомию" - скачать презентации по Биологии
Презентация на тему "Путешествие в страну насекомию" - скачать презентации по Биологии Презентация на тему "Класс млекопитающие или звери" - скачать презентации по Биологии
Презентация на тему "Класс млекопитающие или звери" - скачать презентации по Биологии Класс Пресмыкающиеся (Reptilia)
Класс Пресмыкающиеся (Reptilia) Содержание животных в доме
Содержание животных в доме Эволюционная теория Ч.Дарвина
Эволюционная теория Ч.Дарвина Презентация на тему "Красная книга" - скачать презентации по Биологии
Презентация на тему "Красная книга" - скачать презентации по Биологии Система дыхания
Система дыхания Семейство Нимфейные
Семейство Нимфейные Презентация на тему "Дыхание и кровообращение" - скачать презентации по Биологии
Презентация на тему "Дыхание и кровообращение" - скачать презентации по Биологии