Содержание
- 2. Строение поджелудочной железы Инсулин, строение, функция и регуляция секреции Глюкагон, строение, функция и регуляция секреции Другие
- 3. СТРОЕНИЕ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ
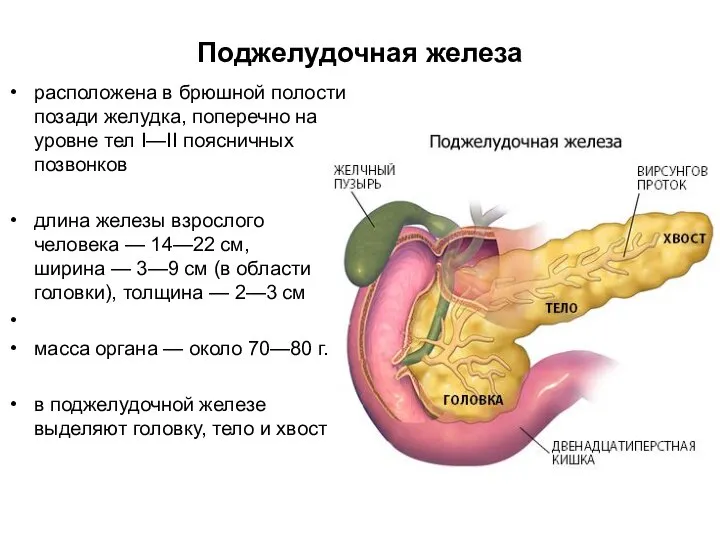
- 4. Поджелудочная железа расположена в брюшной полости позади желудка, поперечно на уровне тел I—II поясничных позвонков длина
- 5. Поджелудочная железа играет ключевую роль в эндокринной и экзокринной функции в желудочно-кишечном тракте экзокринная функция (через
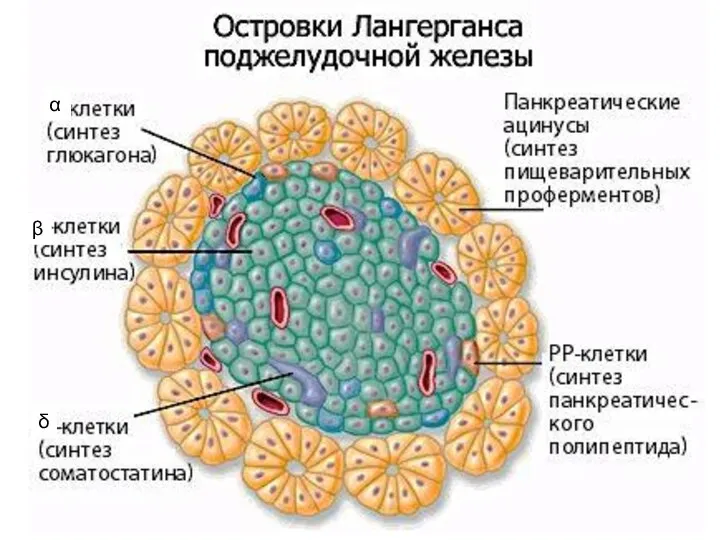
- 6. α β δ
- 7. α-клетки (15-20%) – глюкагон (мобилизация глюкозы в крови) ?гипергикемия, β-клетки (65-80% ) – инсулин (транспорт глюкозы
- 8. Паракринные и аутокринные взаимодействия между клетками островков инсулин (β-клетки) может угнетать собственную секрецию (аутокринный эффект) и
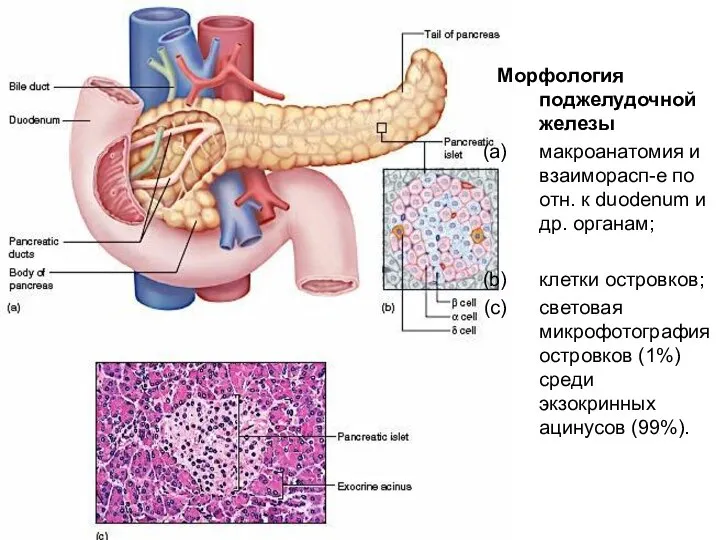
- 9. Морфология поджелудочной железы макроанатомия и взаиморасп-е по отн. к duodenum и др. органам; клетки островков; световая
- 10. 2. ИНСУЛИН, СТРОЕНИЕ, ФУНКЦИЯ И РЕГУЛЯЦИЯ СЕКРЕЦИИ
- 11. Инсулин, строение, рецепция, регуляция секреции, действие. Инсулин – анаболический гормон, секретируемый на пике пищеварения пептид с
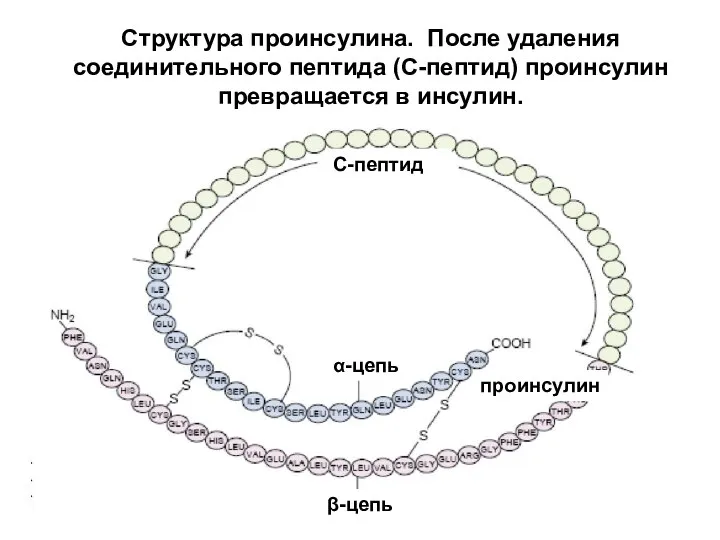
- 12. Структура проинсулина. После удаления соединительного пептида (С-пептид) проинсулин превращается в инсулин. С-пептид α-цепь проинсулин β-цепь
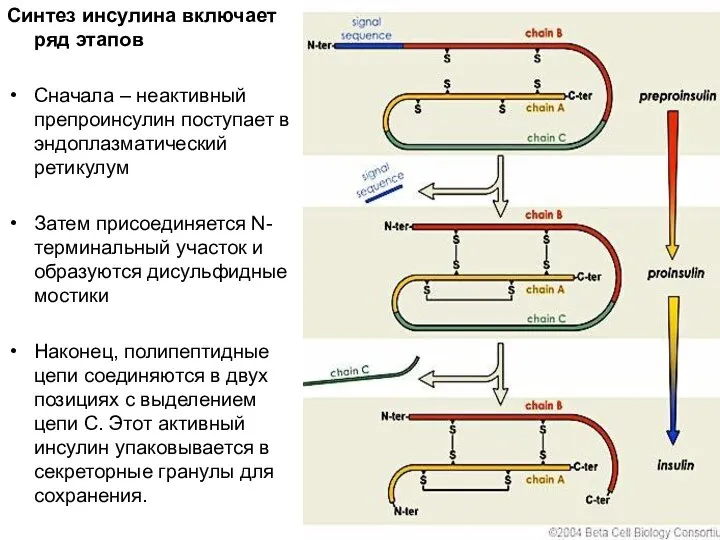
- 13. Синтез инсулина включает ряд этапов Сначала – неактивный препроинсулин поступает в эндоплазматический ретикулум Затем присоединяется N-терминальный
- 14. В норме секрет β клеток содержит 90-97% инсулина и эквимолярные количества C-пептида остальное – проинсулин C
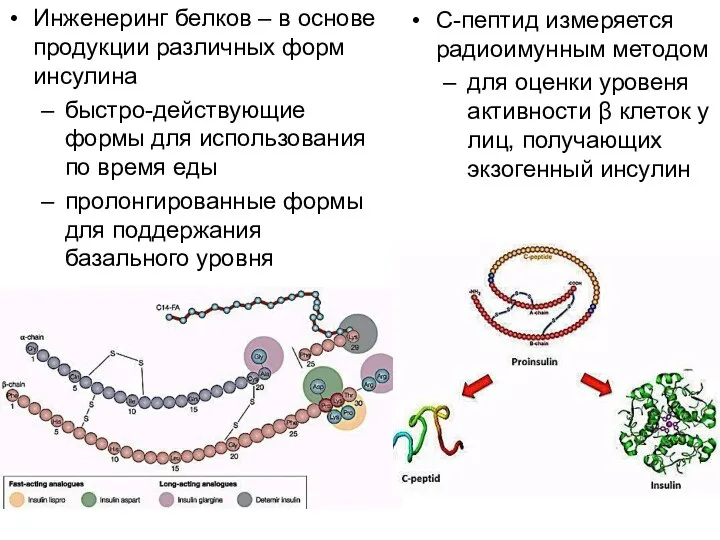
- 15. C-пептид измеряется радиоимунным методом для оценки уровеня активности β клеток у лиц, получающих экзогенный инсулин Инженеринг
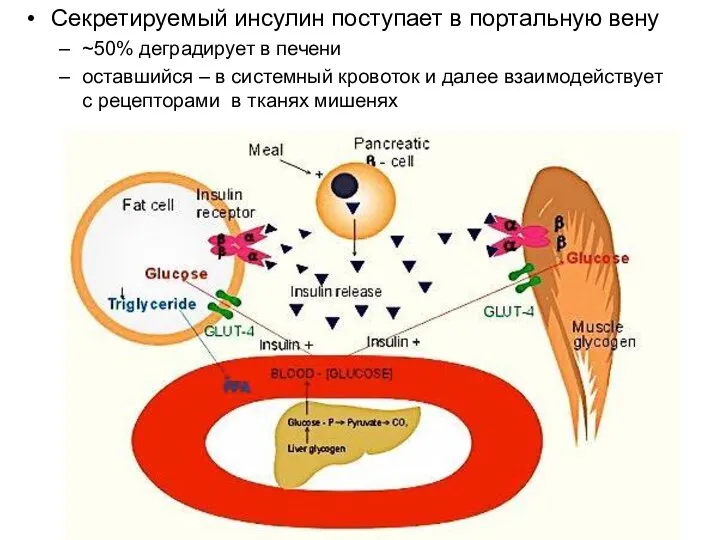
- 16. Секретируемый инсулин поступает в портальную вену ~50% деградирует в печени оставшийся – в системный кровоток и
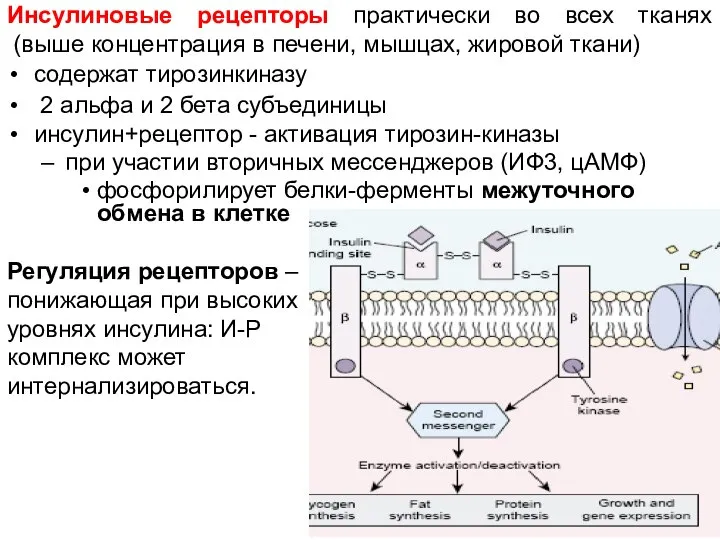
- 17. Инсулиновые рецепторы практически во всех тканях (выше концентрация в печени, мышцах, жировой ткани) cодержат тирозинкиназу 2
- 18. Факторы, стимулирующие секрецию инсулина бета-клетками глюкоза – ключевой регулятор!!! а также стимулируют секрецию И. аминокислоты, кетоновые
- 19. Транспорт глюкозы. Переносчики глюкозы у млекопитающих (GLUT 1-13) Вторично-активный транспорт (Na/глюкоза) по типу симпорта: SGLT 1-2
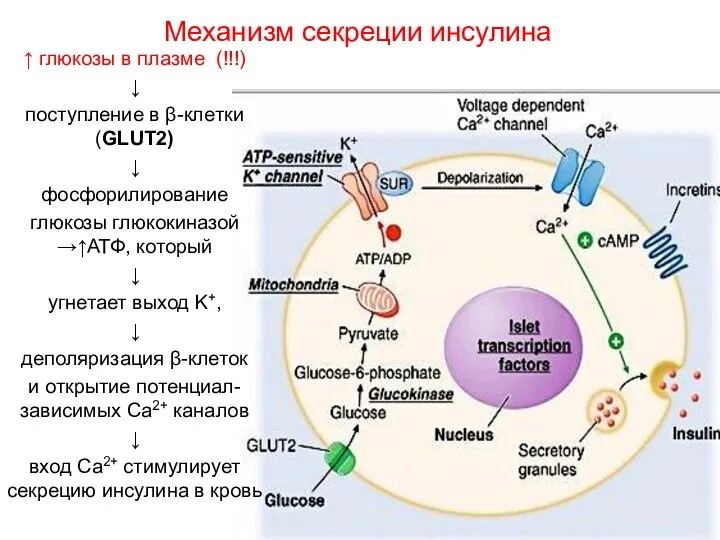
- 20. Механизм секреции инсулина ↑ глюкозы в плазме (!!!) ↓ поступление в β-клетки (GLUT2) ↓ фосфорилирование глюкозы
- 21. Также активируют секрецию инсулина инкретины кишечного происхождения (glucose insulinotropic peptide [GIP], глюкагоно-подобный пептид (glucagon-like peptide-1 [GLP-1]),
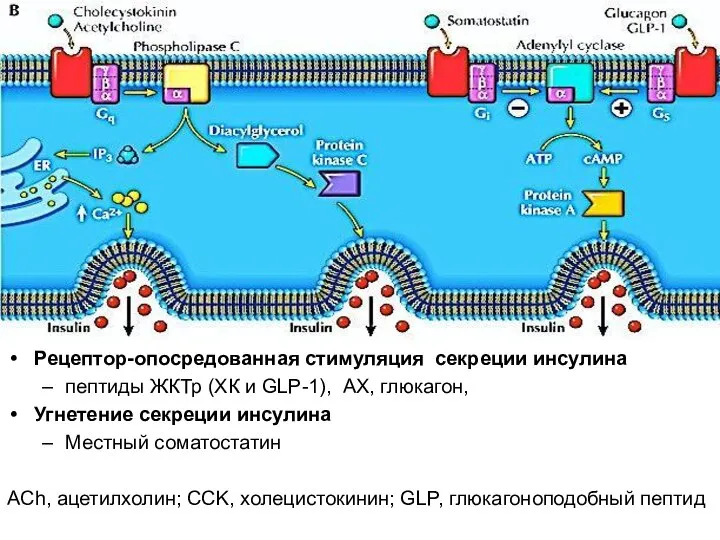
- 22. Рецептор-опосредованная стимуляция секреции инсулина пептиды ЖКТр (ХК и GLP-1), АХ, глюкагон, Угнетение секреции инсулина Местный соматостатин
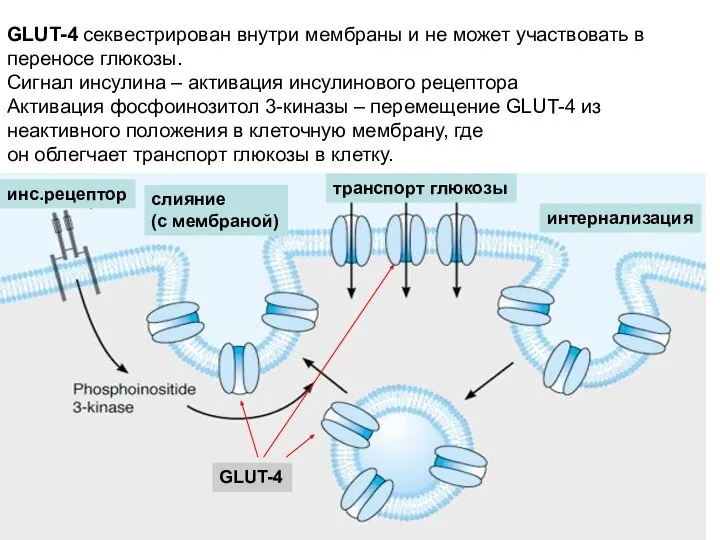
- 23. GLUT-4 секвестрирован внутри мембраны и не может участвовать в переносе глюкозы. Сигнал инсулина – активация инсулинового
- 24. В крови инсулин циркулирует преимущественно в свободной форме; время полураспада в плазме ≈ 6 минут, очищение
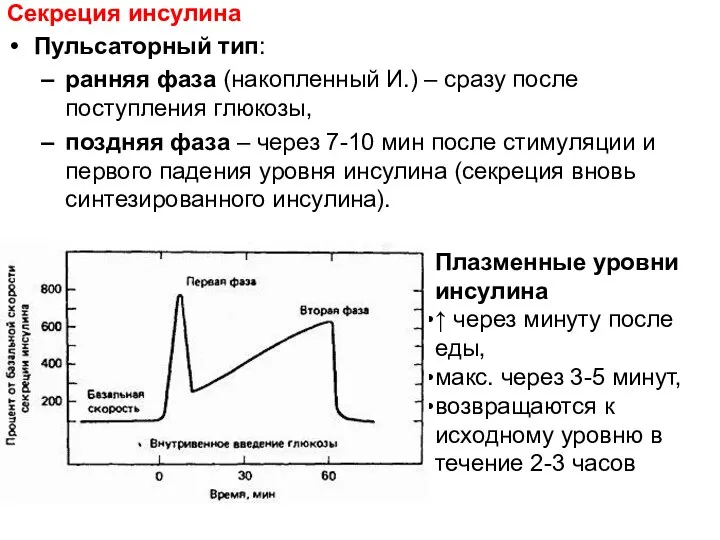
- 25. Секреция инсулина Пульсаторный тип: ранняя фаза (накопленный И.) – сразу после поступления глюкозы, поздняя фаза –
- 26. Таким образом, Главный регулятор секреции инсулина – глюкоза: ↑ г. в плазме стимулирует секрецию И., ↓г.
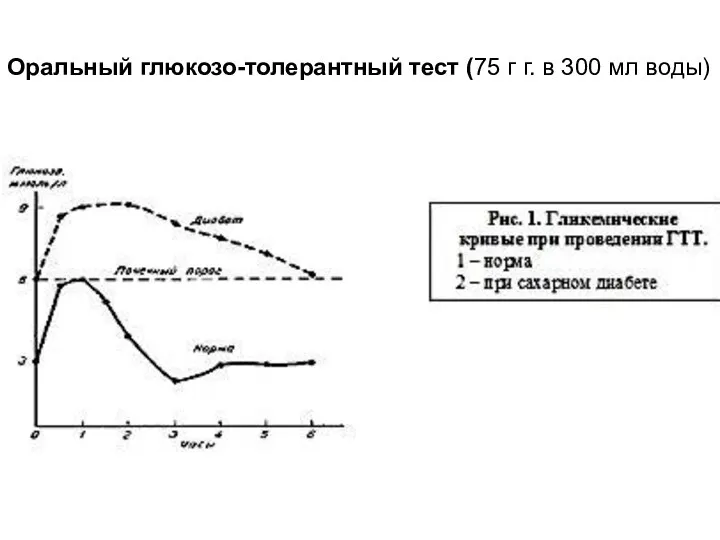
- 27. Оральный глюкозо-толерантный тест (75 г г. в 300 мл воды)
- 29. Эффекты инсулина увеличивает проницаемость плазматических мембран для глюкозы, активирует ключевые ферменты гликолиза, стимулирует образование гликогена из
- 30. Инсулин снижает содержание глюкозы в крови в результате: усиления поглощения клетками глюкозы и других веществ; активации
- 31. Анаболические эффекты И. ↑ поглощение клетками аминокислот (особенно лейцина и валина); ↑ транспорт в клетку ионов
- 32. Инсулин стимулирует фосфорилирование ключевых ферментов межуточного обмена Инсулин-регулируемые ферменты глюкокиназа/гексокиназа (глюкозо-6-фосфатаза), фосфофруктокиназы/фруктоза, бифосфатаза, пируват киназа, пируват
- 33. Эффекты инсулина При отсутствии инсулина ткани захватывают лишь до 40% глюкозы. Скелетные мышцы при посредстве GLUT
- 34. Действие инсулина Быстрое (секунды) Повышение транспорта глюкозы, аминокислот, К+ в инсулин-чувствительные ткани, Промежуточное (минуты) Стимуляция синтеза
- 35. Влияние инсулина на метаболизм глюкозы Инсулин – главный гипогликемический гормон. Гипергликемический эффект вызывают так называемые контринсулярные
- 36. Влияние инсулина на печень ↑захват глюкозы (если уровни глюкозы в крови высоки), рост расхода глюкозы тканями:
- 37. Влияние инсулина на жировую ткань ↑ захвата глюкозы путем активации GLUT-4, ↑ использования глюкозы: ↑гликолиза ↑продукции
- 38. Влияние на обмен жиров ↑липогенез – инсулин активирует липосинтетические ферменты снижает поступление АцКоА в цикл трикарбоновых
- 39. Влияние инсулина на мышцы ↑захвата глюкозы путем повышения количества и активации GLUT-4, ↑использования глюкозы: - ↑гликогенеза,
- 40. Физические упражнения повышают транспорт глюкозы в мышцы даже в отсутствие инсулина: ↓ О2 в тканях стимулирует
- 41. Влияние инсулина на обмен белков стимулирует захват клетками аминокислот, АК, участвующие в глюконеогенезе (аланин, глютамин и
- 42. Влияние инсулина на перемещение калия ↑ перемещение калия в печень и мышечные клетки, ↑ активность Na/K-АТФ-азы
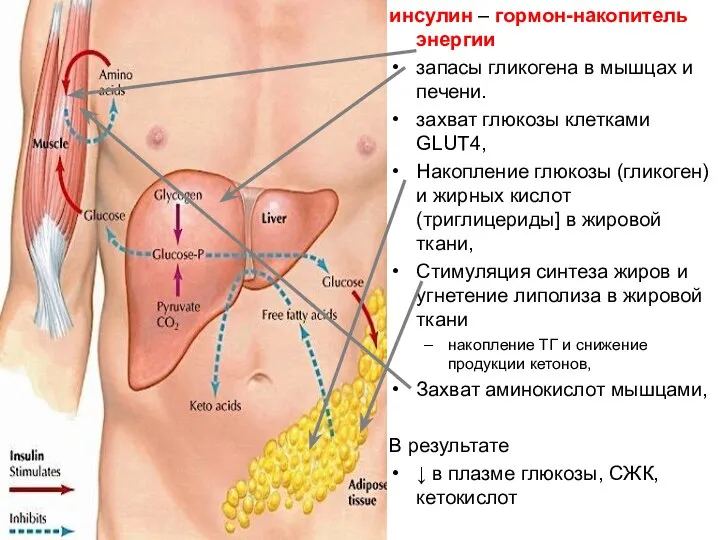
- 43. инсулин – гормон-накопитель энергии запасы гликогена в мышцах и печени. захват глюкозы клетками GLUT4, Накопление глюкозы
- 44. Острая гипогликемия (менее 4 ммол/л) – м.б. после передозировки инсулина: слабость, раздражительность, нарушение моторной координации, головная
- 45. При постепенном падении содержания глюкозы в крови мозг адаптируется путем использования кетоновых тел в качестве источника
- 46. 3. ГЛЮКАГОН, СТРОЕНИЕ, ФУНКЦИИ, РЕГУЛЯЦИЯ СЕКРЕЦИИ
- 47. Глюкагон, строение, рецепция, регуляция, действие катаболический гормон, уровни растут при пищевой депривации, мобилизует гликоген, жиры и
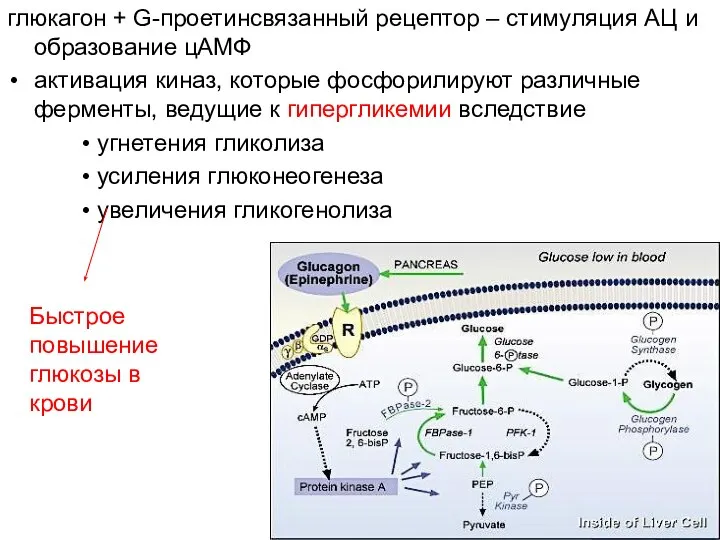
- 48. глюкагон + G-проетинсвязанный рецептор – стимуляция АЦ и образование цАМФ активация киназ, которые фосфорилируют различные ферменты,
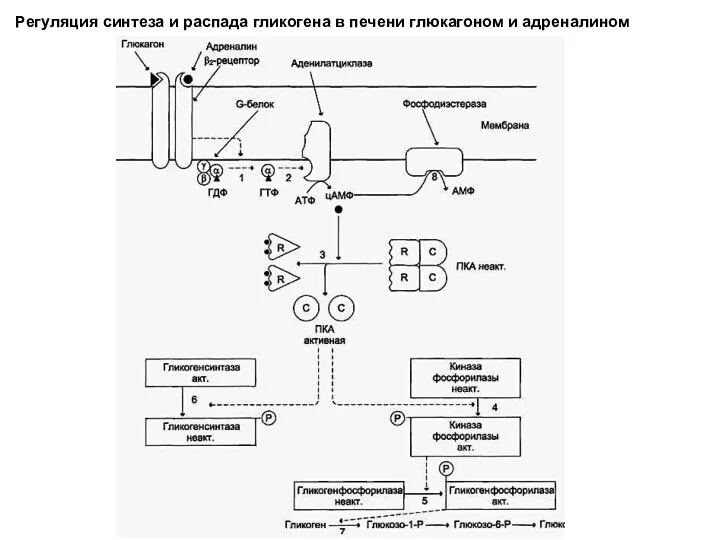
- 49. Регуляция синтеза и распада гликогена в печени глюкагоном и адреналином
- 50. Г. циркулирует в крови в свободной форме и время его жизни коротко (период полураспада около 6
- 51. Влияние Г. на метаболизм углеводов: повышает выделение печенью глюкозы, активирует гликогенолиз и глюконеогенез, тормозит гликолиз в
- 52. Г. и жировая ткань повышает цАМФ в адипоцитах, что стимулирует гормон-чувствительную липазу и усиливает липолиз и
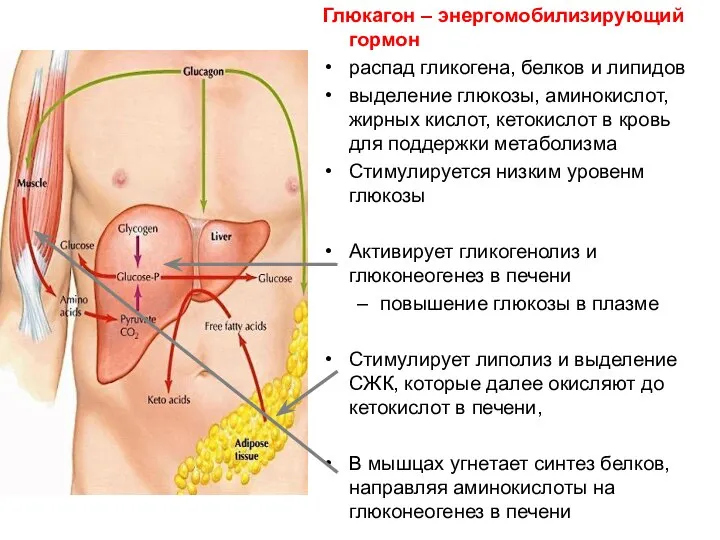
- 53. Глюкагон – энергомобилизирующий гормон распад гликогена, белков и липидов выделение глюкозы, аминокислот, жирных кислот, кетокислот в
- 54. Отношение инсулин/ глюкагон важнее самих уровней гормонов! В норме взаимоотношения между гормонами обратно пропорциональны. Нормальное И/Г
- 55. Уровни глюкозы плазмы и симптомы
- 56. 4. ДРУГИЕ ГОРМОНЫ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ И ИХ РОЛЬ
- 57. Соматостатин - полипептид (14 аминокислот) дельта-клеток время полураспада около 2 минут, предшественники - паракринные эффекты, стимулы
- 58. Аналоги соматостатина используются в фармакотерапии: угнетение глюкагоновой секреции при инсулин-зависимом диабете, инсулиновой секреции при инсулиноме, лечении
- 59. Панкреатический полипептид - 36-аминокислотный пептид (F , или РР - клетки) стимулируют секрецию: богатая белками пища,
- 60. Патология эндокринной функции поджелудочной железы Инсулинзависимый сахарный диабет (диабет I типа, юношеский) – абсолютная инсулиновая недостаточность.
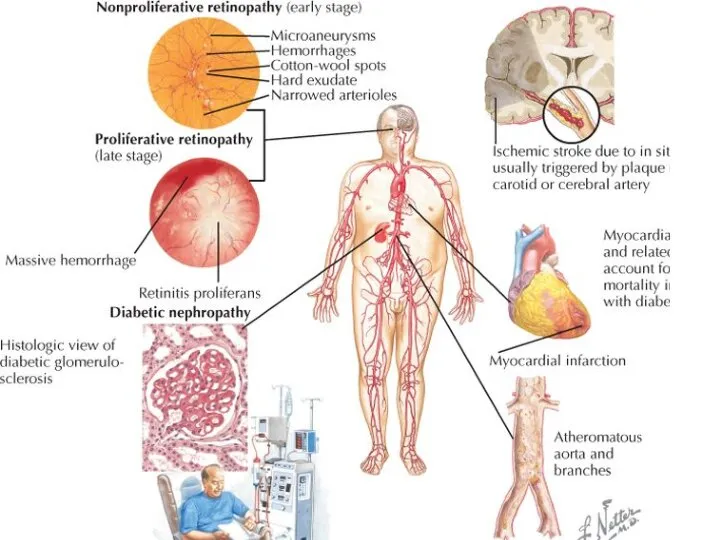
- 61. Осложнения сахарного диабета Диабетическая (кетоацидотическая) кома, Гиперосмолярная (некетоацидотическая) кома – при высоком сахаре крови, Гипогликемическая кома
- 65. Скачать презентацию










![Также активируют секрецию инсулина инкретины кишечного происхождения (glucose insulinotropic peptide [GIP],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/702887/slide-20.jpg)

































 Биоинженерия растений. Культуры клеток и тканей. (Лекция 2)
Биоинженерия растений. Культуры клеток и тканей. (Лекция 2) Мозг Сознание Психология
Мозг Сознание Психология Неандерталец и современный человек: генетическое родство
Неандерталец и современный человек: генетическое родство Развитие и аномалии развития костей
Развитие и аномалии развития костей Отдел Папоротниковидные
Отдел Папоротниковидные Биоокисление и цикл Кребса
Биоокисление и цикл Кребса Органоиды клетки. Рибосомы. Ядро. ЭПС
Органоиды клетки. Рибосомы. Ядро. ЭПС Влияние витаминов на здоровье человека
Влияние витаминов на здоровье человека Микроорганизмы- художники
Микроорганизмы- художники Чутливість, пороги чутливості, абсолютні пороги чутливості
Чутливість, пороги чутливості, абсолютні пороги чутливості Сцепленное наследование. Хромосомная теория наследственности
Сцепленное наследование. Хромосомная теория наследственности Модификация и память
Модификация и память Презентация на тему Медуница
Презентация на тему Медуница Почему необходимо ухаживать за огородом?
Почему необходимо ухаживать за огородом? Методика обучения биологии
Методика обучения биологии Выращивание ягодных и плодовых растений. Размножение
Выращивание ягодных и плодовых растений. Размножение Домашние животные
Домашние животные МИКРОСКОПИЧЕСКОЕ СТРОЕНИЕ ЗУБА План лекции: Общий план строения зуба. Тканевой состав зуба. Источники формирования зу
МИКРОСКОПИЧЕСКОЕ СТРОЕНИЕ ЗУБА План лекции: Общий план строения зуба. Тканевой состав зуба. Источники формирования зу Презентация по биологии по теме «Система кровообращения» Мининой Дарьи ФМЛ №1580 кл.11-7-Б Учитель: Вязовец Н.В.
Презентация по биологии по теме «Система кровообращения» Мининой Дарьи ФМЛ №1580 кл.11-7-Б Учитель: Вязовец Н.В.  Как живые организмы переносят неблагоприятные для жизни условия.
Как живые организмы переносят неблагоприятные для жизни условия. Автор Долгорукова С.В. учитель биологии и географии высшей категории МОУ гимназия № 2 г.Екатеринбурга
Автор Долгорукова С.В. учитель биологии и географии высшей категории МОУ гимназия № 2 г.Екатеринбурга  Дикие и домашние животные
Дикие и домашние животные Proving the variability of species in nature
Proving the variability of species in nature Сердечно-сосудистая система
Сердечно-сосудистая система Презентация на тему Отдел моховидные
Презентация на тему Отдел моховидные  Презентация на тему "Размножение организмов" - скачать презентации по Биологии
Презентация на тему "Размножение организмов" - скачать презентации по Биологии Вопросы для повторения: 1. Перечислите среды обитания живых организмов, с которыми мы познакомились на прошлом уроке. 2. Каковы ус
Вопросы для повторения: 1. Перечислите среды обитания живых организмов, с которыми мы познакомились на прошлом уроке. 2. Каковы ус Презентация на тему "древние пресмыкающиеся" - скачать презентации по Биологии
Презентация на тему "древние пресмыкающиеся" - скачать презентации по Биологии