Содержание
- 2. Ф У Н К Ц И И У Г Л Е В ОД О В -
- 3. - Гидроосмотическая и ионрегулирующая – гетерополисахариды обладают высокой гидрофильностью, отрицательным зарядом и, таким образом, удерживают Н2О,
- 4. К Л А С С И Ф И К А Ц И Я Полисахариды подразделяют на
- 5. М О Н О С А Х А Р И Д Ы Моносахариды – это углеводы,
- 6. Альдозы Кетозы Триозы Тетрозы Пентозы
- 7. Альдозы Кетозы Гексозы
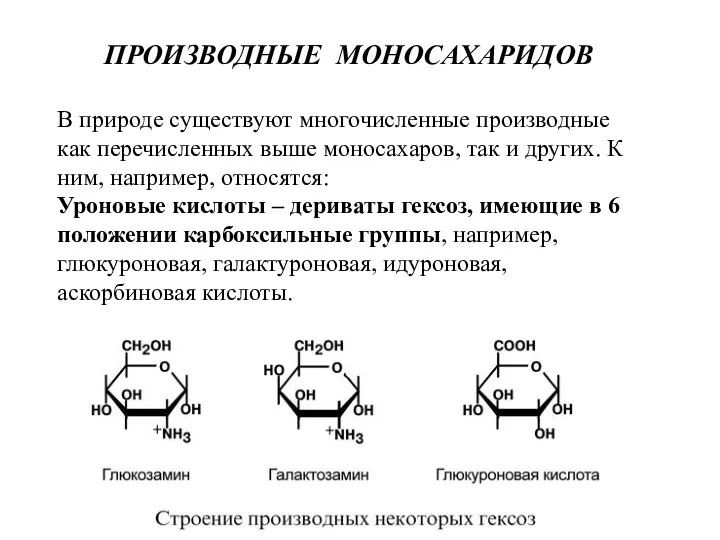
- 8. ПРОИЗВОДНЫЕ МОНОСАХАРИДОВ В природе существуют многочисленные производные как перечисленных выше моносахаров, так и других. К ним,
- 9. Аминосахара – производные моносахаров, содержащие аминогруппы, например, глюкозамин или галактозамин. Эти производные обязательно входят в состав
- 10. Гликозиды – соединения, образующиеся путем конденсации моносахарида (свободного или в составе полисахарида) с гидроксильной группой другого
- 11. Д И С А Х А Р И Д Ы Дисахариды – это углеводы, которые при
- 13. Лактоза – молочный сахар, остаток галактозы связан с глюкозой β1,4-гликозидной связью, содержится в молоке. В некоторых
- 15. П О Л И С А Х А Р И Д Ы Выделяют гомополисахариды, состоящие из
- 16. Амилоза представляет собой неразветвленную цепь с молекулярной массой от 5 до 500 кДа, в которой остатки
- 18. Гликоген – резервный полисахарид животных тканей, в наибольшей мере содержится в печени и мышцах. Структурно он
- 20. ГЕТЕРОПОЛИСАХАРИДЫ Основными представителями гликозаминогликанов является гиалуроновая кислота, хондроитинсульфаты, кератансульфаты и дерматансульфаты, гепарин. Большинство из них характеризуется
- 21. В биохимии используются синонимы – кислые гетерополисахариды (имеют много кислотных групп), гликозаминогликаны (производные глюкозы, содержат аминогруппы).
- 23. И С П О Л Ь З О В А Н И Е У Г Л
- 24. 3. Клиническая медицина: - декстраны используются как компонент кровезаменителей, например, в виде вязкого раствора на 0,9%
- 25. В Н Е Ш Н И Й О Б М Е Н У Г Л Е
- 26. ЖЕЛУДОК Из-за низкой рН амилаза инактивируется, хотя некоторое время расщепление углеводов продолжается внутри пищевого комка. КИШЕЧНИК
- 27. Кроме полостного, имеется еще и пристеночное пищеварение, которое осуществляют: - сахаразо-изомальтазный комплекс (устаревшее название сахараза) –
- 28. О С О Б Е Н Н О С Т И П Е Р Е В
- 29. Еще одной особенностью переваривания углеводов у младенцев является разная скорость гидролиза α-лактозы и β-лактозы. В коровьем
- 30. Н А Р У Ш Е Н И Я П Е Р Е В А Р
- 31. Недостаточность лактазы может проявляться не только у младенцев, но и у взрослых. Примерно у 10-12% людей
- 32. Диагностика. Дифференциальная диагностика нарушений переваривания и всасывания заключается в контроле уровня глюкозы крови после раздельного приема
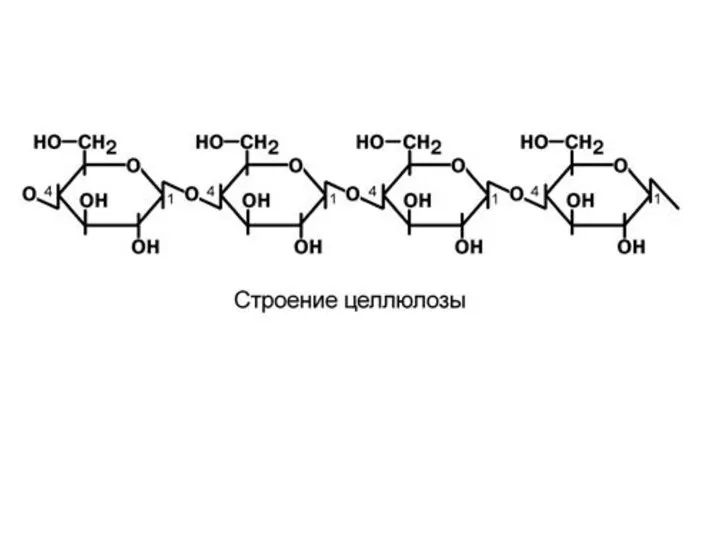
- 33. Р О Л Ь Ц Е Л Л Ю Л О З Ы В П И
- 34. П Е Р Е Н О С Г Л Ю К О З Ы Ч Е
- 35. Примечательно то, что сахар связывается с белком только после того, как с ним свяжется натрий. Белок-транспортер
- 37. Т Р А Н С П О Р Т И З К Р О В И
- 38. Некоторые ткани совершенно нечувствительны к действию инсулина, их называют инсулиннезависимыми. К ним относятся нервная ткань, стекловидное
- 39. Р Е А К Ц И И В З А И М О П Р Е
- 40. П Р Е В Р А Щ Е Н И Е Г А Л А К
- 42. НАРУШЕНИЯ ПРЕВРАЩЕНИЯ ГАЛАКТОЗЫ Нарушения обмена галактозы у детей могут быть вызваны генетическим дефектом одного из ферментов:
- 43. Патогенез. Избыток галактозы превращается в спирт галактитол (дульцитол), накапливающийся в хрусталике и осмотически привлекающий сюда воду.
- 44. Основы лечения. Исключение из рациона молока и других источников галактозы позволяет предотвратить развитие патологических симптомов. Однако
- 45. П Р Е В Р А Щ Е Н И Е Ф Р У К Т
- 46. Особенностью метаболизма фруктозы является то, что фермент фруктокиназа является инсулин-независимым. В результате превращение фруктозы в пировиноградную
- 48. НАРУШЕНИЯ ПРЕВРАЩЕНИЯ ФРУКТОЗЫ Эссенциальная фруктозурия Генетический дефект фруктокиназы приводит к доброкачественной эссенциальной фруктозурии, протекающей безо всяких
- 49. Наследственная фруктозурия Заболевание формируется вследствие наследственных аутосомно-рецессивных дефектов других ферментов обмена фруктозы. Дефект фруктозо-1-фосфатальдолазы проявляется после
- 50. С У Д Ь Б А И И С Т О Ч Н И К И
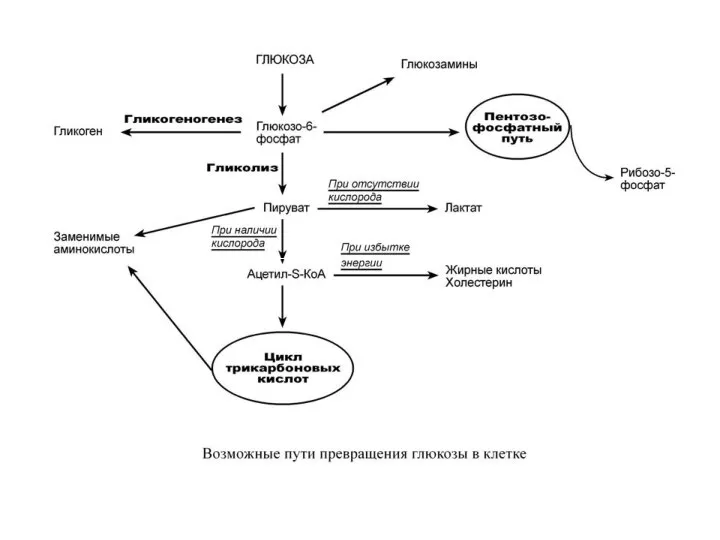
- 51. После проникновения в клетку глюкоза способна превращаться по различным направлениям: - часть глюкозы обязательно используется в
- 53. ФОСФОРИЛИРОВАНИЕ-ДЕФОСФОРИЛИРОВАНИЕ ГЛЮКОЗЫ Попав в любую клетку, глюкоза немедленно фосфорилируется ферментом гексокиназой. Фосфорилирование глюкозы решает сразу несколько
- 54. Дефосфорилирование глюкозы осуществляется глюкозо-6-фосфатазой. Этот фермент есть только в печени и почках. В эпителии канальцев почек
- 55. М Е Т А Б О Л И З М Г Л И К О Г
- 56. Накопление гликогена в мышцах отмечается в период восстановления, особенно при приеме богатой углеводами пищи. В печени
- 57. С И Н Т Е З Г Л И К О Г Е Н А Синтез
- 59. 3. Гликогенсинтаза – образует α-1,4-гликозидные связи и удлиняет гликогеновую цепочку, присоединяя активированный С1 УДФ-глюкозы к С4
- 62. М О Б И Л И З А Ц И Я Г Л И К О
- 63. В гликогенолизе непосредственно участвуют три фермента: Фосфорилаза гликогена (кофермент пиридоксальфосфат) – расщепляет α-1,4-гликозидные связи с образованием
- 64. 3. Амило-α-1,6-глюкозидаза, "деветвящий" фермент – гидролизует α-1,6-гликозидную связь с высвобождением свободной (нефосфорилированной) глюкозы. В результате образуется
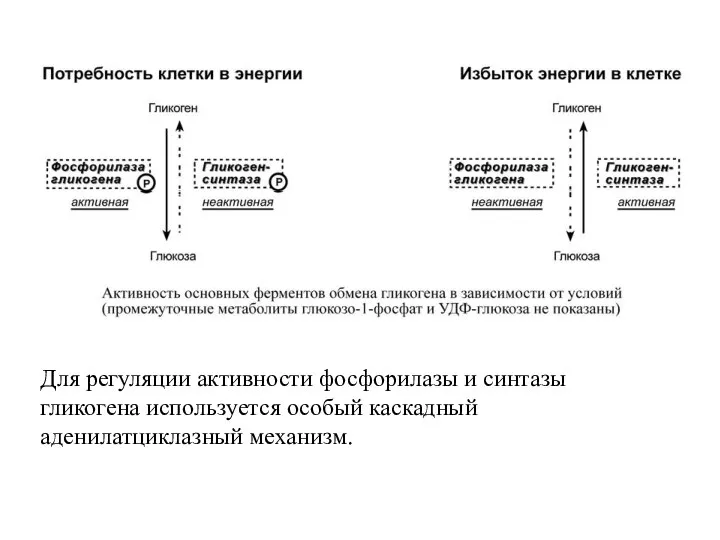
- 66. Р Е Г У Л Я Ц И Я О Б М Е Н А Г
- 67. Скорость фосфорилирования указанных ферментов повышается после воздействия на клетку адреналина, глюкагона и некоторых других гормонов. В
- 68. В клетке осуществляется реципрокная (взаимоисключающая) регуляция. При работе клетки и/или гормональных влияниях активируется протеинкиназа и, как
- 69. Для регуляции активности фосфорилазы и синтазы гликогена используется особый каскадный аденилатциклазный механизм.
- 70. АКТИВАЦИЯ ФОСФОРИЛАЗЫ ГЛИКОГЕНА Скорость гликогенолиза лимитируется только скоростью работы фосфорилазы гликогена. Ее активность может изменяться тремя
- 71. 3. G-белок активирует фермент аденилатциклазу; 4. Аденилатциклаза превращает АТФ в циклический АМФ (цАМФ) – вторичный посредник
- 73. Кроме гормонов, влияющих на активность аденилатциклазы через G-белки, существуют иные способы регуляции этого механизма. Например, после
- 74. Кальций-зависимая активация Активация ионами кальция заключается в активации киназы фосфорилазы не протеинкиназой, а ионами Ca2+ и
- 75. Аллостерическая активация Также существует активация фосфорилазы гликогена с помощью АМФ – аллостерическая активация благодаря присоединению АМФ
- 76. Г Л И К О Г Е Н О В Ы Е Б О Л Е
- 77. Печеночные гликогенозы Самый частый гликогеноз I типа или болезнь фон Гирке обусловлен аутосомно-рецессивным дефектом глюкозо-6-фосфатазы. Из-за
- 78. Гликогеноз III типа или болезнь Форбса-Кори или лимит-декстриноз – это аутосомно-рецессивный дефект амило-α-1,6-глюкозидазы, "деветвящего" фермента, гидролизующего
- 80. Мышечные гликогенозы Для этой группы гликогенозов характерны изменения ферментов мышечной ткани. Это приводит к нарушению энергообеспечения
- 81. АГЛИКОГЕНОЗЫ Агликогенозы – состояния, связанные с отсутствием гликогена. В качестве примера агликогеноза можно привести наследственный аутосомно-рецессивный
- 82. О К И С Л Е Н И Е Г Л Ю К О З Ы
- 84. Вместе с этим, существенное значение также имеет способность пирувата карбоксилироваться в оксалоацетат, особенно эта реакция активна
- 85. Многие клетки организма способны к анаэробному окислению глюкозы. Для эритроцитов он является единственным источником энергии. Клетки
- 86. Г Л И К О Л И З Анаэробное превращение глюкозы локализуется в цитозоле и включает
- 88. Первая реакция гликолиза сводится к превращению глюкозы в реакционно-способное соединение за счет фосфорилирования 6-го, не включенного
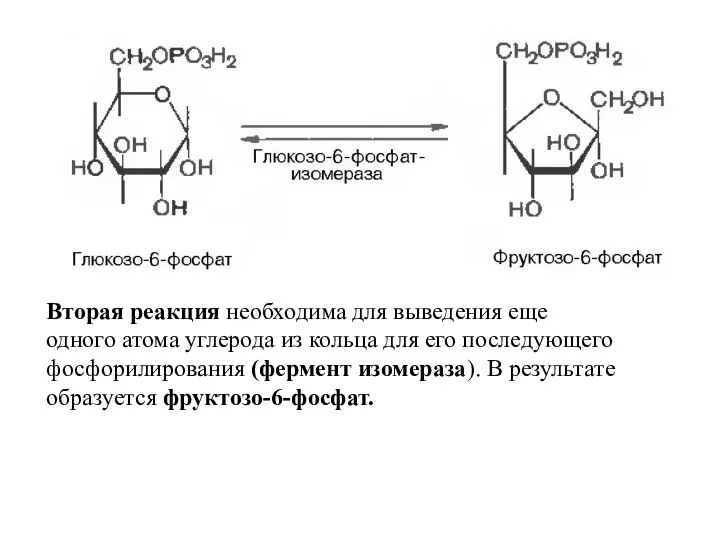
- 89. Вторая реакция необходима для выведения еще одного атома углерода из кольца для его последующего фосфорилирования (фермент
- 90. Третья реакция – фермент фосфофруктокиназа фосфорилирует фруктозо-6-фосфат с образованием почти симметричной молекулы фруктозо-1,6-дифосфата.
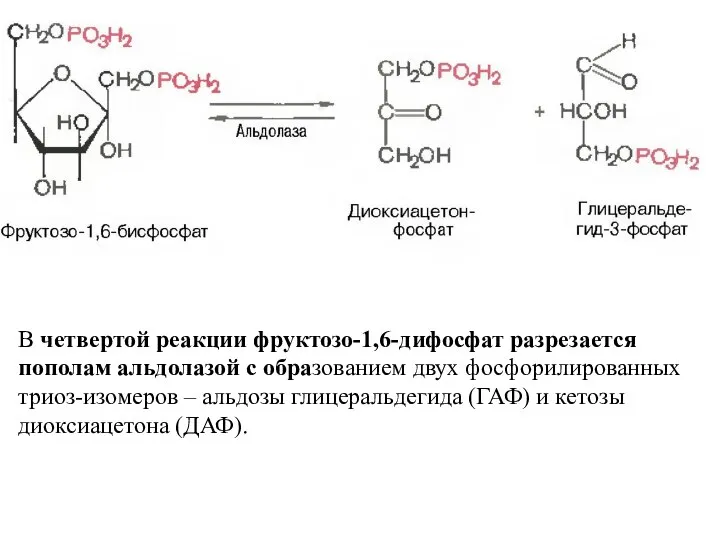
- 91. В четвертой реакции фруктозо-1,6-дифосфат разрезается пополам альдолазой с образованием двух фосфорилированных триоз-изомеров – альдозы глицеральдегида (ГАФ)
- 92. Пятая реакция подготовительного этапа – переход глицеральдегидфосфата и диоксиацетонфосфата друг в друга при участии триозофосфатизомеразы.
- 93. Равновесие реакции сдвинуто в пользу диоксиацетонфосфата, его доля составляет 97%, доля глицеральдегидфосфата – 3%. Эта реакция,
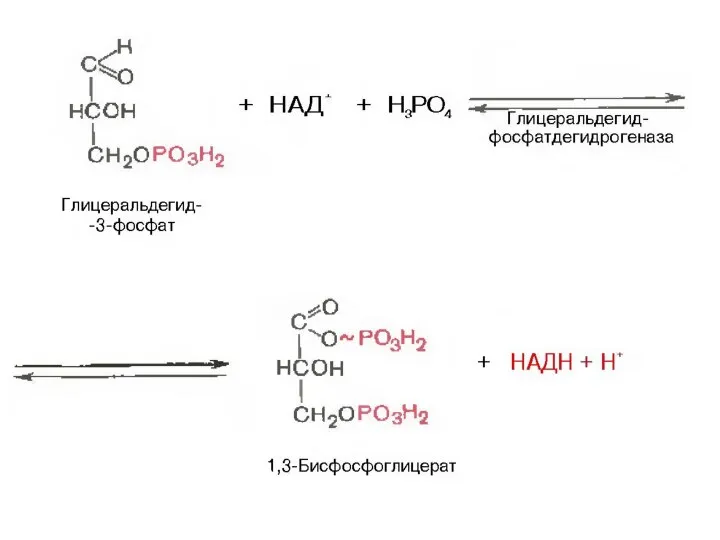
- 94. Второй этап гликолиза Второй этап гликолиза – это освобождение энергии, содержащейся в глицеральдегид-фосфате, и запасание ее
- 96. В седьмой реакции (фермент фосфоглицераткиназа) - энергия фосфоэфирной связи, заключенная в 1,3-дифосфоглицерате тратится на образование АТФ.
- 97. Восьмая реакция – синтезированный в предыдущей реакции 3-фосфоглицерат под влиянием фосфоглицератмутазы изомеризуется в 2-фосфоглицерат.
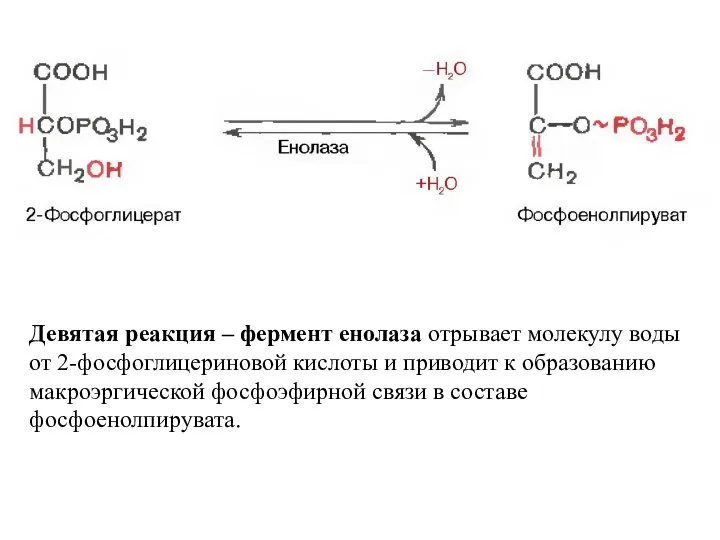
- 98. Девятая реакция – фермент енолаза отрывает молекулу воды от 2-фосфоглицериновой кислоты и приводит к образованию макроэргической
- 99. Десятая реакция гликолиза – еще одна реакция субстратного фосфорилирования -- заключается в переносе пируваткиназой макроэргического фосфата
- 100. Последняя реакция бескислородного окисления глюкозы, одиннадцатая – образование молочной кислоты из пирувата под действием лактатдегидрогеназы. Важно
- 101. Г Л И К О Л И Т И Ч Е С К А Я О
- 103. Э Н Е Р Г Е Т И Ч Е С К И Й Э Ф
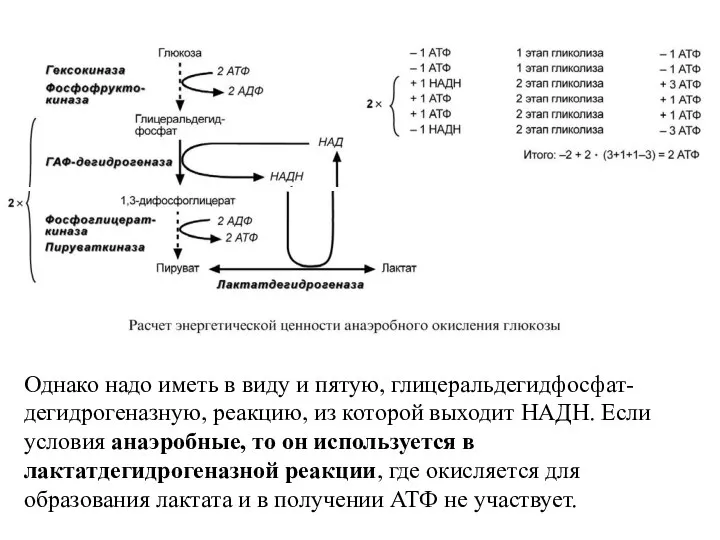
- 104. Анаэробное окисление На подготовительном этапе на активацию глюкозы затрачивается 2 молекулы АТФ, фосфат каждой из которых
- 105. Однако надо иметь в виду и пятую, глицеральдегидфосфат-дегидрогеназную, реакцию, из которой выходит НАДН. Если условия анаэробные,
- 106. Аэробное окисление Если в клетке имеется кислород, то НАДН из шестой реакции гликолиза направляется в митохондрию,
- 107. Образовавшийся в гликолизе пируват в аэробных условиях превращается в ПВК-дегидрогеназном комплексе в ацетил-S-КоА, при этом образуется
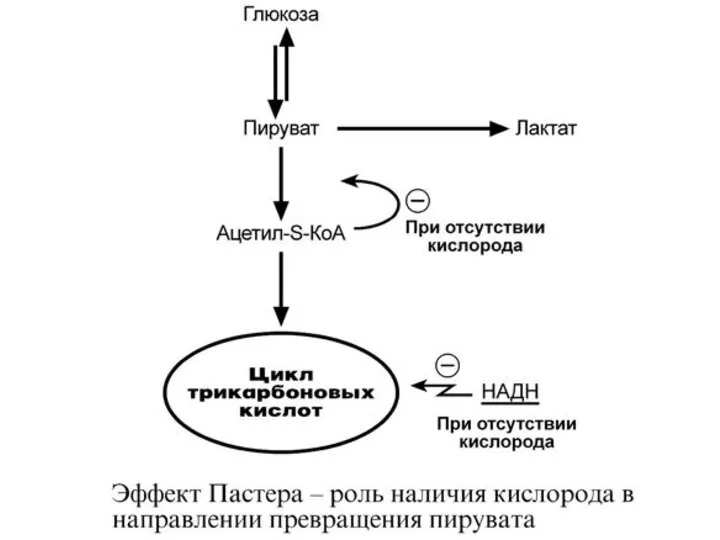
- 109. Э Ф Ф Е К Т П А С Т Е Р А Эффект Пастера –
- 111. Ч Е Л Н О Ч Н Ы Е С И С Т Е М Ы
- 112. Глицеролфосфатный челночный механизм Ключевыми ферментами глицеролфосфатного челнока являются изоферменты глицерол-3-фосфат-дегидрогеназы – цитоплазматический и митохондриальный. Они отличаются
- 114. Малат-аспартатный челночный механизм Этот механизм более сложен: постоянно идущие в цитоплазме реакции трансаминирования аспартата поставляют оксалоацетат,
- 116. Скачать презентацию







































































































 Ткани, их строение, местонахождение и функции
Ткани, их строение, местонахождение и функции Животные Африки
Животные Африки Авторы: Топильская Вероника ученица 9 класса Учитель: Сидельникова И.М.
Авторы: Топильская Вероника ученица 9 класса Учитель: Сидельникова И.М. Презентация на тему Синантропные животные
Презентация на тему Синантропные животные Водоросли. Общая характеристика водорослей
Водоросли. Общая характеристика водорослей Процессы диффузии в организме человека. Подготовил: Савченко Анна Руководитель: Владимир Овчинников
Процессы диффузии в организме человека. Подготовил: Савченко Анна Руководитель: Владимир Овчинников  Удобрения
Удобрения Государственный реестр селекционных достижений
Государственный реестр селекционных достижений Корень. Строение и функции
Корень. Строение и функции Сохранение биологического разнообразия
Сохранение биологического разнообразия Презентация на тему "Профілактика ВІЛ/СНІДу" - скачать бесплатно презентации по Биологии
Презентация на тему "Профілактика ВІЛ/СНІДу" - скачать бесплатно презентации по Биологии Обобщение Тема: мхи, лишайники, папоротники, голосеменные.
Обобщение Тема: мхи, лишайники, папоротники, голосеменные. Круговорот азота в природе
Круговорот азота в природе LAMARK (1)
LAMARK (1) Предпосылки возникновения учения Ч. Дарвина
Предпосылки возникновения учения Ч. Дарвина Взаимодействие аллельных и неаллельных генов. Автор: Качаева Л.А., учитель биологии, МБОУ «ООШ №4».
Взаимодействие аллельных и неаллельных генов. Автор: Качаева Л.А., учитель биологии, МБОУ «ООШ №4». Зимующие птицы
Зимующие птицы Круглые черви. Признаки круглых червей
Круглые черви. Признаки круглых червей Приспособленность организмов к действию факторов среды
Приспособленность организмов к действию факторов среды La reazione a catena della DNA polimerasi
La reazione a catena della DNA polimerasi Окружающий мир 3 класс Животные Красной книги
Окружающий мир 3 класс Животные Красной книги Как животные к зиме готовятся (для дошкольников)
Как животные к зиме готовятся (для дошкольников) Проращивание фасоли
Проращивание фасоли Презентация на тему "Дигибридное скрещивание" - скачать презентации по Биологии
Презентация на тему "Дигибридное скрещивание" - скачать презентации по Биологии Парнокопытные животные
Парнокопытные животные Основные опасности
Основные опасности Центральная нервная система. Спинной мозг
Центральная нервная система. Спинной мозг Көбею. Жынысты және жыныссыз көбеюдің түрлері
Көбею. Жынысты және жыныссыз көбеюдің түрлері