Содержание
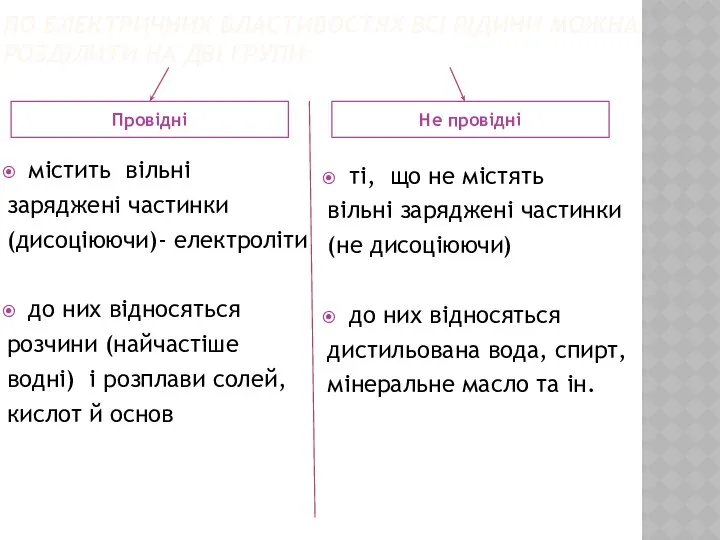
- 2. По електричних властивостях всі рідини можна розділити на дві групи: Провідні Не провідні містить вільні заряджені
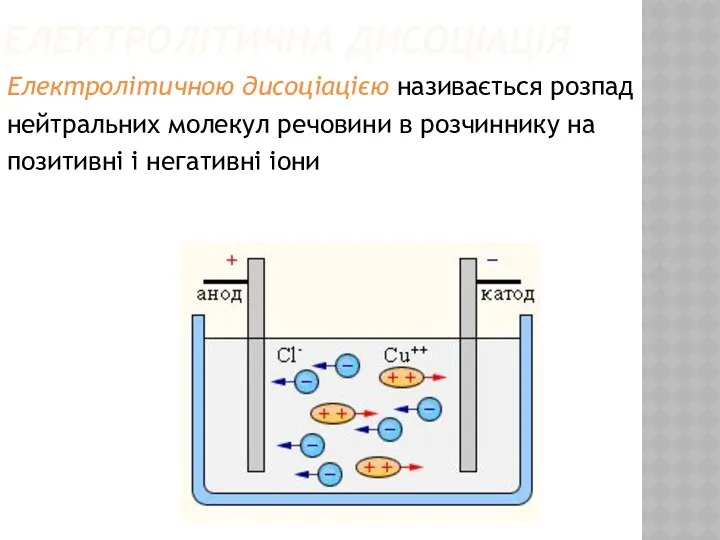
- 3. Електролітична дисоціація Електролітичною дисоціацією називається розпад нейтральних молекул речовини в розчиннику на позитивні і негативні іони
- 4. Розчини солей, кислот і підстав, здатні проводити електричний струм, називаються електролітами.
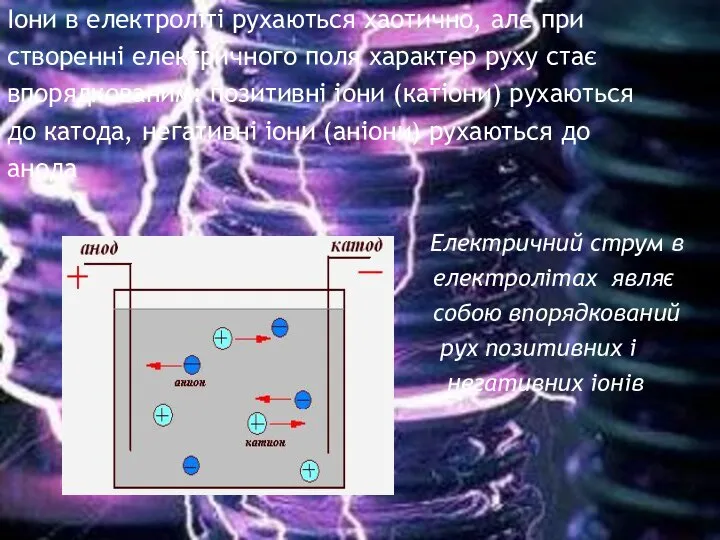
- 5. Іони в електроліті рухаються хаотично, але при створенні електричного поля характер руху стає впорядкованим: позитивні іони
- 6. Проходження електричного струму через електроліт обов'язково супроводжується виділенням речовини в твердому або газоподібному стані на поверхні
- 8. Майкл Фарадей на основі експериментів з різними електролітами встановив, що при електролізі маса m виділяється на
- 9. Існують не тільки рідкі, але і тверді електроліти. Прикладом твердого електроліту може служити скло. У складі
- 10. Застосування Явище електролізу застосовується на практиці для одержання багатьох металів з розчину солей. За допомогою електролізу
- 12. Скачать презентацию






 Интеллектуальная игра «Физбой» по физике
Интеллектуальная игра «Физбой» по физике Диоды средней мощности
Диоды средней мощности Механика. Основные понятия кинематики
Механика. Основные понятия кинематики Густав Роберт Кирхгов
Густав Роберт Кирхгов Сила тяжести, вес тела
Сила тяжести, вес тела Кафедра общей физики и молекулярной электроники
Кафедра общей физики и молекулярной электроники Свет в нашей жизни
Свет в нашей жизни Обратимые и необратимые термодинамические процессы. (Лекция 8)
Обратимые и необратимые термодинамические процессы. (Лекция 8) Дисперсия. Интерференция. Дифракция
Дисперсия. Интерференция. Дифракция Постоянный ток
Постоянный ток BCS Theory of Superconductivity
BCS Theory of Superconductivity Измерение расхода и количества вещества
Измерение расхода и количества вещества Закон Гука. Деформация. (Занятие 1)
Закон Гука. Деформация. (Занятие 1) «Интерактивная мозаика»-2017. Знатоки физики 8 класс
«Интерактивная мозаика»-2017. Знатоки физики 8 класс Лазер
Лазер Исследование силовых выпрямителей. (Раздел 1)
Исследование силовых выпрямителей. (Раздел 1) Закон сохранения импульса
Закон сохранения импульса Лекція 6. Визначення напружень при згинанні. Умови міцності при згинанні
Лекція 6. Визначення напружень при згинанні. Умови міцності при згинанні Основы радиационной дозиметрии
Основы радиационной дозиметрии  Осветительная и оптическая системы спектральных приборов
Осветительная и оптическая системы спектральных приборов Physical Output
Physical Output Выполнили: Быкова Наталья; Мертенс Алёна; Пермякова Лина; Гизатулина Нина Руководитель: Попова Ирина Александровна
Выполнили: Быкова Наталья; Мертенс Алёна; Пермякова Лина; Гизатулина Нина Руководитель: Попова Ирина Александровна Магнитное поле. Применение правил буравчика, правой и левой руки
Магнитное поле. Применение правил буравчика, правой и левой руки Электромагнитные волны
Электромагнитные волны Механизмы релаксации напряженно-деформированного состояния металла деталей машин. Модели вязко-хрупкого перехода
Механизмы релаксации напряженно-деформированного состояния металла деталей машин. Модели вязко-хрупкого перехода Ядерные реакции и их воздействия
Ядерные реакции и их воздействия Миражи
Миражи Дислокации в кристаллах. Влияние дислокаций на механические свойства кристаллов
Дислокации в кристаллах. Влияние дислокаций на механические свойства кристаллов