Содержание
- 2. Энтропия Адиабатические процессы в термодинамических системах могут быть равновесными и неравновесными. Для характеристики равновесного адиабатического процесса
- 5. Следовательно, S = const, адиабатный процесс по другому называют – изоэнтропийным процессом. Энтропия системы пропорциональна массе
- 6. Изопроцессы могут быть изображены графически в координатных системах, по осям которых отложены параметры состояния. давление p
- 7. Удобство координатной системы р, V В масштабе чертежа внешняя работа изображается площадью, ограниченной кривой процесса 1—2
- 8. Круговые (замкнутые) процессы Совокупность термодинамических процессов, в результате которых система возвращается в исходное состояние, называется круговым
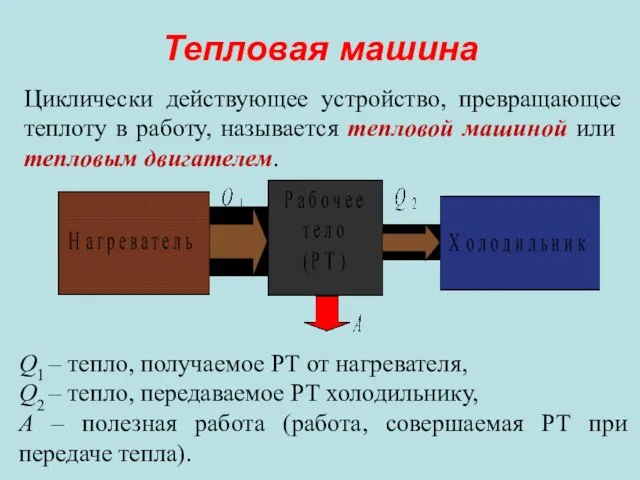
- 9. Тепловая машина Циклически действующее устройство, превращающее теплоту в работу, называется тепловой машиной или тепловым двигателем. Q1
- 12. Для того чтобы поршень совершил полезную работу, необходимо выполнить условие: А2 Процесс 2–1: – первое начало
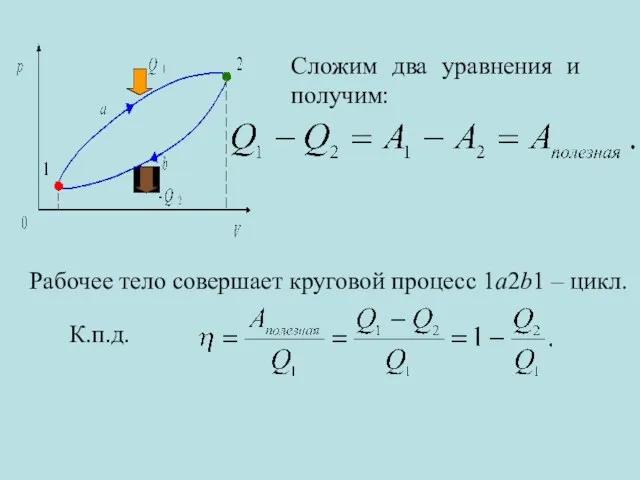
- 13. Сложим два уравнения и получим: Рабочее тело совершает круговой процесс 1a2b1 – цикл. К.п.д.
- 14. Процесс возвращения рабочего тела в исходное состояние происходит при более низкой температуре. Следовательно, для работы тепловой
- 15. Цикл Карно Никола Леонард Сади Карно –французский офицер инженерных войск, в 1824 г. опубликовал сочинение «Размышления
- 16. из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей и холодильников, наибольшим КПД обладают обратимые
- 17. Цикл Карно.
- 18. Процесс А-В – изотермическое расширение Процесс В-С – адиабатическое расширение γ – коэффициент Пуассона. Цикл Карно
- 19. Процесс С-D – изотермическое сжатие Процесс D-A – адиабатическое сжатие Цикл Карно
- 21. КПД цикла Карно η Если Т2 = 0, то η = 1, что невозможно, т.к. абсолютный
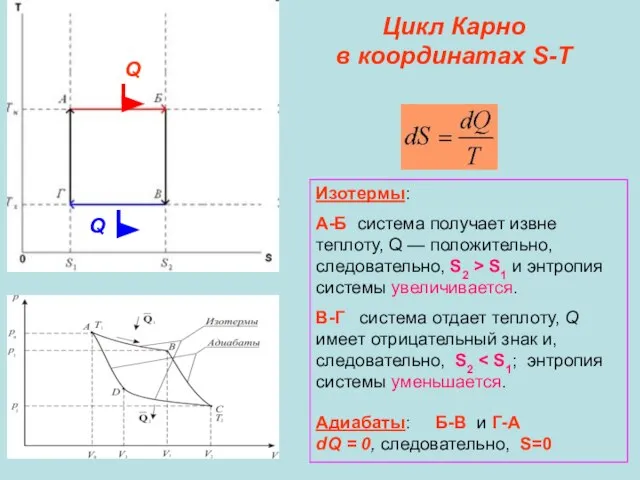
- 22. Цикл Карно в координатах S-T Изотермы: А-Б система получает извне теплоту, Q — положительно, следовательно, S2
- 23. Теоремы Карно. К.п.д. η обратимой идеальной тепловой машины Карно не зависит от рабочего вещества. 2. К.п.д.
- 24. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 25. Функция состояния, дифференциал которой , называется – энтропией. Энтропия обозначается S – это отношение полученной или
- 26. При любом необратимом процессе в замкнутой системе энтропия возрастает. выражение dS > 0 называют неравенством Клаузиуса.
- 27. Так как для каждого из подвергнутых исследованию круговых процессов сумма равна нулю, то выражение универсально, т.е.
- 28. 1. круговые процессы, в течение которых система только получает, но не отдает теплоту, невозможны. В этом
- 29. 2. круговые процессы, в течение которых система только отдает теплоту, но не получает невозможны. Тогда все
- 30. осуществить такой круговой процесс, в результате которого система полностью превращала бы в механическую работу всю полученную
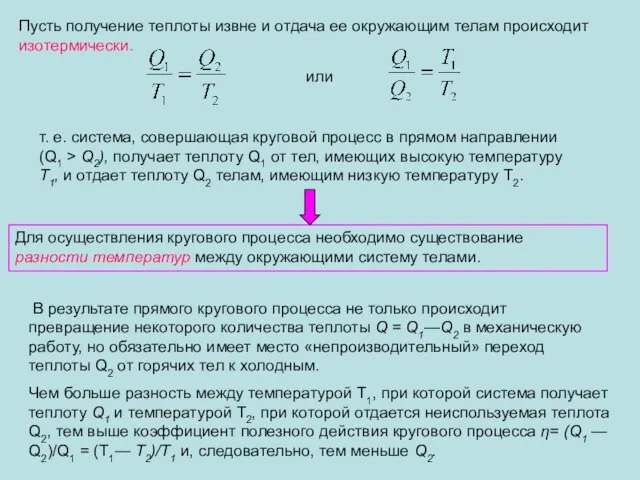
- 31. Пусть получение теплоты извне и отдача ее окружающим телам происходит изотермически. или т. е. система, совершающая
- 32. В результате круговых процессов, идущих в обратном направлении, система получает теплоту Q1 от окружающих тел, имеющих
- 33. Второе начало термодинамики 1) невозможны круговые процессы, в результате которых система только получала бы извне теплоту
- 34. Совершение над газом работы на элементарном участке dh. Совершаемая работа показана красными лампочками Тепловое движение молекул
- 35. U2-U1=Q - A Применяя это соотношение к круговым процессам, полагали U1= U2, и поэтому Q =
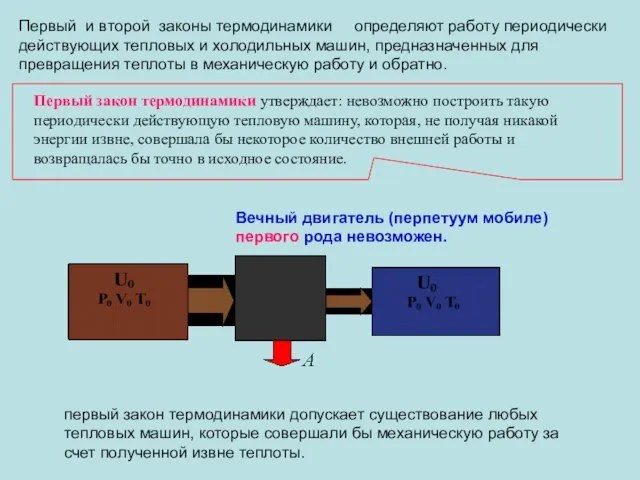
- 36. Первый и второй законы термодинамики определяют работу периодически действующих тепловых и холодильных машин, предназначенных для превращения
- 37. Q =Q Второй закон термодинамики ограничивает возможности превращения теплоты в механическую работу: невозможно построить такую периодически
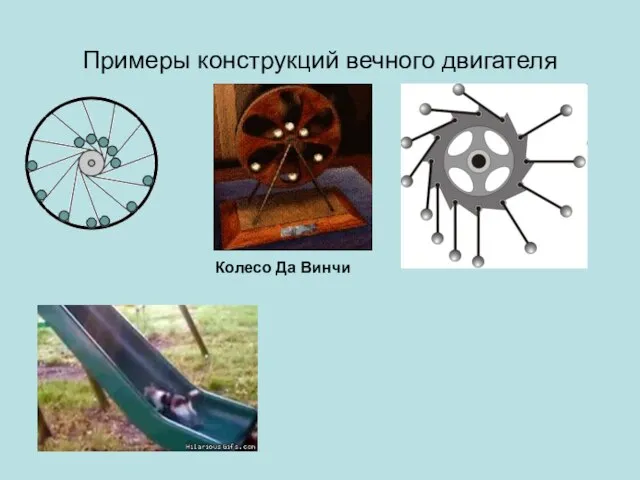
- 38. Примеры конструкций вечного двигателя Колесо Да Винчи
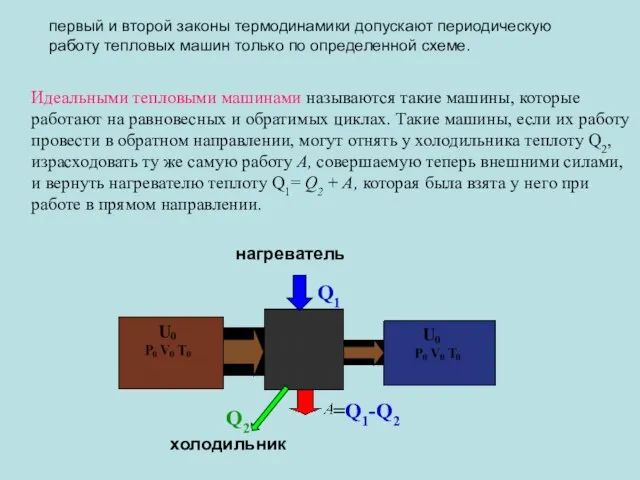
- 39. Q1 =Q1-Q2 Q2 нагреватель холодильник Идеальными тепловыми машинами называются такие машины, которые работают на равновесных и
- 40. Можно показать, что при заданных температурах источника теплоты Т1 и холодильника Т2 коэффициент полезного действия КПД
- 41. Идеальный газ
- 42. Идеальным газом называется газ, который удовлетворяет следующим условиям: Идеальный газ 1) собственный объем частиц (молекул или
- 43. Выведем «основное уравнение кинетической теории газов», связывающее давление газа со скоростями движения его частиц. Основное уравнение
- 44. Согласно второму закону Ньютона, это изменение должно быть вызвано силой, приложенной со стороны стенки к частицам
- 45. Мы предполагали, что скорости молекул одинаковы; если же в газе имеются молекулы с разными скоростями vкв
- 46. Функцию f(v) = ΔNI(N ·Δv), показывающую относительное число молекул, приходящихся на единицу интервала скоростей, называют функцией
- 48. Уравнение состояния идеального газа Пусть в объеме V при давлении р и температуре Т находятся N
- 49. при данном р и Т V ~ М ~ N ~ N, тогда k – коффициент
- 51. Скачать презентацию









































 Синтез комбинационных устройств
Синтез комбинационных устройств Презентация по физике "«Единицы измернений»" - скачать
Презентация по физике "«Единицы измернений»" - скачать  Лекция 20 Тема: Реальные газы. Уравнение Ван-дер-Вальса. Фазовые переходы.
Лекция 20 Тема: Реальные газы. Уравнение Ван-дер-Вальса. Фазовые переходы.  Использование энергии солнца на земле
Использование энергии солнца на земле Жан Батист Перрен. Опыт Перрена
Жан Батист Перрен. Опыт Перрена Программа испытаний автомобилей
Программа испытаний автомобилей Звуковой резонанс презентация Апачиди Лиза 9 а
Звуковой резонанс презентация Апачиди Лиза 9 а Физика как наука в истории человечества
Физика как наука в истории человечества Полет на Марс – Что ждет добровольцев?
Полет на Марс – Что ждет добровольцев?  Изучение микроструктуры процессов релаксации в плазме
Изучение микроструктуры процессов релаксации в плазме Презентация Спектры и спектральный анализ
Презентация Спектры и спектральный анализ  Презентация по физике Модели атома
Презентация по физике Модели атома  Ядерный реактор
Ядерный реактор Закон Ома
Закон Ома Аттестационная работа. Kidwind project. Результаты участия
Аттестационная работа. Kidwind project. Результаты участия Діелектрики в електричному полі. Конденсатори
Діелектрики в електричному полі. Конденсатори  А звезды тем не менее, так близко , но все также далеки… История исследования космоса и развитие космонавти
А звезды тем не менее, так близко , но все также далеки… История исследования космоса и развитие космонавти Оптика Лекция 15
Оптика Лекция 15  Приборы обработки звука внутри и снаружи
Приборы обработки звука внутри и снаружи Явище електромагнітної індукції. Досліди Фарадея. Правило Ленца
Явище електромагнітної індукції. Досліди Фарадея. Правило Ленца ОПОРНЫЕ КОНСПЕКТЫ ПО ФИЗИКЕ МЕХАНИКА 9 КЛАСС
ОПОРНЫЕ КОНСПЕКТЫ ПО ФИЗИКЕ МЕХАНИКА 9 КЛАСС Радиациялық сәулелену
Радиациялық сәулелену Основы слесарно-сборочных и электромонтажных работ. Обязанности электромонтера по ремонту и обслуживанию электрооборудования
Основы слесарно-сборочных и электромонтажных работ. Обязанности электромонтера по ремонту и обслуживанию электрооборудования Ядерный реактор
Ядерный реактор Статичне електричне поле. (Лекція 11)
Статичне електричне поле. (Лекція 11) Физические основы магнитного метода контроля
Физические основы магнитного метода контроля Начальный участок струи. Проектирование ствола
Начальный участок струи. Проектирование ствола Классификация навигационных систем. Параметры движения в пространстве
Классификация навигационных систем. Параметры движения в пространстве