Феноменологическая термодинамика Энтропия и ее статистический смысл. Критическая изотерма. Эффект Джоуля-Томсона. (Лекция 12)
Содержание
- 2. Содержание предыдущей лекции Феноменологическая термодинамика Термодинамическое равновесие и температура. Внутренняя энергия. Закон равномерного распределения энергии по
- 3. Контрольный вопрос Теплоемкость одноатомного газа при повышении температуры: а) растет, б) не изменяется, в) понижается, г)
- 4. Содержание сегодняшней лекции Феноменологическая термодинамика Энтропия и ее статистический смысл. Энтропия как количественная мера хаотичности. Второе
- 5. Энтропия и ее статистический смысл Теплопередача от более нагретого тела к менее нагретому – выравнивание температур.
- 6. Энтропия и ее статистический смысл Закрытый сосуд: стремление к более равномерному распределению молекул – переход от
- 7. Энтропия и ее статистический смысл Направленность всех процессов во Вселенной к беспорядку. Стремление изолированной системы перейти
- 8. Энтропия и ее статистический смысл Макросостояние системы – одна из возможных реализаций совокупности микросостояний системы, описываемое
- 9. Энтропия и ее статистический смысл Предположение: равновероятность реализации различных микросостояний в изолированной системе. Эксперимент: вероятность реализации
- 10. Энтропия и ее статистический смысл Возможность реализации конкретного макросостояния различными способами, каждому из которых соответствует некоторое
- 11. Второе начало термодинамики - (закон возрастания энтропии): энтропия изолированной системы может либо только возрастать, либо по
- 12. Второе начало термодинамики Обратимый процесс: энтропия постоянна (dS = 0) → S = const. Необратимый процесс:
- 13. Теорема Нернста (третье начало термодинамики) Упорядоченное или неслучайное состояние – состояние, осуществляемое небольшим числом способов. Энтропия
- 14. Энтропия как количественная мера хаотичности Использование понятия «энтропия» для определения направленности процессов в природе.
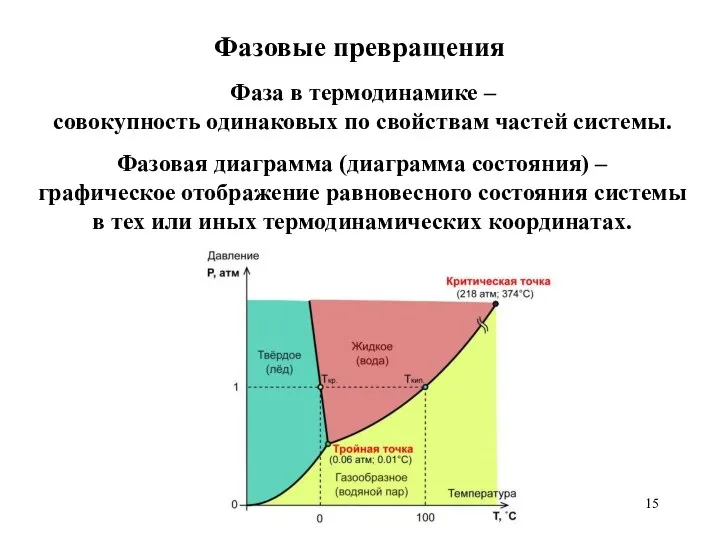
- 15. Фазовые превращения Фаза в термодинамике – совокупность одинаковых по свойствам частей системы. Фазовая диаграмма (диаграмма состояния)
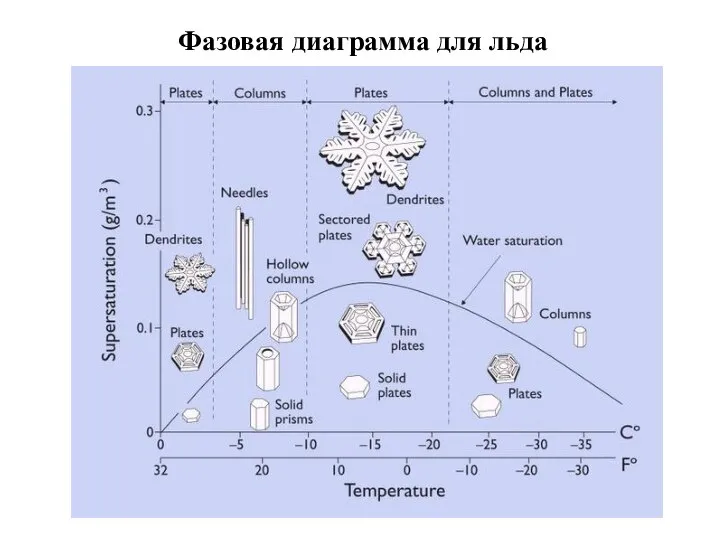
- 16. Фазовая диаграмма для льда
- 17. Уравнение Клапейрона-Клаузиуса Уравнение Клапейрона-Клаузиуса – термодинамическое уравнение, относящееся к квазистатическим (равновесным) процессам перехода вещества из одной
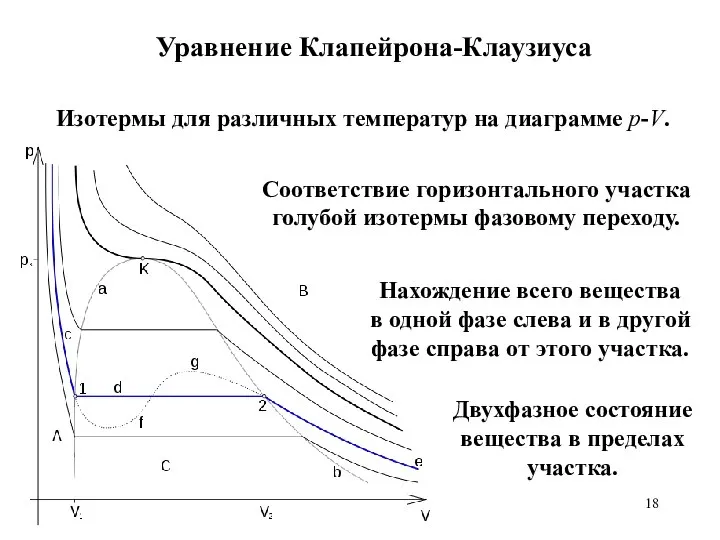
- 18. Уравнение Клапейрона-Клаузиуса Изотермы для различных температур на диаграмме p-V. Соответствие горизонтального участка голубой изотермы фазовому переходу.
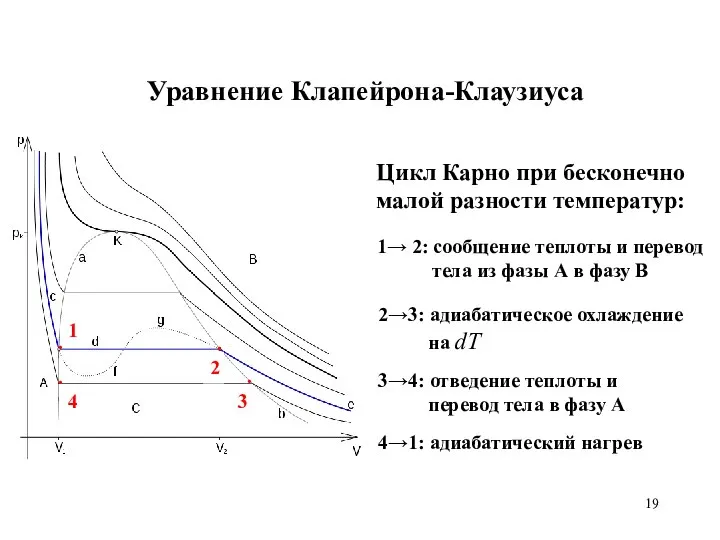
- 19. Уравнение Клапейрона-Клаузиуса 2→3: адиабатическое охлаждение на dT Цикл Карно при бесконечно малой разности температур: 1→ 2:
- 20. Уравнение Клапейрона-Клаузиуса
- 21. Уравнение Клапейрона-Клаузиуса уравнение Клапейрона-Клаузиуса, описывающее зависимость равновесного давления от температуры для однокомпонентной системы, состоящей из двух
- 22. Реальные газы Повышение давления и понижение температуры – увеличение плотности реального газа. Необходимость введения поправок и
- 23. Реальные газы p – давление, оказываемое на газ извне (равное давлению газа на стенки сосуда), a
- 24. Реальные газы Связь поправки Vм c объемом, занимаемым самими молекулами.
- 25. Критическая изотерма Ван-дер-Ваальсовский газ – воображаемый газ, точно подчиняющийся уравнению Ван-дер-Ваальса. Уравнения изотерм для Ван-дер-Ваальсовского газа
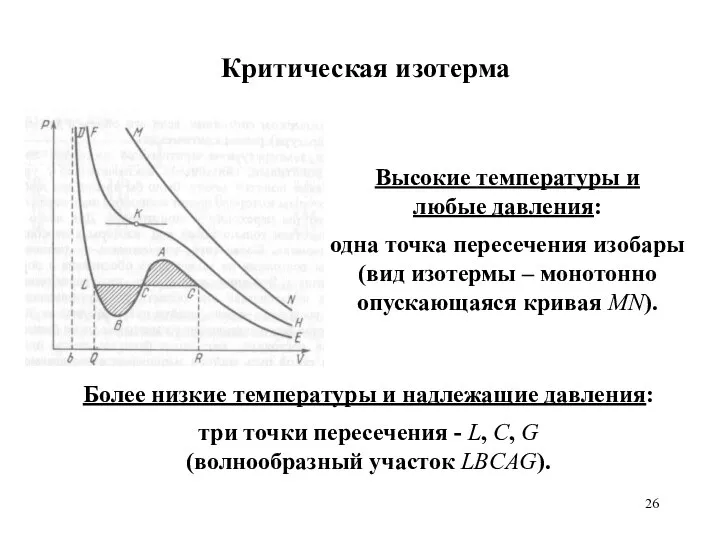
- 26. Критическая изотерма Высокие температуры и любые давления: одна точка пересечения изобары (вид изотермы – монотонно опускающаяся
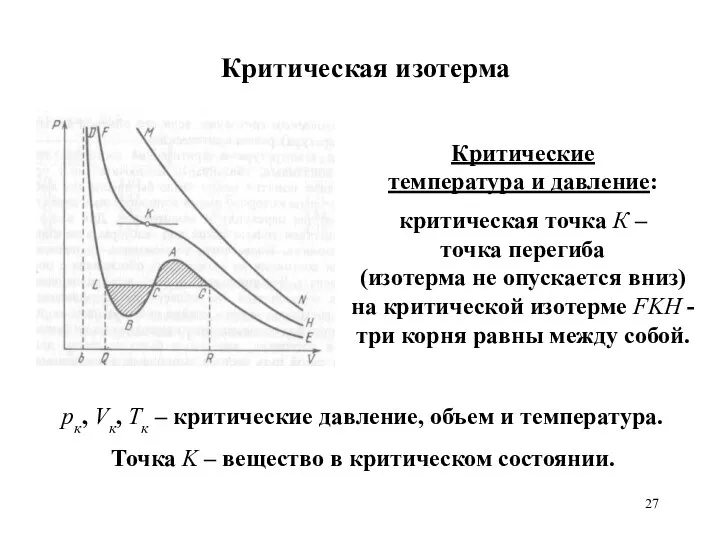
- 27. Критическая изотерма Критические температура и давление: критическая точка К – точка перегиба (изотерма не опускается вниз)
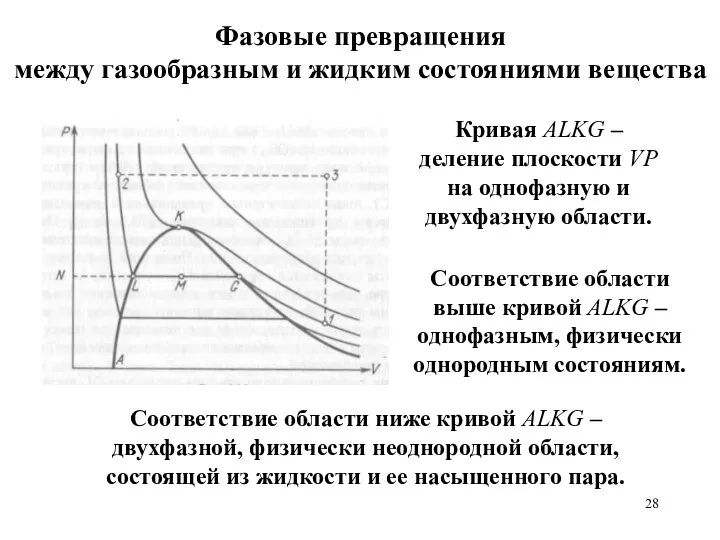
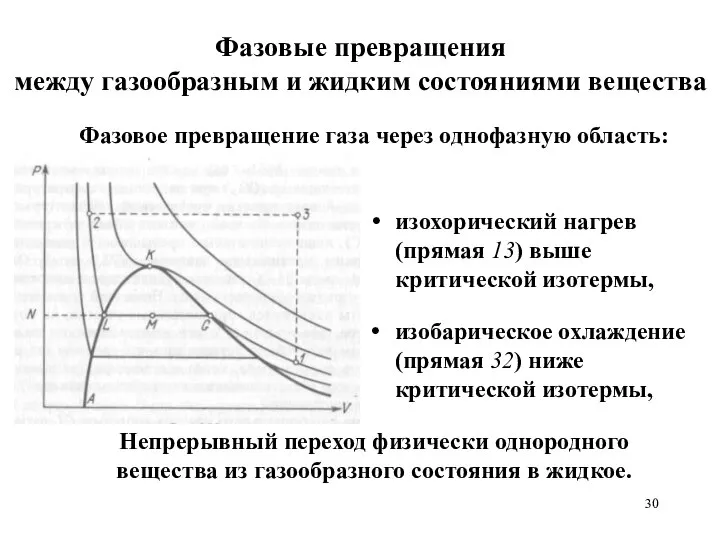
- 28. Фазовые превращения между газообразным и жидким состояниями вещества Кривая АLKG – деление плоскости VP на однофазную
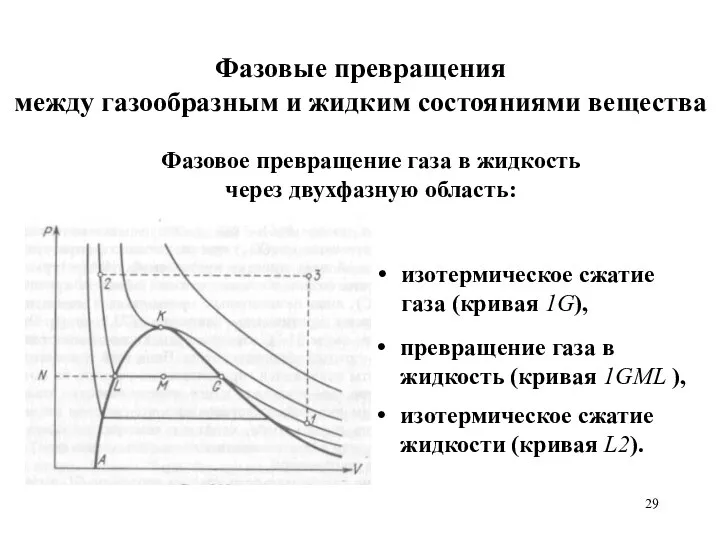
- 29. Фазовые превращения между газообразным и жидким состояниями вещества изотермическое сжатие газа (кривая 1G), превращение газа в
- 30. Фазовые превращения между газообразным и жидким состояниями вещества изохорический нагрев (прямая 13) выше критической изотермы, изобарическое
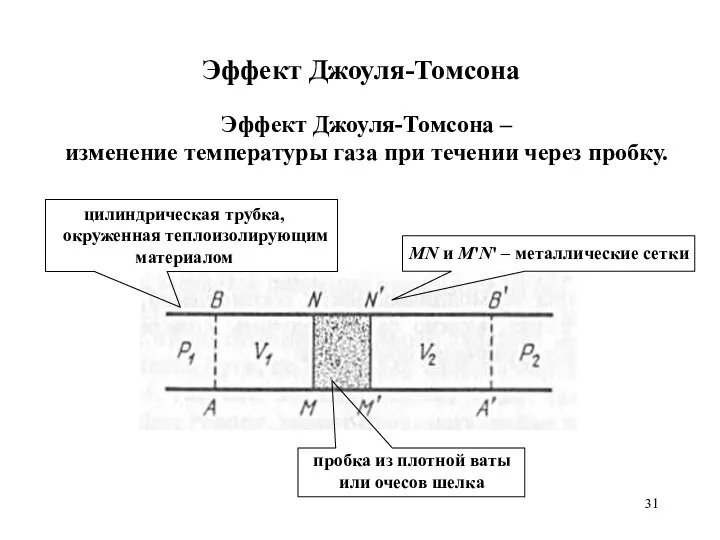
- 31. Эффект Джоуля-Томсона MN и M'N' – металлические сетки пробка из плотной ваты или очесов шелка Эффект
- 32. Эффект Джоуля-Томсона Ламинарное и медленное течение газа через пробку под действием разности давлений p1 и p2.
- 33. Эффект Джоуля-Томсона V1 – объем пространства ABNM, занимаемый газом до прохождения через пробку, V2 – объем
- 34. Эффект Джоуля-Томсона p1·S·AM = p1V1 – работа, совершаемая над газом, при перемещении границы АВ в положение
- 35. Эффект Джоуля-Томсона Неизменность физического состояния пробки и ее внутренней энергии. 1-ое начало термодинамики для системы: U2
- 36. Эффект Джоуля-Томсона Энтальпия – функция состояния, приращение которой при изобарическом процессе дает теплоту, полученную системой. U2
- 37. Эффект Джоуля-Томсона Вывод: внутренняя энергия идеального газа не зависит от занимаемого им объема. Эксперимент Джоуля-Томпсона: тем
- 39. Скачать презентацию


























 Как электромагнитные волны помогают бороться с пандемией?
Как электромагнитные волны помогают бороться с пандемией? Оптика и механика. Физика для химиков. День пятый
Оптика и механика. Физика для химиков. День пятый Электрическое освещение бытовых и промышленных объектов. Лекция 2
Электрическое освещение бытовых и промышленных объектов. Лекция 2 Cокол тысячелетия 10,08
Cокол тысячелетия 10,08 Магниты. Природное ископаемой магнетит. Искусственные магниты. Постоянный и временный магнит. Электромагниты
Магниты. Природное ископаемой магнетит. Искусственные магниты. Постоянный и временный магнит. Электромагниты Эрнест Резерфорд
Эрнест Резерфорд Спектроскопические методы. Общая характеристика
Спектроскопические методы. Общая характеристика Презентация по физике на тему Приливы, отливы, их использование
Презентация по физике на тему Приливы, отливы, их использование Магнитный поток. Магнитная индукция. Закон электромагнитной индукции. Правило Ленца
Магнитный поток. Магнитная индукция. Закон электромагнитной индукции. Правило Ленца «ДАВЛЕНИЕ ТВЕРДЫХ ТЕЛ»
«ДАВЛЕНИЕ ТВЕРДЫХ ТЕЛ» Оптика
Оптика Дисперсия света
Дисперсия света ПОТЕНЦИАЛЬНАЯ ЭНЕРГИЯ Выполнили: ученицы 7В класса Шандакова Елена Кузенкова Елизавета
ПОТЕНЦИАЛЬНАЯ ЭНЕРГИЯ Выполнили: ученицы 7В класса Шандакова Елена Кузенкова Елизавета  Планы расположения средств автоматизации и проводок
Планы расположения средств автоматизации и проводок Задачи по гидростатике
Задачи по гидростатике Интерференция световых волн (продолжение)
Интерференция световых волн (продолжение) Элементарная теория гироскопа
Элементарная теория гироскопа Электронная подсистема. Вырожденный электронный газ (лекция 16)
Электронная подсистема. Вырожденный электронный газ (лекция 16) Отдел образования администрации Тальменского района Муниципальное казенное общеобразовательное учреждение «Зайцевская средн
Отдел образования администрации Тальменского района Муниципальное казенное общеобразовательное учреждение «Зайцевская средн Электродвижущая сила. Закон Ома для полной цепи
Электродвижущая сила. Закон Ома для полной цепи Скибицкая Светлана Викторовна, учитель физики, первая квалификационная категория муниципальное бюджетное общеобразовательно
Скибицкая Светлана Викторовна, учитель физики, первая квалификационная категория муниципальное бюджетное общеобразовательно Ультразвуковая ванна
Ультразвуковая ванна Тема: Решение задач по теме: «Давление твердых тел , жидкостей и газов»
Тема: Решение задач по теме: «Давление твердых тел , жидкостей и газов» Рентгеновские спектральные методы
Рентгеновские спектральные методы SVOJSTVA (2)
SVOJSTVA (2) Одномерные изоэнтропные движения газа
Одномерные изоэнтропные движения газа Презентация по физике тема « Линзы »
Презентация по физике тема « Линзы » Задачи к ГОСам. Ж. д. путь
Задачи к ГОСам. Ж. д. путь