Содержание
- 2. Молекулярно-кинетическая теория изучает процессы в макроскопических системах, состоящих из огромного числа частиц.
- 3. Для исследования процессов в макросистемах применяются статистический и термодинамический методы. Статистический метод основан на том, что
- 4. Основой молекулярно-кинетической теории являются три положения. 1. Все тела состоят из атомов, молекул или ионов. В
- 5. 2. Частицы вещества находятся в непрерывном хаотичном движении, интенсивность которого пропорциональна температуре вещества. Экспериментальным доказательством этого
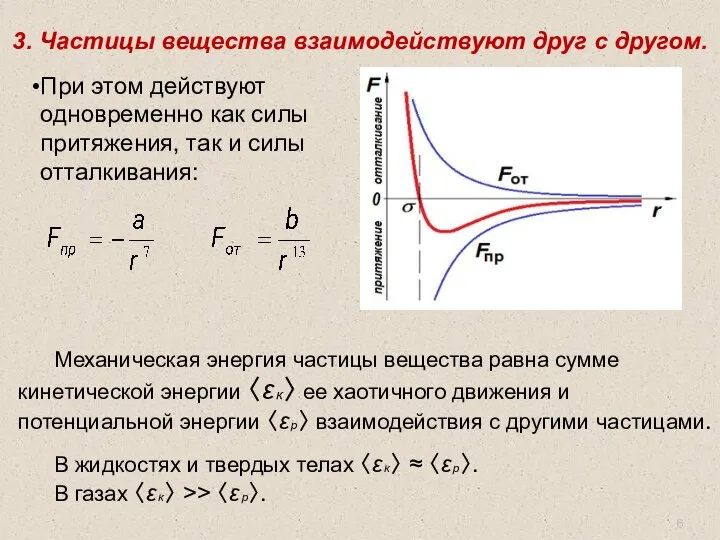
- 6. 3. Частицы вещества взаимодействуют друг с другом. При этом действуют одновременно как силы притяжения, так и
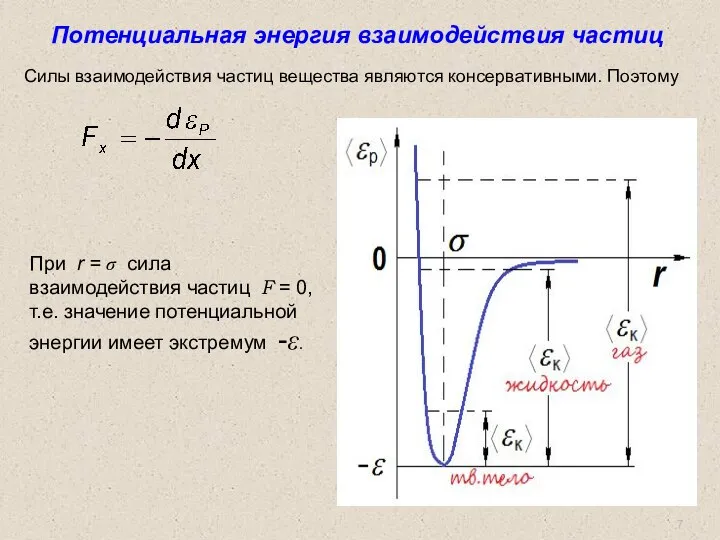
- 7. Потенциальная энергия взаимодействия частиц Силы взаимодействия частиц вещества являются консервативными. Поэтому При r = σ сила
- 8. В твердом теле частицы совершают малые хаотические колебания около положения равновесия σ. В жидкостях частицы совершают
- 9. Идеальный газ удовлетворяет условиям: Между частицами отсутствуют силы взаимодействия. Суммарный объём всех частиц газа пренебрежимо мал
- 10. Основное уравнение МКТ (уравнение Клаузиуса) Давление – это макроскопическое проявление хаотичного теплового движения частиц газа. Давление
- 11. Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона) 1834, 1874 где p – давление; V – объём; m
- 12. Средняя кинетическая энергия поступательного движения частиц газа Среднеквадратичная скорость теплового движения частиц газа
- 13. . Закон Максвелла – распределение молекул идеального газа по скоростям и энергиям теплового движения Частицы газа
- 14. Это объясняется тем, что в газе при термодинамическом равновесии устанавливается некоторое стационарное распределение частиц газа по
- 15. При выводе функции распределения f(v) Максвелл использовал МКТ, теорию вероятностей и следующие предположения: Газ идеальный и
- 16. Во всем интервале скоростей 0 ≤ v то есть площадь под кривой f(v) равна единице при
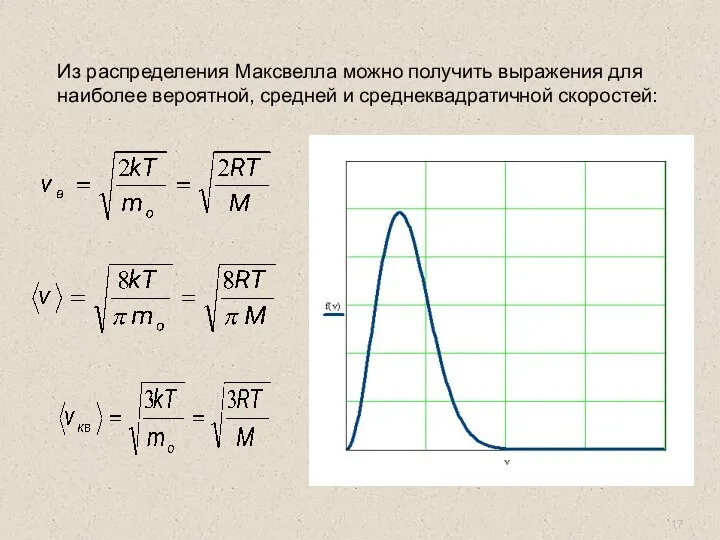
- 17. Из распределения Максвелла можно получить выражения для наиболее вероятной, средней и среднеквадратичной скоростей:
- 18. От распределения по скоростям можно перейти к распределению частиц по энергиям теплового движения: Многочисленные эксперименты с
- 19. Распределение Больцмана Любой газ находится в потенциальном поле тяготения Земли. Если бы не было тяготения, то
- 20. В предположении, что потенциальное поле однородно, масса всех молекул одинакова и температура газа на любой высоте
- 21. Используя уравнение p = nkT, можно получить выражение для давления атмосферы на любой высоте h над
- 22. ТЕРМОДИНАМИКА
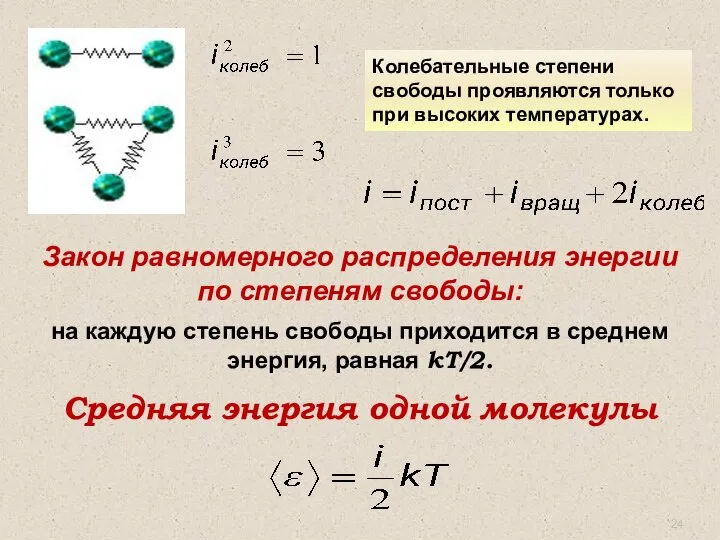
- 23. Число степеней свободы – это наименьшее число координат, полностью определяющих положение молекулы в пространстве.
- 24. Закон равномерного распределения энергии по степеням свободы: на каждую степень свободы приходится в среднем энергия, равная
- 25. Внутренняя энергия – это суммарная кинетическая энергия теплового движения всех частиц системы и потенциальная энергия их
- 26. Количество теплоты δQ – это энергия переданная одним телом другому при теплообмене без совершения работы: Существует
- 27. Работа и теплота не являются функцией состояния, поэтому малое количество работы и теплоты обозначаются δA и
- 28. Нулевой закон термодинамики: не зависимо от начального состояния системы в ней при фиксированных внешних условиях установится
- 29. Первый закон термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение системой
- 30. Теплоёмкость. Реальные газы.
- 31. Работа газа при конечном изменении объема от V1 до V2 Работа в термодинамике при бесконечно малом
- 32. Изохорический процесс V = const Подведенная к системе теплота идет только на изменение внутренней энергии системы.
- 33. Изобарический процесс р = const
- 34. Изотермический процесс T = const Чтобы температура газа не изменялась, надо к газу подводить теплоту в
- 35. Адиабатический процесс – процесс без теплообмена системы с окружающей средой Работа совершается за счет уменьшения внутренней
- 36. Теплоёмкостью называется количество теплоты, необходимое для повышения температуры системы на 1 К: Величина δQ зависит от
- 37. Согласно квантовой теории энергия молекулы может принимать не любые значения, а лишь определенный ряд дискретных значений.
- 38. РЕАЛЬНЫЕ ГАЗЫ Модель идеального газа позволяет описать поведение разреженных газов при достаточно высоких температурах. При повышенных
- 39. Действие сил притяжения между молекулами реального газа приводит к появлению дополнительного давления, которое учитывается поправкой a:
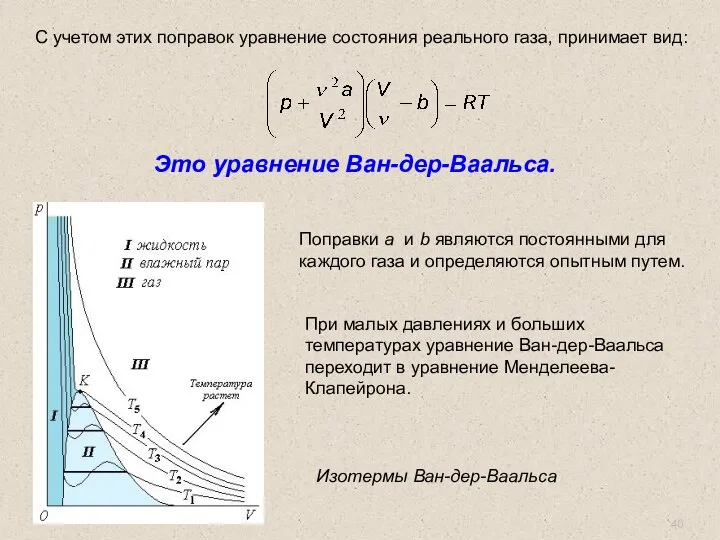
- 40. С учетом этих поправок уравнение состояния реального газа, принимает вид: Поправки a и b являются постоянными
- 41. Тепловые двигатели
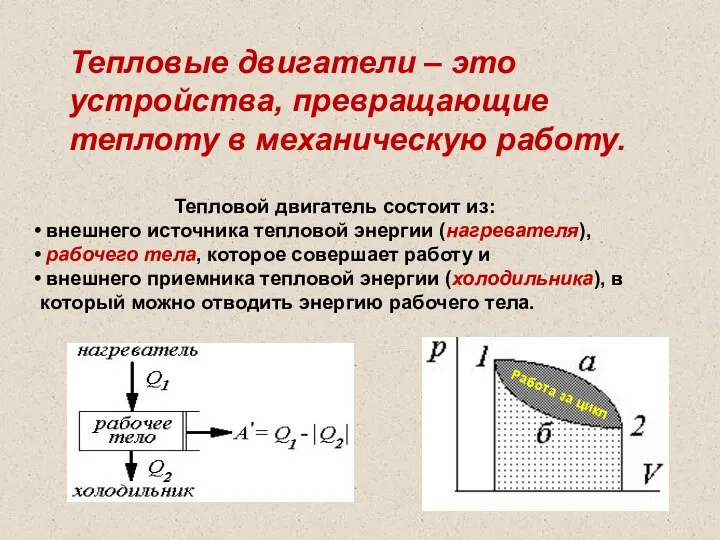
- 42. Тепловой двигатель состоит из: внешнего источника тепловой энергии (нагревателя), рабочего тела, которое совершает работу и внешнего
- 43. Для длительной работы теплового двигателя необходима цикличность работы: после расширения рабочего тела должно следовать его сжатие.
- 44. Поскольку ни количество теплоты, ни совершенная системой работа не являются функциями состояния, величина КПД зависит от
- 45. Цикл Карно Изотерма 1-2. Рабочее тело совершает работу за счет полученной от нагревателя теплоты Q1. Адиабата
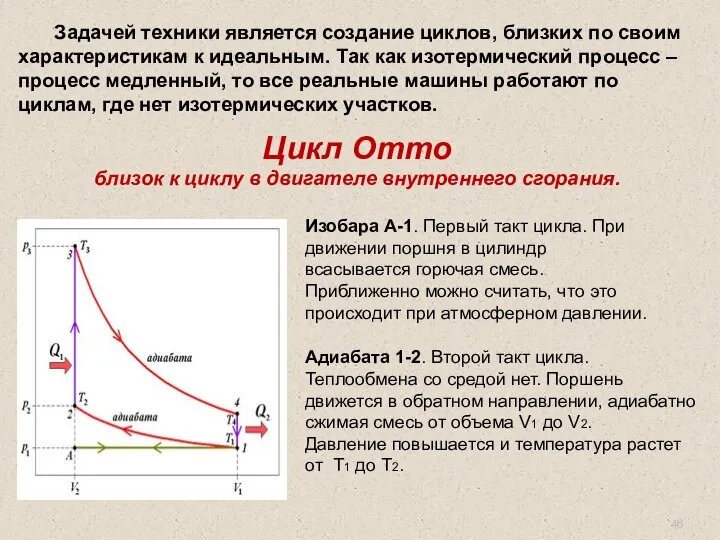
- 46. Задачей техники является создание циклов, близких по своим характеристикам к идеальным. Так как изотермический процесс –
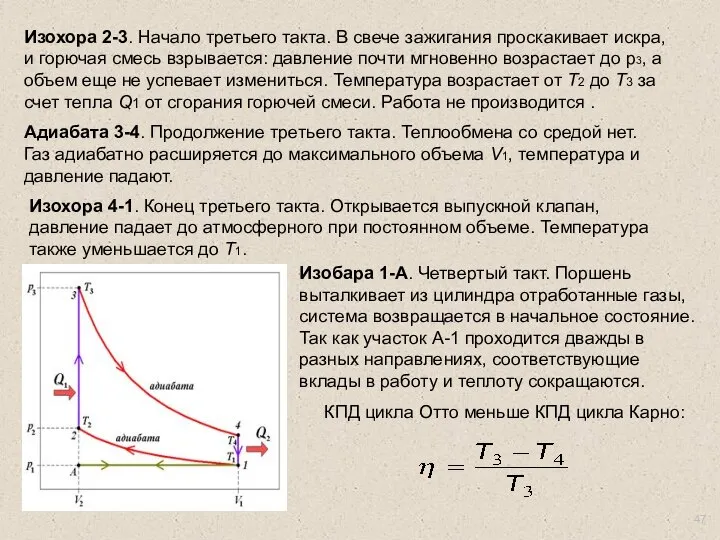
- 47. , . Изохора 2-3. Начало третьего такта. В свече зажигания проскакивает искра, и горючая смесь взрывается:
- 48. Цикл Дизеля Изобара А-1. При ходе поршня в цилиндр засасывается воздух при атмосферном давлении р1, объем
- 49. Второй закон термодинамики
- 50. Второй закон термодинамики Основоположником второго закона термодинамики считается Сади Карно. В этом же направлении работали Клаузиус
- 51. Формулировки второго закона термодинамики Постулат: «Вечный двигатель второго рода невозможен». Формулировка Карно: «Коэффициент полезного действия идеальной
- 52. До сих пор для характеристики состояния термодинамической системы мы использовали внутреннюю энергию U. С ее помощью
- 53. КПД любого двигателя меньше КПД двигателя, работающего на идеальном газе по обратимому циклу. Используя обе формулы
- 54. В общем случае любое изменение состояния системы можно представить как результат бесконечно большого числа бесконечно малых
- 55. Энтропия обладает следующими свойствами. Энтропия однозначна, т.е. любому состоянию системы присуще единственное значение энтропии. Энтропия аддитивна,
- 56. Так как реальные процессы необратимы, то можно утверждать, что все процессы в замкнутой системе ведут к
- 57. Макросостояние термодинамической системы определяется значениями параметров p, V, T. Число способов, т.е. число микросостояний, которыми реализуется
- 58. Например, пусть в сосуде имеется N = 10 частиц. Число способов, которыми можно осуществить макросостояние «В
- 59. Больцман связал величину энтропии с термодинамической вероятностью Это уравнение выражает статистическое толкование энтропии: увеличение энтропии изолированной
- 60. При абсолютном нуле температуры всякое тепловое движение прекращается, и все молекулы находятся в состоянии с наинизшей
- 61. Явления переноса
- 62. Равновесное состояние в молекулярно-кинетической теории рассматривается как состояние полной хаотичности движения молекул. Любое неравновесное состояние всегда
- 63. Явления переноса: диффузия – перенос массы; внутреннее трение (вязкость) – перенос импульса; теплопроводность – перенос энергии.
- 64. Эффективный диаметр σ молекулы – это расстояние, на которое сближаются центры молекул при столкновении Среднее число
- 65. 〈v〉 - средняя относительная скорость движения молекул; n – концентрация молекул газа; р – давление газа;
- 66. Диффузия – это обусловленное тепловым движением выравнивание концентраций в смеси нескольких веществ. Этот процесс наблюдается в
- 67. Умножив обе части уравнения на массу одной молекулы, получим закон Фика где ρ - плотность газа.
- 68. В наиболее общем случае, когда диффузия не является одномерной, т.е. концентрация диффундирующего вещества изменяется не только
- 69. Внутреннее трения (вязкость) Внешнее трение возникает при относительном смещении двух твердых тел, находящихся в контакте. Внутреннее
- 70. Пусть два слоя газа 1 и 2 движутся параллельно друг другу со скоростями u1 и u2.
- 71. Сила трения, действующая на площадь S при ламинарном течении Можно показать, что С повышением температуры вязкость
- 72. Теплопроводность – это перенос тепла между телами или в пределах одного тела при наличии градиента температуры,
- 73. Закон теплопроводности Фурье: плотность теплового потока прямо пропорциональна градиенту температуры λ – коэффициент теплопроводности; dT/dx –
- 74. Сходство математических выражений для явлений переноса обусловлено общностью молекулярных механизмов, лежащих в основе явлений диффузии, внутреннего
- 76. Скачать презентацию

































































 Поляризация света
Поляризация света Электричество и магнетизм
Электричество и магнетизм Электрощит питания судов с берега. Стартерный пуск судового дизель-генератора. (Билет 13)
Электрощит питания судов с берега. Стартерный пуск судового дизель-генератора. (Билет 13) Редукторы. Передаточное отношение редуктора
Редукторы. Передаточное отношение редуктора Презентация по физике "Свойства твердых тел" - скачать
Презентация по физике "Свойства твердых тел" - скачать  Озоновый слой атмосферы. Ультрафиолетовое излучение
Озоновый слой атмосферы. Ультрафиолетовое излучение Акустика. Природа звука. Скорость звука. Эффект Доплера
Акустика. Природа звука. Скорость звука. Эффект Доплера Полевые транзисторы FET (field-effect transistor). Устройство, принципы работы полевых транзисторов различных типов
Полевые транзисторы FET (field-effect transistor). Устройство, принципы работы полевых транзисторов различных типов Требования к химическому производству, показатели химического производства и процесса. (Тема 2-3)
Требования к химическому производству, показатели химического производства и процесса. (Тема 2-3) Коротаева И. А. МОУ СОШкола №98
Коротаева И. А. МОУ СОШкола №98 Презентация Манометр Прибор, измеряющий давление, большее или меньшее атмосферного
Презентация Манометр Прибор, измеряющий давление, большее или меньшее атмосферного Применение дифракционного метода суммирования в геолокации
Применение дифракционного метода суммирования в геолокации Тепловые излучения и фотоны
Тепловые излучения и фотоны Историческая справка. Звук в воздухе
Историческая справка. Звук в воздухе Тормозные системы автомобиля. Устройство и работа
Тормозные системы автомобиля. Устройство и работа Аттестационная работа. Образовательная программа элективного курса по физике для учащихся 9-х классов
Аттестационная работа. Образовательная программа элективного курса по физике для учащихся 9-х классов Анализ характерных ошибок при решении ЕГЭ по физике. Систематизация и тренды
Анализ характерных ошибок при решении ЕГЭ по физике. Систематизация и тренды Шкала электромагнитных излучений
Шкала электромагнитных излучений Исследование минералов под микроскопом
Исследование минералов под микроскопом Методы синтеза наноматериалов
Методы синтеза наноматериалов Магнитное поле в вакууме
Магнитное поле в вакууме Механические волны. Звук
Механические волны. Звук Сонячна енергетика
Сонячна енергетика Системы пожарной сигнализации и пожаротушения
Системы пожарной сигнализации и пожаротушения Формирование северного сияния
Формирование северного сияния Задачи на движение. Схемы, таблицы, решения
Задачи на движение. Схемы, таблицы, решения Магнитные подшипники
Магнитные подшипники Дефекты кристаллического строения
Дефекты кристаллического строения