Содержание
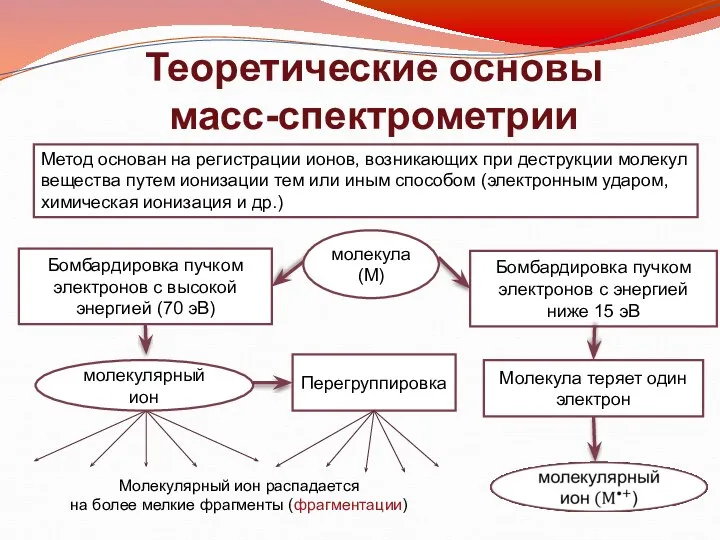
- 2. Теоретические основы масс-спектрометрии Метод основан на регистрации ионов, возникающих при деструкции молекул вещества путем ионизации тем
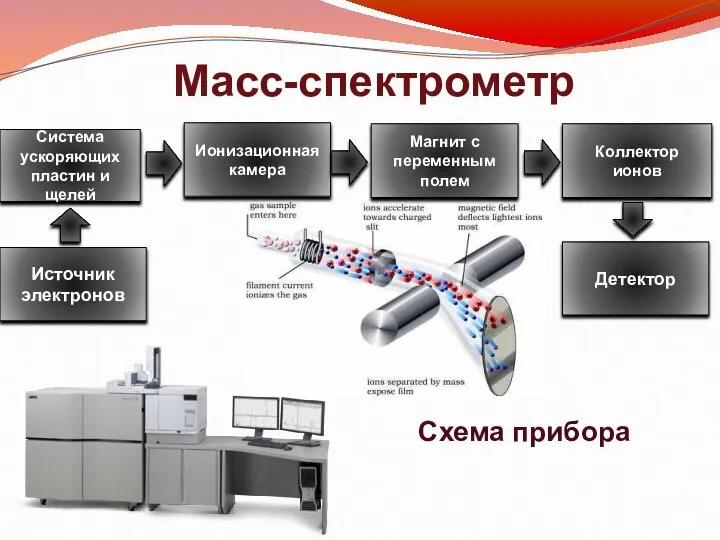
- 3. Масс-спектрометр Источник электронов Детектор Схема прибора
- 4. Масс-спектр Представляет собой графическую запись зависимости относительной интенсивности заряженных осколков молекулы в процентах (%) от отношения
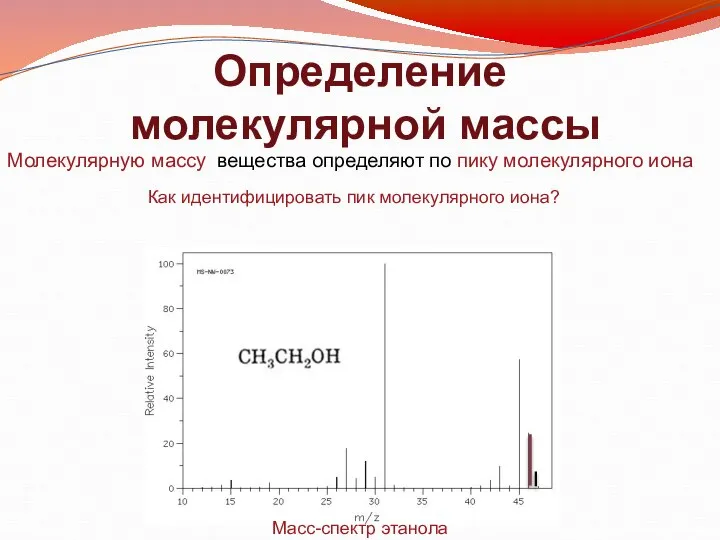
- 5. Определение молекулярной массы Молекулярную массу вещества определяют по пику молекулярного иона Масс-спектр этанола Как идентифицировать пик
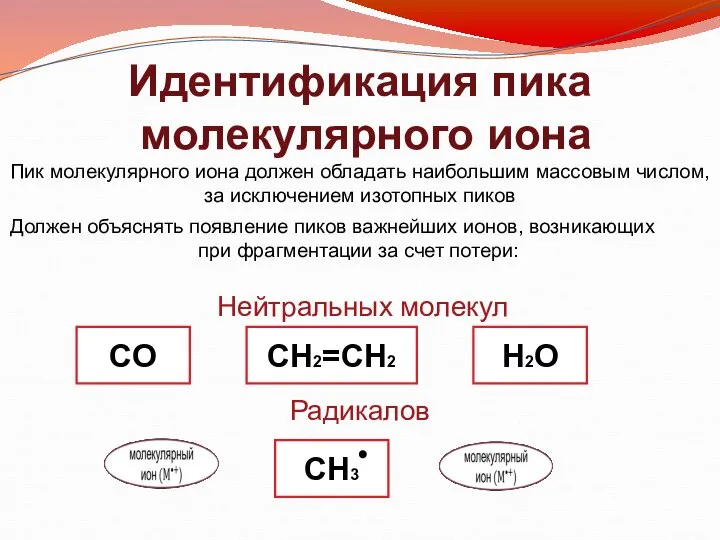
- 6. Идентификация пика молекулярного иона Пик молекулярного иона должен обладать наибольшим массовым числом, за исключением изотопных пиков
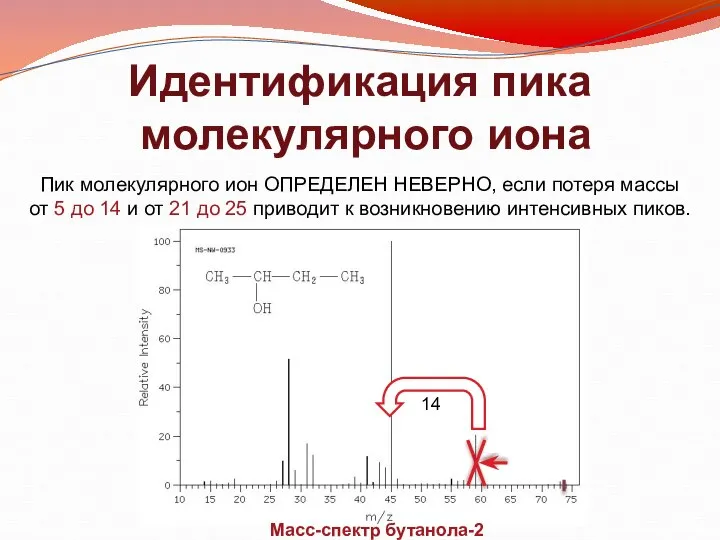
- 7. Идентификация пика молекулярного иона Пик молекулярного ион ОПРЕДЕЛЕН НЕВЕРНО, если потеря массы от 5 до 14
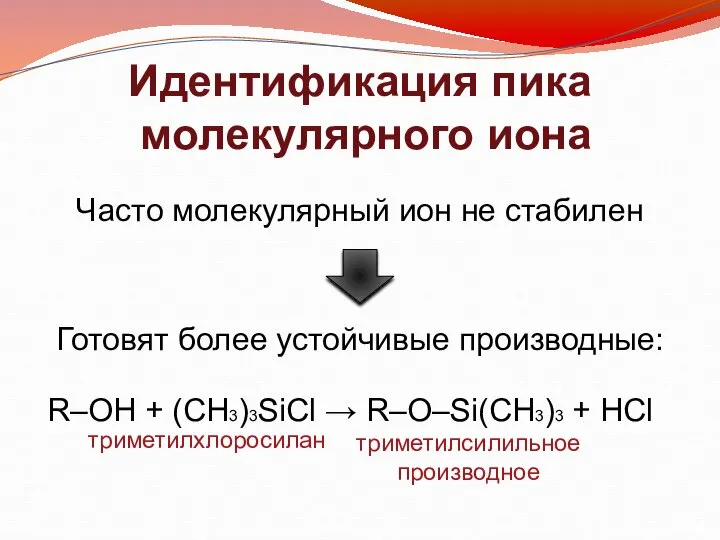
- 8. Идентификация пика молекулярного иона Готовят более устойчивые производные: R–OH + (CH3)3SiCl → R–O–Si(CH3)3 + HCl триметилхлоросилан
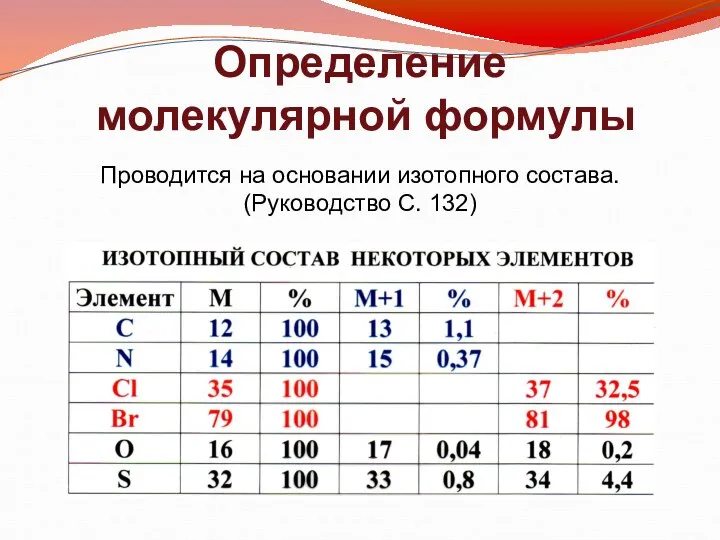
- 9. Определение молекулярной формулы Проводится на основании изотопного состава. (Руководство С. 132)
- 10. Анализ пика M+2 Если интенсивность пика М+2 меньше, чем 4,4% - в молекуле нет серы, хлора
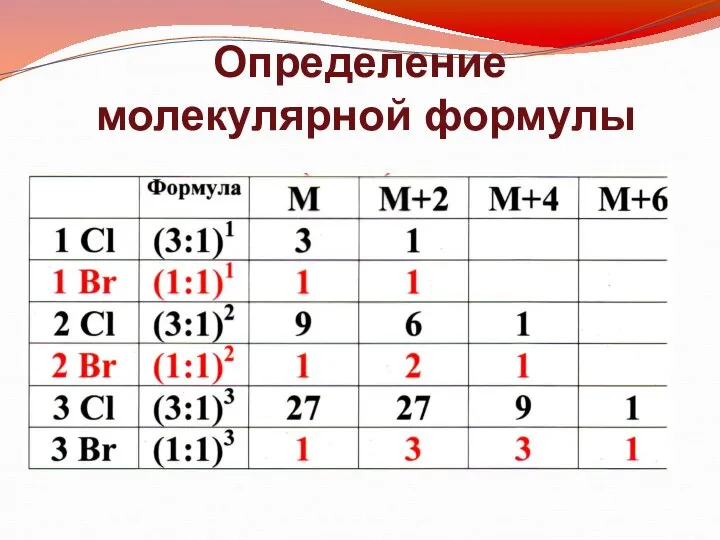
- 11. Определение молекулярной формулы
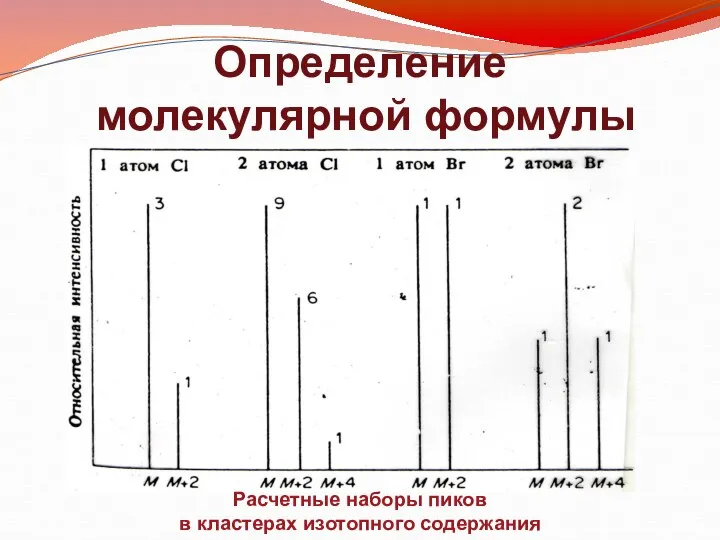
- 12. Определение молекулярной формулы Расчетные наборы пиков в кластерах изотопного содержания
- 13. 3. Анализ пика M+1 По пику М+1 определяют число атомов углерода: Определение молекулярной формулы
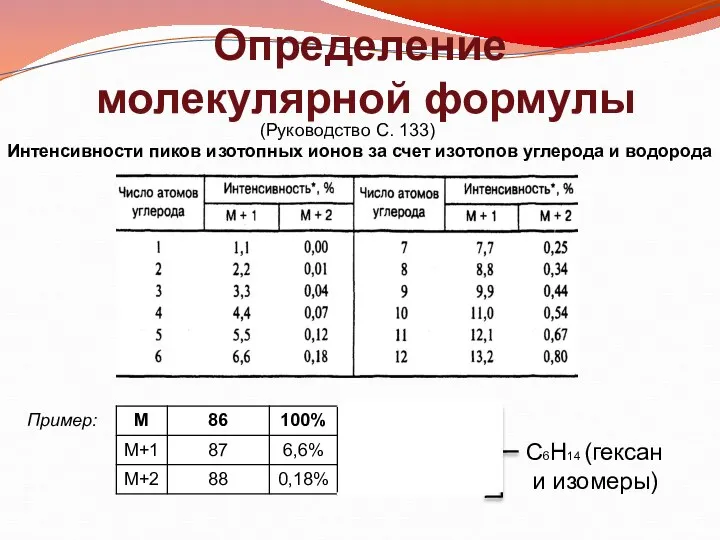
- 14. Определение молекулярной формулы (Руководство С. 133) Пример: С6Н14 (гексан и изомеры) Интенсивности пиков изотопных ионов за
- 15. Определение молекулярной формулы Если по пику М+2 обнаружены кислород и сера, то из интенсивности пика М+1
- 16. Определение молекулярной формулы Для идентификации атомов азота пользуются азотным правилом: Нечетная молекулярная масса Нечетное число атомов
- 17. Для характеристики структуры молекулы удобно пользоваться показателем водородной ненасыщенности Н = nc – (nH + nHal)/2
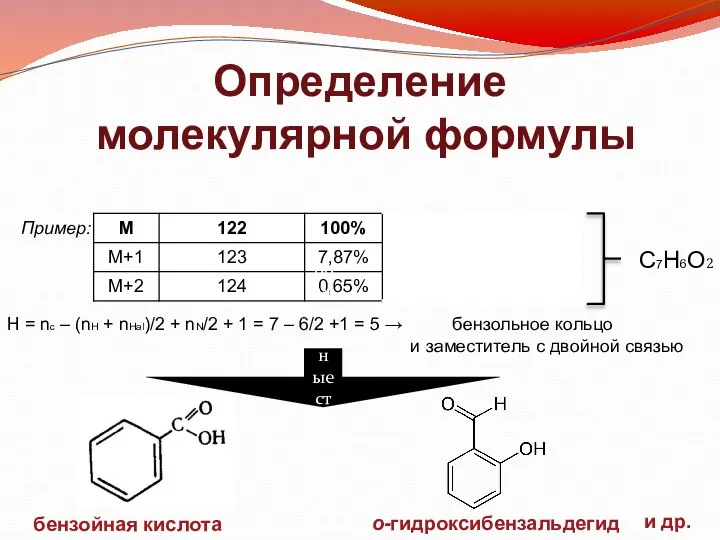
- 18. Определение молекулярной формулы Пример: С7Н6О2 Н = nc – (nH + nHal)/2 + nN/2 + 1
- 19. Определение молекулярной формулы Пример: С3Н8О Н = nc – (nH + nHal)/2 + nN/2 + 1
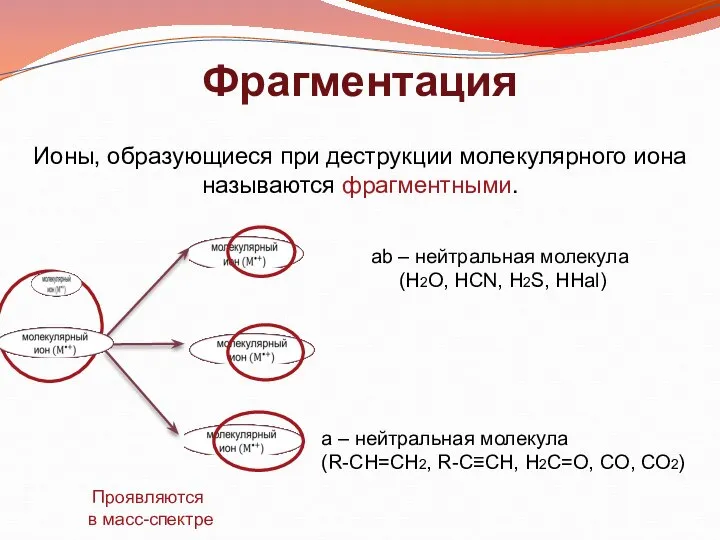
- 20. Фрагментация Ионы, образующиеся при деструкции молекулярного иона называются фрагментными. ab – нейтральная молекула (H2O, HCN, H2S,
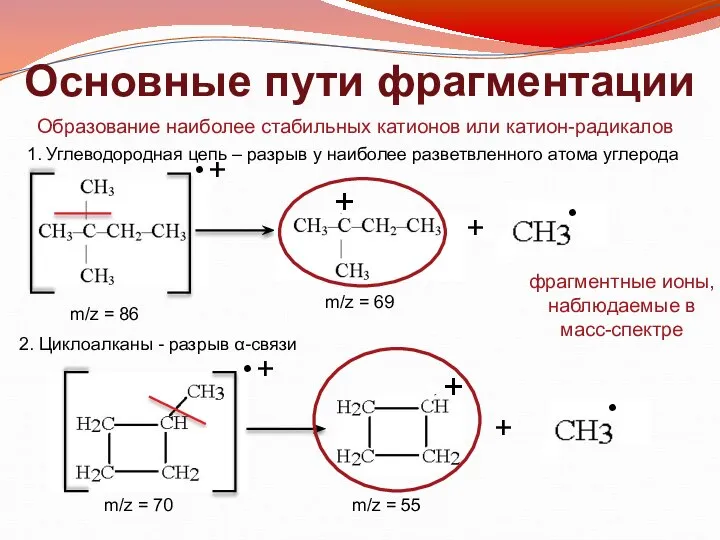
- 21. Основные пути фрагментации 1. Углеводородная цепь – разрыв у наиболее разветвленного атома углерода 2. Циклоалканы -
- 22. Основные пути фрагментации 4. Соединения с гетероатомом – разрыв β-связи + • m/z = 46 m/z
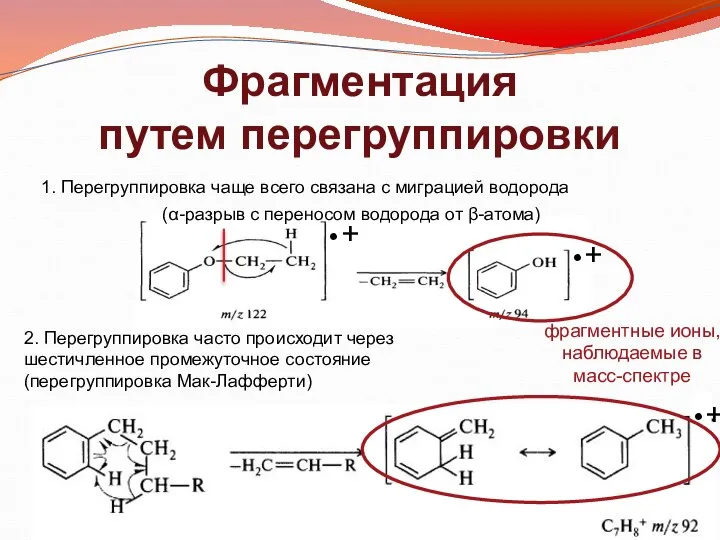
- 23. Фрагментация путем перегруппировки 1. Перегруппировка чаще всего связана с миграцией водорода 2. Перегруппировка часто происходит через
- 25. Скачать презентацию








 Почему самолеты не падают
Почему самолеты не падают Андрей Дмитриевич Сахаров
Андрей Дмитриевич Сахаров Развитие навыков смыслового чтения и работы с текстом на уроках физики
Развитие навыков смыслового чтения и работы с текстом на уроках физики Исследование зависимости уровня воды от различных параметров
Исследование зависимости уровня воды от различных параметров Удельная теплоёмкость ( 8 класс)
Удельная теплоёмкость ( 8 класс) Сравнение энергоисточников
Сравнение энергоисточников Презентация по физике "Собирающие линзы" - скачать
Презентация по физике "Собирающие линзы" - скачать  Решение задач. Закон сохранения энергии
Решение задач. Закон сохранения энергии Звук и вибрация
Звук и вибрация Конвекция. Основные положения переноса теплоты. (Тема 2. Лекции 6,7)
Конвекция. Основные положения переноса теплоты. (Тема 2. Лекции 6,7) Аттестационная работа. Проведение энергетического исследования на предприятиях и учреждениях ЖКХ
Аттестационная работа. Проведение энергетического исследования на предприятиях и учреждениях ЖКХ Оценки качества переходных процессов
Оценки качества переходных процессов Презентация по физике "Физика и методы научного познания" - скачать
Презентация по физике "Физика и методы научного познания" - скачать  Работу выполнили Учащиеся 10 а класса МОУ СОШ №19 Пономарева Алена Докучаев Денис Залавский Сергей Прокопенко Сергей
Работу выполнили Учащиеся 10 а класса МОУ СОШ №19 Пономарева Алена Докучаев Денис Залавский Сергей Прокопенко Сергей Альберт Эйнштейн Я был третируем моими профессорами, которые не любили меня из-за моей независимости и закрыли мне путь в науку…
Альберт Эйнштейн Я был третируем моими профессорами, которые не любили меня из-за моей независимости и закрыли мне путь в науку… Электричество. Электростатика
Электричество. Электростатика Атомның планетарлық моделі
Атомның планетарлық моделі Урок повторения Световые кванты
Урок повторения Световые кванты МАНОМЕТРЫ 7 КЛАСС Автор: учитель физики МОУ «СОШ № 1» г. Ивантеевки Гагарина Марианна Сергеевна
МАНОМЕТРЫ 7 КЛАСС Автор: учитель физики МОУ «СОШ № 1» г. Ивантеевки Гагарина Марианна Сергеевна Электромагнитное излучение на границе раздела сред и в структурированном веществе. Оптическая микроскопия ближнего поля
Электромагнитное излучение на границе раздела сред и в структурированном веществе. Оптическая микроскопия ближнего поля Системы создания плазмы. Плазменные установки
Системы создания плазмы. Плазменные установки Спектры периодических и непериодических сигналов
Спектры периодических и непериодических сигналов Внутренняя энергия, теплопередача, работа
Внутренняя энергия, теплопередача, работа Термическая обработка металлов
Термическая обработка металлов Космические ЯЭУ
Космические ЯЭУ Возбуждение петлей. Возбуждение штырем. Возбуждение зондовым возбудителем
Возбуждение петлей. Возбуждение штырем. Возбуждение зондовым возбудителем Качество изображения астрономических объективов и изображений математически-смоделированного точечного источника
Качество изображения астрономических объективов и изображений математически-смоделированного точечного источника Жизнь и творчество Д.И. Менделеева Подготовил ученик 8а Карбушев Максим
Жизнь и творчество Д.И. Менделеева Подготовил ученик 8а Карбушев Максим