Содержание
- 2. ПЛАН 9.1 Дисперсные системы и их классификация. 9.2 Получение и очистка коллоидных растворов. 9.3 Строение мицелл
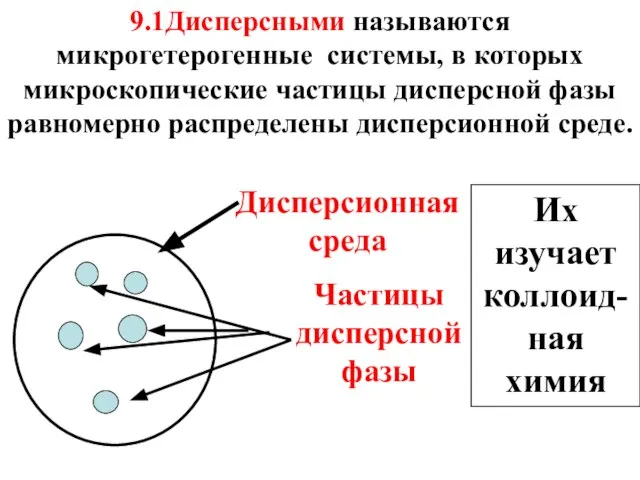
- 3. Дисперсионная среда Частицы дисперсной фазы 9.1Дисперсными называются микрогетерогенные системы, в которых микроскопические частицы дисперсной фазы равномерно
- 4. Классификация дисперсных систем 1) По степени дисперсности Коллоидно-дисперсные 10‾9 Грубо- дисперсные 10‾7 α- диаметр частицы дисперсной
- 5. 2) По степени взаимодействия дисперсной фазы и дисперсионной среды Под их взаимодействием понимают образование сольватных оболочек
- 6. Лиофильные - это системы, в которых сильно выражен эффект сольватации (растворы ВМС и ПАВ). Они устойчивы;
- 7. 3) По отсутствию или наличию межмолекулярного взаимодействия между частицами дисперсной фазы Свободно-дисперсные – частицы не связаны
- 8. 4) По агрегатному состоянию дисперсной фазы и дисперсионной среды
- 11. 9.2 Для получения коллоидных растворов используют: 1)метод диспергирования, 2)метод конденсации
- 12. Метод диспергирования– дробление крупных частиц до коллоидной степени дисперсности.
- 13. Диспергирование можно осуществлять : а) механическим дроблением (шаровые, коллоидные мельницы); б) электрическим распылением в вольтовой дуге
- 14. г) метод пептизации- дробление свежеприготовленных осадков на отдельные коллоидные частицы при добавлении небольшого количества электролита-пептизатора в
- 15. Ионы электролита-пептизатора адсорбируются на поверхности частиц осадка, сообщая им одноименный электрический заряд и способствуя переходу во
- 16. Пептизация имеет большое биологическое значение: рассасывание атеросклеротических бляшек, почечных и печеночных камней происходит под воздействием лекарственных
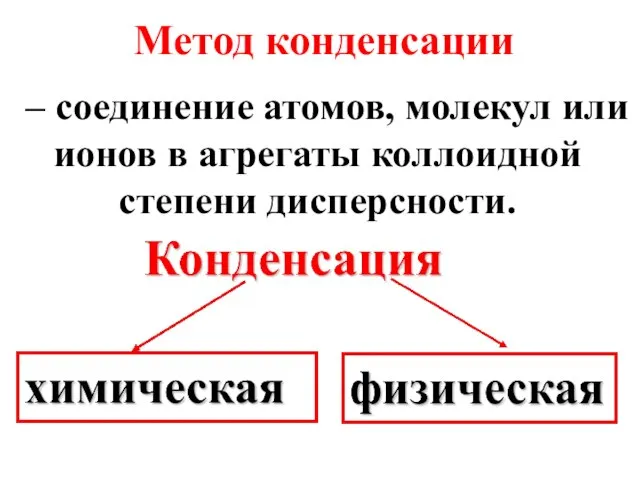
- 17. Метод конденсации – соединение атомов, молекул или ионов в агрегаты коллоидной степени дисперсности.
- 18. В основе химической конденсации лежат химические реакции, протекающие с образованием труднорастворимых соединений.
- 19. ОВР H[AuCl4] + 3 H2O2 → 2 Au ↓+ + 8 HCl + 3 O2 получение
- 20. гидролиз FeCl3 + 3 H2O ⮀ Fe(OH)3↓ + 3 HCl ионный обмен AgNO3 + KI →
- 21. Получение дисперсных систем методом физической конденсации выполняют: (а)путем замены растворителя (в раствор добавляют жидкость, в которой
- 22. В организме превалирующим является конденсационный метод. Одним из немногих примеров диспергирования является эмульгирование жиров в кишечнике.
- 23. Методы очистки золей Диализ и электродиализ– очистка золей от электролитов Ультрафильтрация-отделение дисперсной фазы от дисперсионной среды
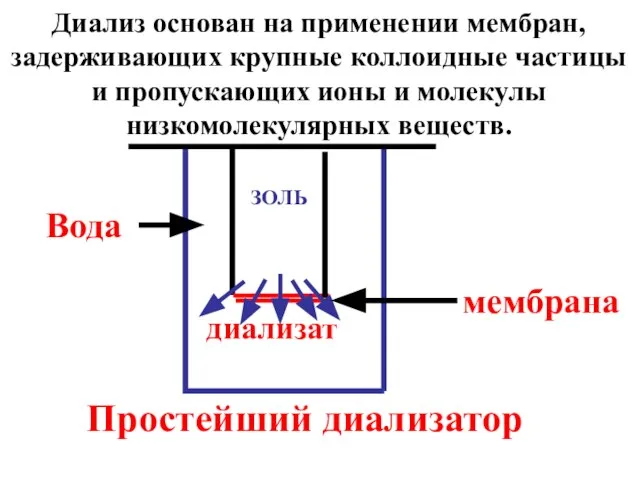
- 24. диализат ЗОЛЬ мембрана Простейший диализатор Вода Диализ основан на применении мембран, задерживающих крупные коллоидные частицы и
- 25. Диализ протекает медленно, но он может быть ускорен путем пропускания электрического тока через золь, подлежащий очистке.
- 26. Ультрафильтрация осуществляется путем продавливания золя через плотные фильтры, непроницаемые для частиц дисперсной фазы.
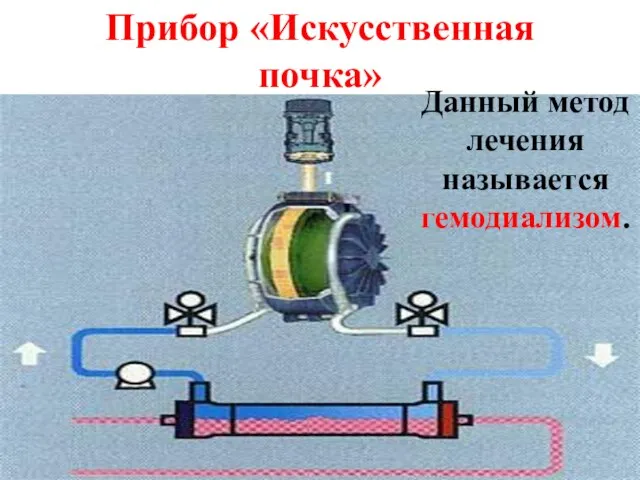
- 27. Процесс ультрафильтрации лежит в основе работы почек. Примером сочетания диализа и ультрафильтрации является аппарат "искусственная почка",
- 28. Прибор «Искусственная почка» Данный метод лечения называется гемодиализом.
- 29. 9.3 Согласно мицеллярной теории, золь состоит из мицелл и интермицеллярной жидкости.
- 30. Мицелла – это электронейтральная частица дисперсной фазы, окруженная двойным электрическим слоем ионов. Интермицеллярная жидкость – это
- 31. Основу мицеллы составляют микрокристаллы трудно-растворимого вещества, называемые агрегатом. В результате избирательной адсорбции на поверхности агрегата адсорбируются
- 32. Пример. Рассмотрим строение мицеллы золя AgI, образующегося в результате реакции: AgNO3 + KI → AgI +
- 33. Электролит в избытке (AgNO3) является стабилизатором т.к. сообщает устойчивость коллоидным частицам. Из его ионов формируется двойной
- 34. Формула мицеллы AgI {[m AgI] n Ag+ (n - x)NO3-}x+x NO3- агрегат ПОИ ПРИ ПРИ ядро
- 35. ПОИ – потенциалопредляющие ионы, адсорбирующиеся на поверхности агрегата, ПРИ – противоионы, адсорбирующиеся на поверхности ядра; они
- 36. Коллоидная частица (гранула) – это часть мицеллы, состоящая из агрегата и адсорбционного слоя. Заряд гранулы рассчитывают
- 37. Образование двойного электрического слоя (ДЭС) приводит к тому, что на поверхности раздела адсорбционного и диффузного слоя
- 38. ξ– потенциал служит мерой устойчивости коллоидных частиц, мерой размеров межклеточных пространств in vivo.
- 39. 9.4 Физические свойства коллоидных растворов Молекулярно-кинетические Оптические Электро-кинетические
- 40. Важнейшие молекулярно-кинетические свойства 1) Броуновское движение – хаотическое движение частиц дисперсной фазы под воздействием ударов молекул
- 41. 2) Диффузия – самопроизвольный процесс выравнивания концентраций частиц по всему объему раствора в результате броуновского движения.
- 42. Особые оптические свойства дисперсных систем обусловлены тем, что размеры коллоидных частиц сопоставимы с длиной волны видимого
- 43. Если луч света направить на коллоидный раствор, то его путь будет обнаруживаться на темном фоне в
- 44. Электрокинетическими явлениями называются процессы, протекающие в золях под воздействием внешнего электрического поля. К ним относят электрофорез
- 45. Электрофорез- это направленное движение коллоидных частиц под действием внешнего электрического поля относительно неподвижной дисперсионной среды (был
- 46. Электрофорез применяется для диагностики и контроля за ходом болезни. Его используют для введения лекарственных веществ в
- 47. Электроосмос – это движение дисперсионной среды относительно неподвижной дисперсной фазы через полупроницаемую мембрану во внешнем электрическом
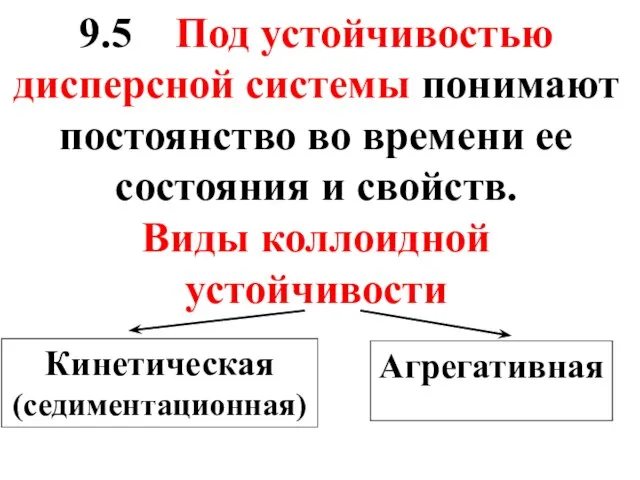
- 48. 9.5 Под устойчивостью дисперсной системы понимают постоянство во времени ее состояния и свойств. Виды коллоидной устойчивости
- 49. Причиной кинетической устойчивости является броуновское движение, которое противодействует оседанию частиц под действием силы тяжести.
- 50. Агрегативная устойчивость золей обусловлена наличием у коллоидных частиц одноименных электрических зарядов, препятствующих их слипанию при столкновении.
- 51. Чем больше заряд частицы, тем выше ее электрокинетический потенциал и стабильнее золь.
- 52. При нарушении агрегативной устойчивости золей происходит их коагуляция.
- 53. Коагуляция - процесс объединения коллоидных частиц в более крупные агрегаты вследствие полной или частичной потери электрических
- 54. Коагуляцию может вызывать: (а) изменение температуры, (б) увеличение концентрации дисперсной фазы, (в) механическое воздействие, (г) добавление
- 55. Коагуляция электролитами протекает в живом организме, т.к. коллоидные растворы клеток находятся в соприкосновении с электролитами, содержащимися
- 56. Все сильные электролиты вызывают коагуляцию золей при увеличении их концентрации в растворе до некоторого значения, называемого
- 57. Порог коагуляции (γ) – это минимальное количество электролита, которое надо добавить к 1 л золя, чтобы
- 58. Коагулирующие действие электролитов описывается правилом Шульце – Гарди: коагуляцию вызывают ионы, заряд которых противоположен заряду гранулы.
- 59. Дерягин и Ландау показали, что γI : γII : γIII = 1 1 1 16 26
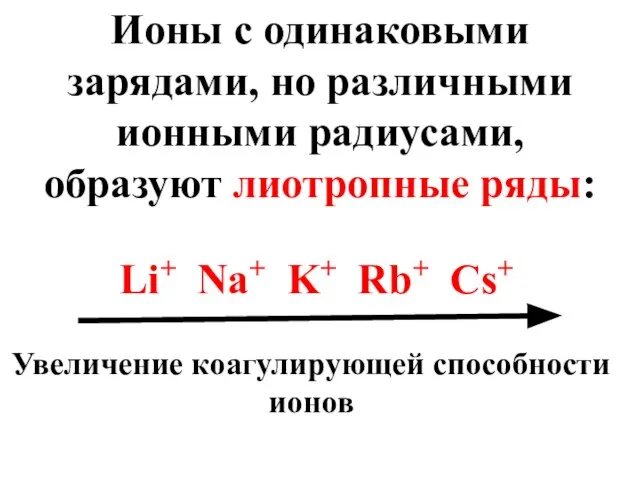
- 60. Правило Шульце - Гарди носит приблизительный характер, т.к. не учитывает влияние ионных радиусов на коагулирующую способность
- 61. Ионы с одинаковыми зарядами, но различными ионными радиусами, образуют лиотропные ряды: Li+ Na+ K+ Rb+ Cs+
- 62. Процесс коагуляции золя характеризуется определенной величиной скорости коагуляции, которую можно определить как изменение числа коллоидных частиц
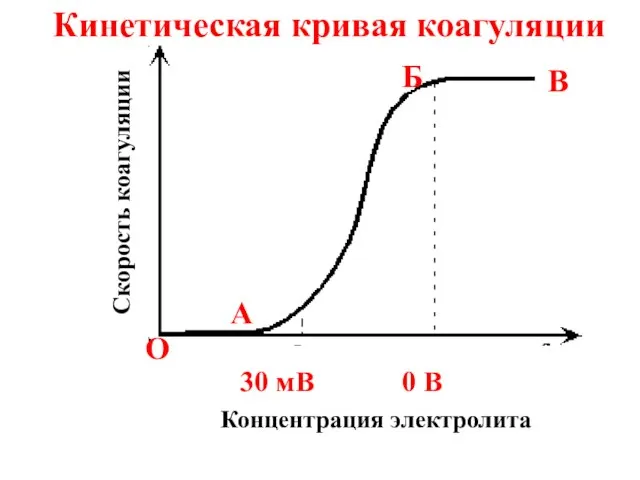
- 63. Кинетическая кривая коагуляции Скорость коагуляции Концентрация электролита 0 В 30 мВ O A Б B
- 64. Отрезок ОА отвечает периоду скрытой коагуляции, при которой золь сохраняет свою устойчивость.
- 65. В точке А начинается явная коагуляция, которая соответствует уменьшению ξ-потенциала коллоидных частиц до 30 мВ.
- 66. На участке БВ скорость коагуляции достигает максимального значения; этот отрезок кинетической кривой соответствует периоду быстрой коагуляции(ζ-потенциал
- 67. При коагуляции золя смесью электролитов можно наблюдать: а) явление аддитивности - суммирование коагулирующего действия ионов; б)
- 68. в) явление синергизма - усиление коагулирующего действия одного иона в присутствии другого.
- 69. Коагуляция может происходить при смешении золей с различными знаками заряда их частиц (взаимная коагуляция).
- 70. Такой тип коагуляции применяется в санитарно-гигиенической практике при очистке воды от взвешенных коллоидных частиц.
- 72. Скачать презентацию















![ОВР H[AuCl4] + 3 H2O2 → 2 Au ↓+ + 8](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/514727/slide-18.jpg)












![Формула мицеллы AgI {[m AgI] n Ag+ (n - x)NO3-}x+x NO3-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/514727/slide-33.jpg)
































 Слесарное дело
Слесарное дело Магнитные материалы (магнетики)
Магнитные материалы (магнетики) Открытие антипротона
Открытие антипротона Понятие термодинамики
Понятие термодинамики Презентация по физике Никола Тесла
Презентация по физике Никола Тесла  Кинетическая теория газов Расстояние между молекулами вещества, находящегося в газовой фазе обычно значительно больше, чем р
Кинетическая теория газов Расстояние между молекулами вещества, находящегося в газовой фазе обычно значительно больше, чем р Законы сохранения. Работа и энергия. (Тема 3)
Законы сохранения. Работа и энергия. (Тема 3) Аеродинамічні характеристики літак. Прояв стисливості повітря при обтіканні крила повітряним потоком. (Лекція 6.3.2)
Аеродинамічні характеристики літак. Прояв стисливості повітря при обтіканні крила повітряним потоком. (Лекція 6.3.2) Вес тела, движущегося с ускорением
Вес тела, движущегося с ускорением Діелектрики та провідники в електричному полі
Діелектрики та провідники в електричному полі Жоғарғы жиілікті разрядты зерттеудің маңыздылығы. Айнымалы электр өрісіндегі разрядтардың түрлері
Жоғарғы жиілікті разрядты зерттеудің маңыздылығы. Айнымалы электр өрісіндегі разрядтардың түрлері Различные схемы питания СВЭ и контактной сети
Различные схемы питания СВЭ и контактной сети Спектральный анализ. История открытия и современность
Спектральный анализ. История открытия и современность Закон всемирного тяготения
Закон всемирного тяготения Механика деформируемого твердого тела
Механика деформируемого твердого тела Механические свойства металлов
Механические свойства металлов Скорость при прямолинейном равномерном движении тела
Скорость при прямолинейном равномерном движении тела Электрические машины постоянного тока
Электрические машины постоянного тока Кинематика
Кинематика Теплообменные аппараты
Теплообменные аппараты Шахтный интерферометр
Шахтный интерферометр Электрический привод
Электрический привод Биологиялық жүйелер люминесценциясы. (Дәріс 15)
Биологиялық жүйелер люминесценциясы. (Дәріс 15) Колебания
Колебания УРОК ФИЗИКИ В 10 КЛАССЕ Температура Учитель Кононов Геннадий Григорьевич СОШ № 29 Славянский район Краснодарс
УРОК ФИЗИКИ В 10 КЛАССЕ Температура Учитель Кононов Геннадий Григорьевич СОШ № 29 Славянский район Краснодарс Давление. Сила давления. Билет 18
Давление. Сила давления. Билет 18 Магнетизм. Магнитостатика. Магнитное взаимодействие
Магнетизм. Магнитостатика. Магнитное взаимодействие Принцип действия тепловых двигателей. КПД тепловых двигателей Цель урока: раскрыть физические принципы действия тепловых двигат
Принцип действия тепловых двигателей. КПД тепловых двигателей Цель урока: раскрыть физические принципы действия тепловых двигат