Содержание
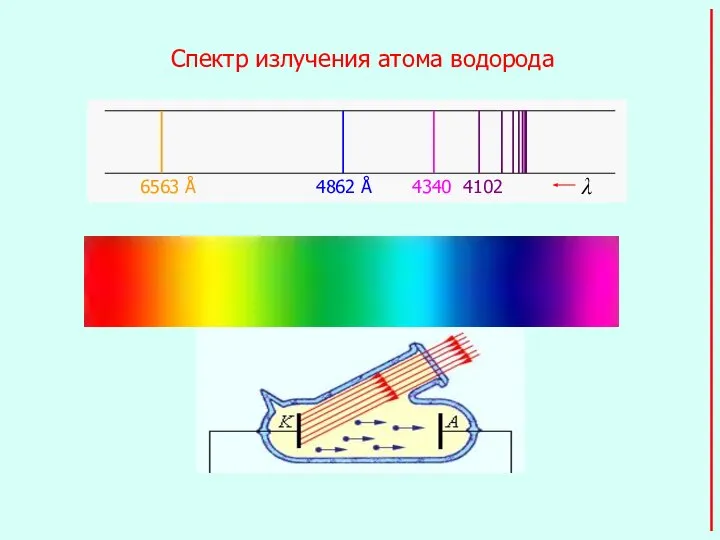
- 2. Спектр излучения атома водорода Фотоэффект
- 3. Для описания явлений микромира ( масштаб Свяжем теорию с практикой …
- 4. §1. Корпускулярные свойства излучения
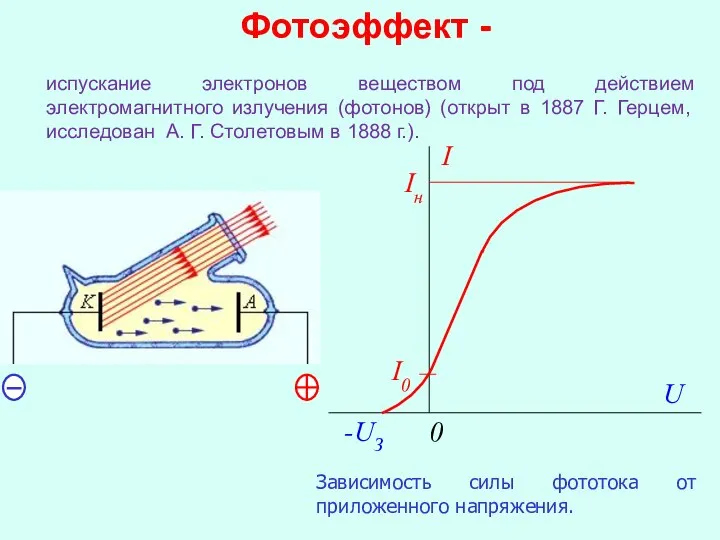
- 5. I Iн I0 0 -UЗ U Зависимость силы фототока от приложенного напряжения. Фотоэффект - испускание электронов
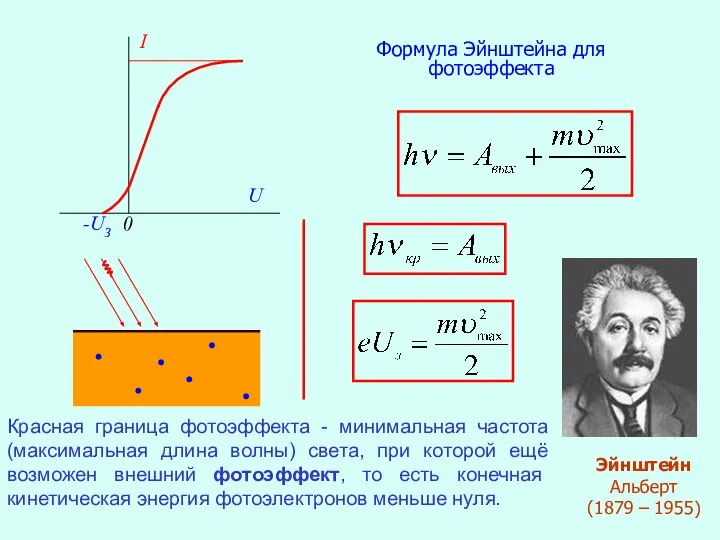
- 6. I 0 -UЗ U Формула Эйнштейна для фотоэффекта Эйнштейн Альберт (1879 – 1955) Красная граница фотоэффекта
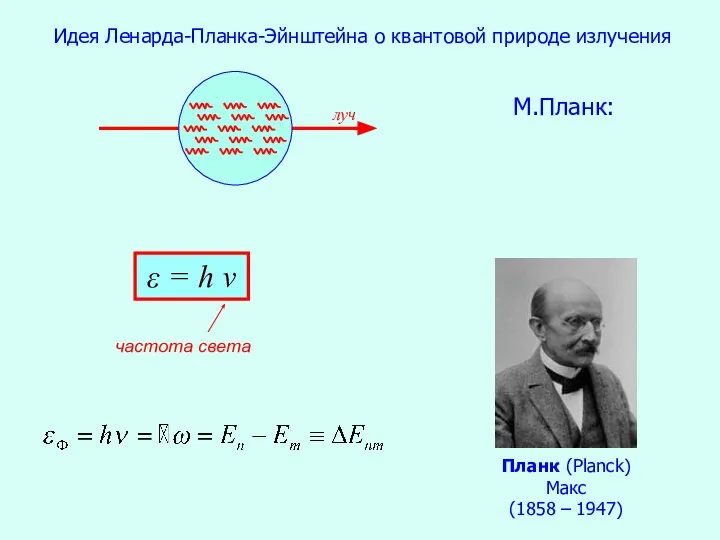
- 7. Идея Ленарда-Планка-Эйнштейна о квантовой природе излучения М.Планк: ε = h ν Планк (Planck) Макс (1858 –
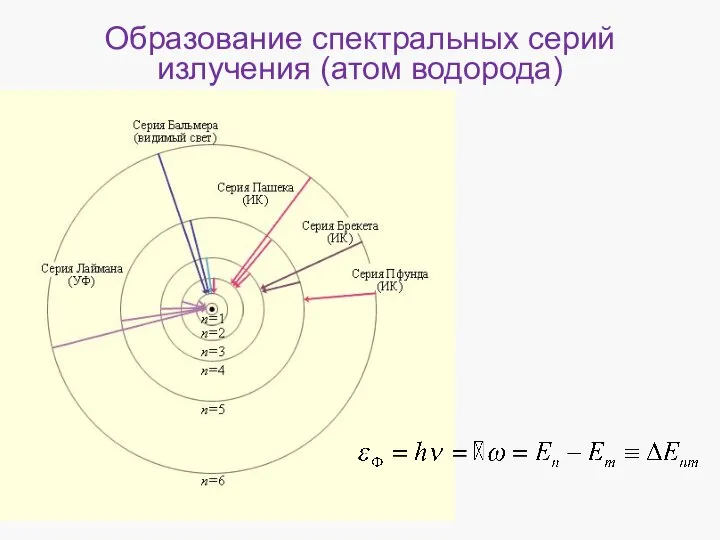
- 8. Образование спектральных серий излучения (атом водорода)
- 9. Характеристики фотона h=6,63 .10 -34 Дж . с постоянная Планка Энергия: Масса: Масса покоя: Импульс: длина
- 10. §2. Гипотеза де Бройля. Волна де Бройля. Проявления волновых свойств частиц 8
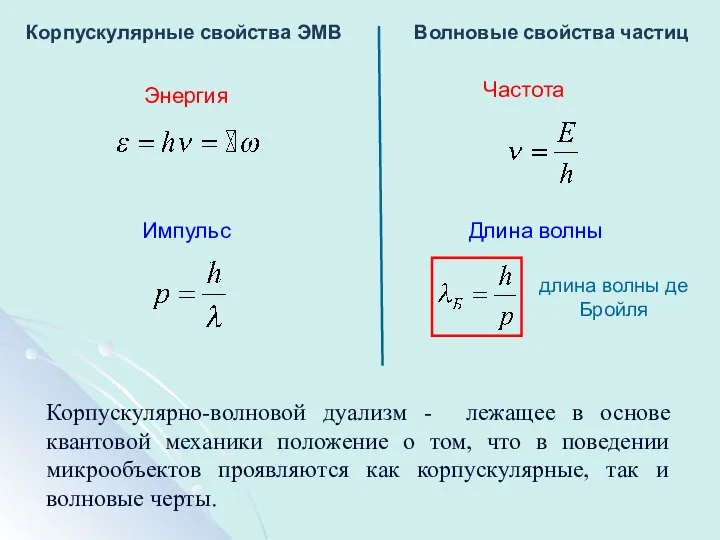
- 11. Корпускулярные свойства ЭМВ Волновые свойства частиц Энергия Частота Импульс Длина волны длина волны де Бройля Корпускулярно-волновой
- 12. Картина дифракции электронов на поликристаллическом образце при длительной экспозиции (a) и при короткой экспозиции (b) Опыты
- 13. § 3. Особенности описания движения микрочастиц. Соотношения неопределенностей
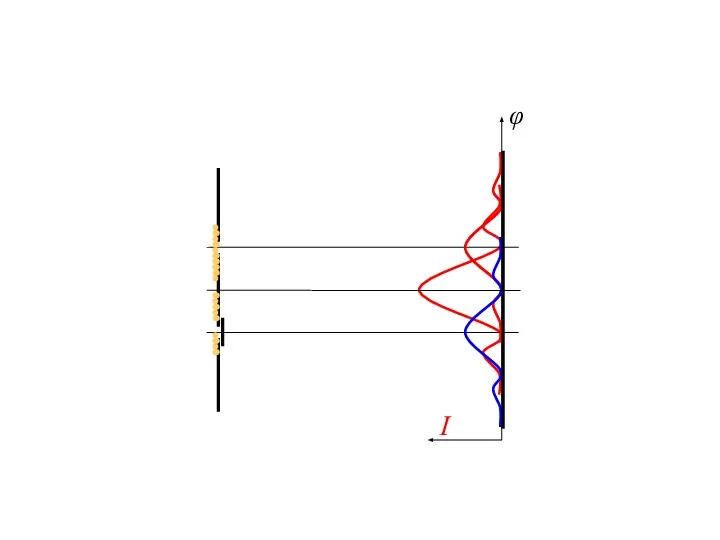
- 14. I φ Дифракция электронов на одной и двух щелях Приписать отдельным электронам определенную траекторию невозможно!
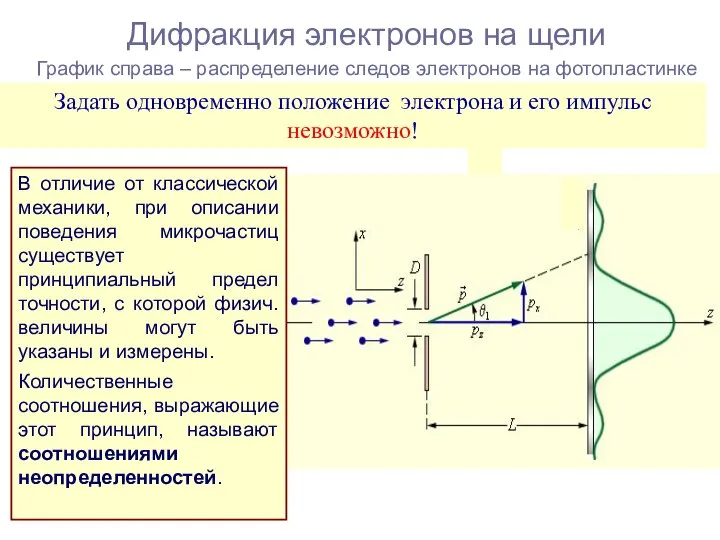
- 15. Дифракция электронов на щели График справа – распределение следов электронов на фотопластинке Задать одновременно положение электрона
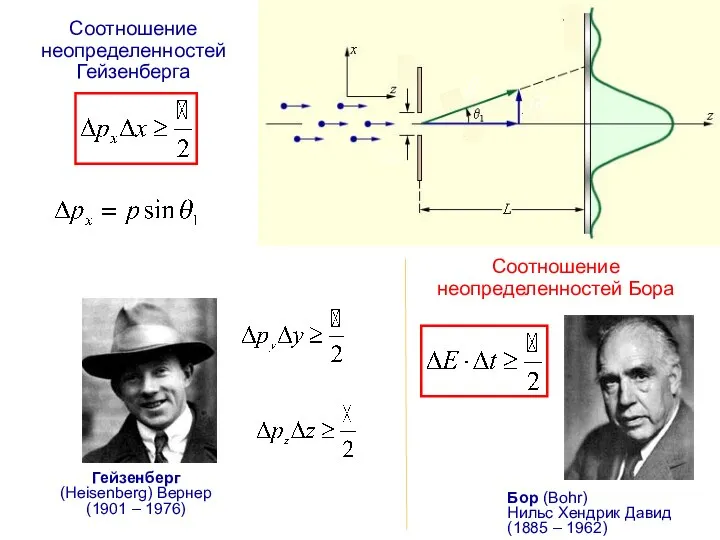
- 16. Соотношение неопределенностей Гейзенберга Гейзенберг (Heisenberg) Вернер (1901 – 1976) Соотношение неопределенностей Бора Бор (Bohr) Нильс Хендрик
- 17. В природе объективно не существует состояний частицы с точно определенными значениями х и рх. Для измерения
- 18. - методологический принцип, сформулированный Нильсом Бором применительно к квантовой физике, согласно которому, для того чтобы наиболее
- 19. §3. Уравнение Шрёдингера Шрёдингер (Schrödinger) Эрвин (1887 – 1961)
- 20. волновая функция – решение ур. Шредингера Движению частицы Шрёдингер сопоставил плоскую волну: - уравнение Шрёдингера для
- 21. Свойства волновой функции 1. Однозначна и непрерывна. 2. Физический смысл ВФ - вероятность обнаружения частицы в
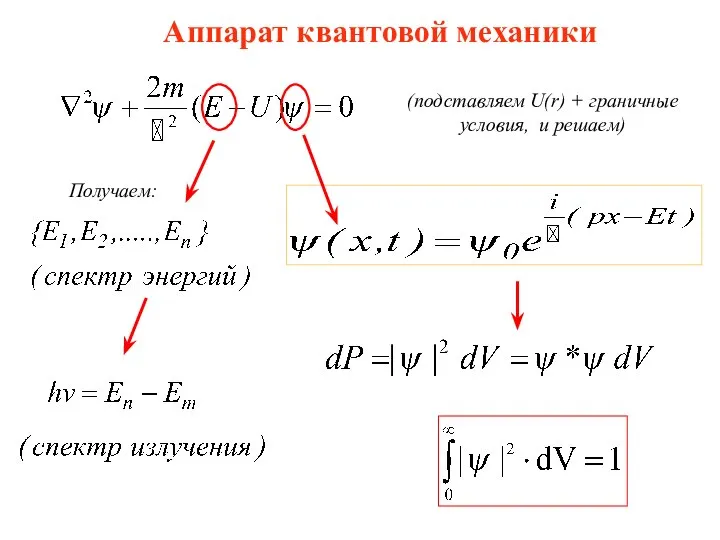
- 22. Аппарат квантовой механики (подставляем U(r) + граничные условия, и решаем) Получаем:
- 23. § 4. Уравнение Шредингера для атома водорода. Квантовые числа 13
- 24. 1. E > 0 - значение энергии изменяется непрерывно. 2. E U r 0 n =
- 25. Решение уравнения Шредингера для электрона в атоме водорода: n = 1,2,3,.. - главное квантовое число l
- 26. Физический смысл (n, l, m) в атоме водорода Главное квантовое число n определяет энергию уровня: Орбитальное
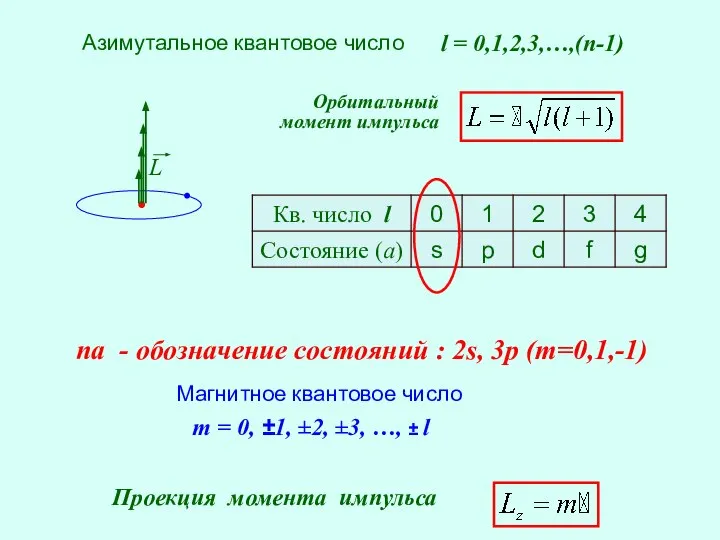
- 27. Азимутальное квантовое число l = 0,1,2,3,…,(n-1) m = 0, ±1, ±2, ±3, …, ± l Магнитное
- 28. § 5. Спин элементарных частиц. Фермионы и бозоны. Принцип Паули Паули Вольфганг Эрнст (1890 – 1958)
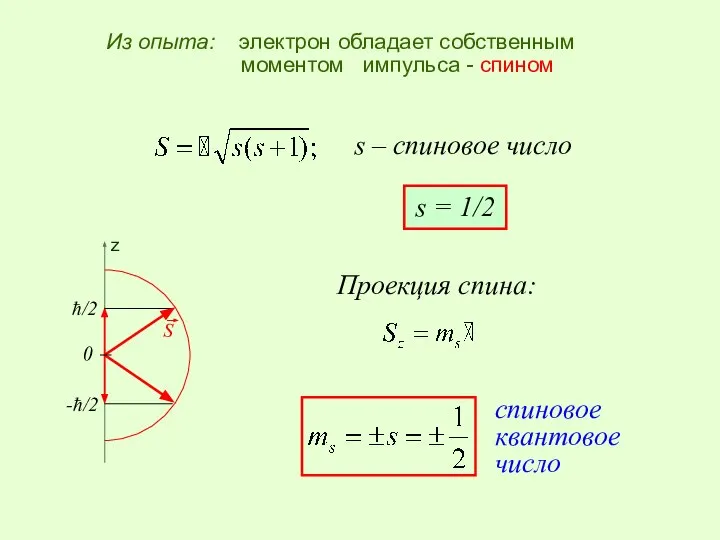
- 29. Из опыта: электрон обладает собственным моментом импульса - спином s – спиновое число s = 1/2
- 30. Бозе-частицы (бозоны) – частицы с целочисленным спином или спином, равным нулю: мезоны (s = 0), фотоны
- 31. s = 1/2 Для электрона и других легких частиц (позитрон, мюоны, нейтрино) 1. s = 0
- 33. Скачать презентацию


















 Лекция №2 Люминесцентный анализ
Лекция №2 Люминесцентный анализ Подготовка к итоговой проверочной работе по физике (6 класс)
Подготовка к итоговой проверочной работе по физике (6 класс) Презентация по физике "радиоактивность" - скачать
Презентация по физике "радиоактивность" - скачать  Радиоактивность . Строение атома.
Радиоактивность . Строение атома. Intake and exhaust manifold, design. (Part 1)
Intake and exhaust manifold, design. (Part 1) РЕНТГЕНОВСКИЕ ЛУЧИ
РЕНТГЕНОВСКИЕ ЛУЧИ Принцип работы ядерного реактора
Принцип работы ядерного реактора Действие жидкости и газа на погруженное в них тело
Действие жидкости и газа на погруженное в них тело Основные характеристики звеньев и систем. Временные характеристики
Основные характеристики звеньев и систем. Временные характеристики Анодные процессы при коррозии металлов
Анодные процессы при коррозии металлов Фотографии камеры Вильсона и треков частиц, полученных в камере Вильсона
Фотографии камеры Вильсона и треков частиц, полученных в камере Вильсона Колебания. Основные определения
Колебания. Основные определения Характеристика гидропривода. Классификация гидропривода. Преимущества и недостатки гидропривода. (Лекция 1)
Характеристика гидропривода. Классификация гидропривода. Преимущества и недостатки гидропривода. (Лекция 1) Электромагнитные колебания. (Лекция 28)
Электромагнитные колебания. (Лекция 28) Кінематика поступального та обертального руху
Кінематика поступального та обертального руху Графическое представление прямолинейного равномерного движения
Графическое представление прямолинейного равномерного движения Рация - переносное приёмо-передающее устройство
Рация - переносное приёмо-передающее устройство Презентация по физике "Изобарный процес" - скачать
Презентация по физике "Изобарный процес" - скачать  Электрондар. Электрон туралы жалпы түсінік
Электрондар. Электрон туралы жалпы түсінік Электризация тел
Электризация тел Упругие волны. (Тема 5)
Упругие волны. (Тема 5) Экспериментальное доказательство существования стационарных состояний атомов (опыты Д. Франка и Г. Герца)
Экспериментальное доказательство существования стационарных состояний атомов (опыты Д. Франка и Г. Герца) Закон сохранения и превращения энергии в механических и тепловых процессах.
Закон сохранения и превращения энергии в механических и тепловых процессах.  Сила трения
Сила трения Альтернативный шнекоход
Альтернативный шнекоход Термодинамикалық жүйе, процесс және тепе-теңдік
Термодинамикалық жүйе, процесс және тепе-теңдік Экосистема поля
Экосистема поля Некоторые вопросы физики магнитных явлений
Некоторые вопросы физики магнитных явлений