Содержание
- 2. Такое поведение объясняется квантованием энергии молекул. В области низких температур величина теплоемкости CV= 3R/2, что соответствует
- 3. Характеристическая температура для вращения молекул определяется ф-лой Тr = ħ2/kI. Для молекулы Н2: I = 2mR2
- 4. § 2.7. ПОЛИТРОПИЧЕСКИЕ ПРОЦЕССЫ Политропическими называют процессы, при которых теплоемкость системы С является постоянной величиной. Можно
- 5. § 3.5. ЭНТРОПИЯ И ВЕРОЯТНОСТЬ Установим связь между макроскопической формулиров-кой 2-го начала dS ≥ δQ/T и
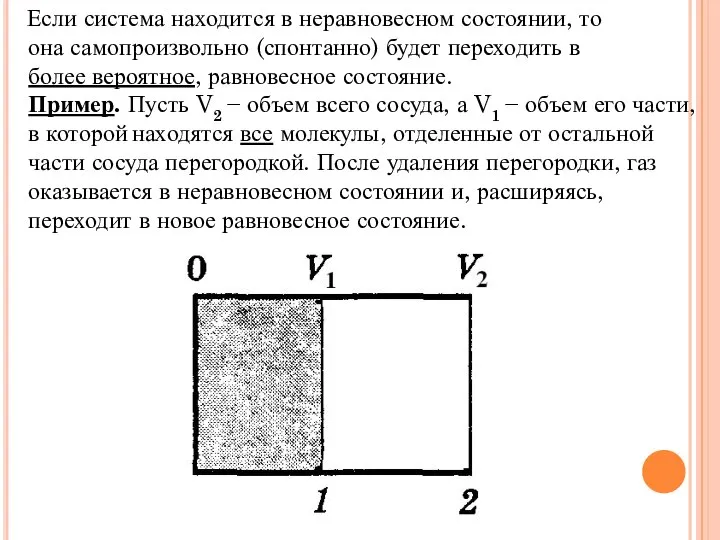
- 6. Если система находится в неравновесном состоянии, то она самопроизвольно (спонтанно) будет переходить в более вероятное, равновесное
- 7. Вместе с тем, согласно 2-му началу, все самопроизвольные процессы в замкнутых макросистемах сопровождаются увеличением энтропии. Поэтому
- 8. Здесь в качестве такого процесса можно использовать изотермическое квазиравновесное расширение где N = νNA − число
- 9. Т.к. положение некоторой другой молекулы не зависит от того, где находится 1-я, то число её микросостояний
- 10. Переход к более вероятному состоянию с бóльшим значе-нием энтропии представляет собой переход к более беспорядочному состоянию.
- 11. Например, в состоянии равновесия число молекул, нахо- дящихся в объёме V1 сосуда, обычно близко к среднему
- 12. § 3.6. ТЕОРЕМА НЕРНСТА Теорема Нернста утверждает: при приближении темпе- ратуры к абсолютному нулю энтропия стремится
- 13. ГЛАВА 4. ТВЕРДЫЕ ТЕЛА § 4.1. Типы кристаллов Под твердыми телами здесь понимаются кристалличес-кие в-ва. Другой
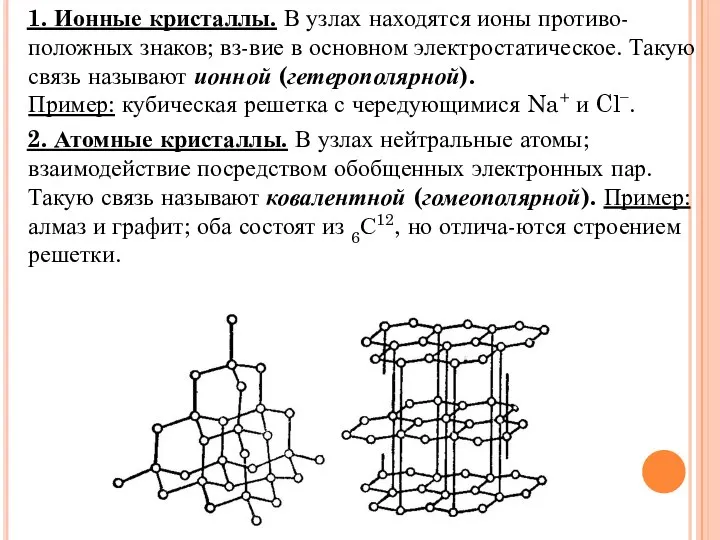
- 14. 1. Ионные кристаллы. В узлах находятся ионы противо-положных знаков; вз-вие в основном электростатическое. Такую связь называют
- 15. 3. Молекулярные кристаллы. В узлах молекулы с ориентированными в направлении соседей дипольными моментами. Такое взаимодействие между
- 16. § 4.2. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ П. Классическая теория. Простейшая модель тв. тела − кристаллич. решетка, в
- 18. Скачать презентацию













 Термодинамика и теплопередача. Техническая термодинамика
Термодинамика и теплопередача. Техническая термодинамика История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия
История изобретения паровых машин. Работу выполнила ученица 8б класса МКОУ СОШ пгт Подосиновец Пунченко Анастасия Методы спектроскопии в исследовании биополимеров
Методы спектроскопии в исследовании биополимеров Потенциальная энергия Физика, 7 класс
Потенциальная энергия Физика, 7 класс Методика фотохронографической регистрации пространственно-временных параметров лазерного излучения
Методика фотохронографической регистрации пространственно-временных параметров лазерного излучения Гидравлический пресс
Гидравлический пресс Физические свойства пористого кремния
Физические свойства пористого кремния Презентация по физике "Строение твердого вещества" - скачать
Презентация по физике "Строение твердого вещества" - скачать  Устройство увеличительных приборов
Устройство увеличительных приборов Конструкция авотмобиля
Конструкция авотмобиля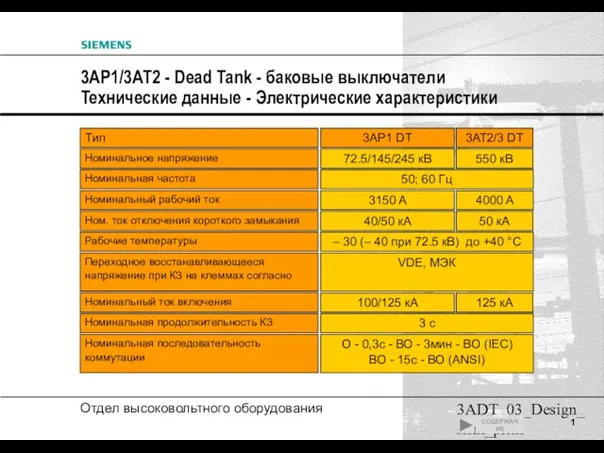 Технические характеристики баковых выключателей 3AP1
Технические характеристики баковых выключателей 3AP1 Взамодія тіл. Імпульс. Закон збереження імпульсу
Взамодія тіл. Імпульс. Закон збереження імпульсу Тепловые явления. Школа Юных физиков (8 класс)
Тепловые явления. Школа Юных физиков (8 класс) Закон сохранения импульса
Закон сохранения импульса Телескоп
Телескоп Презентация по физике "Электроэнергия" - скачать
Презентация по физике "Электроэнергия" - скачать  Свариваемость сталей и сплавов
Свариваемость сталей и сплавов Механические волны. Звук
Механические волны. Звук Выполнение судовых работ. Средства связи, сигналы
Выполнение судовых работ. Средства связи, сигналы Презентация по физике "Физика и космическая еда" - скачать
Презентация по физике "Физика и космическая еда" - скачать  Утюг – мой друг Автор: Абросимова А. Б. , ученица 8 класса МОУ Слободской СОШ им. Г. Н. Пономарёва 2010г.
Утюг – мой друг Автор: Абросимова А. Б. , ученица 8 класса МОУ Слободской СОШ им. Г. Н. Пономарёва 2010г. Термодинамические циклы холодильных машин
Термодинамические циклы холодильных машин Структура и спектральнолюминесцентные свойства микрокристаллических трубок на основе ZrO2
Структура и спектральнолюминесцентные свойства микрокристаллических трубок на основе ZrO2 УРОК ФИЗИКИ В 10 КЛАССЕ Решение задач. Идеальный газ Учитель Кононов Геннадий Григорьевич СОШ № 29 Славянский район
УРОК ФИЗИКИ В 10 КЛАССЕ Решение задач. Идеальный газ Учитель Кононов Геннадий Григорьевич СОШ № 29 Славянский район  Параметрические цепи
Параметрические цепи Аттестационная работа. Методическая разработка Легоконструирование
Аттестационная работа. Методическая разработка Легоконструирование Влияние электромагнитных излучений на живые организмы
Влияние электромагнитных излучений на живые организмы Составление формул
Составление формул