Содержание
- 2. Фаза – гомогенная часть системы отделенная от других частей поверхностью раздела и имеющая во всех точках
- 3. Правило фаз С = K + N – Ф С – число степеней свободы – число
- 4. С = K + N – Ф К – число независимых компонентов Компонент – вещество, которое
- 5. Фазовая диаграмма – график, изображающий области существования фаз в координатах независимых параметров (например, р – Т,
- 6. Фазовая диаграмма серы С = К + 2 – Ф С = 3 – Ф
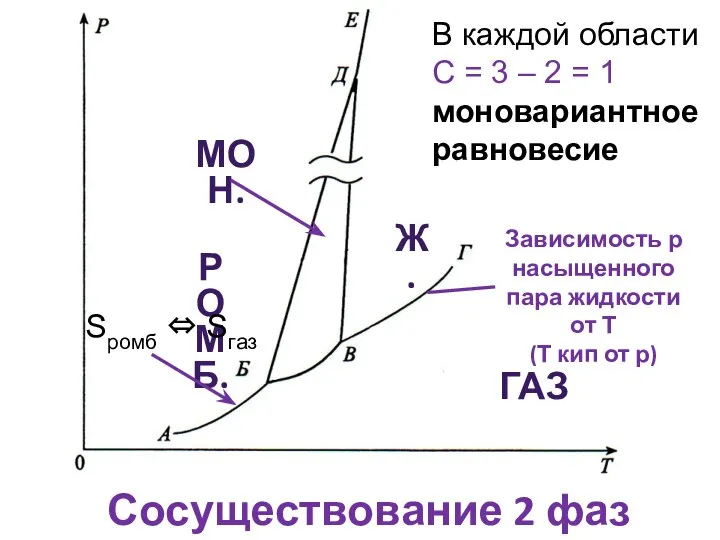
- 7. РОМБ. ГАЗ Ж. МОН. Области существования фаз В каждой области С = 3 – 1 =
- 8. РОМБ. ГАЗ Ж. МОН. Зависимость р насыщенного пара жидкости от Т (Т кип от р) Сосуществование
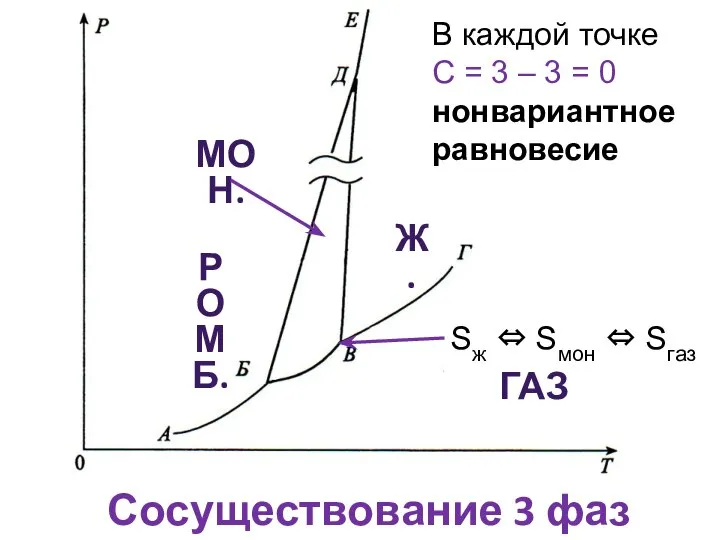
- 9. РОМБ. ГАЗ Ж. МОН. Сосуществование 3 фаз В каждой точке С = 3 – 3 =
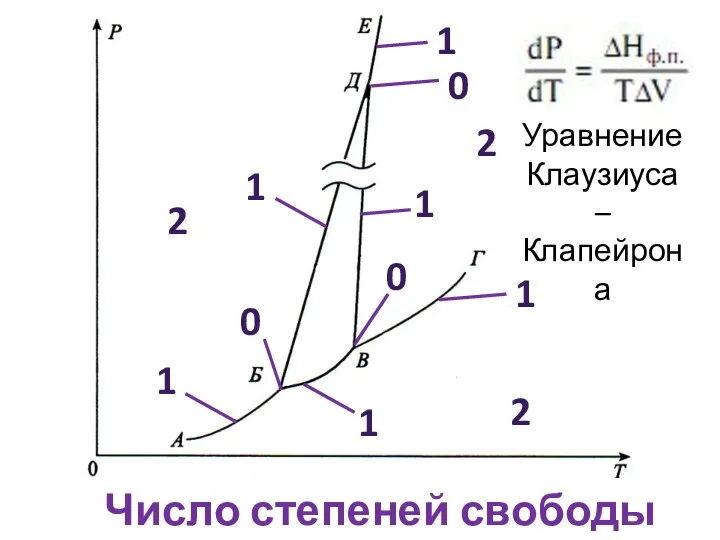
- 10. 2 2 2 1 1 1 1 1 1 0 0 0 Число степеней свободы Уравнение
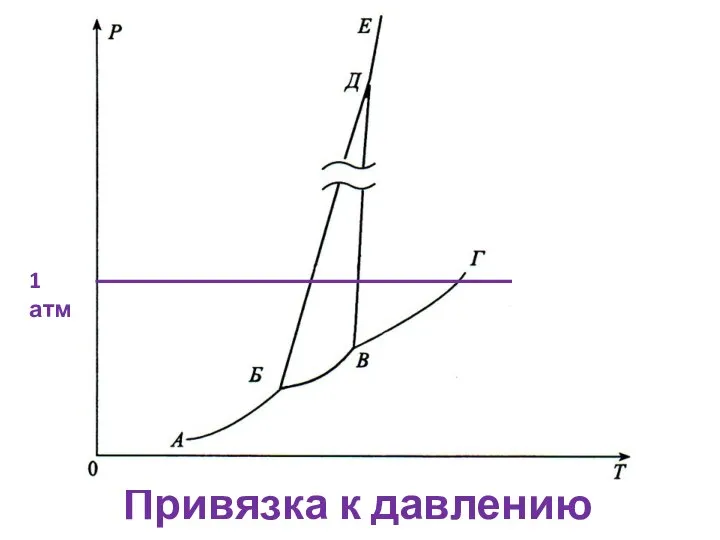
- 11. Привязка к давлению 1 атм
- 12. Привязка к температурам 1 атм 95о 119о 444о
- 13. Закон Рауля и его следствия 1 атм Н2О Тзам Тзам 0 Ткип 0 Ткип
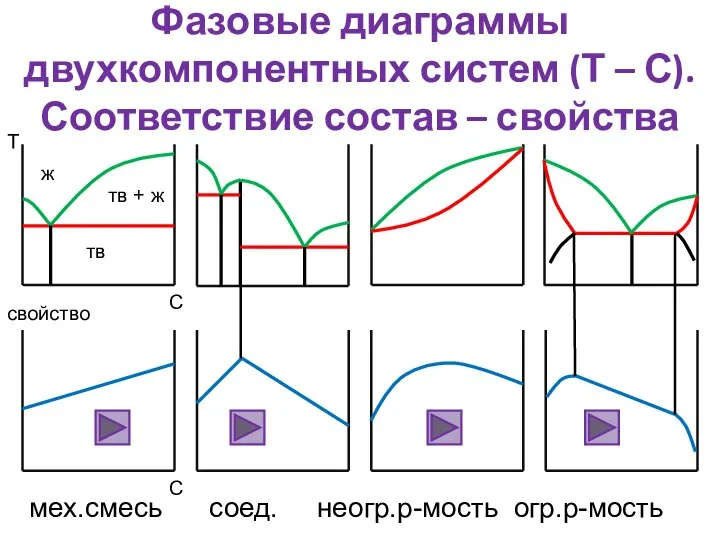
- 14. Фазовые диаграммы двухкомпонентных систем (Т – С). Соответствие состав – свойства мех.смесь соед. неогр.р-мость огр.р-мость тв
- 15. Фазовая диаграмма двухкомпонентной системы (участок жидкость – пар)
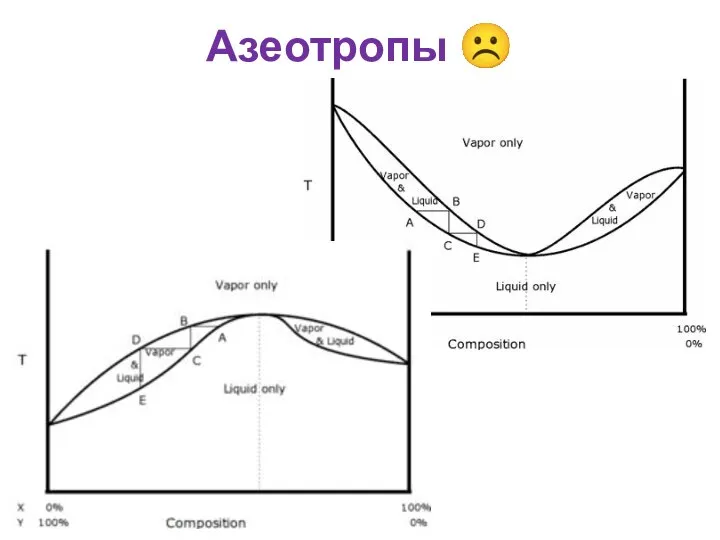
- 16. Азеотропы ☹
- 17. Диаграмма (не фазовая ☹)
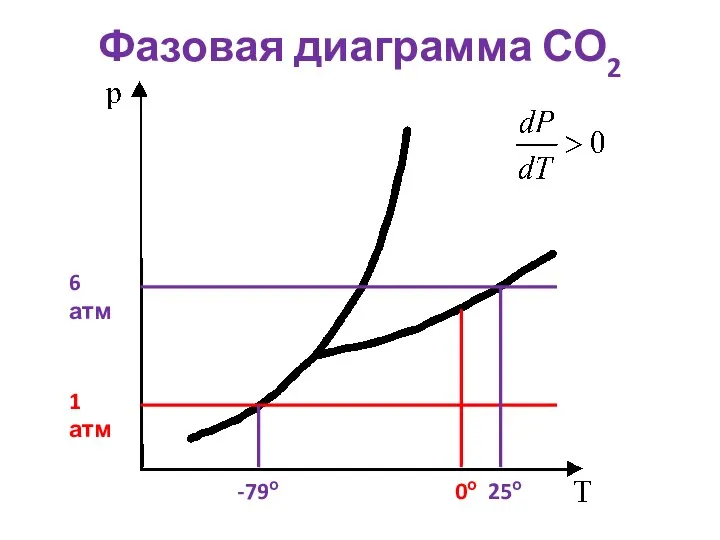
- 19. Фазовая диаграмма СО2 1 атм -79о 6 атм 25о 0о
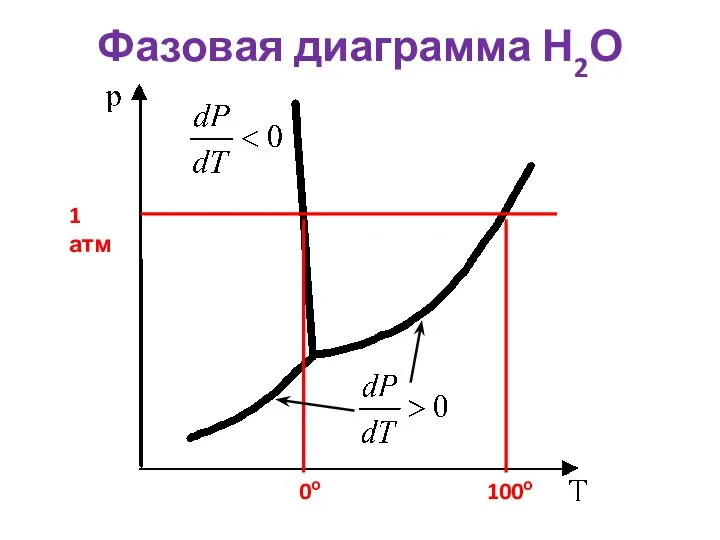
- 20. Фазовая диаграмма Н2О 1 атм 0о 100о
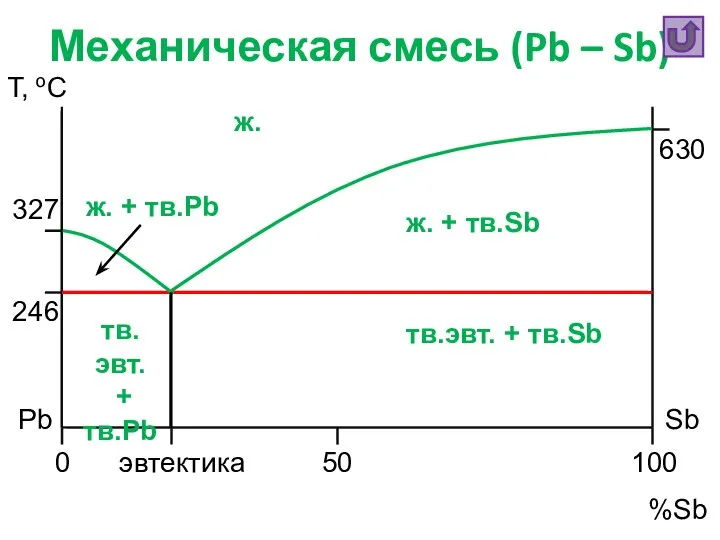
- 22. Механическая смесь (Pb – Sb) Т, oC %Sb Pb Sb 0 50 100 630 327 246
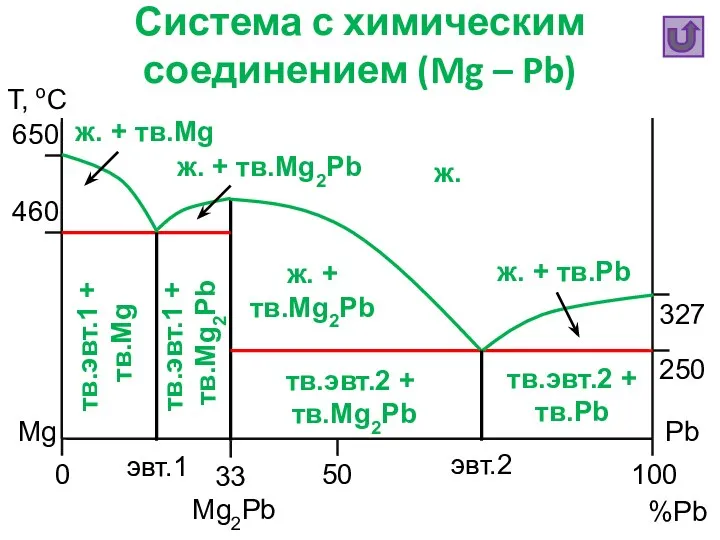
- 23. Система с химическим соединением (Mg – Pb) Т, oC %Pb Mg Pb 0 50 100 327
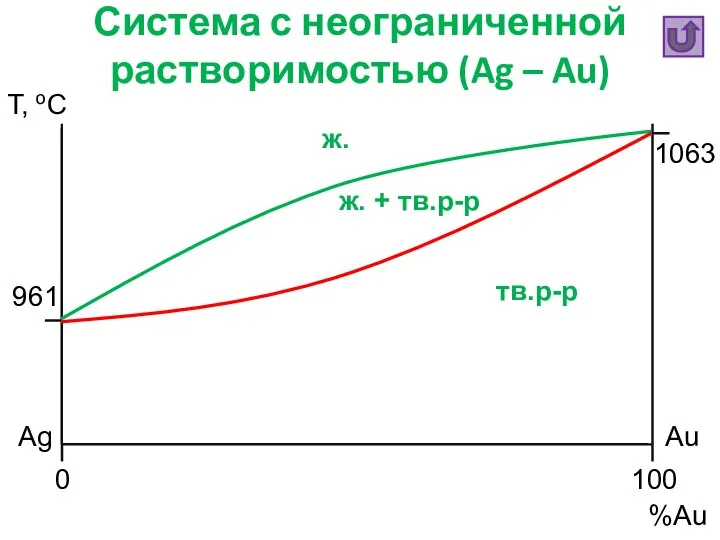
- 24. Система с неограниченной растворимостью (Ag – Au) Т, oC %Au Ag Au 0 100 1063 961
- 26. Скачать презентацию











 Area, size and mass
Area, size and mass Схемы электрических соединений на стороне 6-10 кВ. (Лекция 12)
Схемы электрических соединений на стороне 6-10 кВ. (Лекция 12) Свариваемость сталей и сплавов
Свариваемость сталей и сплавов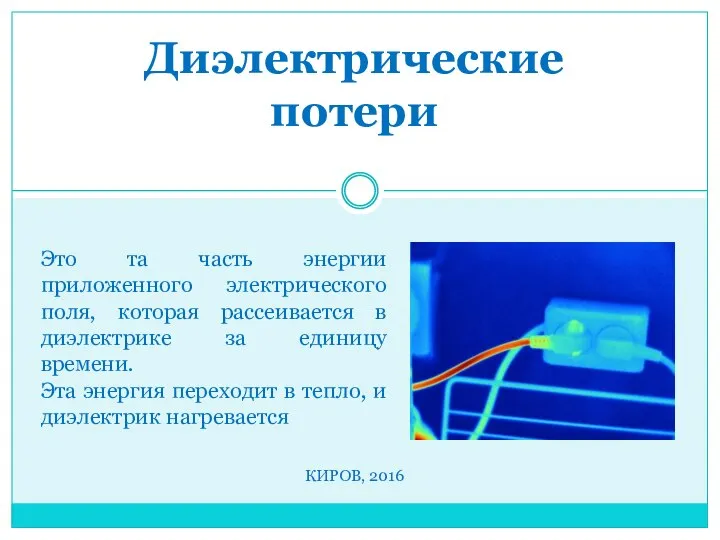 Диэлектрические потери
Диэлектрические потери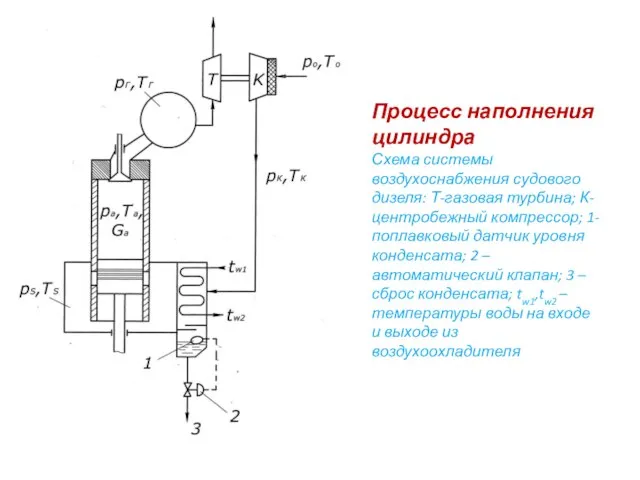 Процесс наполнения цилиндра. Схема системы воздухоснабжения судового дизеля
Процесс наполнения цилиндра. Схема системы воздухоснабжения судового дизеля Химическая термодинамика
Химическая термодинамика Скачать презентацию Действие электрического тока на человека
Скачать презентацию Действие электрического тока на человека  Релаксация спинового ансамбля
Релаксация спинового ансамбля Специальная теория относительности. Относительность одновременности. Постулаты Эйнштейна
Специальная теория относительности. Относительность одновременности. Постулаты Эйнштейна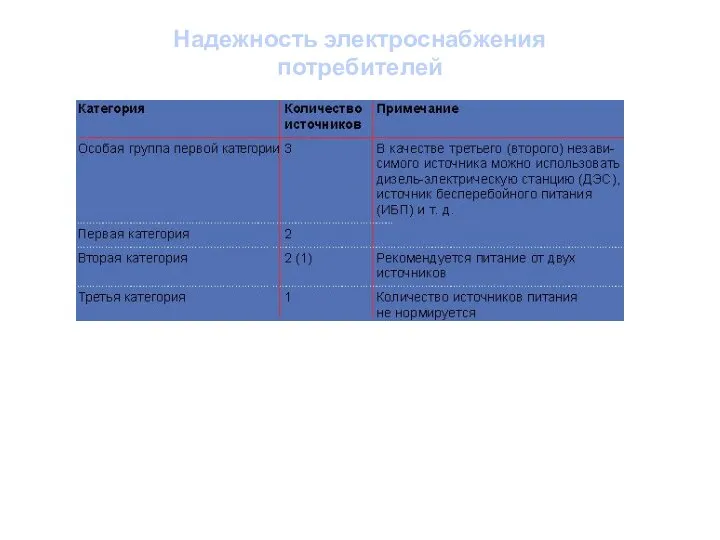 Надежность электроснабжения потребителей
Надежность электроснабжения потребителей Дифракция волн
Дифракция волн Форма и характеристики электрических сигналов. Анализ
Форма и характеристики электрических сигналов. Анализ Мономолекулярные слои (Пленки Ленгмюра-Блоджетт)
Мономолекулярные слои (Пленки Ленгмюра-Блоджетт)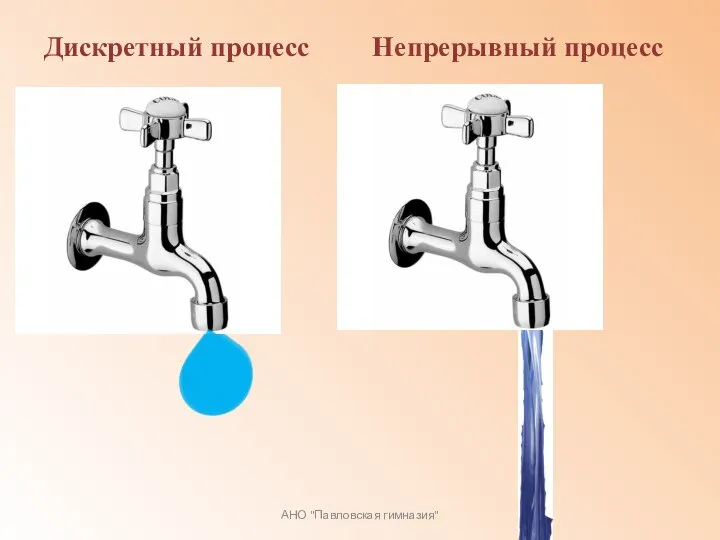 Дискретный процесс. Непрерывный процесс. Производная
Дискретный процесс. Непрерывный процесс. Производная Реактивное движение
Реактивное движение Исследование минералов под микроскопом
Исследование минералов под микроскопом Жидко-солевой реактор. (Лекция 14)
Жидко-солевой реактор. (Лекция 14) Сходство и различие работы крыла в воздушной и водной среде
Сходство и различие работы крыла в воздушной и водной среде Аттестационная работа. На тему: «Методическая разработка занятия «Что такое магнит?»
Аттестационная работа. На тему: «Методическая разработка занятия «Что такое магнит?»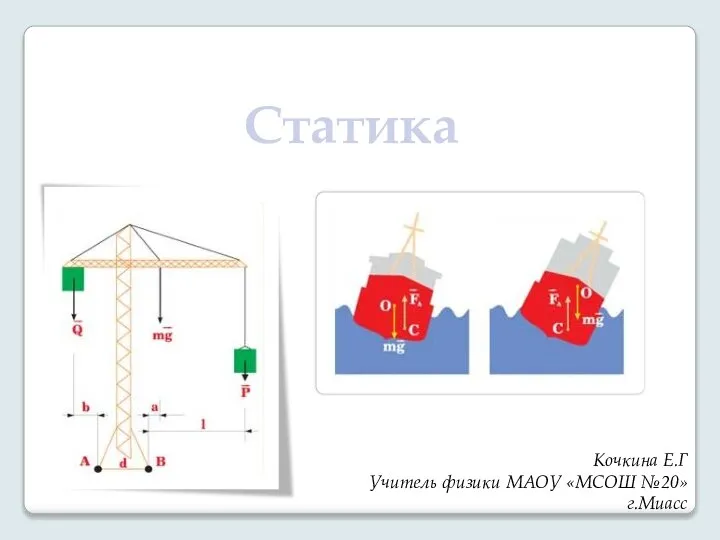 Статика. Равновесие тел
Статика. Равновесие тел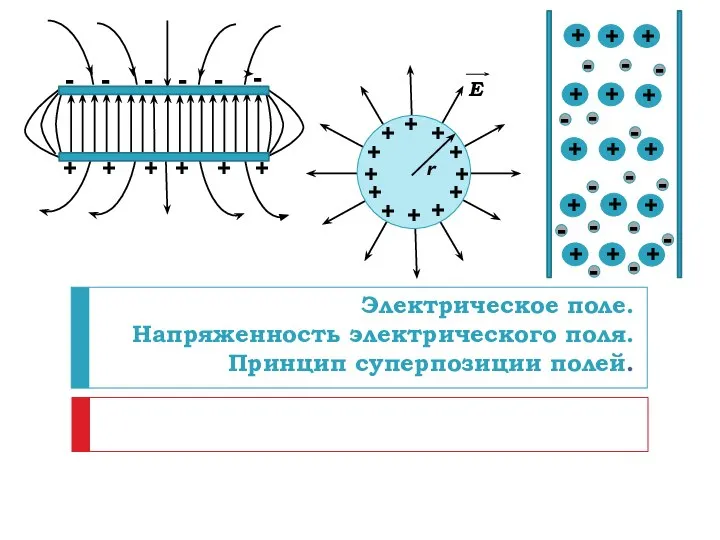 Электрическое поле. Напряженность электрического поля. Принцип суперпозиции полей
Электрическое поле. Напряженность электрического поля. Принцип суперпозиции полей Техническая эксплуатация. Жизненный цикл РЭО
Техническая эксплуатация. Жизненный цикл РЭО Открытие радиоактивности
Открытие радиоактивности Модели атомов. Опыт Резерфорда.
Модели атомов. Опыт Резерфорда.  Инфракрасное излучение
Инфракрасное излучение Лабораторная работа. Определите вид фотоаппарата
Лабораторная работа. Определите вид фотоаппарата Статистическая теория радиотехнических систем. Случайные процессы и величины. (Лекция 2)
Статистическая теория радиотехнических систем. Случайные процессы и величины. (Лекция 2) Фотоэффект. (11 класс)
Фотоэффект. (11 класс)