Содержание
- 2. Вычислить: тепловой эффект реакции; изменение энтропии; изменение изобарного потенциала системы; значение константы равновесия Кр для заданной
- 3. Химическая термодинамика разрабатывает способы, позволяющие вычислять свойства вещества на основе знаний об индивидуальных молекулах, дает точные
- 4. - макроскопическая физическая система, состоящая из большого числа частиц (не требующая для своего описания привлечения микроскопических
- 5. 1ое начало термодинамики (1.1) (1.1,1.2)Тепловой эффект реакции, протекающей при постоянном давлении, равен изменению энтальпии ΔНr. Энтальпией
- 6. (1.2) Тепловой эффект определяют при выполнении следующих условий: 1) реакция должна пройти необратимо и до конца;
- 7. (1.2) Тепловой эффект определяют при выполнении следующих условий: 1) реакция должна пройти необратимо и до конца;
- 8. Cтандартное состояние За стандартное состояние для газа принят газ, обладающий свойствами идеального газа при давлении в
- 9. Стандартный тепловой эффект реакции (1.3) Стандартный тепловой эффект реакции равен разности между суммой стандартных теплот образований
- 10. Стандартный тепловой эффект реакции (1.4) Стандартный тепловой эффект реакции равен разности между суммой стандартных теплот сгорания
- 11. Теплоемкость (1.5) Теплоемкостью системы называют количество теплоты ΔQ, которое необходимо сообщить системе, чтобы нагреть ее на
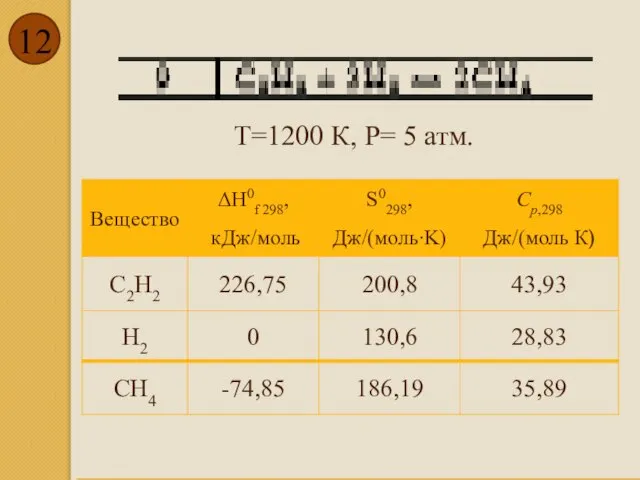
- 12. T=1200 К, P= 5 атм.
- 13. Расчет теплового эффекта реакции при произвольной температуре(1.6) Чтобы рассчитать тепловой эффект при заданной температуре Т, уравнение
- 14. Энтропия (1.8) Термодинамическая энтропия — термодинамическая функция, характеризующая меру необратимой превращения теплоты в энергию в системе.
- 15. (1.8) Энтропия характеризует: число состояний, в которых система проводит все время; чем больше энтропия, тем больше
- 16. (1.8) Изменение энтропии при протекании химической реакции рассчитывают с применением табличных данных о значениях стандартной энтропии
- 17. . Изменение энтропии для необратимого процесса рассчитывают, рассматривая путь, по которому протекает процесс, в несколько стадий.
- 18. Второе начало термодинамики (1.7) Энтропия замкнутой системы не убывает: dS ≥ 0. Для любого бесконечно малого
- 19. Процессы (1.7,1.8) Самопроизвольными называют процессы, которые протекают без внешних воздействий (например, течение воды сверху вниз). Несамопроизвольными
- 20. Энергия Гиббса 1.9 Энергией Гиббса называют функцию состояния, определяемую уравнением G = U + pV –
- 21. Энергия Гиббса 1.10 Для расчета изобарного потенциала реакции, протекающей при температуре, для которой отсутствуют табличные данные,
- 22. Константа равновесия(1.11) Нельзя изменить парциального давления (концентрации) ни одного из веществ, участвующих в реакции, чтобы это
- 23. Химическое сродство (1.11) Под химическим сродством понимают способность вещества вступать в химические реакции. Способность же химических
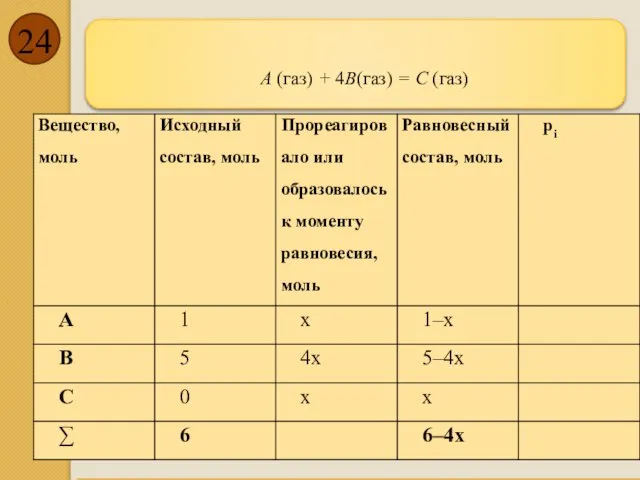
- 24. А (газ) + 4В(газ) = С (газ)
- 25. Составленное уравнение для Кр превращается в равенство: после логарифмирования которого имеем: lg Кр = lgM –
- 26. ФАЗОВЫЕ РАВНОВЕСИЯ.
- 27. Равновесия, которые устанавливаются в неоднородной (многофазной) системе называются фазовыми равновесиями. Они составляют особую область физической химии
- 28. Фаза. Условия фазового равновесия (2.1) Фазой называют однородную часть материальной вселенной, ограниченную поверхностью раздела и обладающую
- 29. Правило фаз Гиббса (2.2) Число степеней свободы (число интенсивных переменных, которым можно одновременно задать произвольные значения)
- 30. Идеальный раствор (2.3) Идеальными называются растворы, в которых энергия взаимодействия между разнородными молекулами (связь типа А-В)
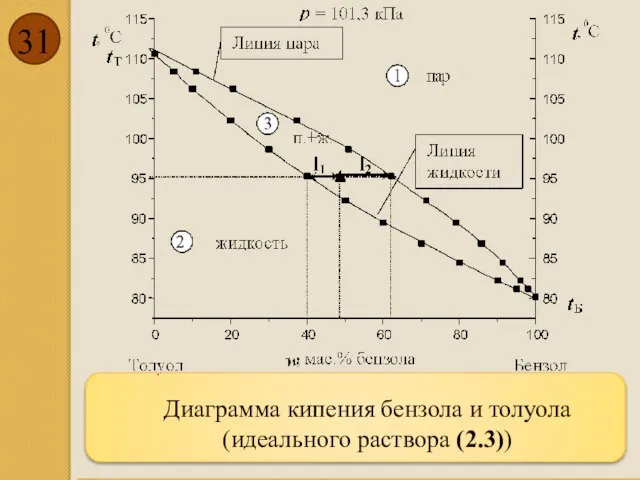
- 31. Диаграмма кипения бензола и толуола (идеального раствора (2.3))
- 32. Свойства реальных жидких смесей в большей или меньшей степени отклоняются от идеальных. Причины отклонения можно свести
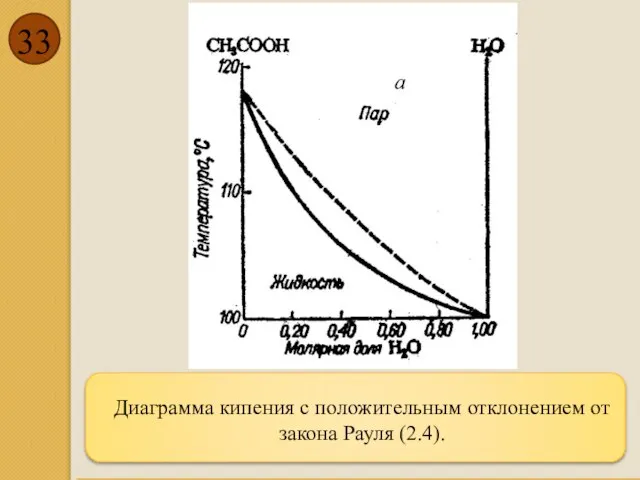
- 33. Диаграмма кипения с положительным отклонением от закона Рауля (2.4).
- 34. В противоположном случае – при укрупнении молекул (при ассоциации) или при более прочных связях типа А-В,
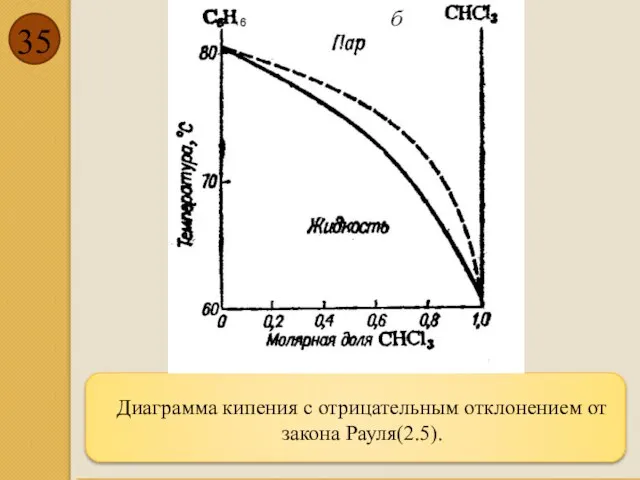
- 35. Диаграмма кипения с отрицательным отклонением от закона Рауля(2.5).
- 36. Пар, по сравнению с жидкостью, обогащен бензолом, температура кипения которого ниже, чем температура кипения толуола (Слайд
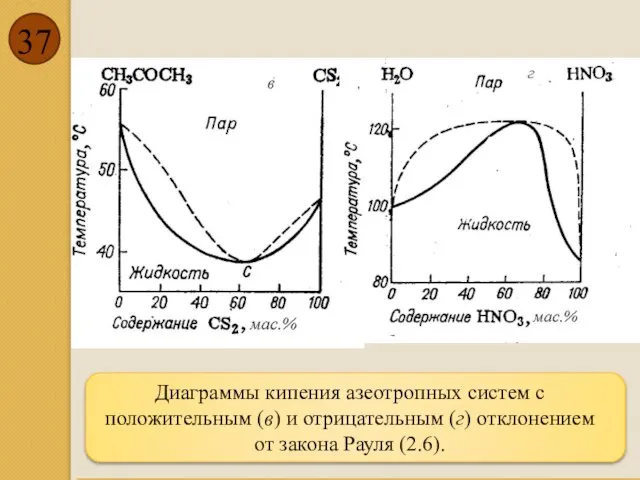
- 37. Диаграммы кипения азеотропных систем с положительным (в) и отрицательным (г) отклонением от закона Рауля (2.6).
- 38. Ректификационная колонна
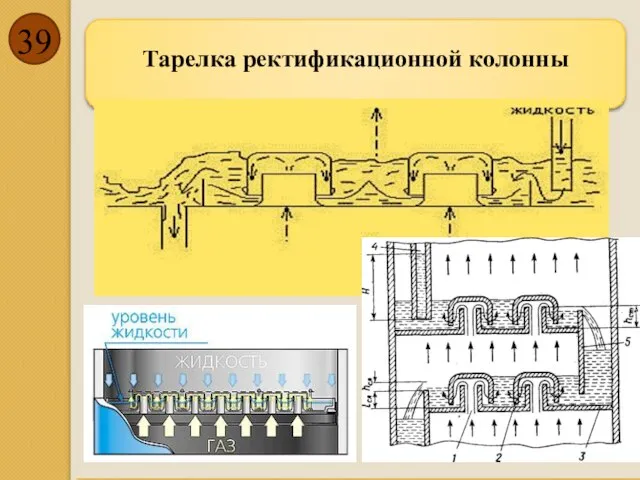
- 39. Тарелка ректификационной колонны
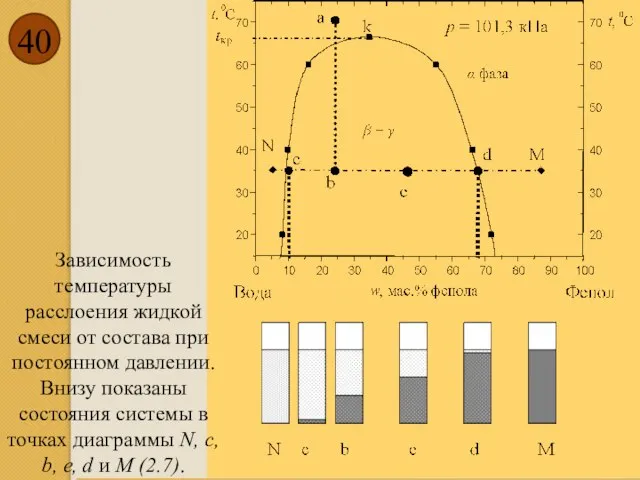
- 40. Зависимость температуры расслоения жидкой смеси от состава при постоянном давлении. Внизу показаны состояния системы в точках
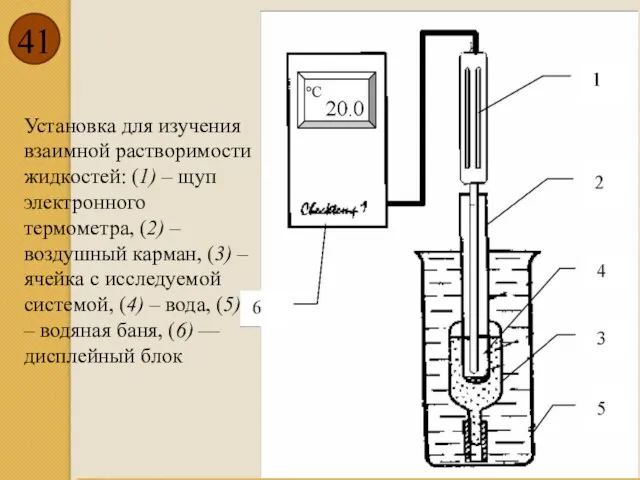
- 41. Установка для изучения взаимной растворимости жидкостей: (1) – щуп электронного термометра, (2) – воздушный карман, (3)
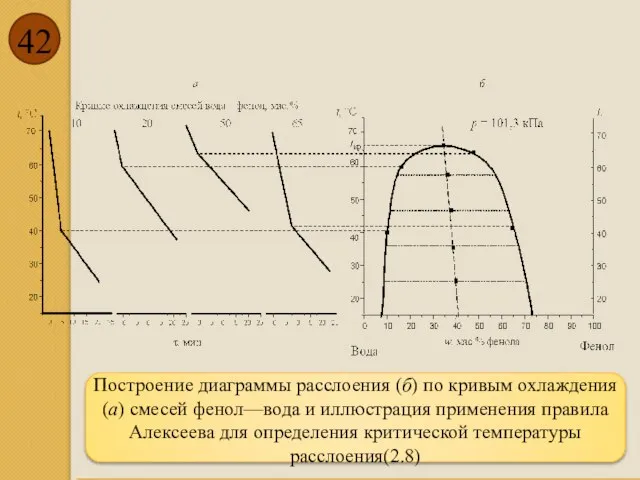
- 42. Построение диаграммы расслоения (б) по кривым охлаждения (а) смесей фенол—вода и иллюстрация применения правила Алексеева для
- 43. ЭЛЕКТРОПРОВОДНОСТЬ. КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ.
- 44. Электролиты 3.1 По способности проводить электрический ток все вещества делятся на электролиты (проводящие электрический ток) и
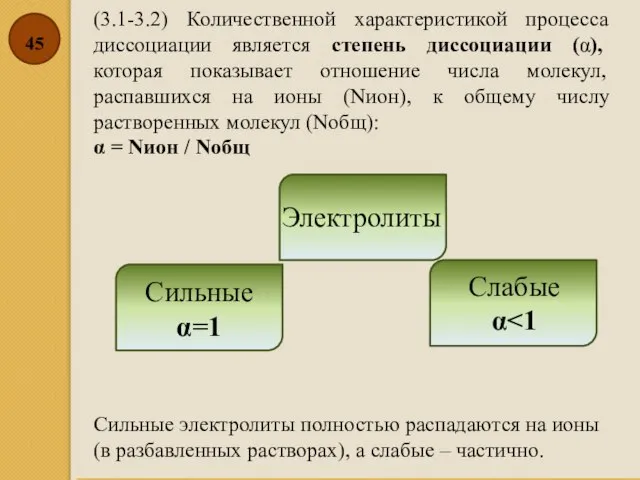
- 45. (3.1-3.2) Количественной характеристикой процесса диссоциации является степень диссоциации (α), которая показывает отношение числа молекул, распавшихся на
- 46. На степень диссоциации влияют (3.1) природа растворителя и электролита: сильными электролитами являются вещества с ионными и
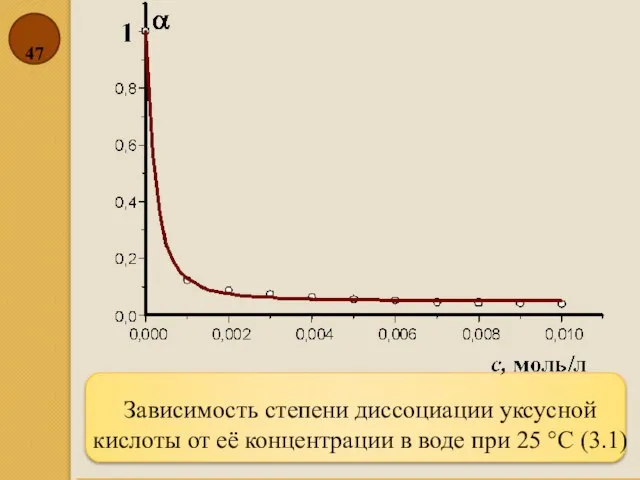
- 47. Зависимость степени диссоциации уксусной кислоты от её концентрации в воде при 25 °C (3.1)
- 48. Активность (ионов) — эффективная концентрация с учетом электростатического взаимодействия между ионами в растворе. Активность отличается от
- 49. (3.2) Константа диссоциации - В общей реакции где комплекс разбивается на x единиц A и y
- 50. (3.2) Закон разбавления Оствальда КА=К++A- Исходя из определения степени диссоциации, для электролита КА в реакции диссоциации
- 51. Электри́ческая проводи́мость - ток, протекающий через образец при приложении к нему единичной разности потенциалов, ед.изм. –
- 52. Удельная электрическая проводимость (3.3) æ = Qαuс Удельная электрическая проводимость æ — это проводимость столба жидкости
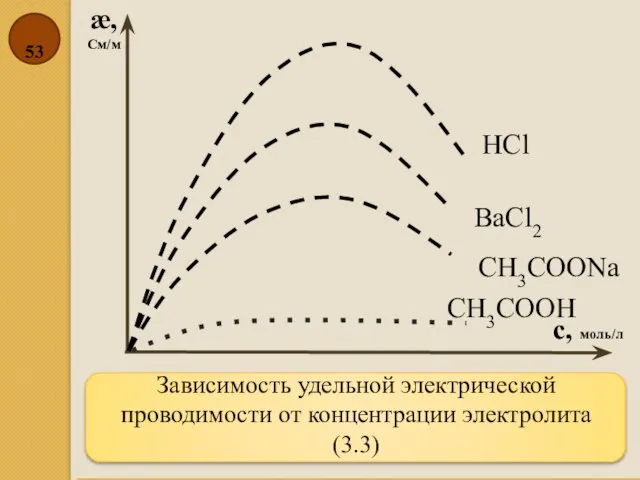
- 53. Зависимость удельной электрической проводимости от концентрации электролита (3.3) æ, См/м с, моль/л HCl BaCl2 CH3COONa CH3COOH
- 54. Млярная электрическая проводимость (3.3) Λ = æ /с = Qαu где Q - электрический заряд; α-
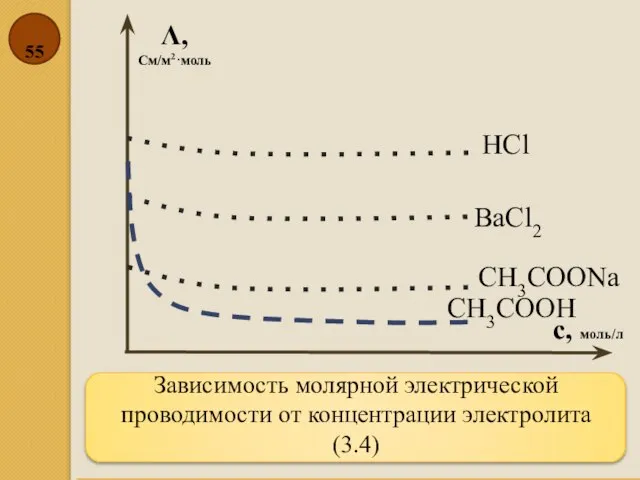
- 55. Зависимость молярной электрической проводимости от концентрации электролита (3.4) Λ, См/м2·моль с, моль/л HCl BaCl2 CH3COONa CH3COOH
- 56. Предельная молярная проводимость (3.5)- - молярная проводимость при бесконечном разбавлении при бесконечном разбавлении (При малых концен
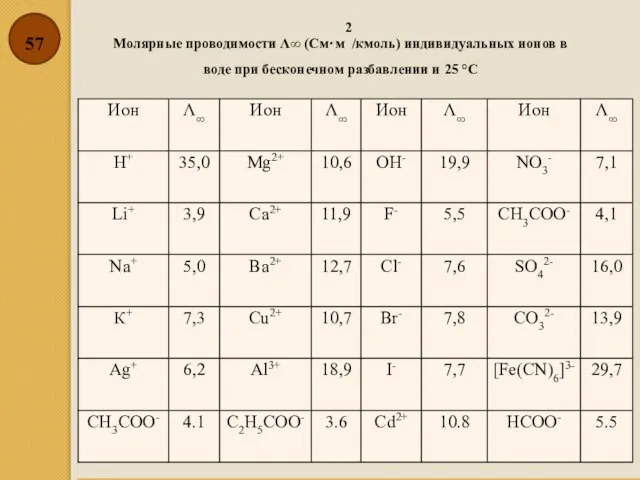
- 57. Молярные проводимости Λ∞ (См⋅м2/кмоль) индивидуальных ионов в воде при бесконечном разбавлении и 25 °С
- 58. (3.2) Закон разбавления Оствальда КА=К++A- Исходя из определения степени диссоциации, для электролита КА в реакции диссоциации
- 59. Определение константы диссоциации (3.6) α= Λ/Λ∞ Λ ≈ Λ∞(K) 1/2 (1 /с)1/2 представляет собой уравнение прямой
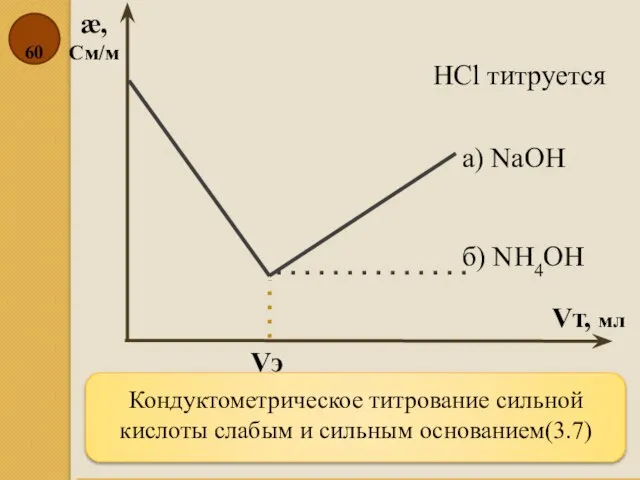
- 60. Кондуктометрическое титрование сильной кислоты слабым и сильным основанием(3.7) æ, См/м Vт, мл HCl титруется б) NH4OH
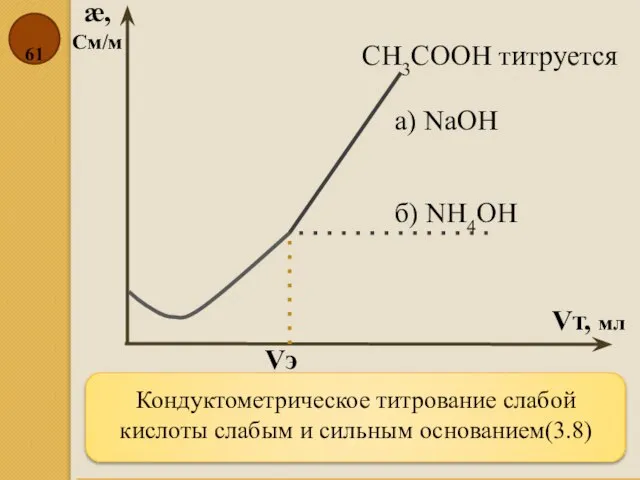
- 61. Кондуктометрическое титрование слабой кислоты слабым и сильным основанием(3.8) æ, См/м Vт, мл CH3COOH титруется б) NH4OH
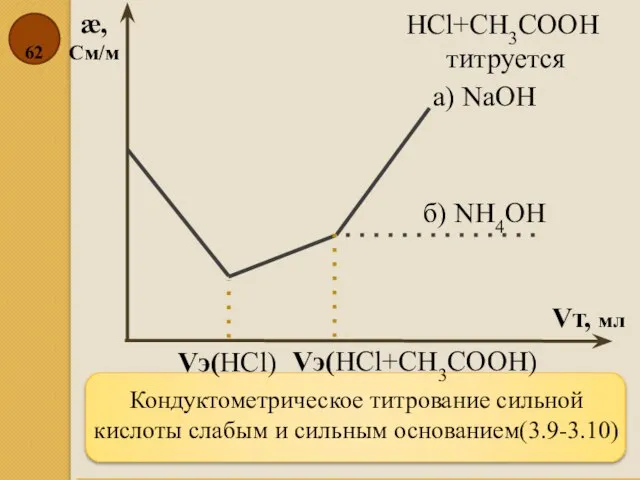
- 62. Кондуктометрическое титрование сильной кислоты слабым и сильным основанием(3.9-3.10) æ, См/м Vт, мл HCl+CH3COOH титруется б) NH4OH
- 63. ИЗМЕРЕНИЕ ЭДС, рН, ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
- 64. Приготовить буферный раствор с заданной величиной рН, определить его буферную емкость β и сравнить ее буферной
- 65. Электро́дный потенциа́л — разность электрических потенциалов между электродом и находящимся с ним в контакте электролитом (чаще
- 66. Уравнение Нернста (4.1) E — электродный потенциал, E0 — стандартный электродный потенциал, измеряется в вольтах; R
- 67. Гальванический элемент Якоби-Даниэля (4.2) Рассмотрим гальванический элемент Якоби-Даниэля. Он состоит из медной пластины, погруженной в раствор
- 68. Классификация электродов(4.3) Электроды подразделяются на обратимые и необратимые. Если изменить направление электрического тока во внешней цепи
- 69. Классификация электродов(4.1)
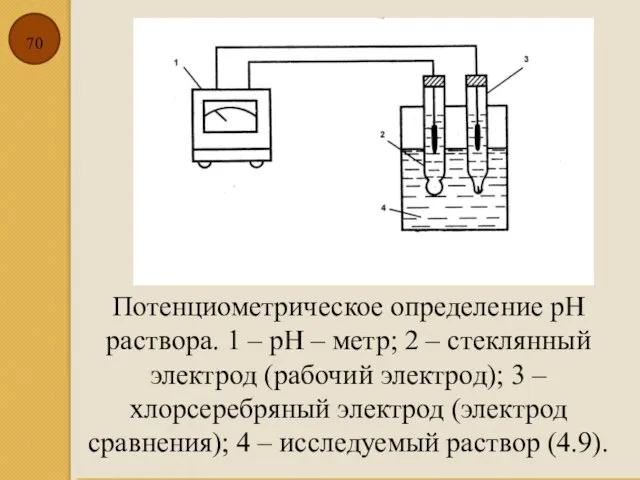
- 70. Потенциометрическое определение рН раствора. 1 – рН – метр; 2 – стеклянный электрод (рабочий электрод); 3
- 71. (4.9, 4.10) Потенциал хингидронного электрода, измеренный относительно промышленного насыщенного хлорсеребрянного электрода Е (т.е. разность между потенциалами
- 72. 4.11 Буферной емкостью β называется количество моль эквивалентов сильной кислоты или щелочи, которое необходимо добавить к
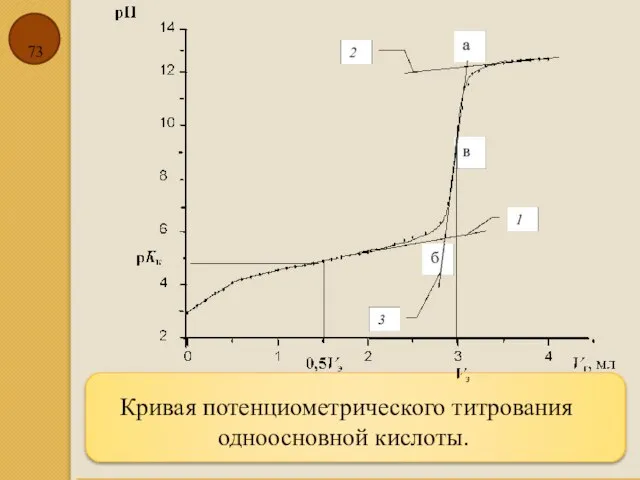
- 73. Кривая потенциометрического титрования одноосновной кислоты.
- 74. ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ И ПОВЕРХНОСТНАЯ АКТИВНОСТЬ ПАВ. АДСОРБЦИЯ ПАВ НА ГРАНИЦЕ ВОДА-ВОЗДУХ.
- 75. Измерить поверхностное натяжение растворов нескольких ПАВ в гомологическом ряду; построить изотермы поверхностного натяжения и рассчитать коэффициент
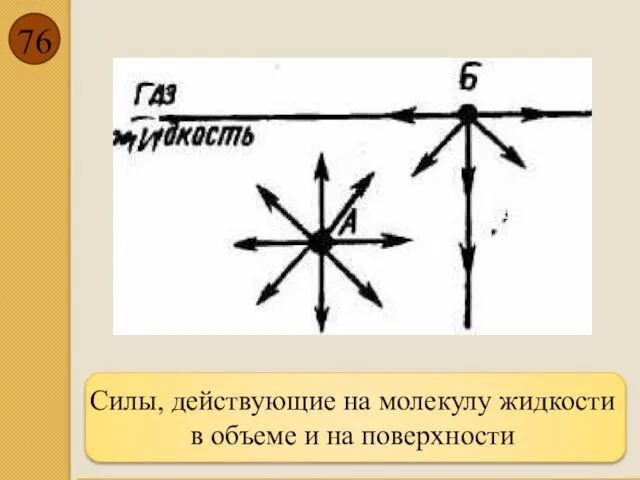
- 76. Силы, действующие на молекулу жидкости в объеме и на поверхности
- 77. Поверхностное натяжение
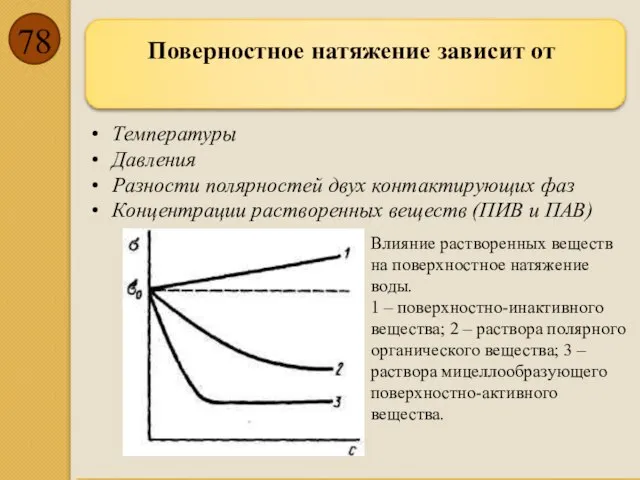
- 78. Поверностное натяжение зависит от Температуры Давления Разности полярностей двух контактирующих фаз Концентрации растворенных веществ (ПИВ и
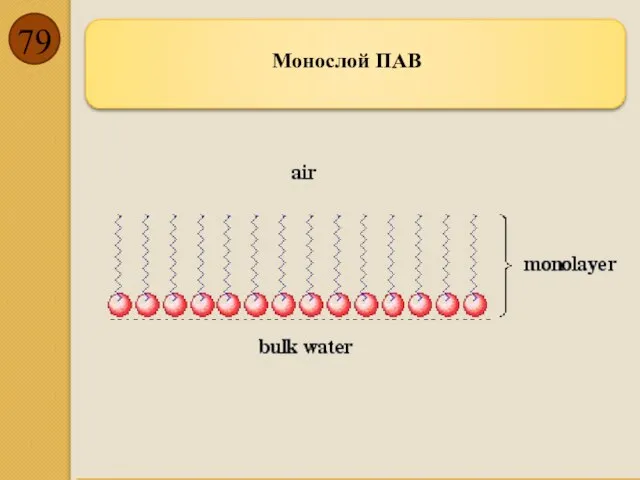
- 79. Монослой ПАВ
- 80. Поверхностная активность g: Поверхностная активность ПАВ характеризует способностью вещества понижать поверхностное натяжение и численно равна уменьшению
- 81. Правило Дюкло - Траубе: Отношение поверхностных активностей gn и gn+1 двух ближайших гомологов называют коэффициентом Траубе
- 82. Методы определения поверхностного натяжения Статические методы: Метод поднятия в капилляре Метод Вильгельми Метод лежачей капли Метод
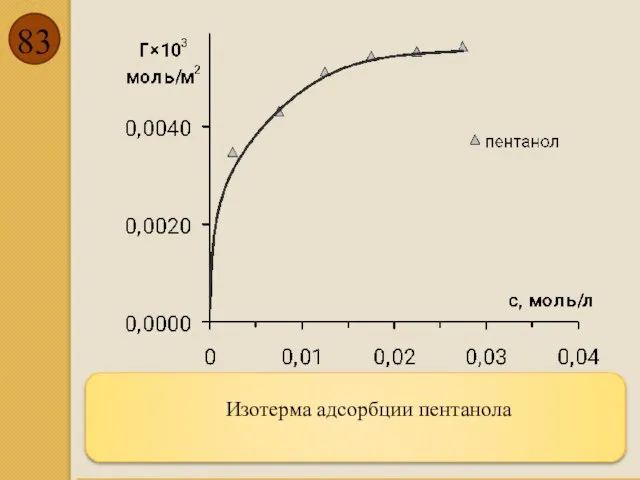
- 83. Изотерма адсорбции пентанола
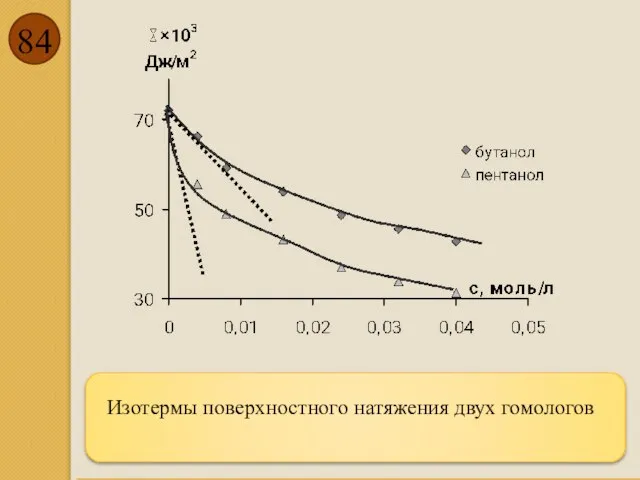
- 84. Изотермы поверхностного натяжения двух гомологов
- 85. Адсорбция Наряду с поверхностным натяжением и поверхностной активностью границу фаз характеризуют удельной адсорбцией (Г, [моль/м2]), под
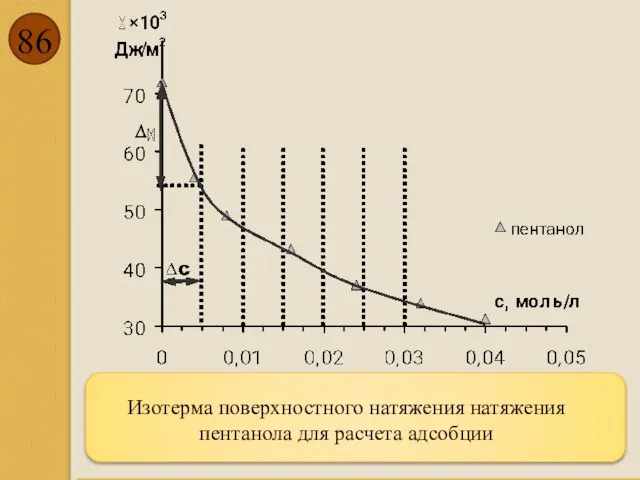
- 86. Изотерма поверхностного натяжения натяжения пентанола для расчета адсобции
- 87. Ленгмюр предположил, что поверхность состоит из одинаковых элементарных участков, каждый из которых может адсорбировать одну молекулу,
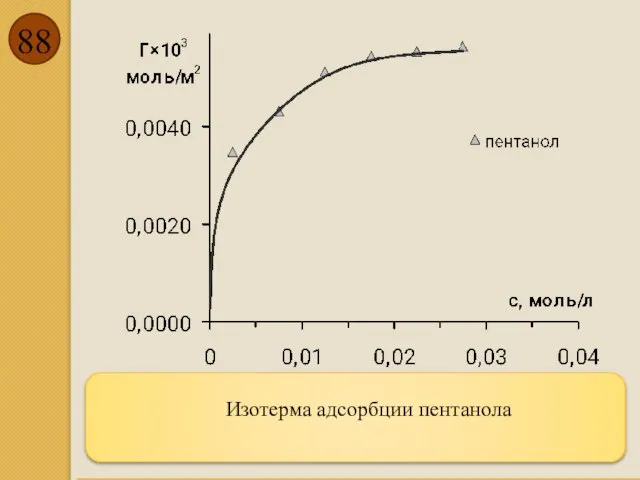
- 88. Изотерма адсорбции пентанола
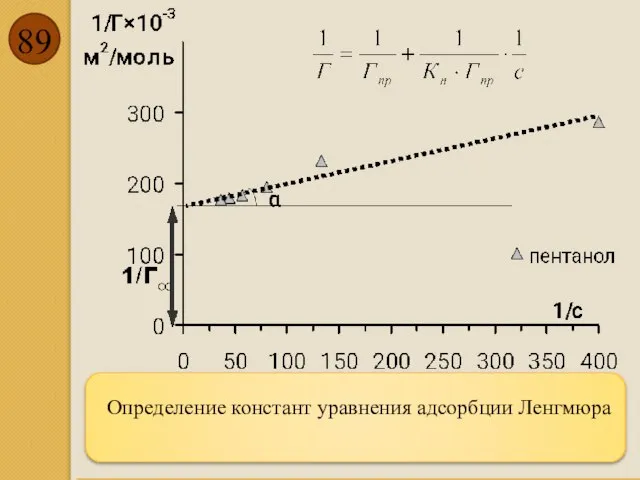
- 89. Определение констант уравнения адсорбции Ленгмюра
- 90. Определив величину Гпр, можно рассчитать площадь S0 (м2), приходящуюся на одну молекулу ПАВ в монослое: Здесь
- 91. Поверхностно-активными веществами (ПАВ) называют вещества, понижающие поверхностное натяжение воды или других растворителей. Молекулы ПАВ имеют дифильную
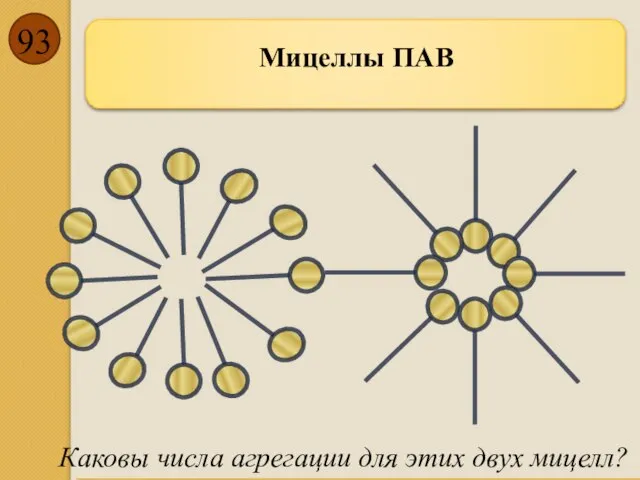
- 92. Мицеллы ПАВ По мере увеличения концентрации ПАВ в растворе число свободных мест на границе раздела вода–воздух
- 93. Мицеллы ПАВ Каковы числа агрегации для этих двух мицелл?
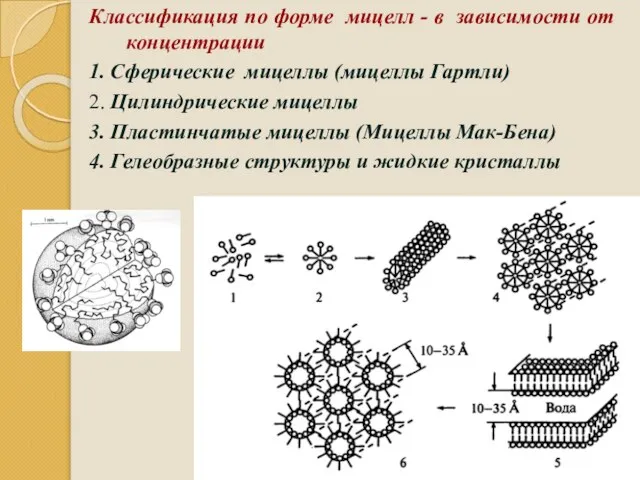
- 94. Классификация по форме мицелл - в зависимости от концентрации 1. Сферические мицеллы (мицеллы Гартли) 2. Цилиндрические
- 95. Формы мицелл
- 96. Критическая концентрация мицелообразования (ККМ) - концентрация ПАВ, при которой в растворе овначинают образываться мицеллы. Критическая концентрация
- 97. Обратное правило Траубе. ККМ прямых мицелл в пределах одного гомологического ряда экспоненциально уменьшается по мере удлинения
- 98. Методы определения По изменению поверхностного натяжения Оптической плотности Молярной электропроводности Моющей способности Осмотическому давлению
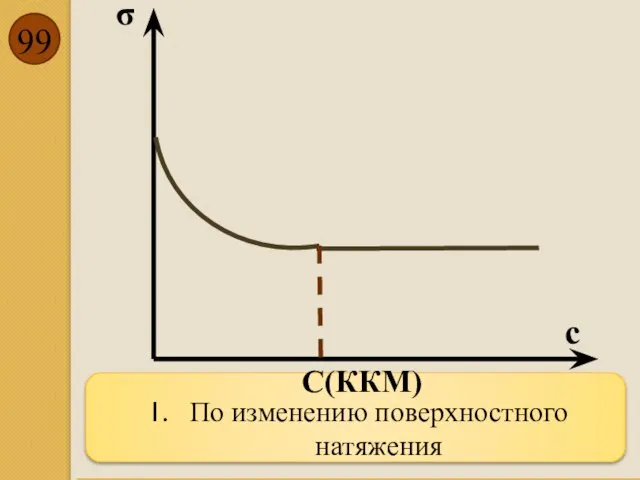
- 99. По изменению поверхностного натяжения σ с С(ККМ)
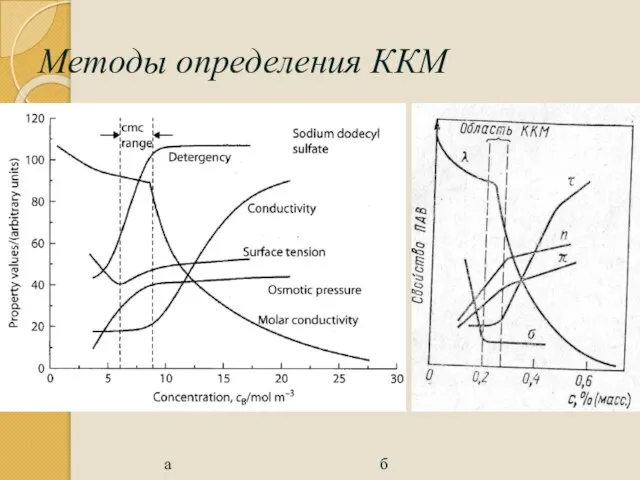
- 100. Методы определения ККМ а б
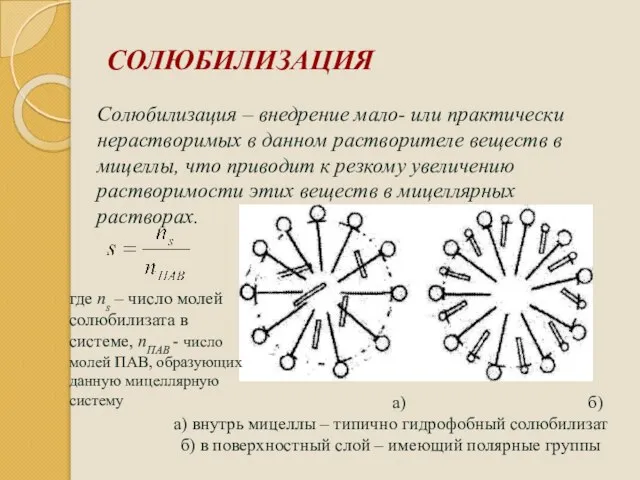
- 101. СОЛЮБИЛИЗАЦИЯ Солюбилизация – внедрение мало- или практически нерастворимых в данном растворителе веществ в мицеллы, что приводит
- 102. ОБРАЗОВАНИЕ И СТРУКТУРА ДЭС. ЗОЛИ. КОАГУЛЯЦИЯ ЗОЛЕЙ.
- 103. Механизмы образования ДЭС 1) Поверхностная ионизация – механизм, при котором ДЭС образуется в результате перехода электронов
- 104. Механизм образования двойного электрического слоя зависит от соотношения химических потенциалов иона в жидкости и твердой фазе
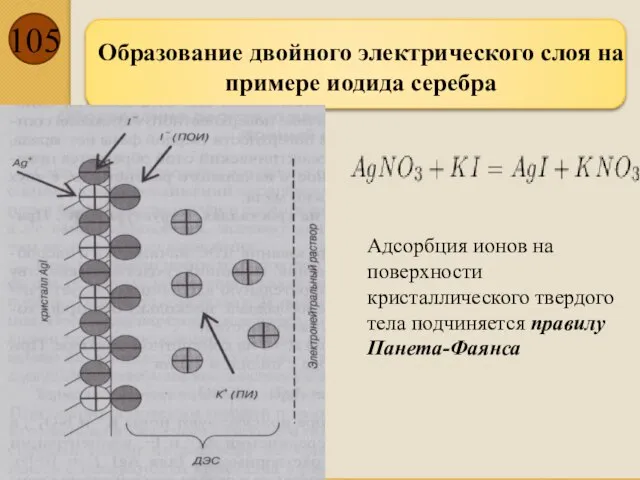
- 105. Образование двойного электрического слоя на примере иодида серебра Адсорбция ионов на поверхности кристаллического твердого тела подчиняется
- 106. - высокодисперсная коллоидная система (коллоидный раствор) с жидкой (лиозоль) или газообразной (аэрозоль) дисперсионной средой, в объеме
- 107. Мицеллы золей на примере йодида серебра AgNO3+KI(изб)→AgI↓+KNO3 {m[АgI] nI-(n-х)К+}х-хК+ Согласно правилу Фаянса на агрегате адсорбируются те
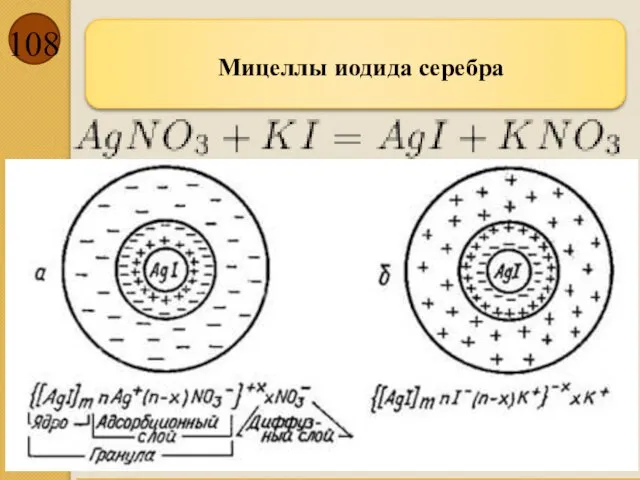
- 108. Мицеллы иодида серебра
- 109. Потенциалы ДЭС ДЭС в целом электронейтрален, поскольку сумма зарядов противоионов равна заряду твердой поверхности. φ-потенциал или
- 110. ζ-потенциал - электрический потенциал в ДЭС на границе между частицей, способной к движению в электрическом поле
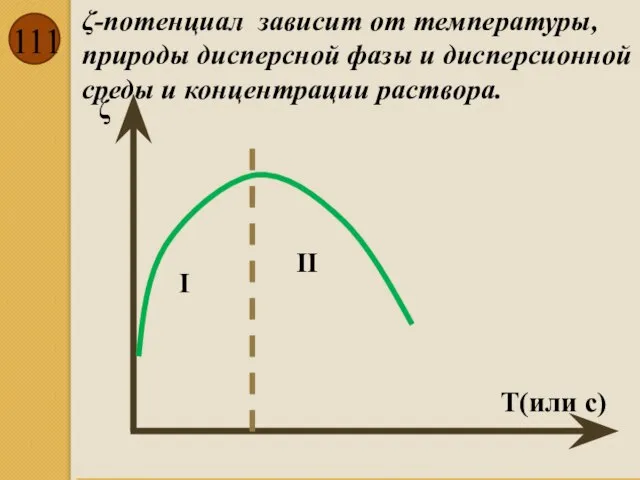
- 111. ζ-потенциал зависит от температуры, природы дисперсной фазы и дисперсионной среды и концентрации раствора. ζ T(или c)
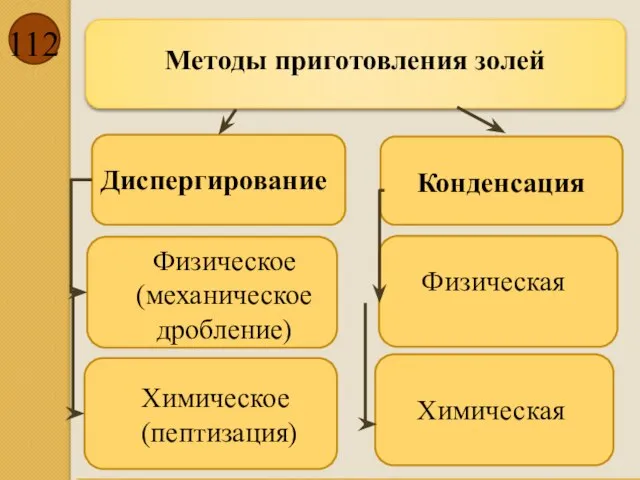
- 112. Методы приготовления золей Диспергирование Конденсация Физическое (механическое дробление) Химическое (пептизация) Физическая Химическая
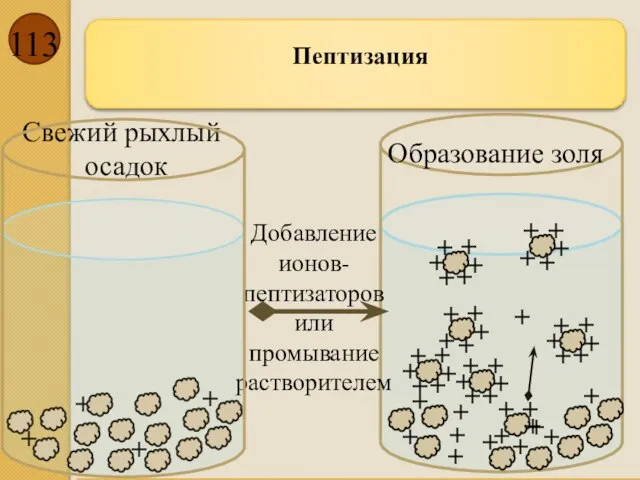
- 113. + + + + + + + Добавление ионов-пептизаторов или промывание растворителем Пептизация Свежий рыхлый осадок
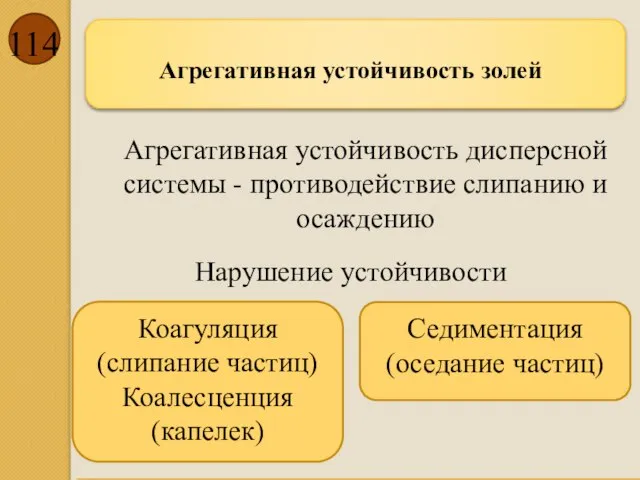
- 114. Агрегативная устойчивость золей Агрегативная устойчивость дисперсной системы - противодействие слипанию и осаждению Коагуляция (слипание частиц) Коалесценция
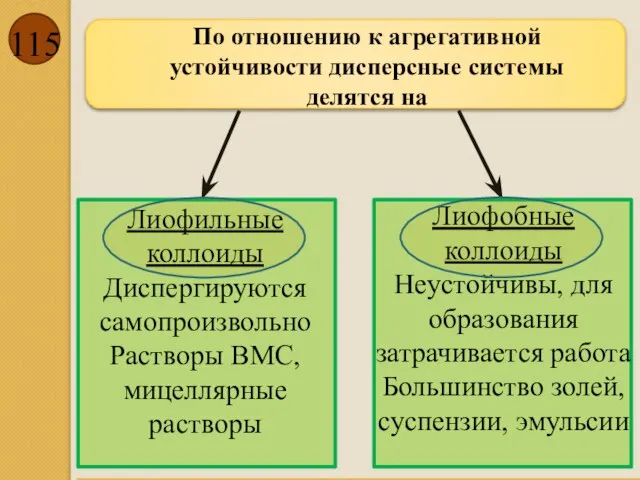
- 115. По отношению к агрегативной устойчивости дисперсные системы делятся на Лиофильные коллоиды Диспергируются самопроизвольно Растворы ВМС, мицеллярные
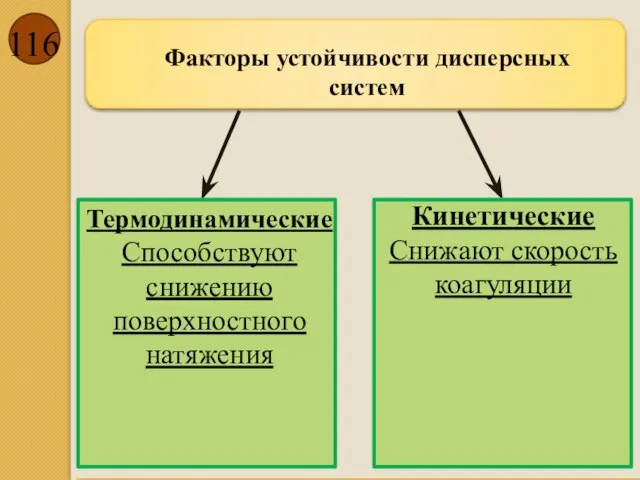
- 116. Факторы устойчивости дисперсных систем Термодинамические Способствуют снижению поверхностного натяжения Кинетические Снижают скорость коагуляции
- 117. Термодинамические Электростатический – создание электростатических сил отталкивания (φ, ζ) Адсорбционно-сольватный Энтропийный (при наличии броуновского движения) способствует
- 118. Кинетические Структурно-механический(и ДЭС, и адсорбционно-сольватные слои, и адсорбированные ПАВ) Гидродинамический - изменение вязкости, плотности д. фазы
- 119. Электролиты Индиффирентные – взаимодействуют с поверхностью только за счет электростатического притяжения, влияют только на ζ-потенциал Неиндифферентные
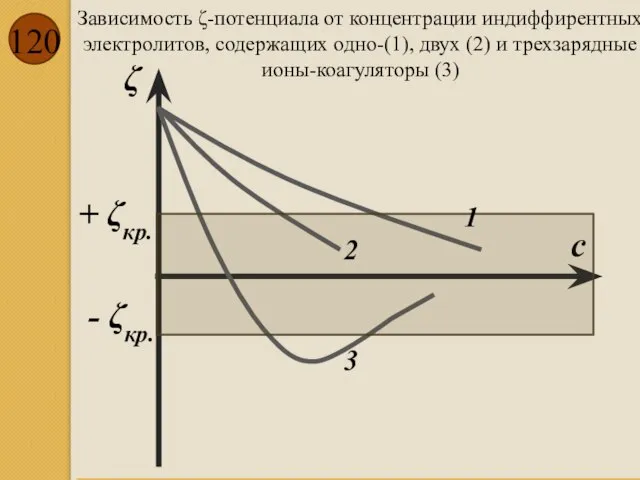
- 120. Зависимость ζ-потенциала от концентрации индиффирентных электролитов, содержащих одно-(1), двух (2) и трехзарядные ионы-коагуляторы (3) + ζкр.
- 121. Коагуляция Добавление электролитов с противоионами (ионами, заряд которых противоположен заряду коллоидной частицы), уменьшает отталкивание между коллоидными
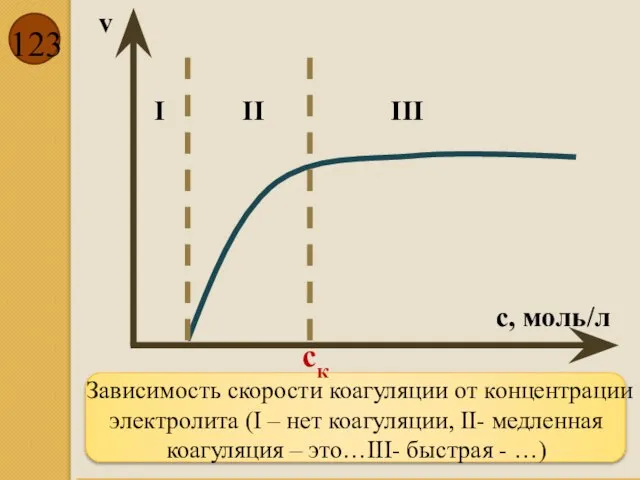
- 122. Порог коагуляции - минимальная концентрация электролита ск (моль/л), вызывающую быструю коагуляцию. Величину 1/ск (л/моль), обратную порогу
- 123. Зависимость скорости коагуляции от концентрации электролита (I – нет коагуляции, II- медленная коагуляция – это…III- быстрая
- 124. Эффект Тиндаля (сравнение истинного раствора и золя)
- 125. Написать мицеллу золя 2KMnO4(изб.)+2NH3·H2O→2MnO2↓ +2KOH+N2+4H2O 2KMnO4+6Na2S2O3(изб.)+4H2O→2MnO2↓+3Na2S4O6+2KOH+6NaOH FeCl3+ K4[Fe(CN)6] (изб.)→ KFe[Fe(CN)6]↓+ 3KCl FeCl3(изб.)+ K4[Fe(CN)6] → KFe[Fe(CN)6]↓+ 3KCl
- 126. «Растворы ВМС»
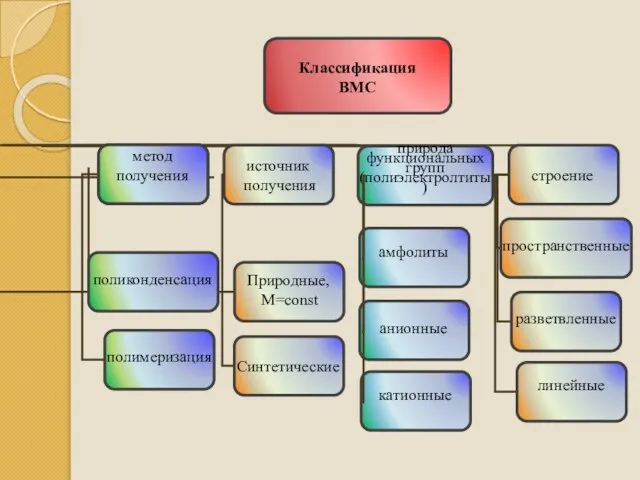
- 127. ВМС - Высокомолекулярные соединения, к которым относя соединения с молекулярной массой порядка 10000-1000000 и выше (для
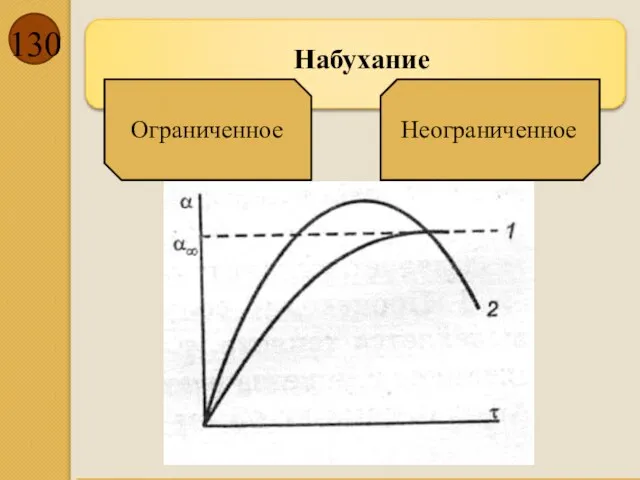
- 129. Набухание — процесс увеличения объёма твёрдого тела вследствие поглощения им из окружающей среды жидкости или пара.
- 130. Набухание Ограниченное Неограниченное
- 131. Изоэлектрическая точка ВМС NН2-СН2-СOOH NН3+-СН2-СOOH в кислой среде присоединяются протоны NН3+-СН2-СOO- - цвиттер-ионная форма (вблизи ИЭТ)
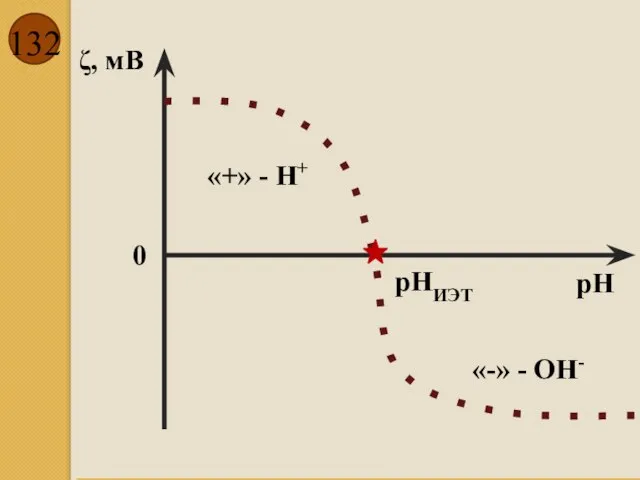
- 132. ζ, мВ рН рНИЭТ 0 «+» - Н+ «-» - ОН-
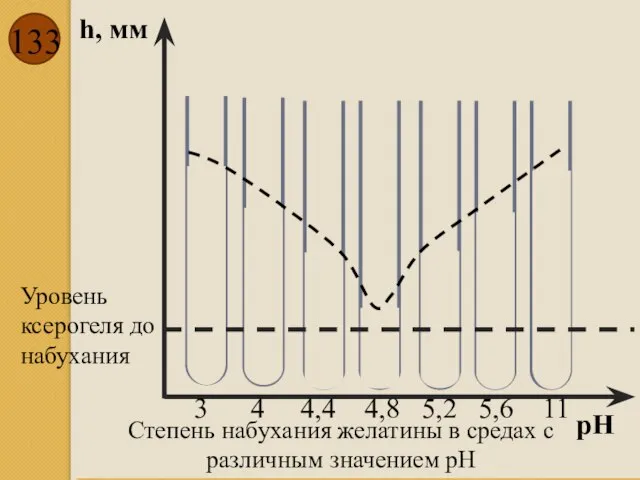
- 133. h, мм рН Степень набухания желатины в средах с различным значением рН Уровень ксерогеля до набухания
- 134. Вязкость
- 135. Измерить относительную вязкость растворов высокомолекулярных веществ (ВМВ) различной концентрации, графически определить характеристическую вязкость и рассчитать среднюю
- 136. Вязкостью η называют силу трения, приходящуюся на единицу площади границы S соприкасающихся слоев жидкости при условии,
- 137. Различают динамическую вязкость (единица измерения (СИ) — Па·с) и кинематическую вязкость (единица измерения в СИ —
- 138. Закон Пуазейля: где υ = V/t – объемная скорость течения жидкости, то есть объем жидкости, протекающий
- 139. Жидкости, течение которых подчиняется закону Пуазейля, называют нормально вязкими, или ньютоновскими. Вязкость ньютоновской жидкости постоянна и
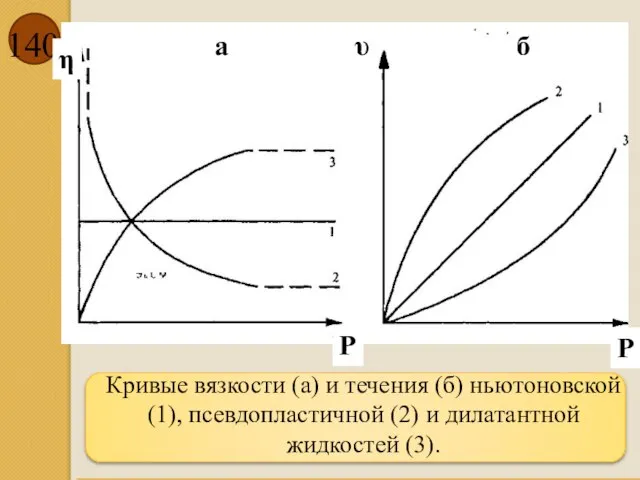
- 140. Кривые вязкости (а) и течения (б) ньютоновской (1), псевдопластичной (2) и дилатантной жидкостей (3). η τ
- 141. Вязкость ликвора, лимфы и плазмы крови достаточно точно описывается ньютоновским законом вязкого течения, она исследуется в
- 142. Вязкость разбавленных систем описывается уравнением Эйнштейна: η = η0 (1+αφ) – α=2,5 для сферических частиц; α=2–
- 143. Кроме вязкости η для оценки реологических свойств растворов используют относительную вязкость ηотн и характеристическую вязкость [η].
- 144. рассчитать приведенную вязкость ηприв: Построить график зависимости приведенной вязкости от концентрации и графически определить характеристическую вязкость
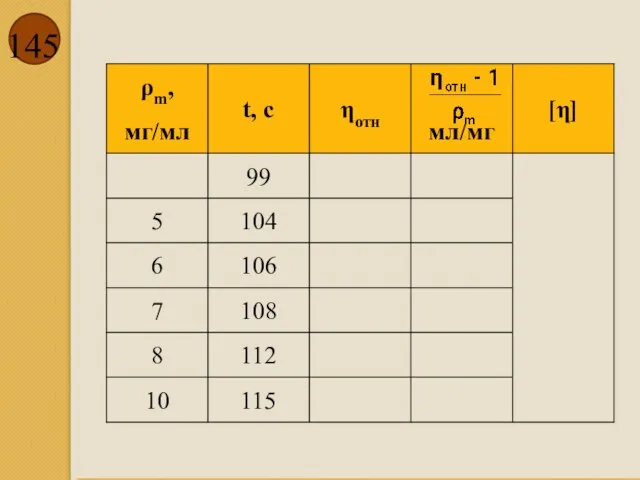
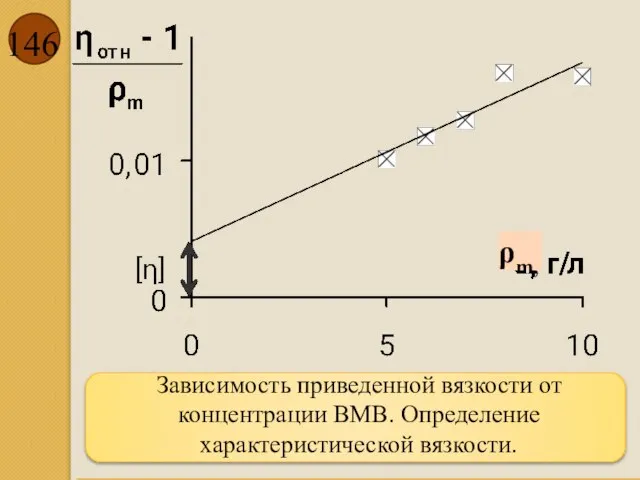
- 146. Зависимость приведенной вязкости от концентрации ВМВ. Определение характеристической вязкости. ρm,
- 148. Скачать презентацию







































































![Мицеллы золей на примере йодида серебра AgNO3+KI(изб)→AgI↓+KNO3 {m[АgI] nI-(n-х)К+}х-хК+ Согласно правилу](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/552106/slide-106.jpg)








![Написать мицеллу золя 2KMnO4(изб.)+2NH3·H2O→2MnO2↓ +2KOH+N2+4H2O 2KMnO4+6Na2S2O3(изб.)+4H2O→2MnO2↓+3Na2S4O6+2KOH+6NaOH FeCl3+ K4[Fe(CN)6] (изб.)→ KFe[Fe(CN)6]↓+ 3KCl](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/552106/slide-124.jpg)














 Коливальний рух у природі і техніці
Коливальний рух у природі і техніці Энергияның негізгі көздері, электрстанцияларының сипаттамасы
Энергияның негізгі көздері, электрстанцияларының сипаттамасы Команда «По» представляет: Закон сохранения импульса. Реактивное движение
Команда «По» представляет: Закон сохранения импульса. Реактивное движение Последовательное соединение проводников
Последовательное соединение проводников Построение эпюр внутренних сил, напряжений и деформаций растяжения-сжатия
Построение эпюр внутренних сил, напряжений и деформаций растяжения-сжатия Резонанс. Колебание
Резонанс. Колебание Измерение параметров, характеризующих светопропускание (светопоглощение) оптических материалов
Измерение параметров, характеризующих светопропускание (светопоглощение) оптических материалов Материалы авиакосмической техники
Материалы авиакосмической техники Презентация по физике "Основы термодинамики" - скачать
Презентация по физике "Основы термодинамики" - скачать  Приборы для измерения температуры
Приборы для измерения температуры Теория горения горючих дисперсных материалов Лекция 7 по теории горения и взрыва для гр. ДБЖ-09
Теория горения горючих дисперсных материалов Лекция 7 по теории горения и взрыва для гр. ДБЖ-09 Устройство машинной иглы. Неполадки
Устройство машинной иглы. Неполадки Методика изучения свойств вещества в курсе физики в системе среднего образования при реализации ФГОС
Методика изучения свойств вещества в курсе физики в системе среднего образования при реализации ФГОС Фазовые переходы
Фазовые переходы Математичний маятник. Коливання тіла на пружині
Математичний маятник. Коливання тіла на пружині Телескопы: линзовые, зеркальные, зеркально-линзовые
Телескопы: линзовые, зеркальные, зеркально-линзовые Оптические методы количественного анализа
Оптические методы количественного анализа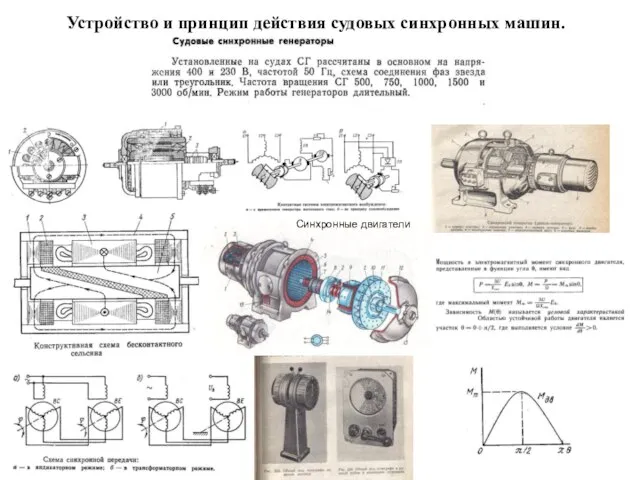 Устройство и принцип действия судовых синхронных машин. Синхронные двигатели. (Билет 14)
Устройство и принцип действия судовых синхронных машин. Синхронные двигатели. (Билет 14)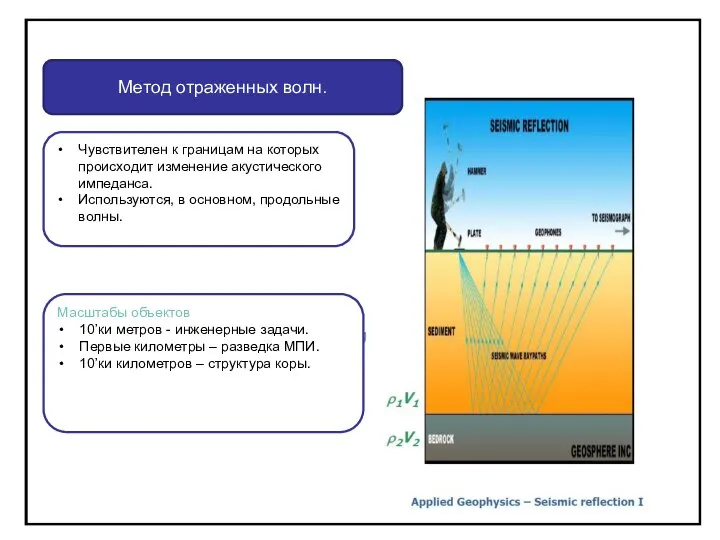 Выборка ОПВ. Прямая волна. Отраженные волны. Поверхностная волна
Выборка ОПВ. Прямая волна. Отраженные волны. Поверхностная волна Лекция 3. Возможные случаи приведения к равнодействующей сил произвольно расположенных в пространстве
Лекция 3. Возможные случаи приведения к равнодействующей сил произвольно расположенных в пространстве Фізика Взаємодії та сили підготувала
Фізика Взаємодії та сили підготувала  Объяснение явлений
Объяснение явлений Вечный двигатель
Вечный двигатель Классификация лазеров
Классификация лазеров Classic tractor parts defination. Lesson 3
Classic tractor parts defination. Lesson 3 Колебательный контур. Электромагнитные колебания
Колебательный контур. Электромагнитные колебания Испарение и конденсация. Эксперимент
Испарение и конденсация. Эксперимент Тема урока: Постоянные магниты.
Тема урока: Постоянные магниты.