Содержание
- 2. СТРОЕНИЕ МНОГОЭЛЕКТРОННЫХ АТОМОВ. ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ Д.И.МЕНДЕЛЕЕВА ОПТИЧЕСКИЕ СПЕКТРЫ. РЕЗУЛЬТИРУЮЩИЙ МОМЕНТ МНОГОЭЛЕКТРОННОГО АТОМА РЕНТГЕНОВСКИЕ СПЕКТРЫ. ЗАКОН
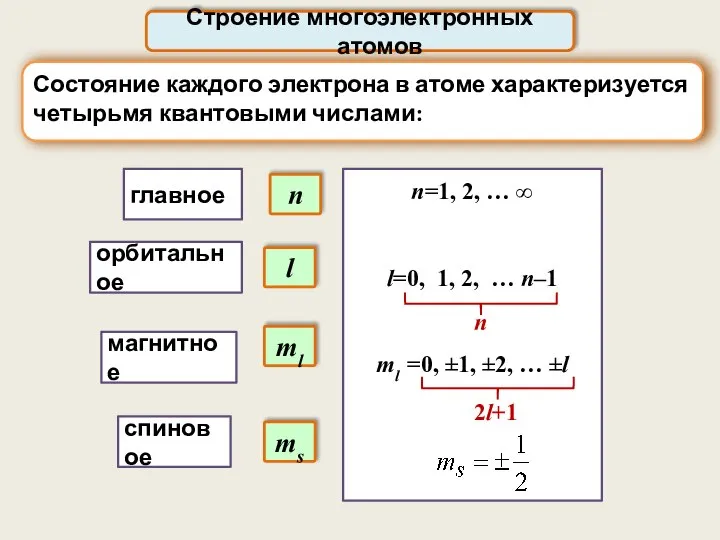
- 3. Строение многоэлектронных атомов n=1, 2, … ∞ l=0, 1, 2, … n–1 ml =0, ±1, ±2,
- 4. В атоме водорода энергия электрона: - зависит от n - слабо зависит от ms - не
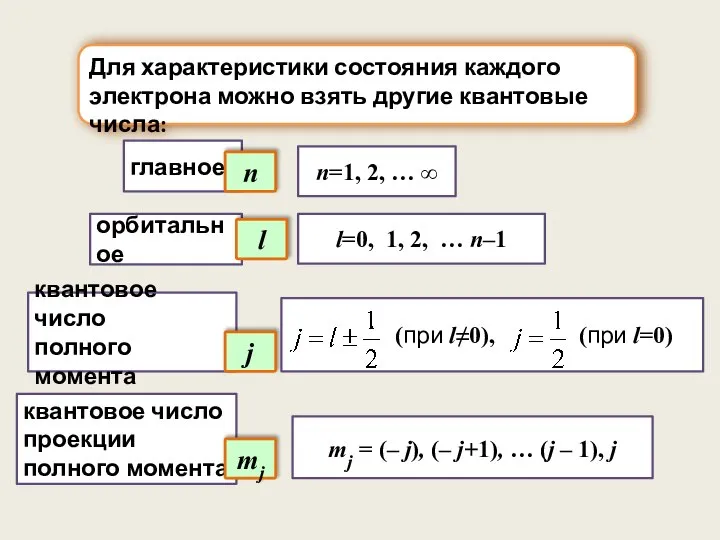
- 5. mj = (– j), (– j+1), … (j – 1), j Для характеристики состояния каждого электрона
- 6. В многоэлектронных атомах состояние каждого электрона определяется теми же квантовыми числами, что и в атоме водорода,
- 7. В одном атоме не может быть двух и более электронов, находящихся в одинаковом стационарном состоянии, то
- 8. Почти всегда: Состояние с большим n обладает большей энергией В нормальном (невозбуждённом) состоянии атома электроны располагаются
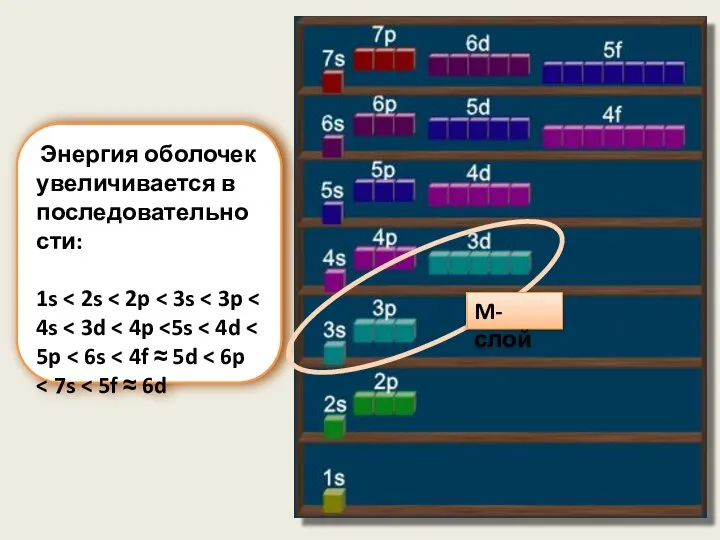
- 9. Энергия оболочек увеличивается в последовательности: 1s M-слой
- 10. Водород 1s Гелий 1s2 K-слой Заполняется K-слой: Водород; электронная конфигурация 1s Гелий; электронная конфигурация 1s2
- 11. Заполняется L-слой; n=2: Литий; три электрона; электронная конфигурация 1s22s Третий электрон слабее связан с ядром Он
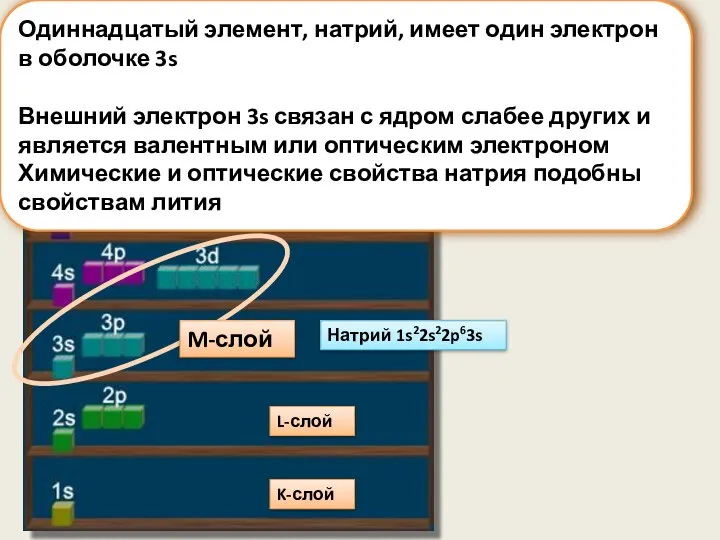
- 12. Одиннадцатый элемент, натрий, имеет один электрон в оболочке 3s Внешний электрон 3s связан с ядром слабее
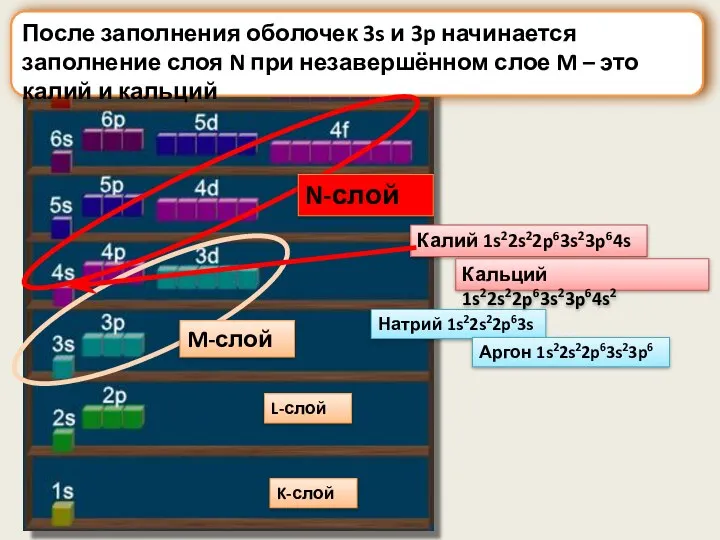
- 13. M-слой После заполнения оболочек 3s и 3p начинается заполнение слоя N при незавершённом слое M –
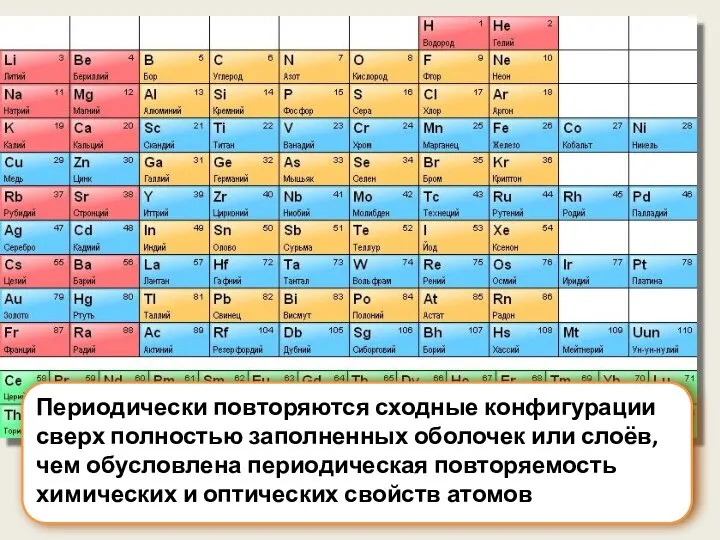
- 14. Периодически повторяются сходные конфигурации сверх полностью заполненных оболочек или слоёв, чем обусловлена периодическая повторяемость химических и
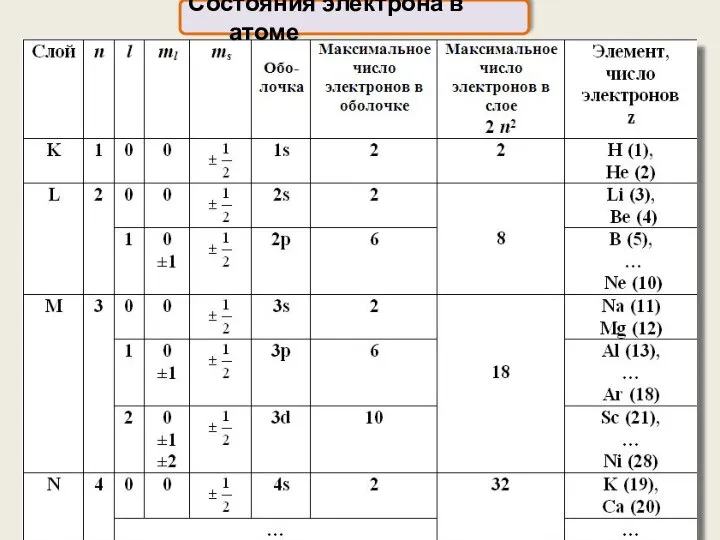
- 15. Состояния электрона в атоме
- 16. Каждый электрон в атоме обладает орбитальным моментом импульса и собственным (спиновым) моментом Механические моменты связаны с
- 17. Все орбитальные моменты электронов атома складываются в результирующий момент Спиновые моменты электронов складываются в результирующий спиновый
- 18. Квантование моментов: L – орбитальное квантовое число атома S – спиновое квантовое число атома J –
- 19. Квантовое число L атома может иметь значения: L = l1+l2, l1+l2–1, l1+l2–2, … |l1– l2| где
- 20. Проекции тоже квантуются: проекция результирующего орбитального момента на некоторое направление Z : mL= – L, –
- 21. С механическими моментами связаны магнитные моменты, которые взаимодействуют между собой Поэтому энергия атома зависит от взаимной
- 22. Если внутренние оболочки атома полностью заполнены, нужно учитывать только внешние, валентные (оптические) электроны Результирующий момент многоэлектронного
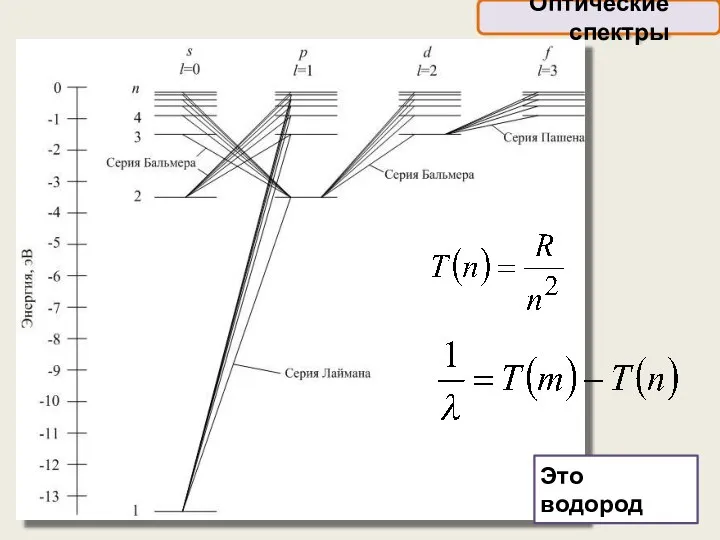
- 23. Оптические спектры, возникающие при переходах слабее всего связанных с ядром оптических (валентных) электронов, лежат в видимой
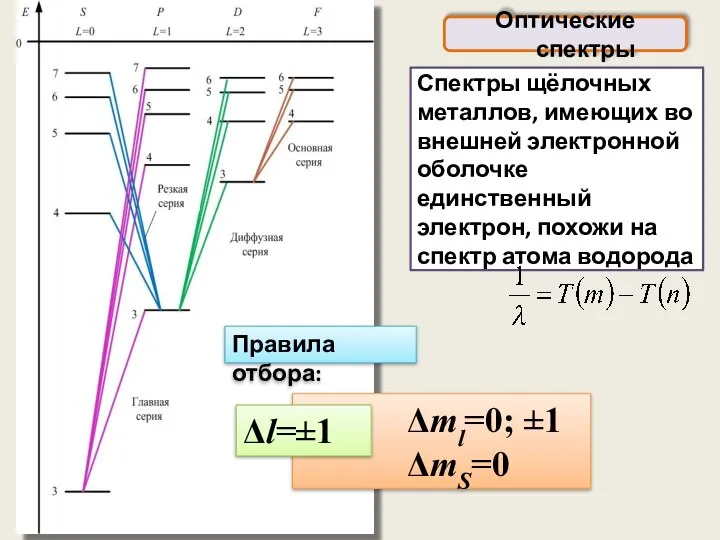
- 24. Оптические спектры Спектры щёлочных металлов, имеющих во внешней электронной оболочке единственный электрон, похожи на спектр атома
- 25. Это водород Оптические спектры
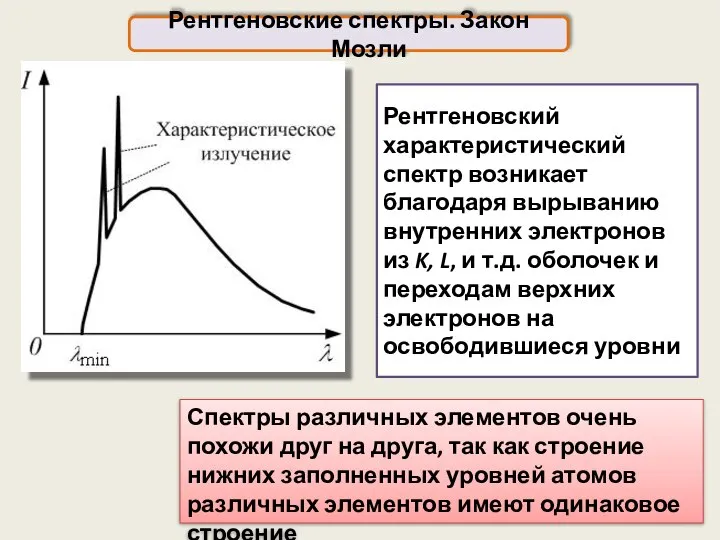
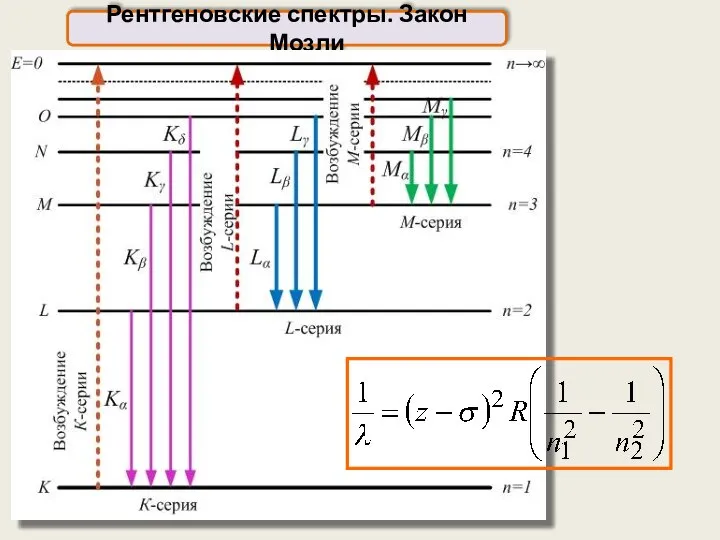
- 26. Рентгеновский характеристический спектр возникает благодаря вырыванию внутренних электронов из K, L, и т.д. оболочек и переходам
- 27. Рентгеновские спектры. Закон Мозли
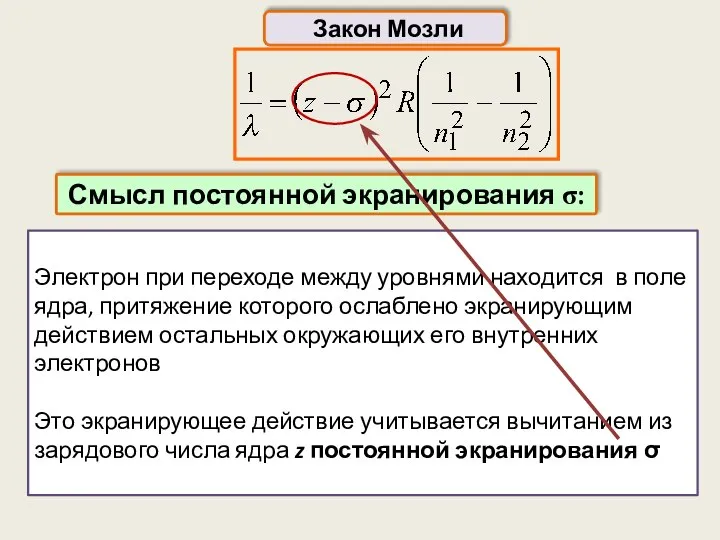
- 28. Электрон при переходе между уровнями находится в поле ядра, притяжение которого ослаблено экранирующим действием остальных окружающих
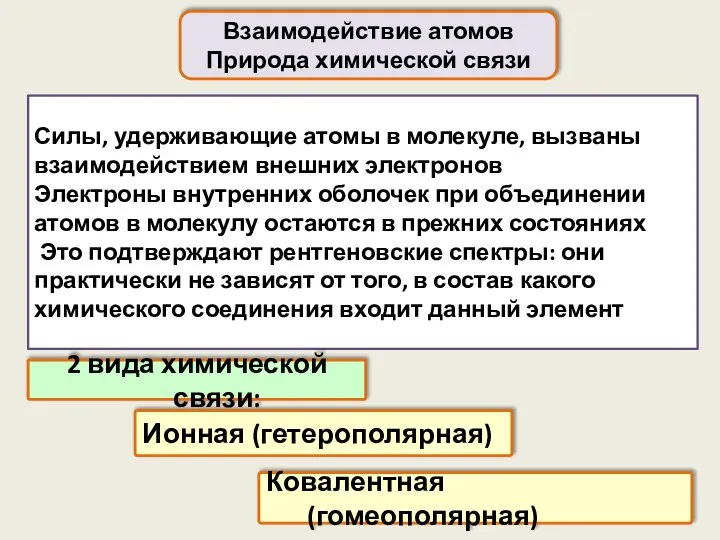
- 29. Силы, удерживающие атомы в молекуле, вызваны взаимодействием внешних электронов Электроны внутренних оболочек при объединении атомов в
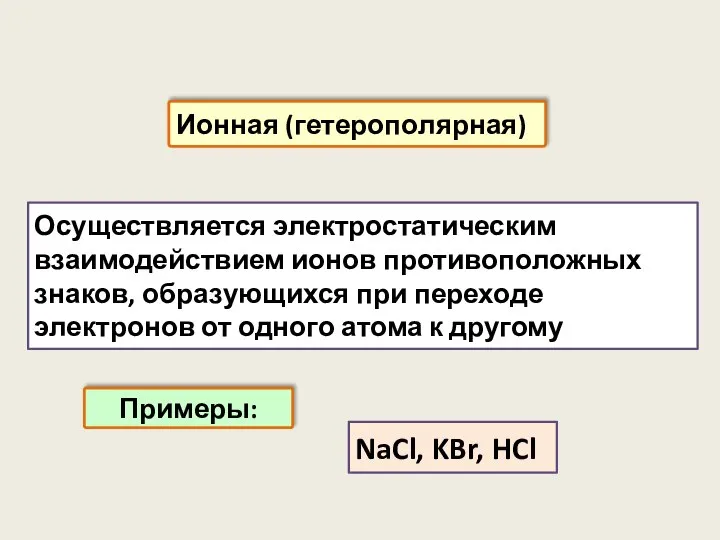
- 30. Осуществляется электростатическим взаимодействием ионов противоположных знаков, образующихся при переходе электронов от одного атома к другому Ионная
- 31. Образуется парами электронов с противоположными спинами Электроны, осуществляющие связь, значительную часть времени проводят в пространстве между
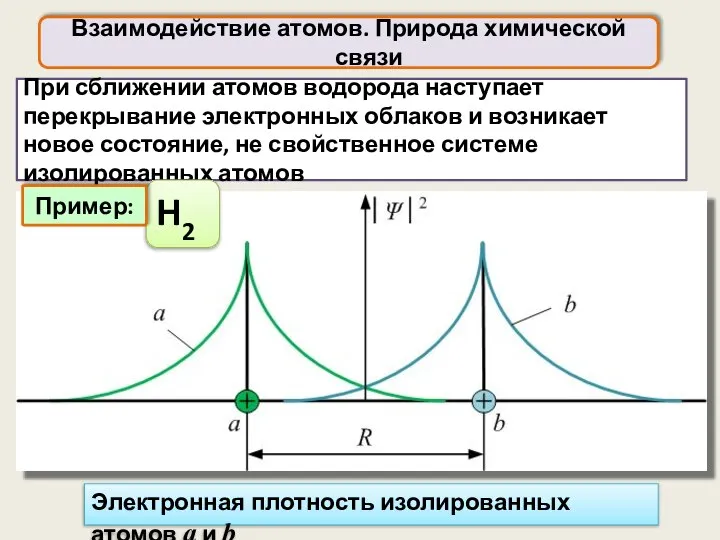
- 32. При сближении атомов водорода наступает перекрывание электронных облаков и возникает новое состояние, не свойственное системе изолированных
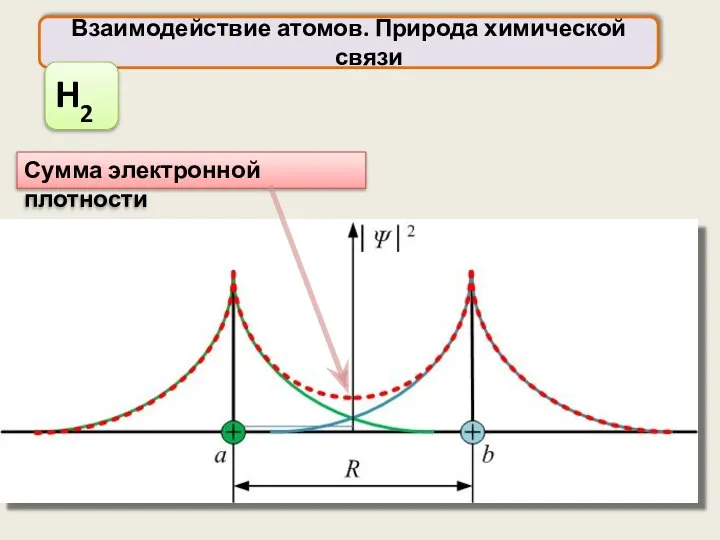
- 33. Взаимодействие атомов. Природа химической связи H2 Сумма электронной плотности
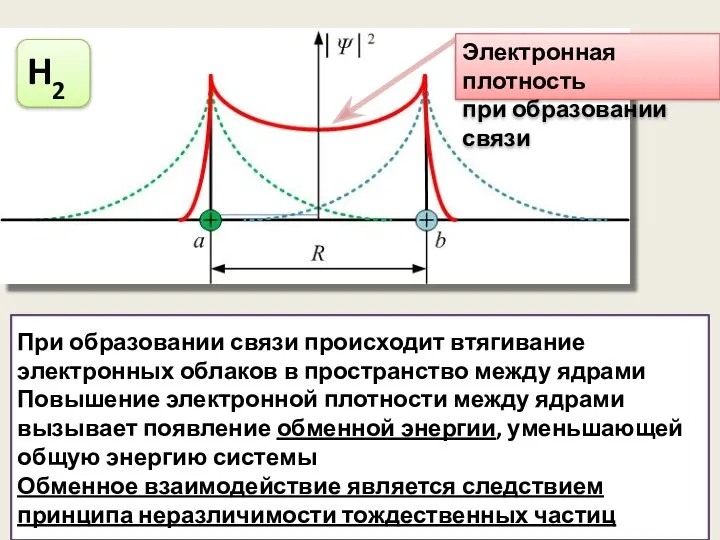
- 34. H2 Электронная плотность при образовании связи При образовании связи происходит втягивание электронных облаков в пространство между
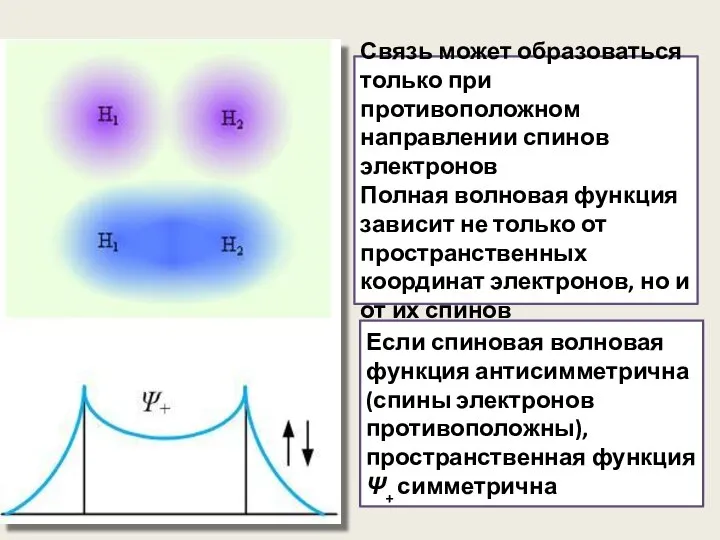
- 35. Связь может образоваться только при противоположном направлении спинов электронов Полная волновая функция зависит не только от
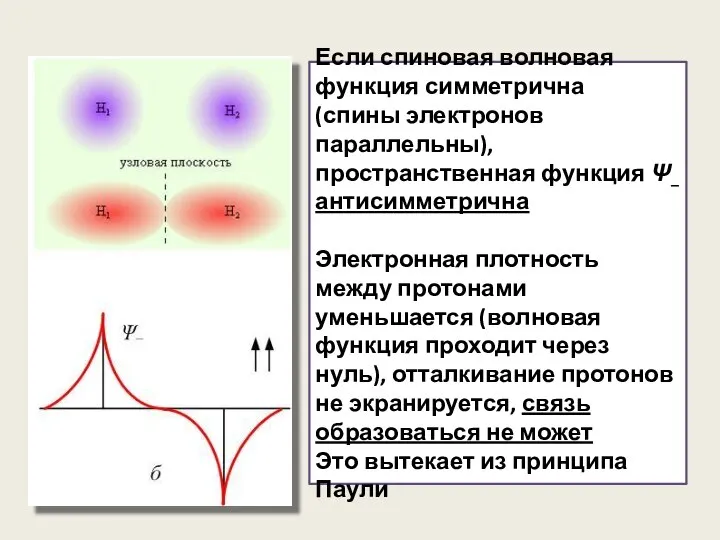
- 36. Если спиновая волновая функция симметрична (спины электронов параллельны), пространственная функция Ψ– антисимметрична Электронная плотность между протонами
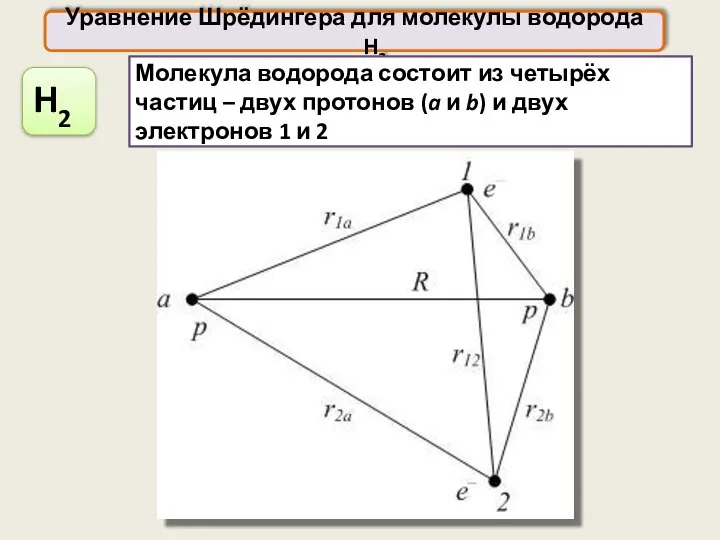
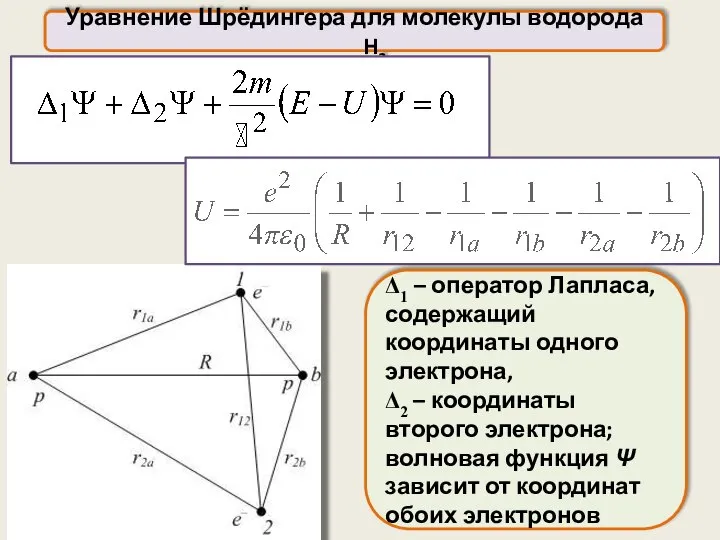
- 37. Уравнение Шрёдингера для молекулы водорода H2 Молекула водорода состоит из четырёх частиц – двух протонов (a
- 38. Уравнение Шрёдингера для молекулы водорода H2 Δ1 – оператор Лапласа, содержащий координаты одного электрона, Δ2 –
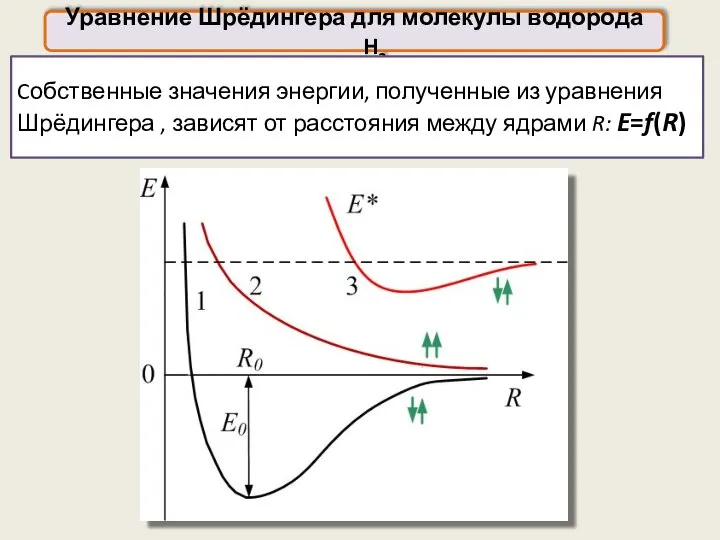
- 39. Уравнение Шрёдингера для молекулы водорода H2 Cобственные значения энергии, полученные из уравнения Шрёдингера , зависят от
- 40. Уравнение Шрёдингера для молекулы водорода H2 Адиабатическое приближение: электронное облако успевает «подстраиваться» под мгновенную конфигурацию ядер
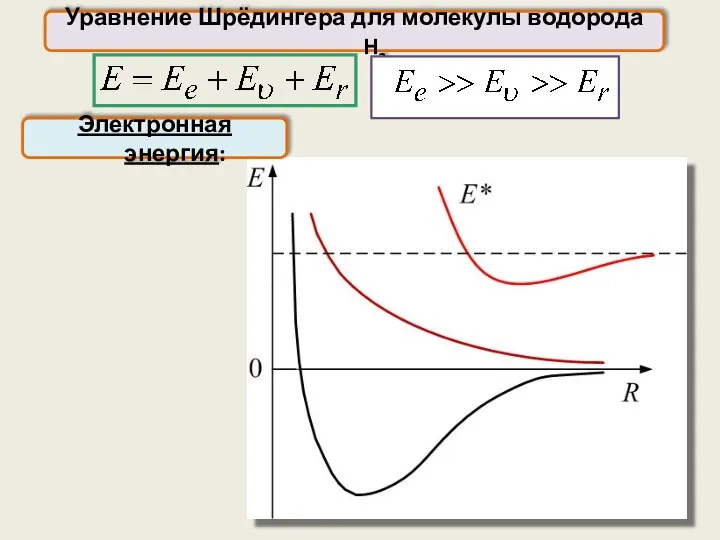
- 41. Уравнение Шрёдингера для молекулы водорода H2 Вращательная Колебательная Электронная Полная энергия: Волновая функция: Отдельные виды энергии
- 42. Уравнение Шрёдингера для молекулы водорода H2 Электронная энергия:
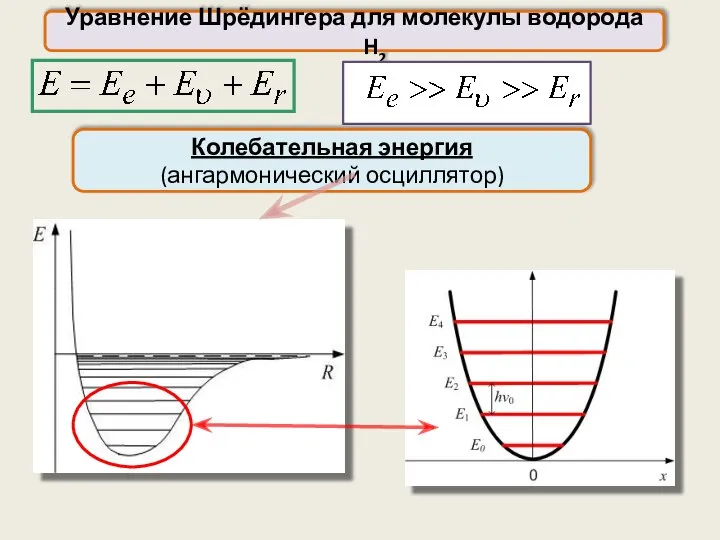
- 43. Уравнение Шрёдингера для молекулы водорода H2 υ=0, 1,2, …, Правило отбора: Колебательная энергия (в приближении гармонического
- 44. Уравнение Шрёдингера для молекулы водорода H2 Колебательная энергия (ангармонический осциллятор)
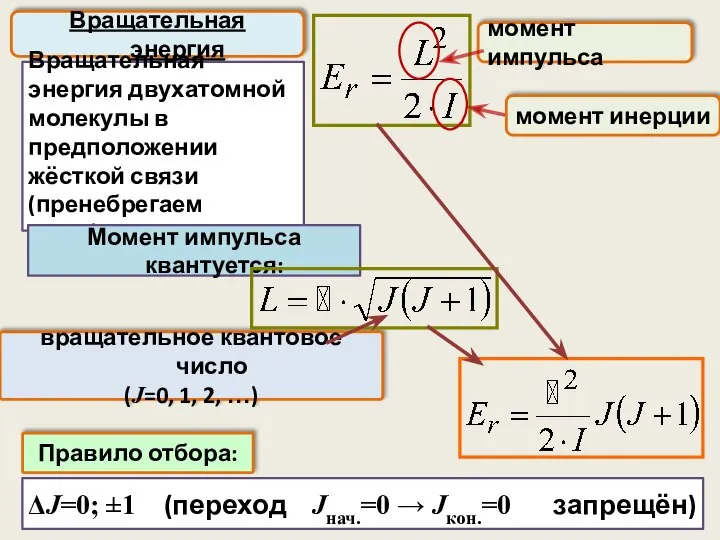
- 45. ΔJ=0; ±1 (переход Jнач.=0 → Jкон.=0 запрещён) Вращательная энергия Вращательная энергия двухатомной молекулы в предположении жёсткой
- 46. Система уровней энергии складывается из сравнительно далеко отстоящих электронных уровней, каждому из которых соответствует свой набор
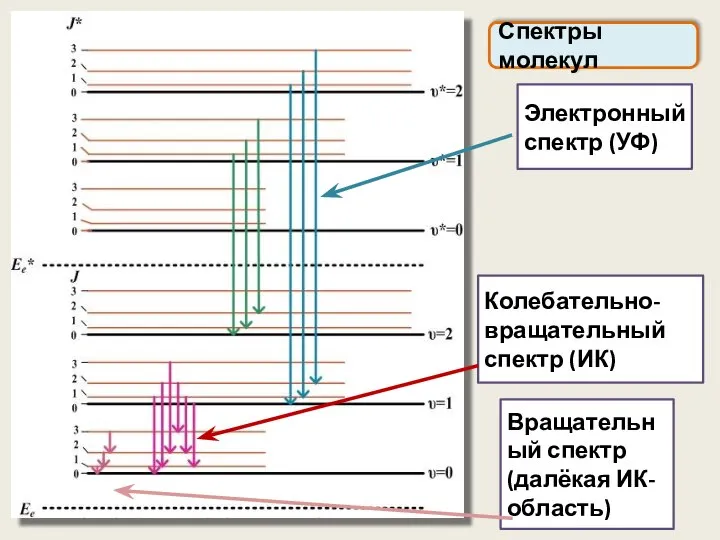
- 47. Спектры молекул Электронный спектр (УФ) Колебательно-вращательный спектр (ИК) Вращательный спектр (далёкая ИК-область)
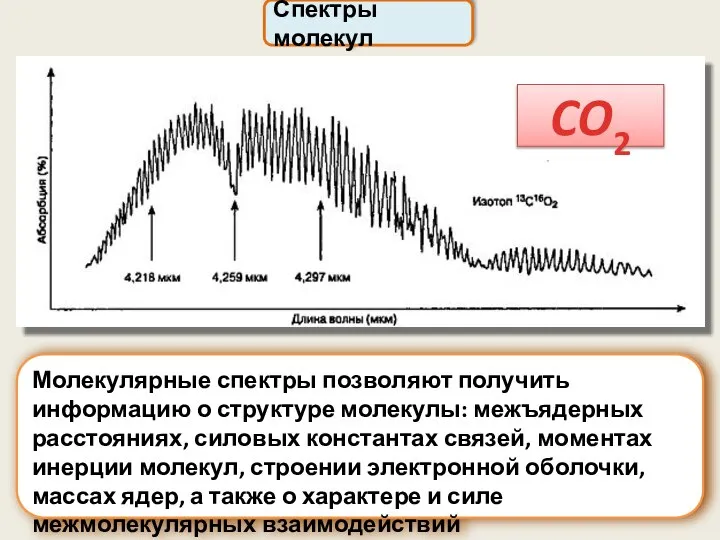
- 48. Спектры молекул Молекулярные спектры позволяют получить информацию о структуре молекулы: межъядерных расстояниях, силовых константах связей, моментах
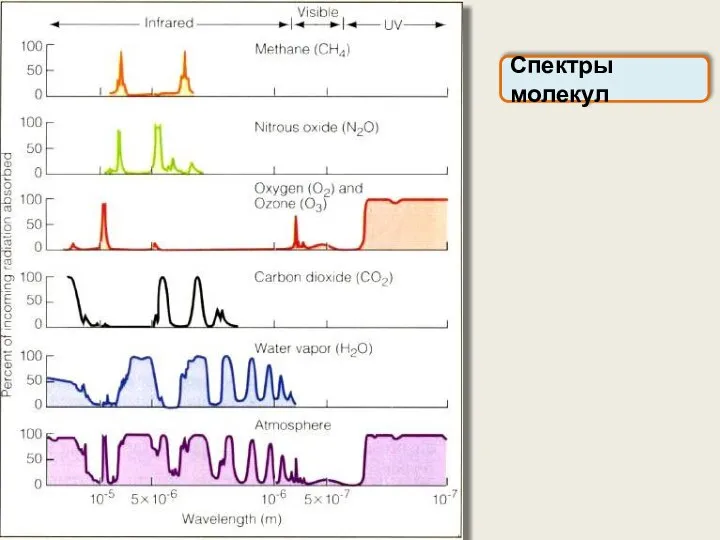
- 49. Спектры молекул
- 50. Правила отбора Если электрон переходит из стационарного состояния, описываемого волновой функцией ψn, в состояние, описываемое волновой
- 51. Правила отбора Если интеграл в выражении равен нулю, то переход n→m запрещён Так возникают правила отбора
- 52. Правила отбора Δl=±1 (орбитальное квантовое число) Δml=0; ±1 (магнитное квантовое число) ΔmS=0 (спиновое квантовое число) ΔL=0;
- 53. Правила отбора Δυ=±1 (колебательное квантовое число) ΔJ=0; ±1 (переход Jнач.=0 → Jкон.=0 запрещён) (вращательное квантовое число)
- 54. Правила отбора Замечания: Правила отбора вытекают из закона сохранения момента импульса: фотон имеет спин s=1, и
- 55. Спонтанное и индуцированное излучение Находясь в стационарном состоянии, электрон не излучает энергии С точки зрения квантовой
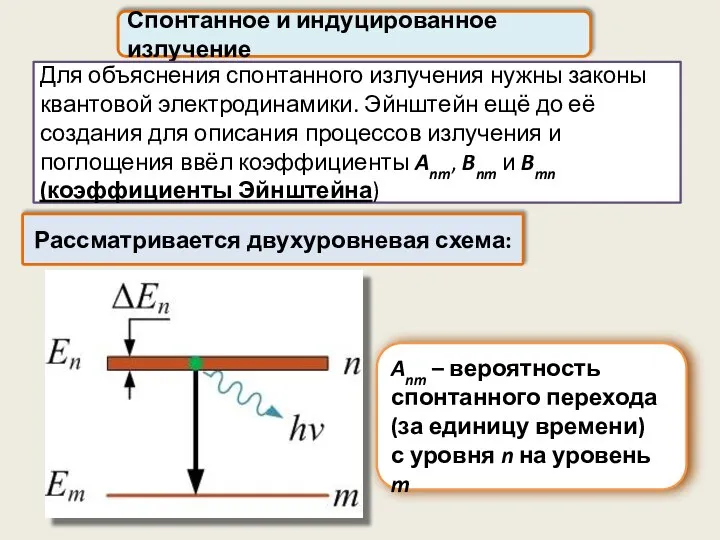
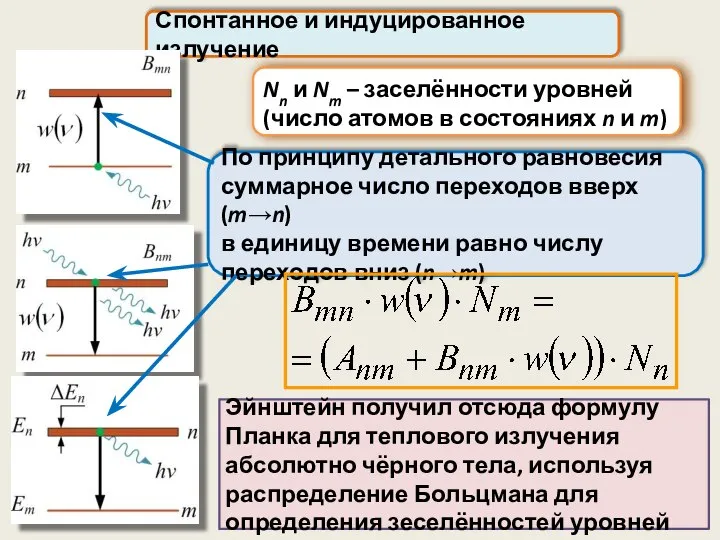
- 56. Спонтанное и индуцированное излучение Рассматривается двухуровневая схема: Для объяснения спонтанного излучения нужны законы квантовой электродинамики. Эйнштейн
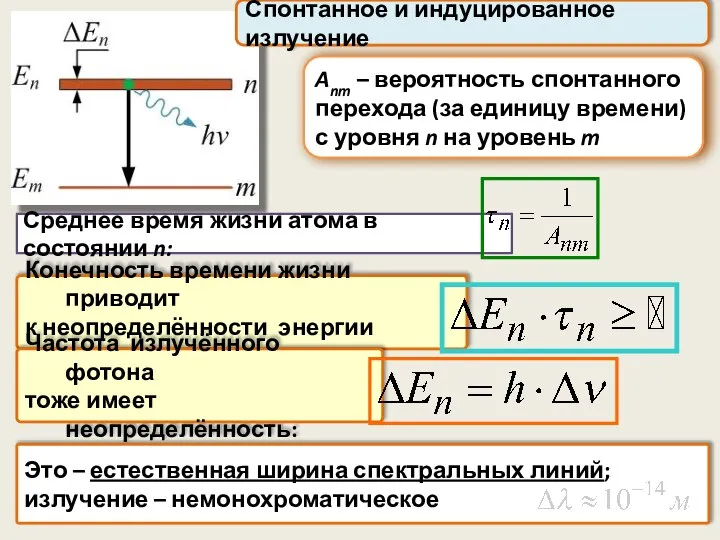
- 57. Anm – вероятность спонтанного перехода (за единицу времени) с уровня n на уровень m Среднее время
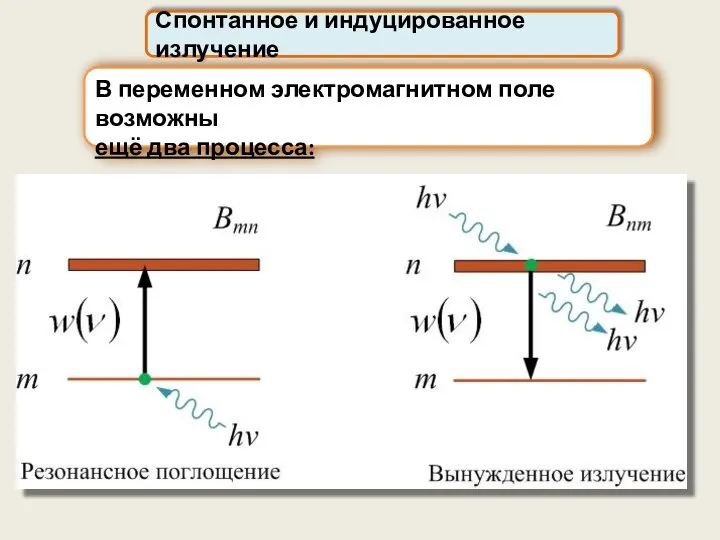
- 58. В переменном электромагнитном поле возможны ещё два процесса: Спонтанное и индуцированное излучение
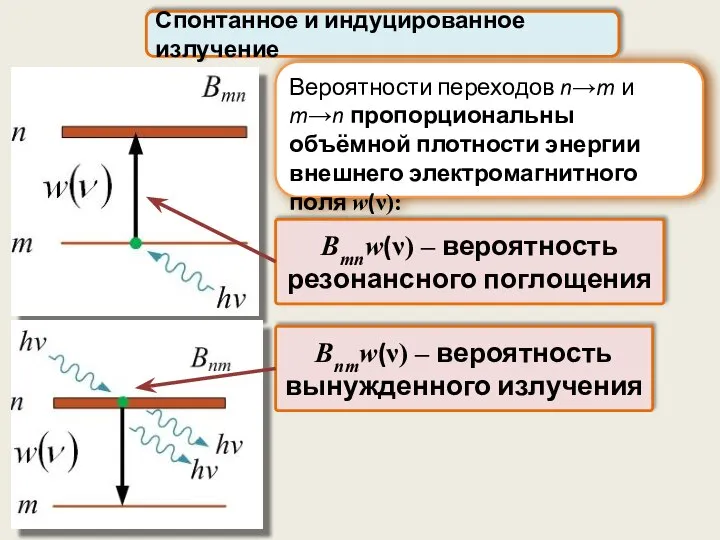
- 59. Вероятности переходов n→m и m→n пропорциональны объёмной плотности энергии внешнего электромагнитного поля w(ν): Спонтанное и индуцированное
- 60. Nn и Nm – заселённости уровней (число атомов в состояниях n и m) Спонтанное и индуцированное
- 61. частота: фаза направление распространения поляризация Вторичный фотон идентичен первичному У них одинаковы: Свойства индуцированного излучения Индуцированное
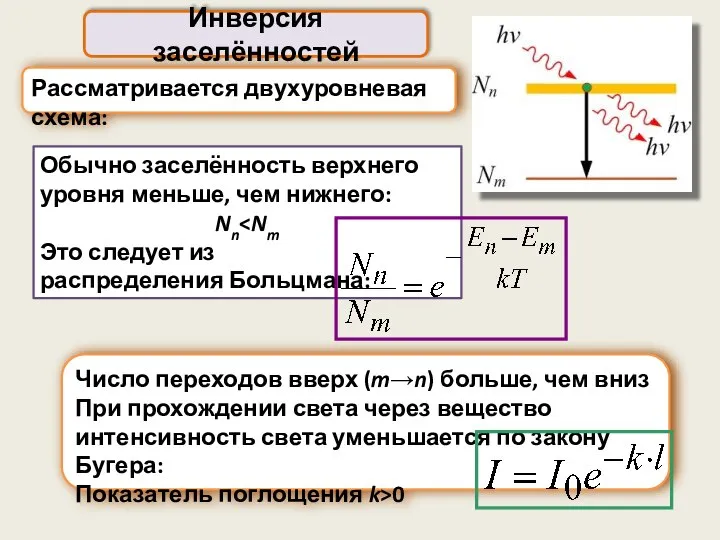
- 62. Рассматривается двухуровневая схема: Инверсия заселённостей Обычно заселённость верхнего уровня меньше, чем нижнего: Nn Это следует из
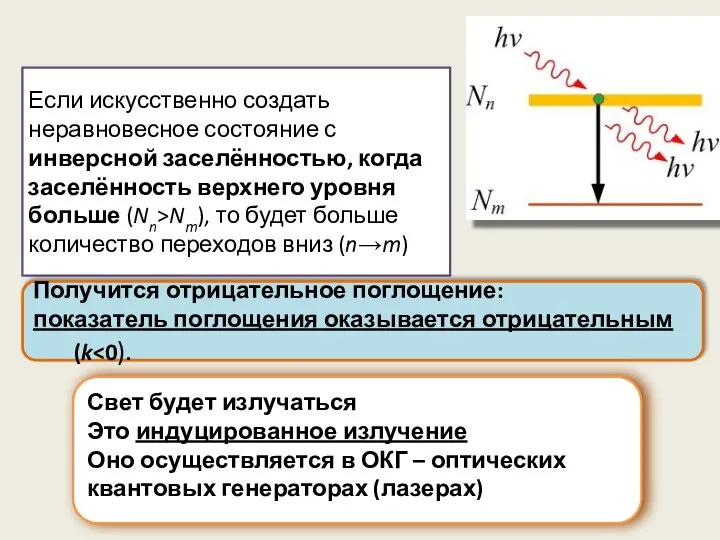
- 63. Если искусственно создать неравновесное состояние с инверсной заселённостью, когда заселённость верхнего уровня больше (Nn>Nm), то будет
- 64. Явление индуцированного излучения было предсказано Эйнштейном в 1917 году Первый оптический квантовый генератор был построен только
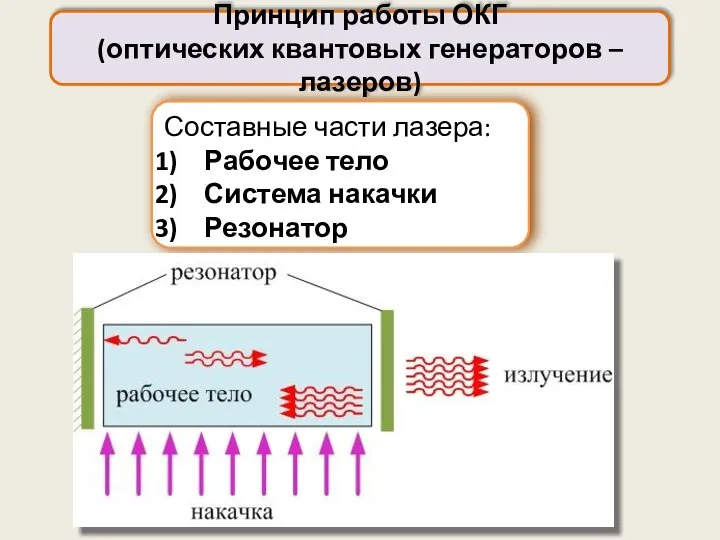
- 65. Составные части лазера: Рабочее тело Система накачки Резонатор Принцип работы ОКГ (оптических квантовых генераторов – лазеров)
- 66. Рабочее тело – активная среда с инверсной заселённостью: газы (чистые или смеси), жидкости (растворы красителей в
- 67. Система накачки – устройство для создания инверсии заселённостей Это может быть: обычная газоразрядная лампа (оптическая накачка
- 68. Система накачки 2
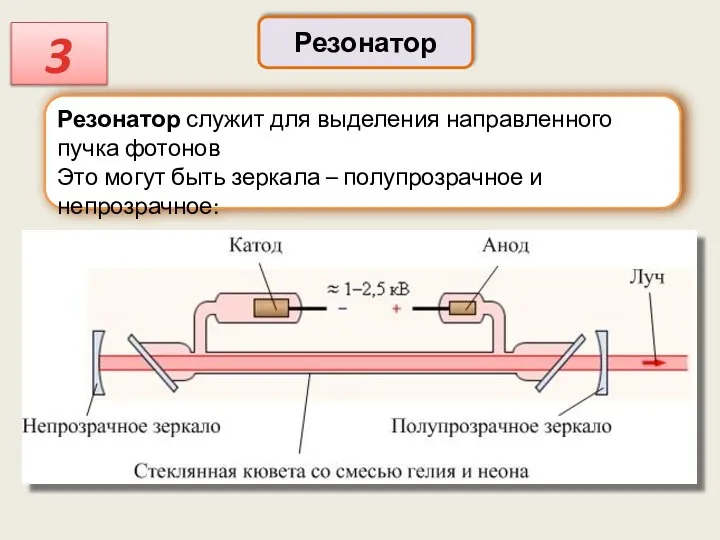
- 69. Резонатор 3 Резонатор служит для выделения направленного пучка фотонов Это могут быть зеркала – полупрозрачное и
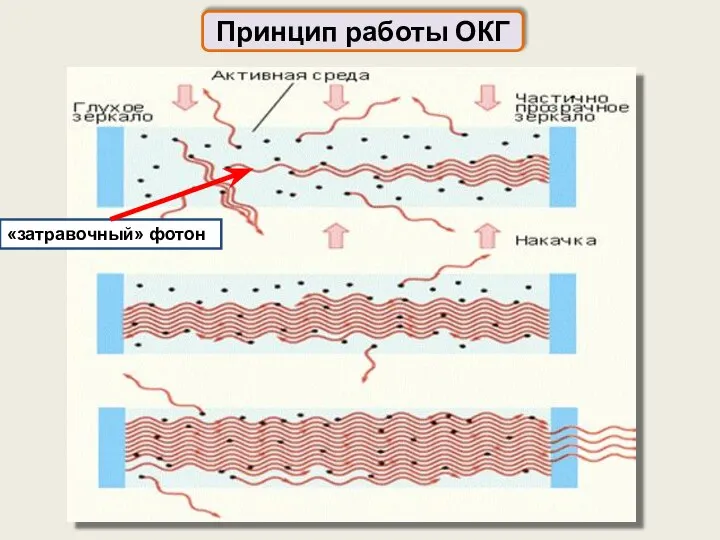
- 70. Принцип работы ОКГ «затравочный» фотон
- 71. Принцип работы ОКГ Для работы лазера недостаточно двухуровневой схемы: при любой мощности накачки число возбужденных атомов
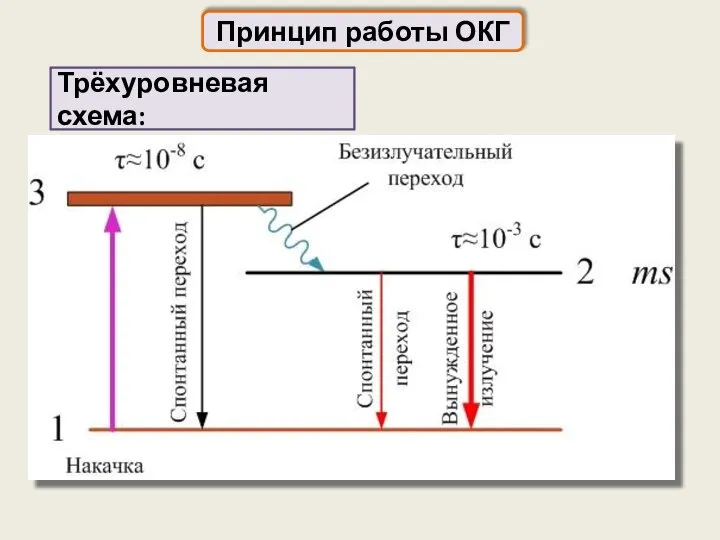
- 72. Принцип работы ОКГ Трёхуровневая схема:
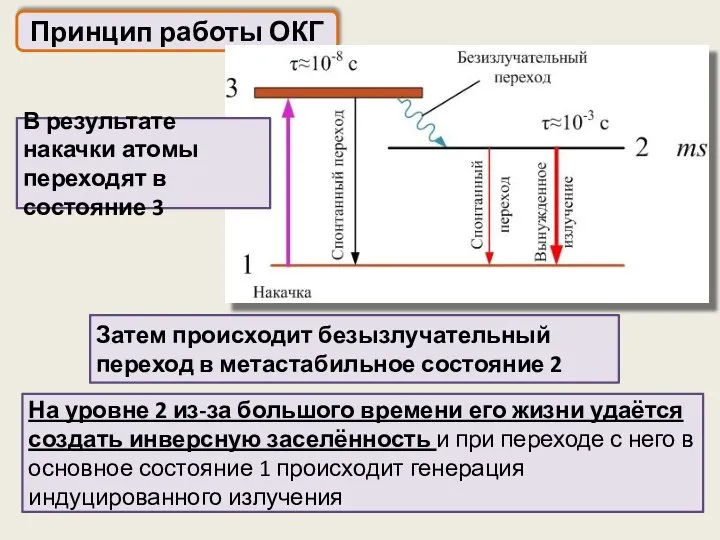
- 73. Принцип работы ОКГ На уровне 2 из-за большого времени его жизни удаётся создать инверсную заселённость и
- 74. Свойства лазерного излучения Монохроматичность Когерентность Длина когерентности гелий-неонового лазера больше диаметра земной орбиты 3. Направленность 4.
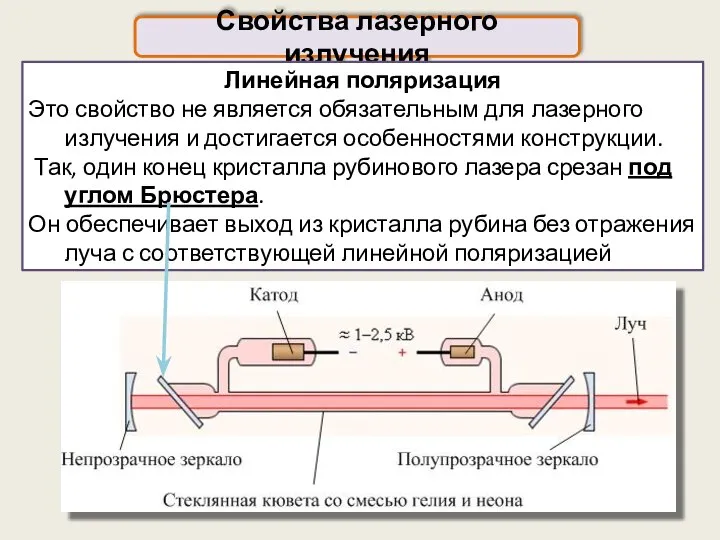
- 75. Свойства лазерного излучения Линейная поляризация Это свойство не является обязательным для лазерного излучения и достигается особенностями
- 77. Скачать презентацию

































 Тестовые вопросы по физике 1-35
Тестовые вопросы по физике 1-35 Ядерная энергетика в автомобилях. Машины с ядерными двигателями
Ядерная энергетика в автомобилях. Машины с ядерными двигателями Характеристика автомобиля как объекта ремонта
Характеристика автомобиля как объекта ремонта Производная в технике, физике и химии
Производная в технике, физике и химии Правка, разметка и резание заготовок из тонколистового металла и проволоки
Правка, разметка и резание заготовок из тонколистового металла и проволоки Антенные решетки. (Лекция 7)
Антенные решетки. (Лекция 7) Магнитное поле
Магнитное поле Термодинаміка. Внутрішня енергія
Термодинаміка. Внутрішня енергія Атом. Состав атомного ядра
Атом. Состав атомного ядра Магниттік күштік микроскопия
Магниттік күштік микроскопия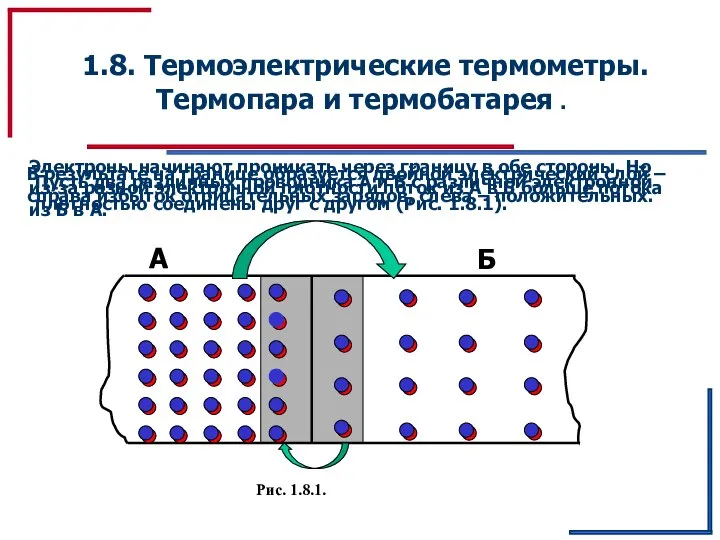 Термоэлектрические термометры. Термопара и термобатарея
Термоэлектрические термометры. Термопара и термобатарея Величины, характеризующие колебательное движение Сформировать знания у школьников о частоте колебаний, амплитуде, периоде, фазе.
Величины, характеризующие колебательное движение Сформировать знания у школьников о частоте колебаний, амплитуде, периоде, фазе. Физические приборы
Физические приборы Аттестационная работа. Программа внедрения инновационных бизнес-технологий, проект: «Новой школе - бизнестехнологии»
Аттестационная работа. Программа внедрения инновационных бизнес-технологий, проект: «Новой школе - бизнестехнологии» Многогрупповое приближение. Технология получения групповых констант. Понятие спектра свертки. Стандартные спектры
Многогрупповое приближение. Технология получения групповых констант. Понятие спектра свертки. Стандартные спектры Жидкости. Строение и свойства жидкостей
Жидкости. Строение и свойства жидкостей Задачи по статике. (10 класс)
Задачи по статике. (10 класс) Типы спектров и постулаты бора
Типы спектров и постулаты бора Жылу және электр энергиясын жинап сақтау
Жылу және электр энергиясын жинап сақтау Механическое движение
Механическое движение Постоянный электрический ток. Характеристики электрической цепи. Действие электрического тока и правила техники безопасности
Постоянный электрический ток. Характеристики электрической цепи. Действие электрического тока и правила техники безопасности Реальный колебательный контур. Визуальная часть. Приложение.
Реальный колебательный контур. Визуальная часть. Приложение. Основные параметры и характеристики передающих антенн
Основные параметры и характеристики передающих антенн Спин – орбитальная связь
Спин – орбитальная связь Мореходность
Мореходность Ағындардың гидродинамикалық құрылымы. Химиялық аппараттарда ағын бөлшектерінің жылдамдығы мен болу уақыты
Ағындардың гидродинамикалық құрылымы. Химиялық аппараттарда ағын бөлшектерінің жылдамдығы мен болу уақыты Радиоволны и радио
Радиоволны и радио Презентация по физике Магнитное поле земли
Презентация по физике Магнитное поле земли