Содержание
- 2. Цель: повторение основных понятий, законов и формул молекулярной физики в соответствии с кодификатором ЕГЭ Элементы содержания,
- 3. Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и
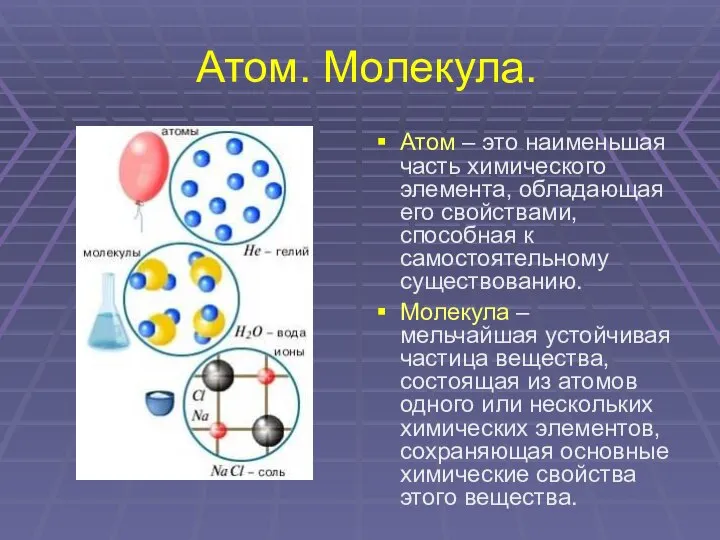
- 4. Атом. Молекула. Атом – это наименьшая часть химического элемента, обладающая его свойствами, способная к самостоятельному существованию.
- 5. Масса молекул. Количество вещества. Относительной молекулярной (или атомной) массой вещества называют отношение массы молекулы (или атома)
- 6. Модели строения твердых тел, жидкостей и газов Молекулы большинства твердых тел расположены в определенном порядке. Такие
- 7. Модели строения твердых тел, жидкостей и газов Расстояния между молекулами жидкости сравнимо с размерами молекул, поэтому
- 8. Модели строения твердых тел, жидкостей и газов Расстояние между молекулами газов намного больше размеров самих молекул,
- 9. Тепловое движение молекул Беспорядочное хаотическое движение молекул называется тепловым движением. Доказательством теплового движения является броуновское движение
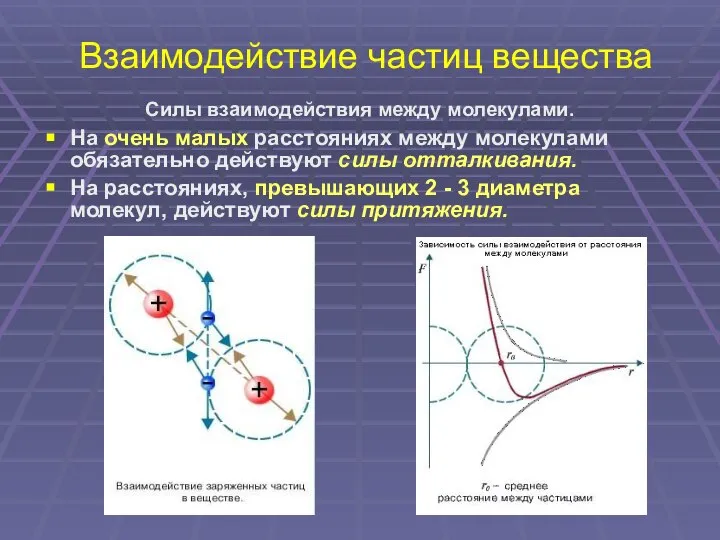
- 10. Взаимодействие частиц вещества Силы взаимодействия между молекулами. На очень малых расстояниях между молекулами обязательно действуют силы
- 11. Идеальный газ – это теоретическая модель газа, в которой пренебрегают размерами и взаимодействиями частиц газа и
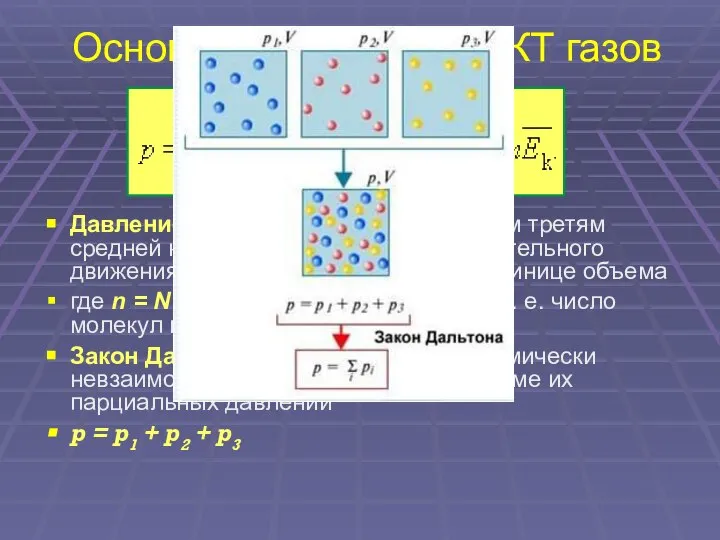
- 12. Основное уравнение МКТ газов Давление идеального газа равно двум третям средней кинетической энергии поступательного движения молекул,
- 13. Абсолютная температура Температура характеризует степень нагретости тела. Тепловое равновесие – это такое состояние системы тел, находящихся
- 14. Абсолютная температура Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. k – постоянная
- 15. Уравнение Менделеева-Клапейрона Уравнение состояния идеального газа – это зависимость между параметрами идеального газа – давлением, объемом
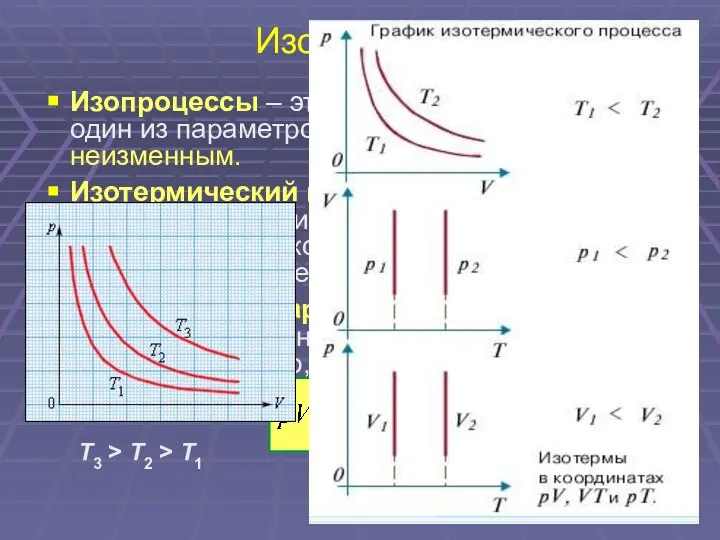
- 16. Изопроцессы Изопроцессы – это процессы, в которых один из параметров (p, V или T) остается неизменным.
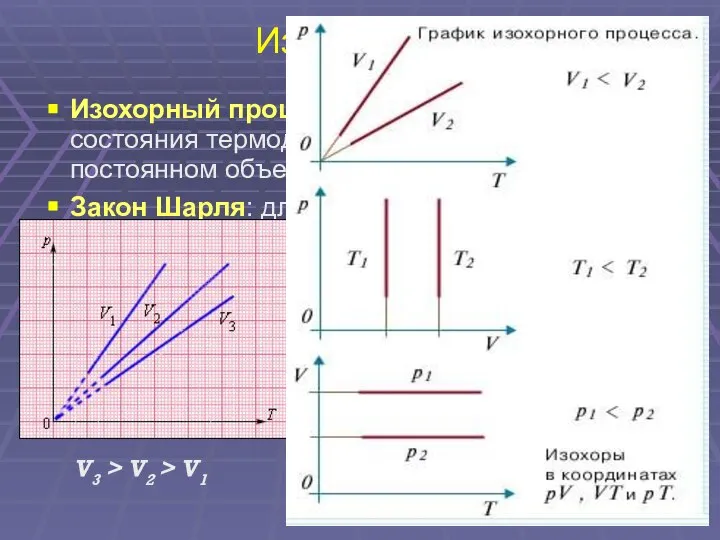
- 17. Изопроцессы Изохорный процесс – это процесс изменения состояния термодинамической системы при постоянном объеме. Закон Шарля: для
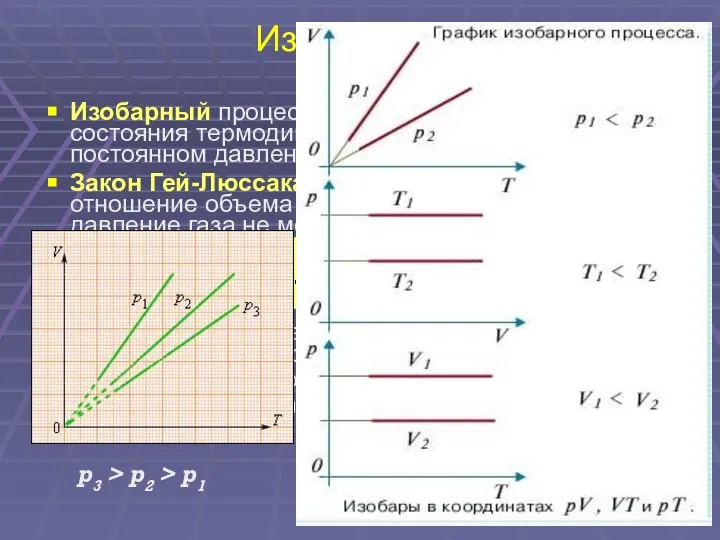
- 18. Изопроцессы Изобарный процесс – это процесс изменения состояния термодинамической системы при постоянном давлении. Закон Гей-Люссака: для
- 19. Взаимные превращения жидкостей и газов Парообразование – это переход вещества из жидкого состояния в газообразное. Конденсация
- 20. Взаимные превращения жидкостей и газов Насыщенные и ненасыщенные пары В закрытом сосуде жидкость и ее пар
- 21. Взаимные превращения жидкостей и газов Кипение Кипение – это парообразование, происходящее по всему объему жидкости. Кипение
- 22. Влажность воздуха Влажность воздуха – это содержание в воздухе водяного пара. Чем больше водяных паров находится
- 23. Изменение агрегатных состояний вещества: плавление и кристаллизация Плавление — переход вещества из твёрдого состояния в жидкое.
- 24. Термодинамика Термодинамика – это теория тепловых процессов, в которой не учитывается молекулярное строение тел. Основные понятия
- 25. Внутренняя энергия Внутренняя энергия тела – это сумма кинетической энергии всех его молекул и потенциальной энергии
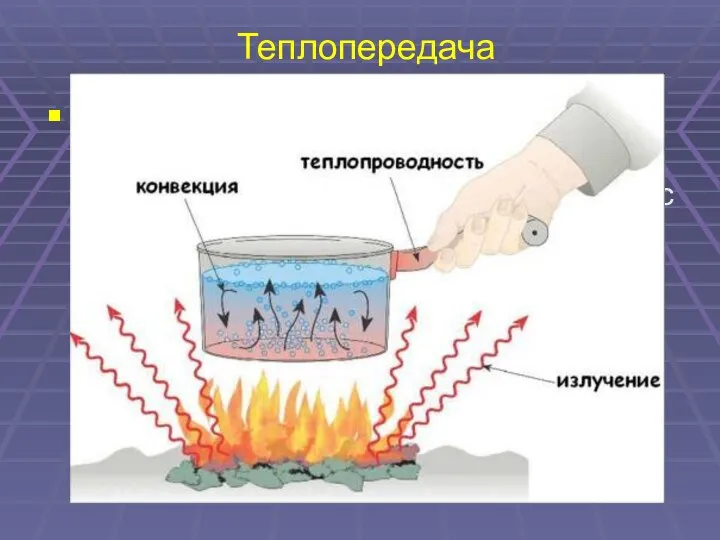
- 26. Теплопередача Теплопередача – это самопроизвольный процесс передачи теплоты, происходящий между телами с разной температурой.
- 27. Количество теплоты Количеством теплоты называют количественную меру изменения внутренней энергии тела при теплообмене (теплопередаче). Количество теплоты,
- 28. Количество теплоты Количество теплоты, необходимое для плавления кристаллического тела или выделяемое телом при отвердевании. λ –
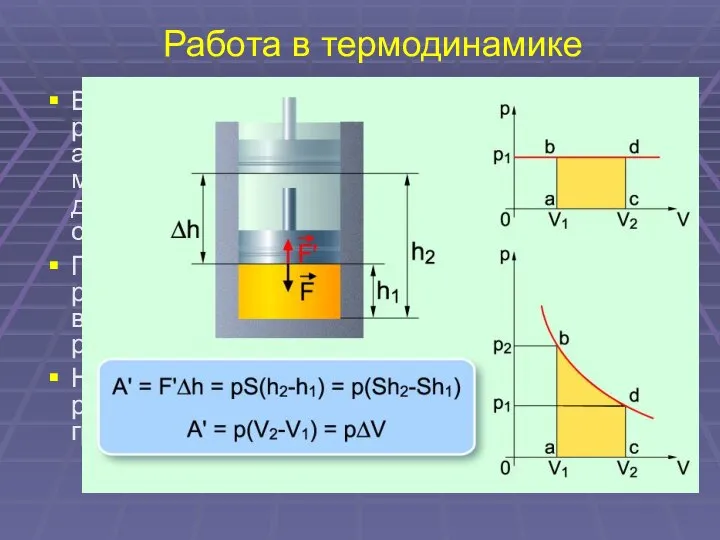
- 29. Работа в термодинамике В термодинамике, в отличие от механики, рассматривается не движение тела как целого, а
- 30. Первый закон термодинамики Первый закон термодинамики – это закон сохранения и превращения энергии для термодинамической системы.
- 31. Применение первого закона термодинамики к различным процессам Изобарный процесс. Количество теплоты, переданное системе, идет на изменение
- 32. Второй закон термодинамики Все процессы самопроизвольно протекают в одном определенном направлении. Они необратимы. Теплота всегда переходит
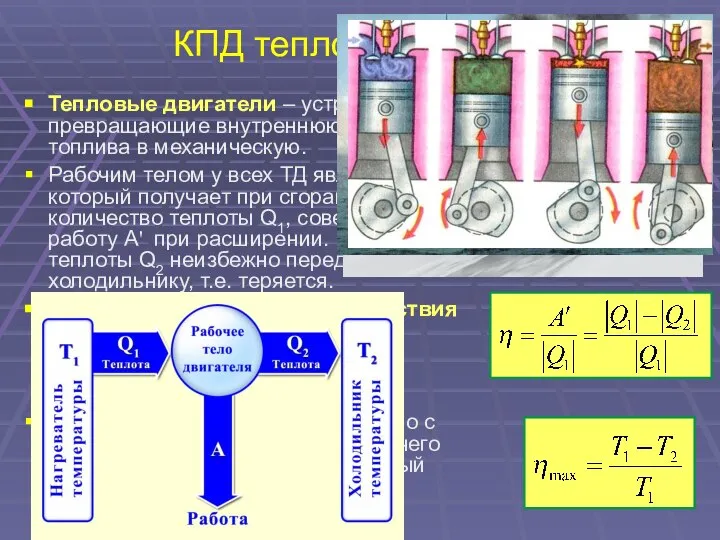
- 33. КПД тепловой машины Тепловые двигатели – устройства, превращающие внутреннюю энергию топлива в механическую. Рабочим телом у
- 34. Рассмотрим задачи:
- 35. Согласно расчетам, температура жидкости должна быть равна 143 К. Между тем термометр в сосуде показывает температуру
- 36. На рисунке показана часть шкалы термометра, висящего за окном. Температура воздуха на улице равна ..... 180С.
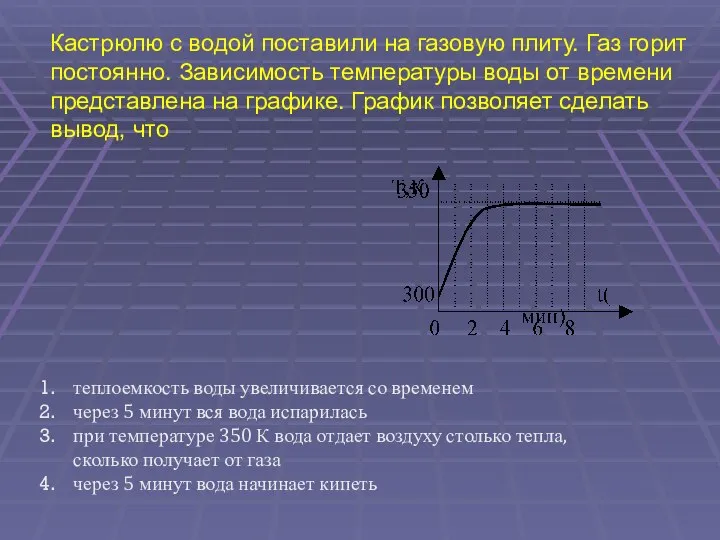
- 37. Кастрюлю с водой поставили на газовую плиту. Газ горит постоянно. Зависимость температуры воды от времени представлена
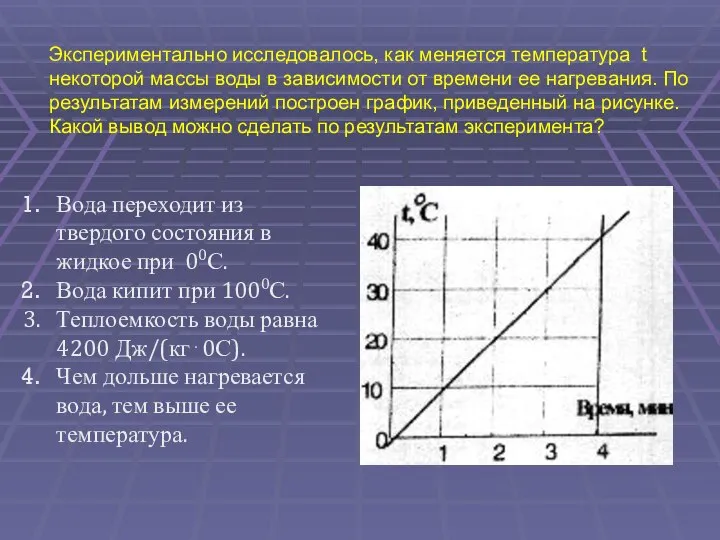
- 38. Экспериментально исследовалось, как меняется температура t некоторой массы воды в зависимости от времени ее нагревания. По
- 39. Тела, имеющие разные температуры, привели в соприкосновение двумя способами ( I и II ). Какое из
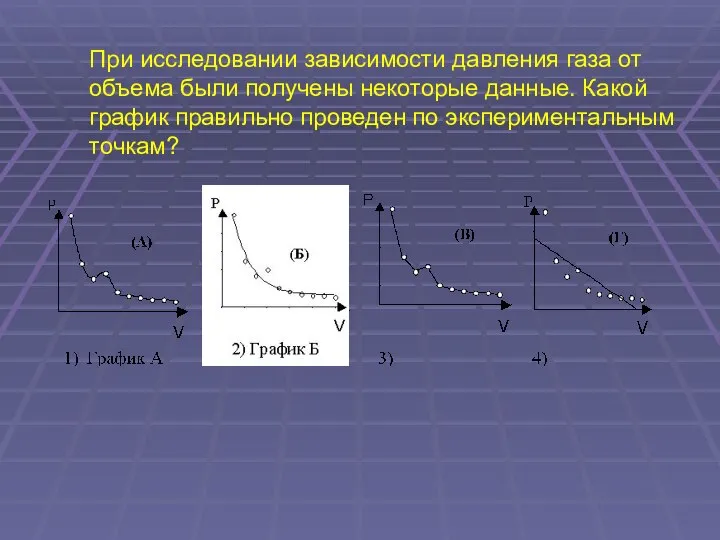
- 40. При исследовании зависимости давления газа от объема были получены некоторые данные. Какой график правильно проведен по
- 41. Какой из перечисленных ниже опытов (А, Б или В) подтверждает вывод молекулярно-кинетической теории о том, что
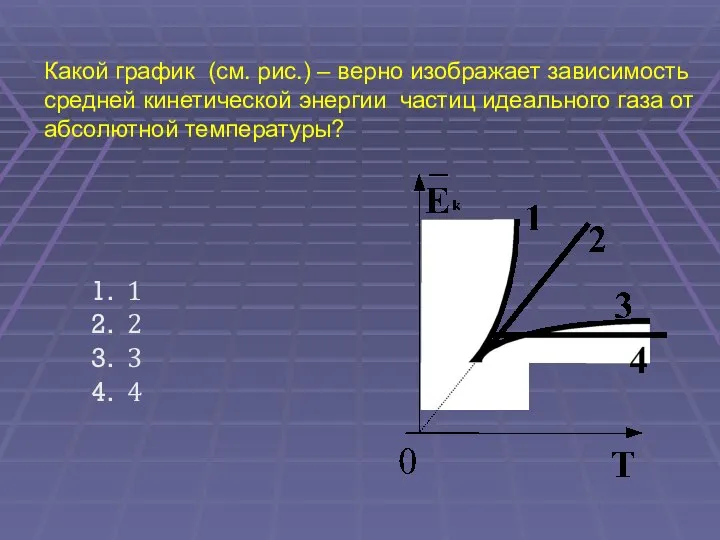
- 42. Какой график (см. рис.) – верно изображает зависимость средней кинетической энергии частиц идеального газа от абсолютной
- 43. В баллоне находится 6 моль газа. Сколько примерно молекул газа находится в баллоне?
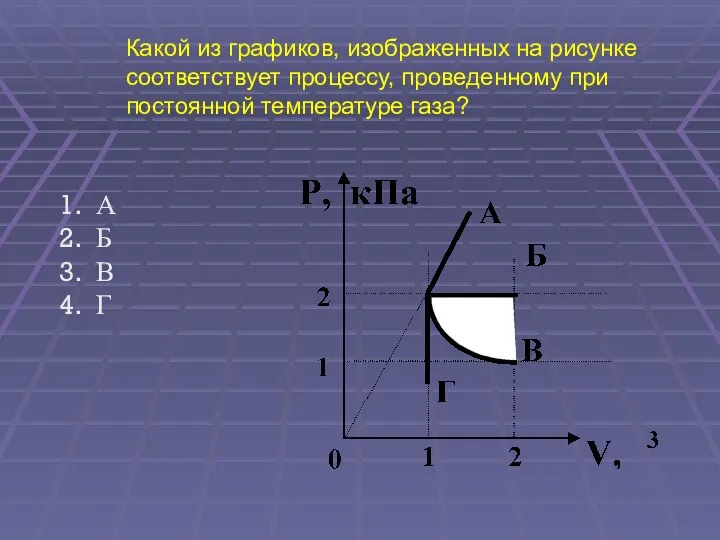
- 44. Какой из графиков, изображенных на рисунке соответствует процессу, проведенному при постоянной температуре газа? А Б В
- 45. При испарении жидкость остывает. Молекулярно-кинетическая теория объясняет это тем, что чаще всего жидкость покидают молекулы, кинетическая
- 46. При сжатии идеального газа объем уменьшился в 2 раза, а температура газа увеличилась в 2 раза.
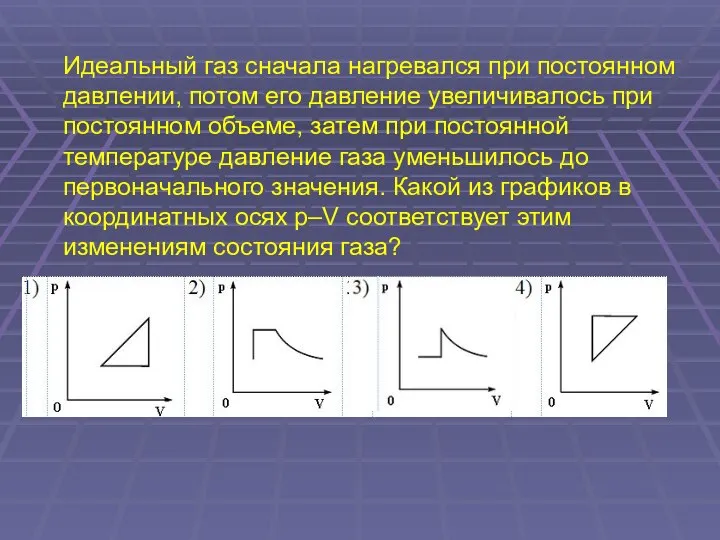
- 47. Идеальный газ сначала нагревался при постоянном давлении, потом его давление увеличивалось при постоянном объеме, затем при
- 48. Какова температура идеального газа в точке 2, если в точке 4 она равна 200К 200 К
- 49. При неизменной концентрации частиц идеального газа средняя кинетическая энергия теплового движения его молекул увеличилась в 3
- 50. На рисунке изображен график зависимости давления газа на стенки сосуда от температуры. Какой процесс изменения состояния
- 51. Температура кипения воды зависит от мощности нагревателя вещества сосуда, в котором нагревается вода атмосферного давления начальной
- 52. На рисунке изображен график плавления и кристаллизации нафталина. Какая из точек соответствует началу отвердевания вещества? точка
- 53. Весной при таянии льда в водоеме температура окружающего воздуха уменьшается увеличивается не изменяется может увеличиваться или
- 54. Идеальному газу сообщили количество теплоты 400 Дж. Газ расширился, совершив работу 600 Дж. Внутренняя энергия газа
- 55. Как изменяется внутренняя энергия кристаллического вещества в процессе его плавления? увеличивается для любого кристаллического вещества уменьшается
- 56. При какой влажности воздуха человек легче переносит высокую температуру воздуха и почему? при низкой, так как
- 57. Экспериментаторы закачивают воздух в стеклянный сосуд, одновременно охлаждая его. При этом температура воздуха в сосуде понизилась
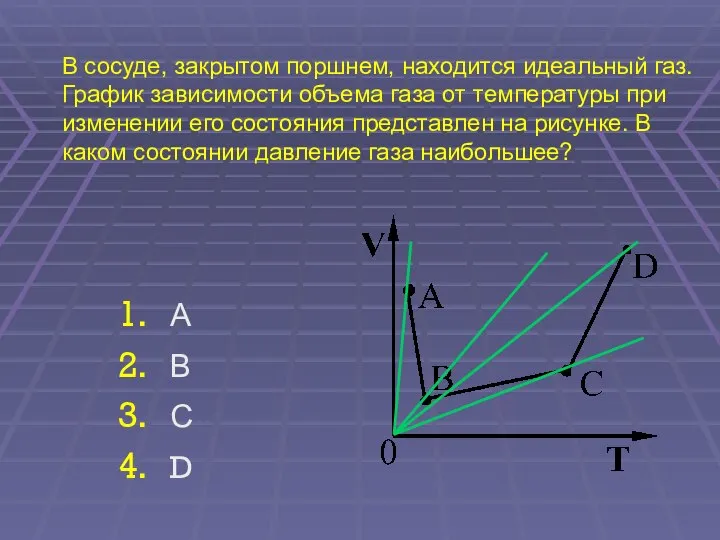
- 58. В сосуде, закрытом поршнем, находится идеальный газ. График зависимости объема газа от температуры при изменении его
- 59. 3 моль водорода находятся в сосуде при температуре Т. Какова температура 3 моль кислорода в сосуде
- 60. При одинаковой температуре 100°С давление насыщенных паров воды равно 105 Па, аммиака — 59⋅105 Па и
- 61. В сосуде постоянного объема находится идеальный газ, массу которого изменяют. На диаграмме (см. рисунок) показан процесс
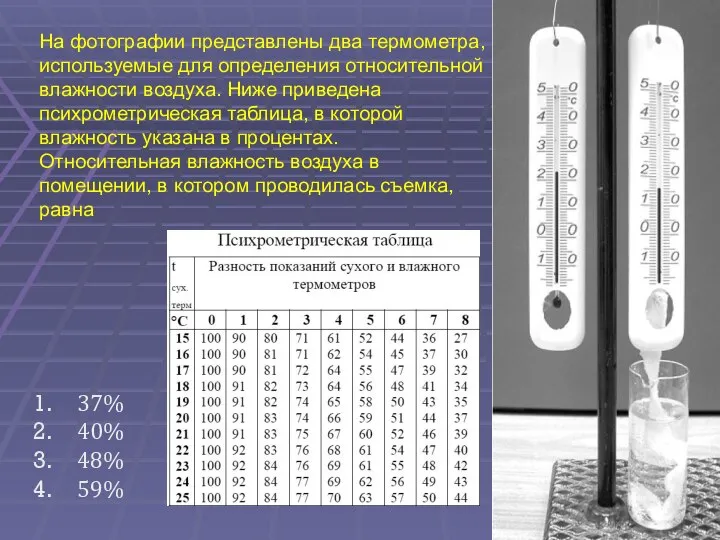
- 62. На фотографии представлены два термометра, используемые для определения относительной влажности воздуха. Ниже приведена психрометрическая таблица, в
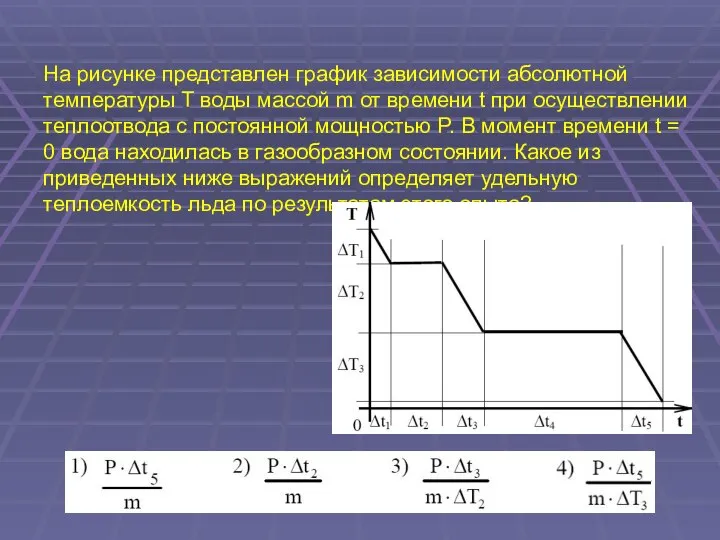
- 63. На рисунке представлен график зависимости абсолютной температуры T воды массой m от времени t при осуществлении
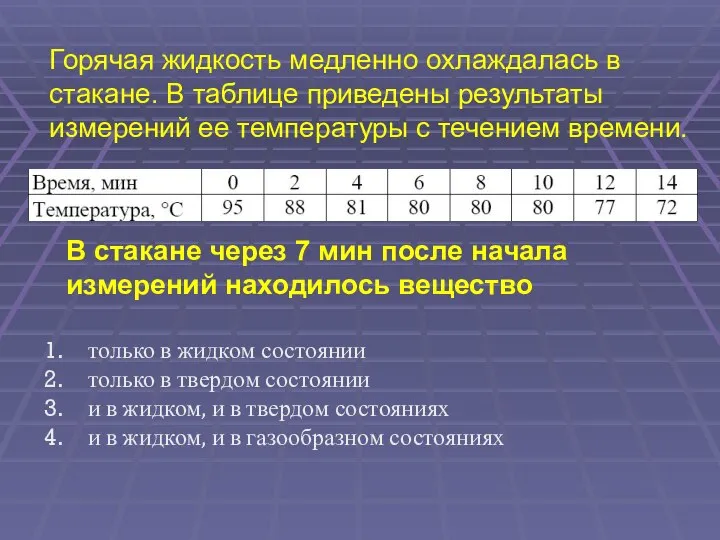
- 64. Горячая жидкость медленно охлаждалась в стакане. В таблице приведены результаты измерений ее температуры с течением времени.
- 65. Используя первый закон термодинамики, установите соответствие между описанными в первом столбце особенностями изопроцесса в идеальном газе
- 66. В сосуде неизменного объема находилась при комнатной температуре смесь двух идеальных газов, по 1 моль каждого.
- 67. После помещения банки на огонь вода в ней нагревалась через тонкую стенку банки от горячих продуктов
- 68. В соответствии с уравнением Клапейрона–Менделеева давление пара в банке резко упало – во-первых, из-за уменьшения массы
- 69. Согласно первому началу термодинамики количество теплоты, необходимое для плавления льда, ΔQ1 = λm, где λ –
- 70. Согласно первому началу термодинамики, количество теплоты Q, переданное газу, идет на изменение его внутренней энергии ΔU
- 72. Скачать презентацию


















































 Выбор линейных реакторов
Выбор линейных реакторов Реологические свойства биологических объектов. Гемодинамика
Реологические свойства биологических объектов. Гемодинамика Презентация по физике "Радиоактивность в физике" - скачать
Презентация по физике "Радиоактивность в физике" - скачать  Броуновское движение. Силы взаимодействия молекул
Броуновское движение. Силы взаимодействия молекул Презентация по физике "Електричний струм в рідинах" - скачать бесплатно
Презентация по физике "Електричний струм в рідинах" - скачать бесплатно Нанотехнологии
Нанотехнологии Тепловое излучение
Тепловое излучение Электромагнитная индукция
Электромагнитная индукция Оформление. Выполнение контрольных работ
Оформление. Выполнение контрольных работ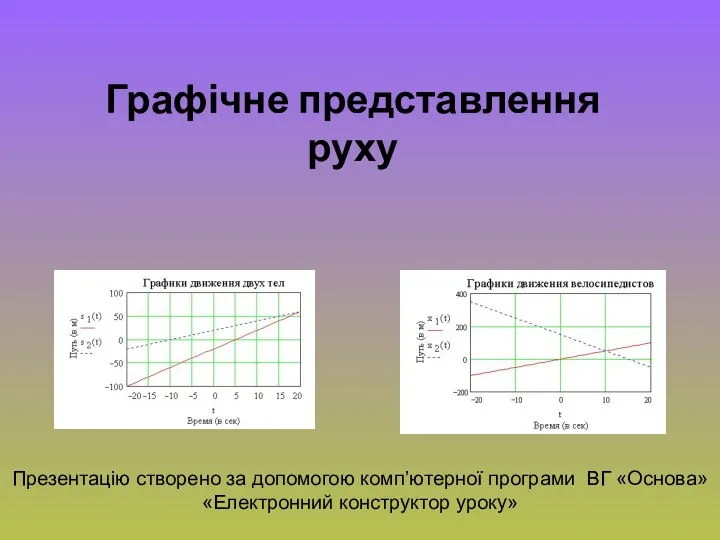 Графічне представлення руху
Графічне представлення руху Трансформаторы и их виды
Трансформаторы и их виды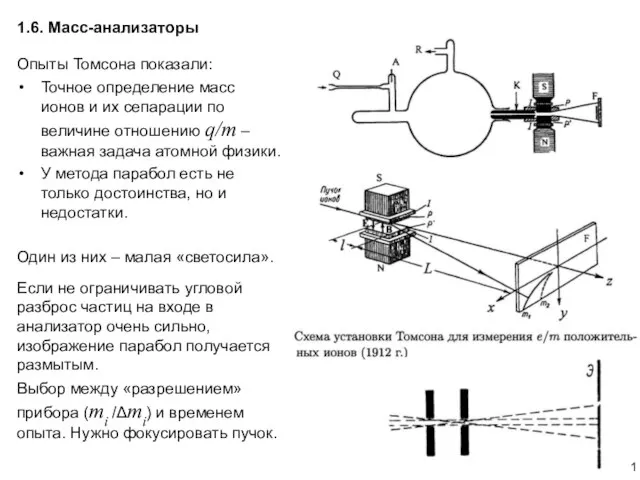 Масс-спектрометры. АФ1.6
Масс-спектрометры. АФ1.6 Действия электрического тока
Действия электрического тока Физические величины и их измерение
Физические величины и их измерение Последовательности и их параметры
Последовательности и их параметры Модель Бабы Яги с резиномоторным двигателем
Модель Бабы Яги с резиномоторным двигателем Взаимодействие ускоренных электронов с веществом: торможение электронов в результате неупругих электронных взаимодействий
Взаимодействие ускоренных электронов с веществом: торможение электронов в результате неупругих электронных взаимодействий Электротехническая механика. Червячная передача
Электротехническая механика. Червячная передача Презентация по физике "Магнітні властивості речовини" - скачать
Презентация по физике "Магнітні властивості речовини" - скачать  Реактивное движение в природе и технике
Реактивное движение в природе и технике Трехфазные цепи. Общие сведения
Трехфазные цепи. Общие сведения Квазікласичне наближення для рівняння Дірака зі скалярно-векторним зв’язком кулонівського типу
Квазікласичне наближення для рівняння Дірака зі скалярно-векторним зв’язком кулонівського типу Struktura hmoty
Struktura hmoty Однотактные преобразователи с потенциальной развязкой
Однотактные преобразователи с потенциальной развязкой Аттестационная работа. Проект по физике «Гаус пушка»
Аттестационная работа. Проект по физике «Гаус пушка» Динамика. (Лекция 3)
Динамика. (Лекция 3) Понятие электрического поля
Понятие электрического поля Приборы для измерения давления и их применения
Приборы для измерения давления и их применения