Содержание
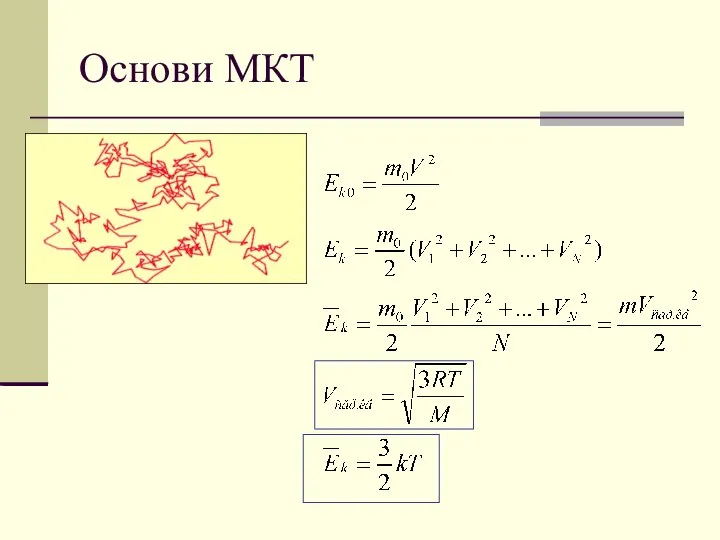
- 2. Основи МКТ
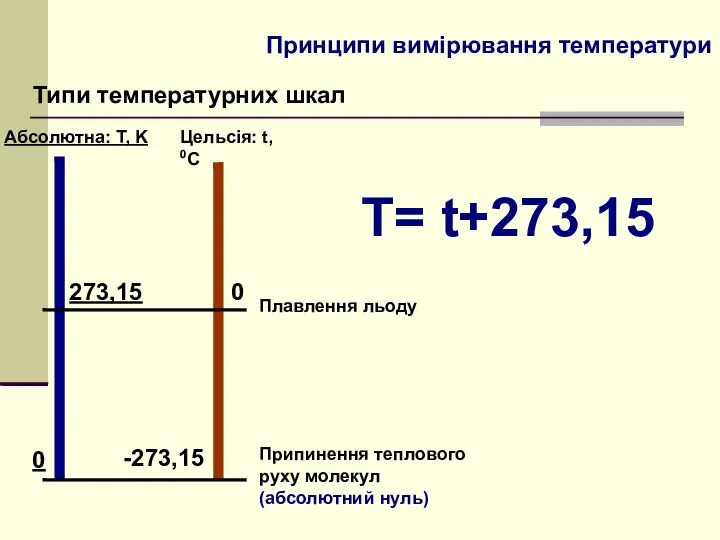
- 3. Принципи вимірювання температури Типи температурних шкал Абсолютна: Т, K Цельсія: t, 0C 0 -273,15 273,15 0
- 4. Принципи вимірювання температури Використання теплового розширення речовин Рідинний термометр Біметалічні термометри Метал 1 α1 Метал 2
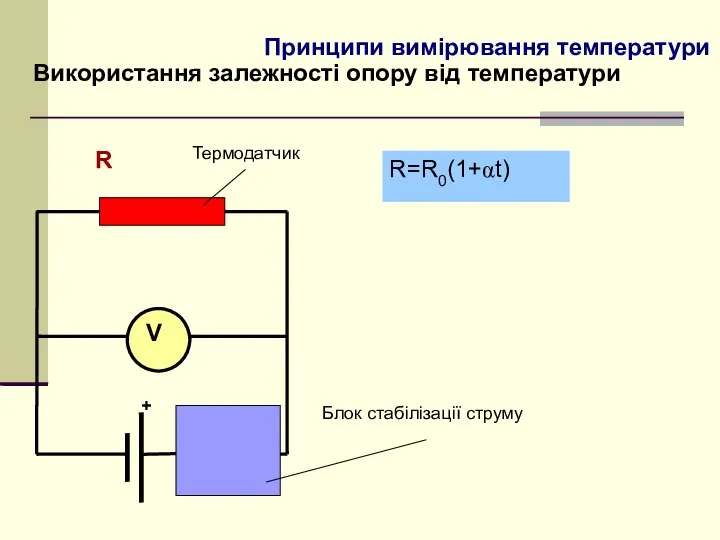
- 5. Принципи вимірювання температури Використання залежності опору від температури R=R0(1+αt) V R Блок стабілізації струму + Термодатчик
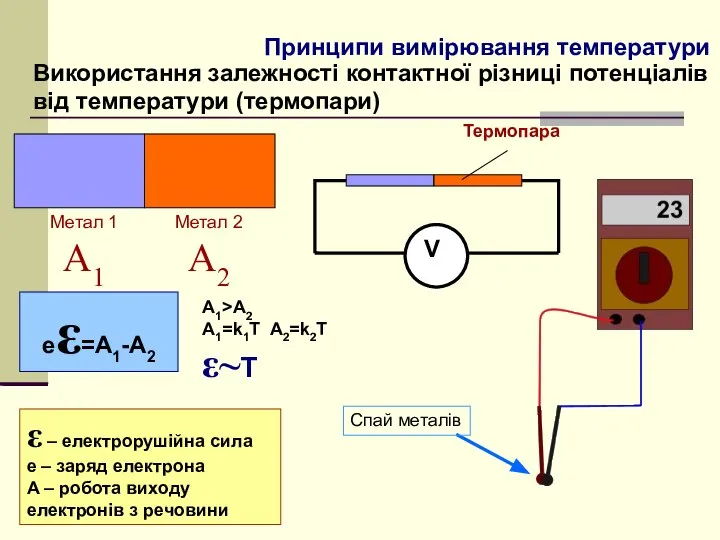
- 6. Принципи вимірювання температури Використання залежності контактної різниці потенціалів від температури (термопари) V Метал 1 Α1 Метал
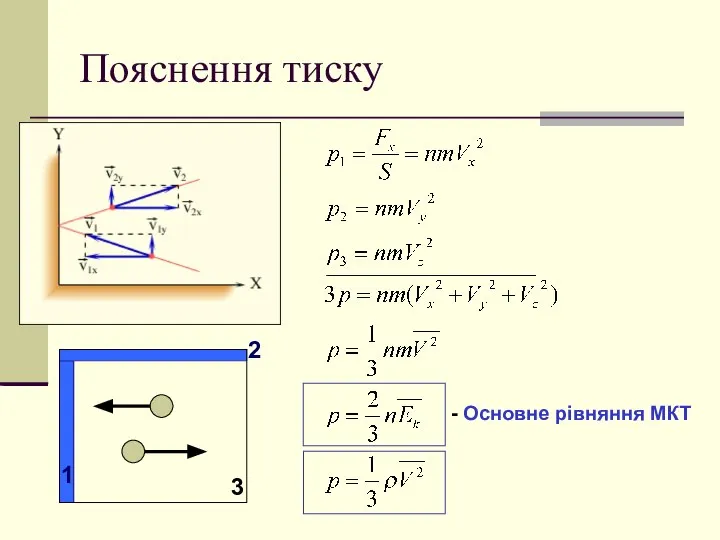
- 7. Пояснення тиску 1 2
- 8. Пояснення тиску 1 2 3 Основне рівняння МКТ
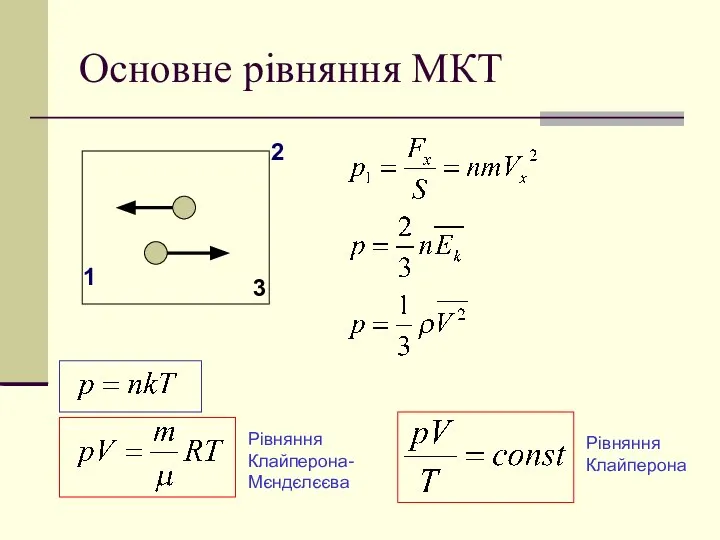
- 9. Основне рівняння МКТ 1 2 3 Рівняння Клайперона- Мєндєлєєва Рівняння Клайперона
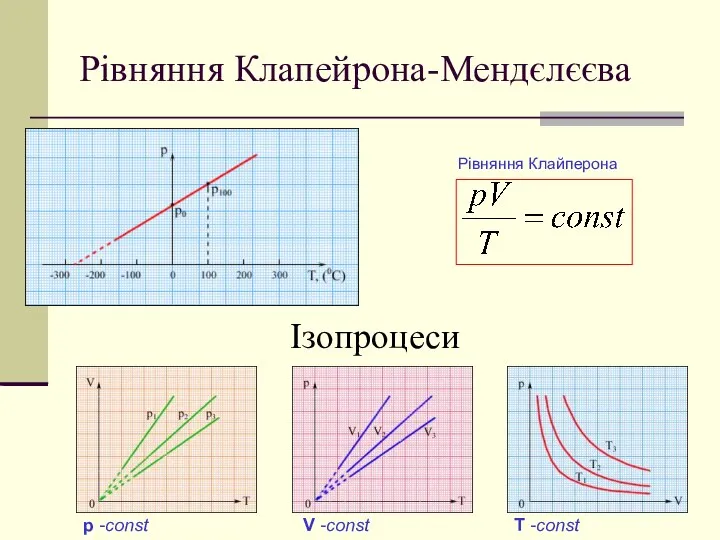
- 10. Рівняння Клапейрона-Мендєлєєва Рівняння Клайперона Ізопроцеси p -const V -const T -const
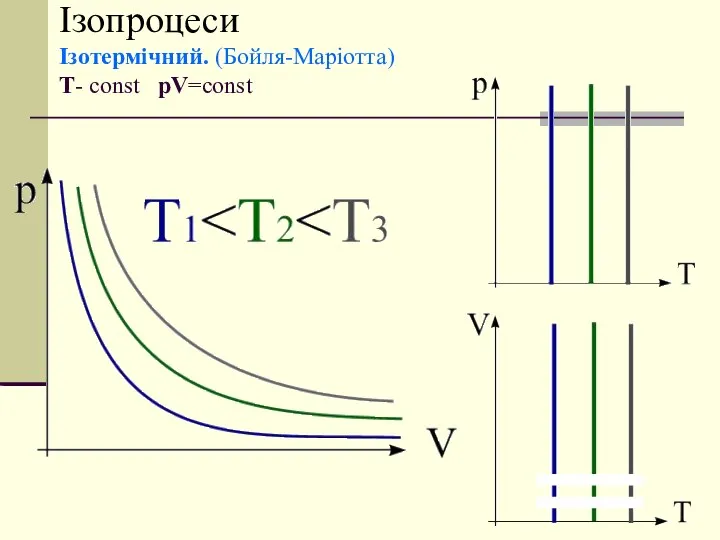
- 11. Ізопроцеси Ізотермічний. (Бойля-Маріотта) T- const pV=const
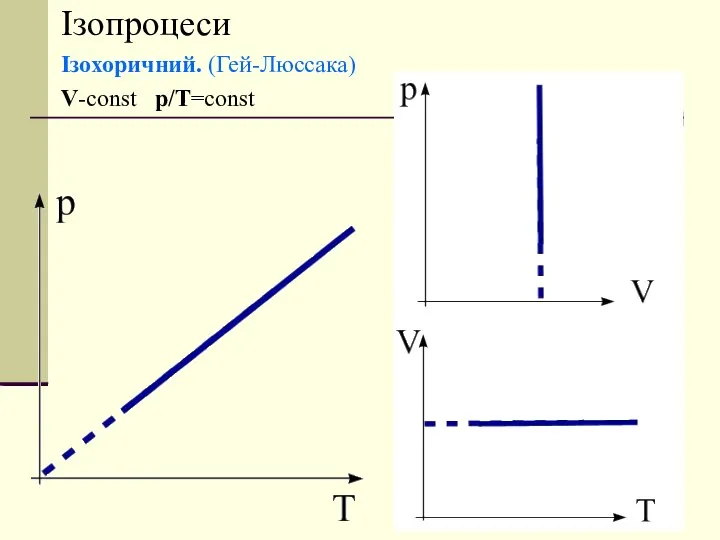
- 12. Ізопроцеси Ізохоричний. (Гей-Люссака) V-const p/T=const
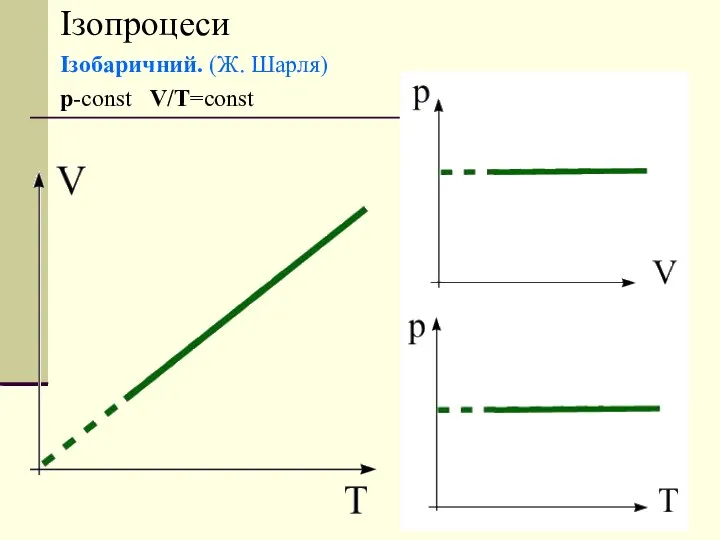
- 13. Ізопроцеси Ізобаричний. (Ж. Шарля) p-const V/T=const
- 14. Реальні гази Рівняння Ван-дер-Ваальса (1873) Ідеальний газ: рівняння Клапейрона-Мендєлєєва
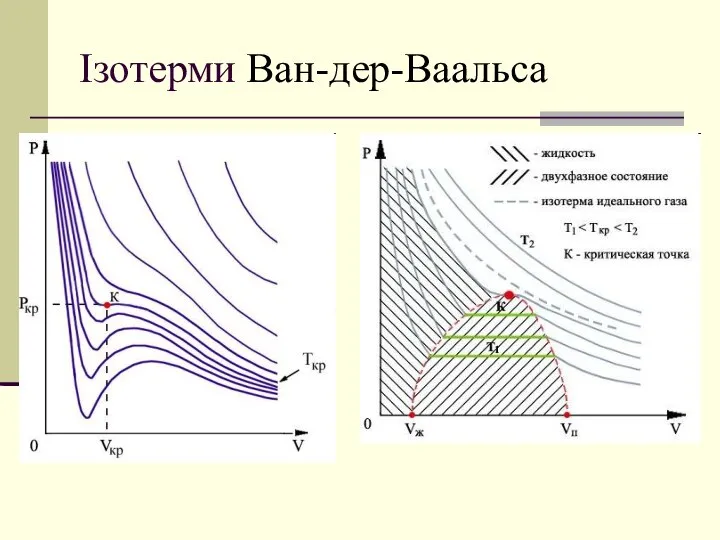
- 15. Ізотерми Ван-дер-Ваальса
- 16. Ізотерми Ван-дер-Ваальса
- 17. Термодинаміка Внутрішня енергія тіла - сума всіх кінетичних та потенціальних енергій взаємодії між собою молекул тіла.
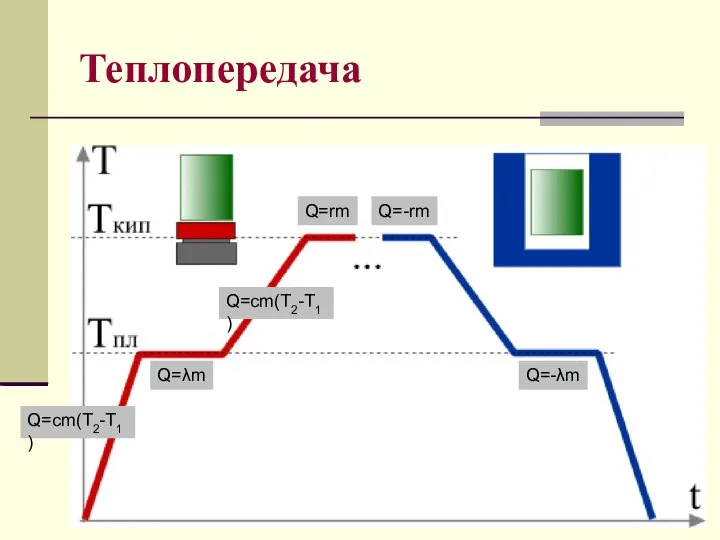
- 18. Теплопередача Q=cm(T2-T1) Q=cm(T2-T1) Q=λm Q=rm Q=-rm Q=-λm
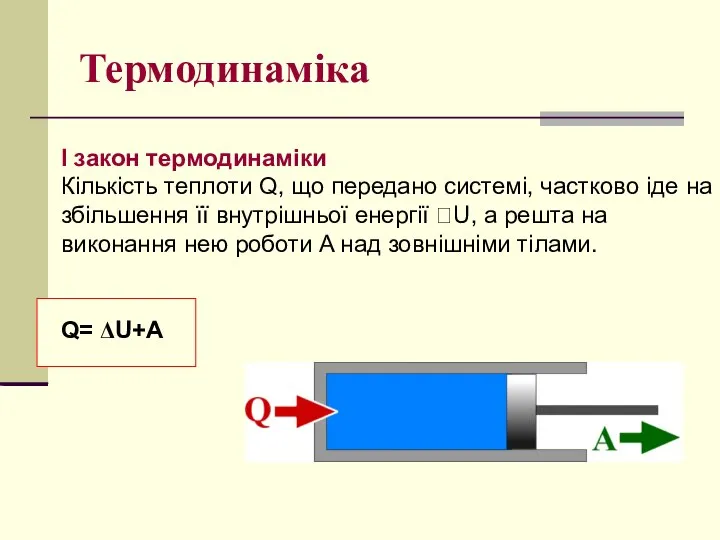
- 19. Термодинаміка I закон термодинаміки Кількість теплоти Q, що передано системі, частково іде на збільшення її внутрішньої
- 20. Внутрішня енергія одноатомний газ: i=3 двоатомний газ: i=5 Теорема про рівномірний розподіл енергії за ступенями вільності:
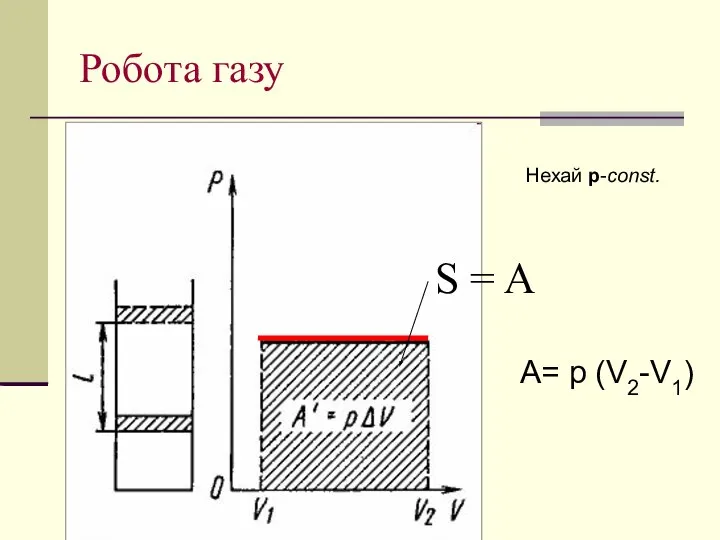
- 21. Робота газу Нехай р-const. S = A A= p (V2-V1)
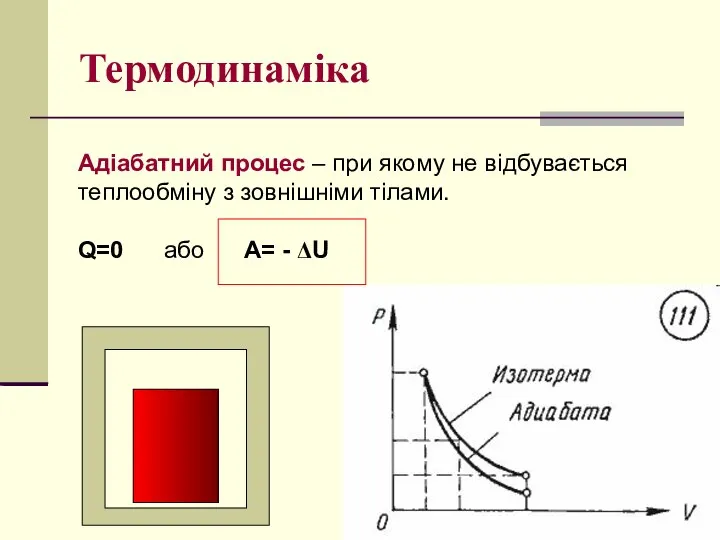
- 22. Термодинаміка Адіабатний процес – при якому не відбувається теплообміну з зовнішніми тілами. Q=0 або A= -
- 23. Термодинаміка Ізотермічний T - const Δ U=0 Q=A Ізобаричний p - const A=p(V 2 -V 1
- 24. Теплоємність газів - співвідношення Майєра:
- 25. Термодинаміка Процес наз. оборотним, якщо він допускає можливіість повернення системи до початкового стану без будь-яких змін
- 26. Термодинаміка II закон термодинаміки Процес, при якому теплота передається від менш нагрітих тіл до більш нагрітих
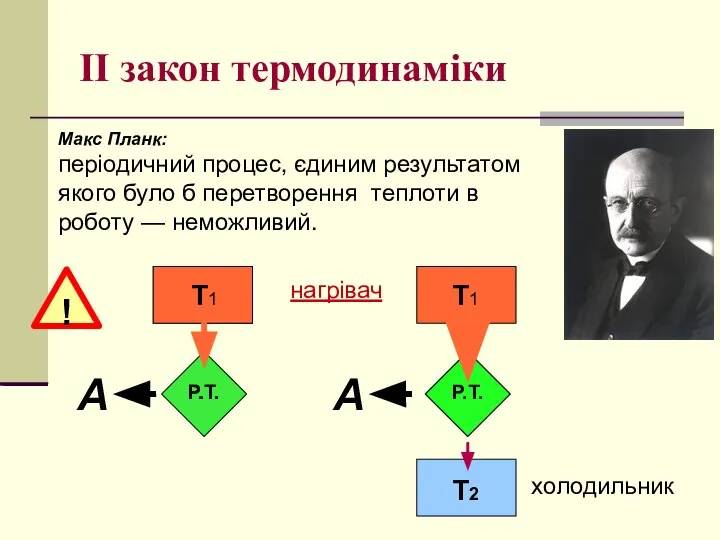
- 27. II закон термодинаміки Макс Планк: періодичний процес, єдиним результатом якого було б перетворення теплоти в роботу
- 28. II закон термодинаміки Уільям То́мсон, лорд Ке́львін Неможливо побудувати теплову машину, яка б виконувала роботу за
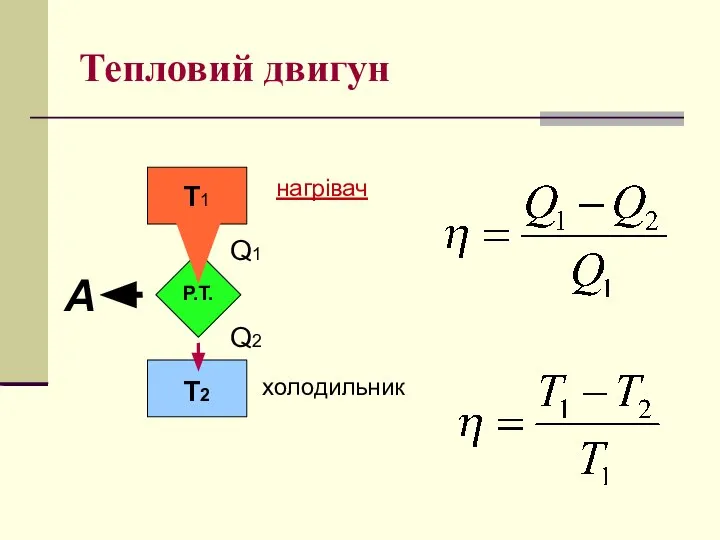
- 29. Тепловий двигун А Т1 Т2 Р.Т. нагрівач холодильник Q1 Q2
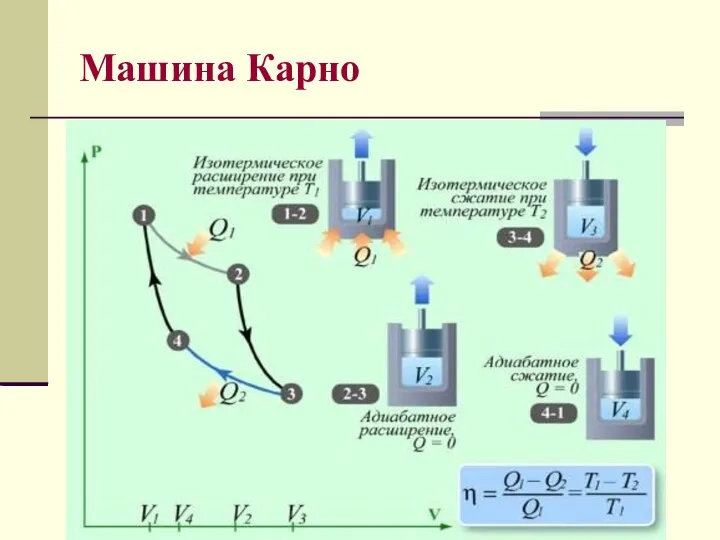
- 30. Машина Карно
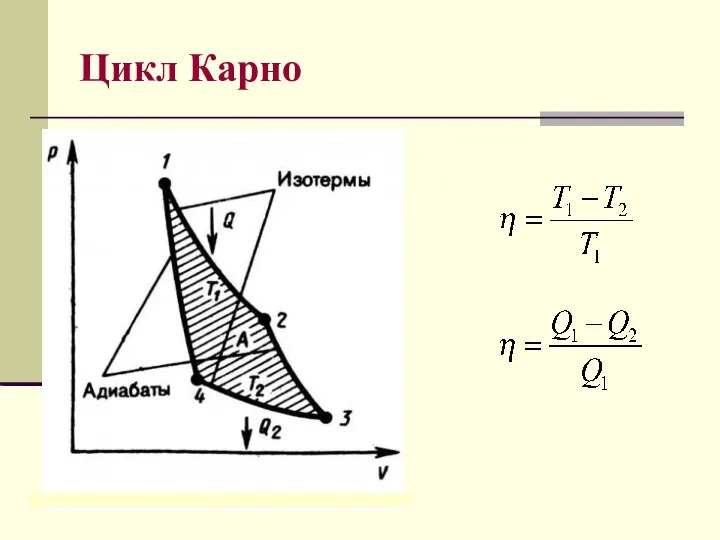
- 31. Цикл Карно
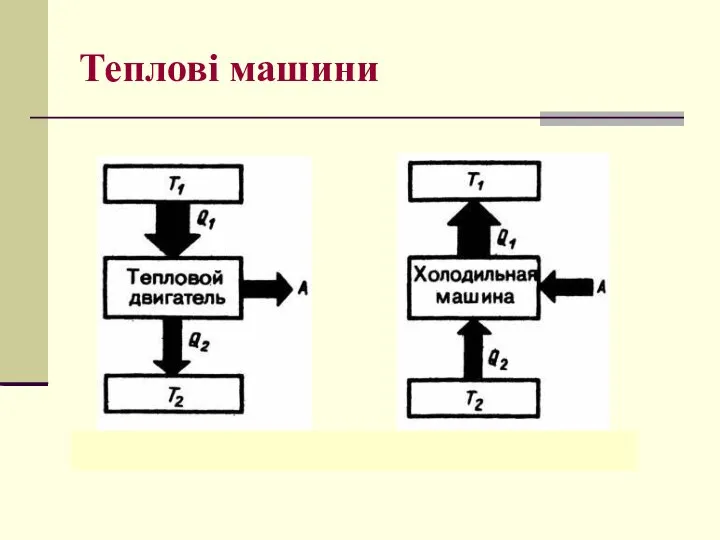
- 32. Теплові машини
- 34. Скачать презентацию











 Механические колебания и волны
Механические колебания и волны Влияние радиации на организм человека
Влияние радиации на организм человека Петля Нестерова. Моделирование движения самолета
Петля Нестерова. Моделирование движения самолета Электрические источники света
Электрические источники света Регулярные линии передачи электромагнитной энергии. Тема 4
Регулярные линии передачи электромагнитной энергии. Тема 4 Магнитные подшипники
Магнитные подшипники Современные тепловые двигатели
Современные тепловые двигатели Динамика твердого тела. Момент силы. Момент инерции. Теорема Штейнера. Основное уравнение динамики вращательного движения
Динамика твердого тела. Момент силы. Момент инерции. Теорема Штейнера. Основное уравнение динамики вращательного движения Электростатика. (Лекция 11)
Электростатика. (Лекция 11) Описание электрического поля
Описание электрического поля Определение оптической силы и фокусного расстояния собирающей линзы
Определение оптической силы и фокусного расстояния собирающей линзы Использование теории размерностей для закрепления основ физический знаний
Использование теории размерностей для закрепления основ физический знаний Колебания
Колебания  Загрязнение воздуха отработавшими газами автомобилей
Загрязнение воздуха отработавшими газами автомобилей Жоғарғы жиілікті разрядты зерттеудің маңыздылығы. Айнымалы электр өрісіндегі разрядтардың түрлері
Жоғарғы жиілікті разрядты зерттеудің маңыздылығы. Айнымалы электр өрісіндегі разрядтардың түрлері Измерения абсолютного значения мощности СВЧ излучения в экспериментах по напылению веществ на пластины кварца и молибдена
Измерения абсолютного значения мощности СВЧ излучения в экспериментах по напылению веществ на пластины кварца и молибдена Презентация Электрические явления в атмосфере
Презентация Электрические явления в атмосфере ПРИМЕНЕНИЕ ЯДЕРНОЙ ЭНЕРГИИ Учащиеся 9 класса: Смолич В. Максимова Н. Учитель: Донская Л.Н.
ПРИМЕНЕНИЕ ЯДЕРНОЙ ЭНЕРГИИ Учащиеся 9 класса: Смолич В. Максимова Н. Учитель: Донская Л.Н.  Синтез зубчатых передач
Синтез зубчатых передач Кернеу бойынша іске қосылатын электрберіліс желісінің максималды ток қорғанысы
Кернеу бойынша іске қосылатын электрберіліс желісінің максималды ток қорғанысы Действия водителя в нештатных (критических) режимах движения
Действия водителя в нештатных (критических) режимах движения Электрическое поле в вакууме. Электромагнитное поле - материальный носитель электромагнитного взаимодействия
Электрическое поле в вакууме. Электромагнитное поле - материальный носитель электромагнитного взаимодействия Лекція 6. Визначення напружень при згинанні. Умови міцності при згинанні
Лекція 6. Визначення напружень при згинанні. Умови міцності при згинанні Важнейшие открытия в современном естествознании. Высокотемпературная сверхпроводимость (ВТСП).
Важнейшие открытия в современном естествознании. Высокотемпературная сверхпроводимость (ВТСП). Ветровой электрогенератор challenergy
Ветровой электрогенератор challenergy Проектно-исследовательская работа «Воздушный змей»
Проектно-исследовательская работа «Воздушный змей» Элементарные частицы
Элементарные частицы Презентация по физике тема « Линзы » Учитель: Деднева О.В. Школа № 770 ЮАО г.Москвы
Презентация по физике тема « Линзы » Учитель: Деднева О.В. Школа № 770 ЮАО г.Москвы