Содержание
- 2. Отличительной чертой термодинамики является введение в совокупность исследуемых видов энергии внутренней энергии тел, что собственно и
- 3. Как известно одним из фундаментальных законов природы является закон сохранения энергии, который гласит «энергия не исчезает
- 4. Термодинамика – это наука о закономерностях превращения энергии в теплоту или работу. Теплота является одним из
- 5. Под процессом совершения работы понимается такой процесс взаимодействия какого-либо тела с другими телами, в результате которого
- 6. Так как, работа является формой энергии в процессе перемещения под действием силы. Действие силы может быть
- 7. Сказанное можно записать уравнением: Q1-2 = ∆U1-2 + L1-2, где Q1-2 – теплота, сообщённая телу при
- 8. Для элементарного изменения состояния системы первый закон термодинамики запишется как δQ = dU + δA или
- 9. Следует отметить, что термодинамика рассматривает определенные системы, так называемые термодинамические системы. Под термодинамической системой понимают совокупность
- 10. Термодинамическая система, внутри которой нет поверхностей раздела, отделяющих друг от друга макроскопические части системы, различающихся по
- 11. Совокупность всех гомогенных частей термодинамической системы, которые в отсутствие внешнего силового воздействия являются физически однородными, называется
- 12. Для исследования термодинамических систем используется термодинамический метод, суть которого заключается в изучении свойств системы взаимодействующих тел
- 13. ПАРАМЕТРЫ СОСТОЯНИЯ Основными параметрами состояния являются давление, температура и удельный (или молярный) объём. Давлением называется физическая
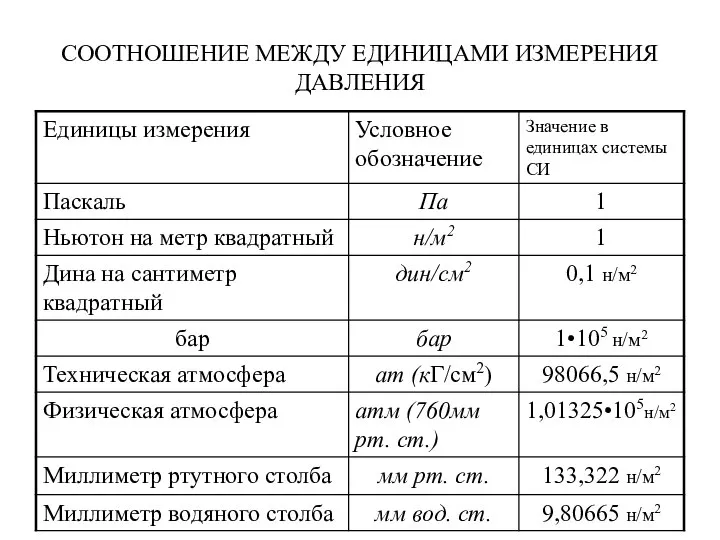
- 14. СООТНОШЕНИЕ МЕЖДУ ЕДИНИЦАМИ ИЗМЕРЕНИЯ ДАВЛЕНИЯ
- 15. Температура – это физическая величина, характеризующая степень нагретости тела т.е. температура характеризует тепловое состояние тела. Измерение
- 16. Шкала Фаренгейта: за начальную точку отсчёта принята (tо =32ºF = 0ºС), за конечную – (tк =
- 17. Уравнение взаимосвязи давления, температуры, удельного объёма называется уравнением состояния. рv = RT, где R – универсальная
- 18. Для каждого вещества характер функциональной связи между р, v и Т индивидуален и, следовательно, термодинамические свойства
- 19. Теплоемкость. Классификация, соотношения различных теплоемкостей. Теплоёмкость (истинная теплоёмкость) вещества называется отношение элементарного количества тепла δQ, сообщённого
- 20. Функцией состояния Состояния термодинамической системы определяется функцией состояния – это такая физическая характеристика системы, изменение которой
- 21. Внутренней энергий U называется энергия системы, зависящая только от её термодинамического состояния. Внутренняя энергия системы равна
- 22. Энтальпией Н (теплосодержанием, тепловой функцией) называется функция состояния термодинамической системы, равная сумме её внутренней энергии и
- 23. Энтропией S называется функция состояния системы, дифференциал которой в элементарном обратимом процессе равен отношению бесконечно малого
- 24. Изохорно-изотермическим потенциалом называется характеристическая функция состояния системы F = U –ТS при независимых переменных Т и
- 25. ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ Если изменять внешние условия, в которых находится термодинамическая система, то будет изменяться и состояние
- 26. Особенности характера каждого из процессов изменения состояния тела определяются теми конкретными физическими условиями, в которых протекает
- 27. Среди различных термодинамических процессов особый интерес представляют так называемые замкнутые или круговые процессы, при которых система,
- 28. ИЗОХОРНЫЙ ПРОЦЕСС Изохорический процесс, при котором объем тела остается в течение всего, процесса неизменным (V =
- 29. Уравнение состояния идеального газа на изохоре запишется рV = RT отсюда (р/Т) = const следовательно для
- 30. Для того чтобы определить параметры состояния 2, нужно знать один из параметров в точке 2 (например,
- 31. Работа расширения системы в изохорном процессе равна нулю. Из соотношения l1-2 = ∫ р dv ,
- 32. Если воспользоваться понятием о средней теплоемкости cvср, то это соотношение можно представить в следующем виде: q2-1
- 33. Если теплоемкость в рассматриваемом интервале температур постоянна (и, следовательно, cv можно вынести за знак интеграла), получаем
- 34. ИЗОБАРНЫЙ ПРОЦЕСС Изобарический процесс, протекающий в условиях постоянного давления на тело (р = const). Если изобарный
- 35. Отсюда следует, что чем выше температура газа, тем больше его удельный объем (т. е. тем меньше
- 36. Количество теплоты, сообщаемой системе при нагреве (или отдаваемой системой при охлаждении) в изобарном процессе, определяется следующим
- 37. Из очевидного соотношения Т2 Т2 h2 (р, Т2) - h1 (р, Т1) = ∫ [(∂h /∂T)]р
- 38. Изменение энтропии в изобарном процессе, т. е. разность энтропий, соответствующих состояниям 1 и 2, определяется из
- 39. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС Изотермический процесс, характеризующийся постоянством температуры тела во время процесса (Т = const). Если известны
- 40. Важно подчеркнуть, что у любых веществ величина (dv/dp)T не может быть положительной и, следовательно, всюду на
- 41. Как следует из приведенного уравнения, работа системы в изотермическом процессе равна убыли свободной энергии системы. Таким
- 42. Изменение энтропии в изотермическом процессе, т. е. разность энтропий, соответствующих состояниям 1 и 2, вычисляется по
- 43. Для идеального газа (dv/dT)p = (R / р); (др/дТ)v = (R / v). Отсюда получаем s2
- 44. АДИАБАТНЫЙ ПРОЦЕСС Адиабатический процесс, когда тело помещено в теплоизолирующую оболочку, не допускающую теплообмена между телом и
- 45. В реальных условиях процесс является адиабатным в тех случаях, когда система снабжена хорошей теплоизоляцией или когда
- 46. Течение газа в этом случае будет адиабатным, так как извне к газу не подводится и от
- 47. Для определения связи между собой параметров различных состояний в обратимом адиабатном процессе определим дифференциальное уравнение изоэнтропного
- 48. термических свойств (р и v) в изоэнтропном процессе. Введем следующее обозначение: k = (∂h/∂u)s Будем называть
- 49. Если в рассматриваемом интервале изменения состояния системы (между точками 1 и 2) показатель изоэнтропы k остается
- 50. Таким образом, для любого состояния системы в изоэнтропном процессе (при условии, что показатель изоэнтропы k остается
- 51. Для твердых тел и жидкостей k весьма велико, причем значение k заметно изменяется с температурой. Так,
- 52. Приведенное уравнение справедливо не только для изоэнтропного, т.е. обратимого адиабатного процесса, но и не обратимого адиабатного
- 53. T2 Отсюда l1-2 = ∫ сv dT. T1 Если пренебречь зависимостью теплоемкости cv идеального газа от
- 54. ПОЛИТРОПНЫЕ ПРОЦЕССЫ Политропными называют термодинамические процессы, удовлетворяющие уравнению pvn = const при произвольном, постоянном для данного
- 55. Понятие о политропных процессах было введено в термодинамике по аналогии с понятием об адиабатных процессах. Уравнение
- 56. Реальные процессы сжатия в газовых двигателях и компрессорах часто не являются ни адиабатными, ни изотермическими, а
- 57. Помимо уже отмеченной нами технической целесообразности введение понятия политропного процесса представляет большую ценность и в методическом
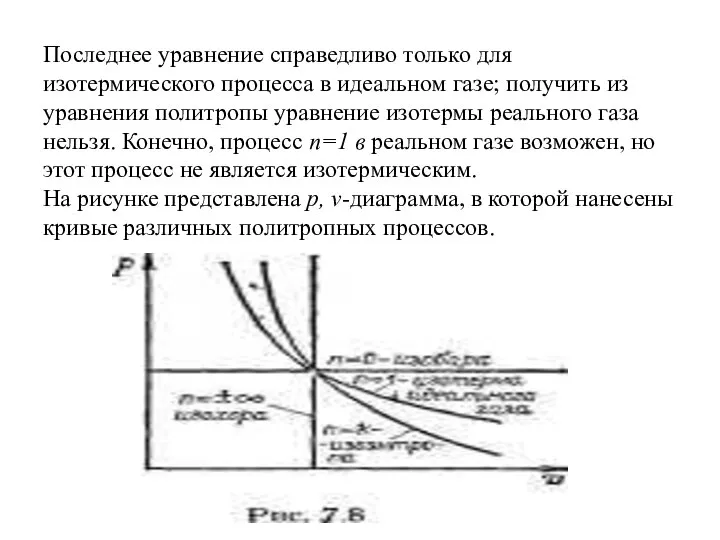
- 58. Последнее уравнение справедливо только для изотермического процесса в идеальном газе; получить из уравнения политропы уравнение изотермы
- 59. Работа расширения системы в политропном процессе между точками 1 в 2 определяется с помощью уравнения 2
- 60. T2 v2 q2-1 = ∫ сv dT + ∫ [Т(∂р/∂Т)v - р]∂v T1 v1 Для расчетов
- 61. Для идеального газа отношение теплоемкости ср к cv представляет собой показатель изоэнтропы идеального газа kид=cр /
- 62. Если теплоемкость сп в рассматриваемом интервале параметров между точками 1 и 2 сохраняется постоянной, то получаем
- 63. ДРОССЕЛИРОВАНИЕ. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА Из опыта известно, что если на пути струи газа или жидкости,
- 64. С процессом дросселирования приходится часто сталкиваться на практике, например при движении воды через неполностью открытый водопроводный
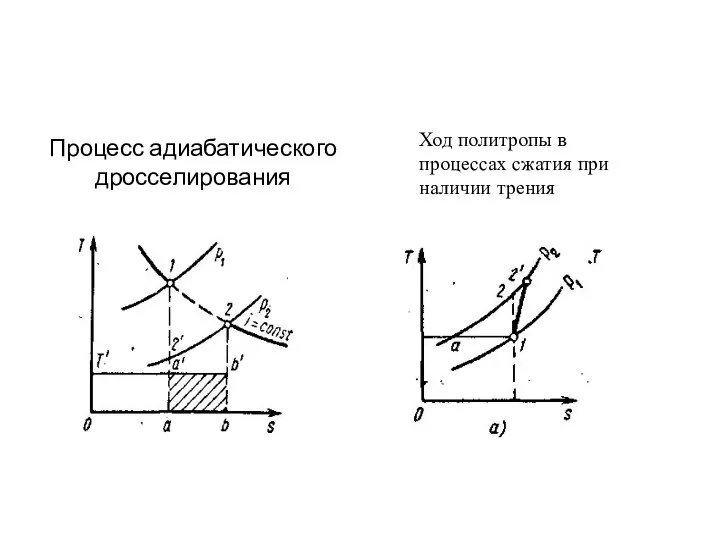
- 65. Процесс адиабатического дросселирования
- 67. Скачать презентацию





























































 Изотопная геология (введение)
Изотопная геология (введение) Диэлектрические потери
Диэлектрические потери Импульс, энергия, законы сохранения. Решение задач
Импульс, энергия, законы сохранения. Решение задач Классификация методов синтеза наноматериалов
Классификация методов синтеза наноматериалов Презентація з фізичного практикуму на тему:”Фізика й науково-технічний прогрес” підготувала: учениця 11-А класу Харківської ЗОШ І-ІІІ ст №102 Антіпова Марія
Презентація з фізичного практикуму на тему:”Фізика й науково-технічний прогрес” підготувала: учениця 11-А класу Харківської ЗОШ І-ІІІ ст №102 Антіпова Марія  Презентация по физике "Напряжение" - скачать
Презентация по физике "Напряжение" - скачать  Зубчатые передачи
Зубчатые передачи Нагревание проводников электрическим током. Закон Джоуля-Ленца
Нагревание проводников электрическим током. Закон Джоуля-Ленца Штормгласс - предсказатель бурь
Штормгласс - предсказатель бурь Передача и использование электроэнергии
Передача и использование электроэнергии Электрическое поле. (лекция 1а)
Электрическое поле. (лекция 1а) Механическое движение и его виды
Механическое движение и его виды Действие магнитного поля на проводник с током. Электрический двигатель
Действие магнитного поля на проводник с током. Электрический двигатель Физические основы термодинамики
Физические основы термодинамики Теплопроводность при наличии внутренних источников теплоты
Теплопроводность при наличии внутренних источников теплоты Ультразвук и инфразвук в природе
Ультразвук и инфразвук в природе Вес воздуха. Атмосферное давление. Выполнил: студент 4 курса Специальность физика Д.Е. Таргоний
Вес воздуха. Атмосферное давление. Выполнил: студент 4 курса Специальность физика Д.Е. Таргоний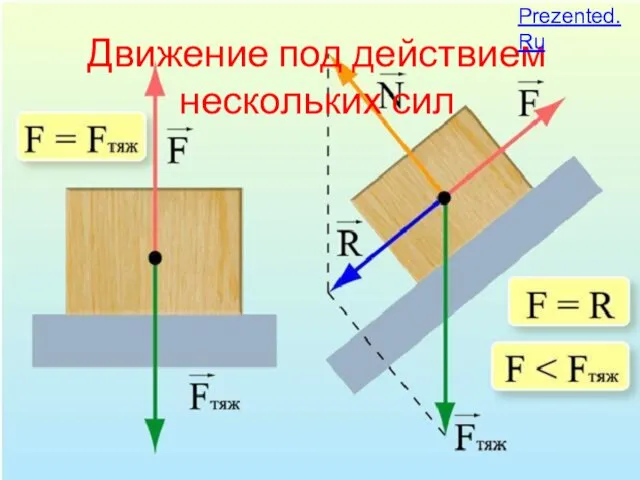 Движение под действием нескольких сил
Движение под действием нескольких сил Современные проблемы технической физики. Самые дорогие научные проекты
Современные проблемы технической физики. Самые дорогие научные проекты Макс Карл Эрнст Людвиг Планк (23.05.1858-04.10.1947)
Макс Карл Эрнст Людвиг Планк (23.05.1858-04.10.1947) Лабораторные работы по физике 8 класс
Лабораторные работы по физике 8 класс Принципы радиосвязи. (8 класс)
Принципы радиосвязи. (8 класс) Индикаторлық галоидты жанарғы
Индикаторлық галоидты жанарғы Электрическое поле
Электрическое поле ПРОЕКТ «Определение средней скорости моего движения.» Выполнил ученик 7Б класса
ПРОЕКТ «Определение средней скорости моего движения.» Выполнил ученик 7Б класса  Светодиодные лампы
Светодиодные лампы Внутренняя энергия. Термодинамика
Внутренняя энергия. Термодинамика Термодинамика поверхностных явлений. (Часть 2)
Термодинамика поверхностных явлений. (Часть 2)