Содержание
- 2. Последовательность изменений состояния системы составляет термодинамический процесс. Всякий процесс изменения состояния системы представляет собой отклонение от
- 3. Предельным понятием является вполне равновесный процесс, который представляет собой совокупность последовательно проходимых системой состояний равновесия. Степень
- 4. Особенности характера каждого из процессов изменения состояния тела определяются теми конкретными физическими условиями, в которых протекает
- 5. Среди различных термодинамических процессов особый интерес представляют так называемые замкнутые или круговые процессы, при которых система,
- 6. ИЗОХОРНЫЙ ПРОЦЕСС Изохорический процесс, при котором объем тела остается в течение всего, процесса неизменным (V =
- 7. Параметры состояния идеального газа на изохоре связаны соотношением: p2 / р1 = Т2 / Т1. В
- 8. Детальное рассмотрение показывает, что в этой области температур изохоры воды имеют вид, показанный на рис. 7.2;
- 9. Работа расширения системы в изохорном процессе равна нулю. Из соотношения l1-2 = ∫ р dv ,
- 10. Если воспользоваться понятием о средней теплоемкости cvср, то это соотношение можно представить в следующем виде: q2-1
- 11. Если теплоемкость в рассматриваемом интервале температур постоянна (и, следовательно, cv можно вынести за знак интеграла), получаем
- 12. ИЗОБАРНЫЙ ПРОЦЕСС Изобарический процесс, протекающий в условиях постоянного давления на тело (р = const). Если изобарный
- 13. Отсюда следует, что чем выше температура газа, тем больше его удельный объем (т. е. тем меньше
- 14. Количество теплоты, сообщаемой системе при нагреве (или отдаваемой системой при охлаждении) в изобарном процессе, определяется следующим
- 15. Из очевидного соотношения Т2 Т2 h2 (р, Т2) - h1 (р, Т1) = ∫ [(∂h /∂T)]р
- 16. Изменение энтропии в изобарном процессе, т. е. разность энтропий, соответствующих состояниям 1 и 2, определяется из
- 17. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС Изотермический процесс, характеризующийся постоянством температуры тела во время процесса (Т = const). Если известны
- 18. Важно подчеркнуть, что у любых веществ величина (dv/dp)T не может быть положительной и, следовательно, всюду на
- 19. Как следует из приведенного уравнения, работа системы в изотермическом процессе равна убыли свободной энергии системы. Таким
- 20. Изменение энтропии в изотермическом процессе, т. е. разность энтропий, соответствующих состояниям 1 и 2, вычисляется по
- 21. Для идеального газа (dv/dT)p = (R / р); (др/дТ)v = (R / v). Отсюда получаем s2
- 22. АДИАБАТНЫЙ ПРОЦЕСС Адиабатический процесс, когда тело помещено в теплоизолирующую оболочку, не допускающую теплообмена между телом и
- 23. В реальных условиях процесс является адиабатным в тех случаях, когда система снабжена хорошей теплоизоляцией или когда
- 24. Течение газа в этом случае будет адиабатным, так как извне к газу не подводится и от
- 25. Для определения связи между собой параметров различных состояний в обратимом адиабатном процессе определим дифференциальное уравнение изоэнтропного
- 26. термических свойств (р и v) в изоэнтропном процессе. Введем следующее обозначение: k = (∂h/∂u)s Будем называть
- 27. Если в рассматриваемом интервале изменения состояния системы (между точками 1 и 2) показатель изоэнтропы k остается
- 28. Таким образом, для любого состояния системы в изоэнтропном процессе (при условии, что показатель изоэнтропы k остается
- 29. Для твердых тел и жидкостей k весьма велико, причем значение k заметно изменяется с температурой. Так,
- 30. Приведенное уравнение справедливо не только для изоэнтропного, т.е. обратимого адиабатного процесса, но и не обратимого адиабатного
- 31. T2 Отсюда l1-2 = ∫ сv dT. T1 Если пренебречь зависимостью теплоемкости cv идеального газа от
- 32. ПОЛИТРОПНЫЕ ПРОЦЕССЫ Политропными называют термодинамические процессы, удовлетворяющие уравнению pvn = const при произвольном, постоянном для данного
- 33. Понятие о политропных процессах было введено в термодинамике по аналогии с понятием об адиабатных процессах. Уравнение
- 34. Реальные процессы сжатия в газовых двигателях и компрессорах часто не являются ни адиабатными, ни изотермическими, а
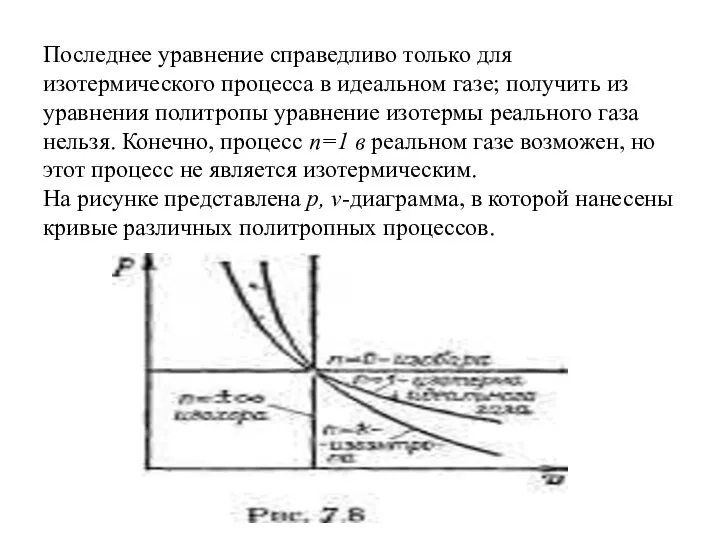
- 35. Помимо уже отмеченной нами технической целесообразности введение понятия политропного процесса представляет большую ценность и в методическом
- 36. Последнее уравнение справедливо только для изотермического процесса в идеальном газе; получить из уравнения политропы уравнение изотермы
- 37. Работа расширения системы в политропном процессе между точками 1 в 2 определяется с помощью уравнения 2
- 38. T2 v2 q2-1 = ∫ сv dT + ∫ [Т(∂р/∂Т)v - р]∂v T1 v1 Для расчетов
- 39. Для идеального газа отношение теплоемкости ср к cv представляет собой показатель изоэнтропы идеального газа kид=cр /
- 40. Если теплоемкость сп в рассматриваемом интервале параметров между точками 1 и 2 сохраняется постоянной, то получаем
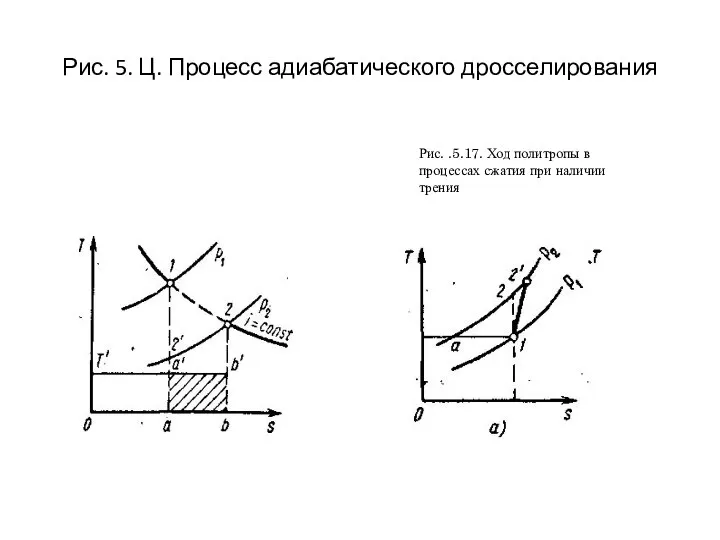
- 41. ДРОССЕЛИРОВАНИЕ. ЭФФЕКТ ДЖОУЛЯ — ТОМСОНА Из опыта известно, что если на пути струи газа или жидкости,
- 42. С процессом дросселирования приходится часто сталкиваться на практике, например при движении воды через неполностью открытый водопроводный
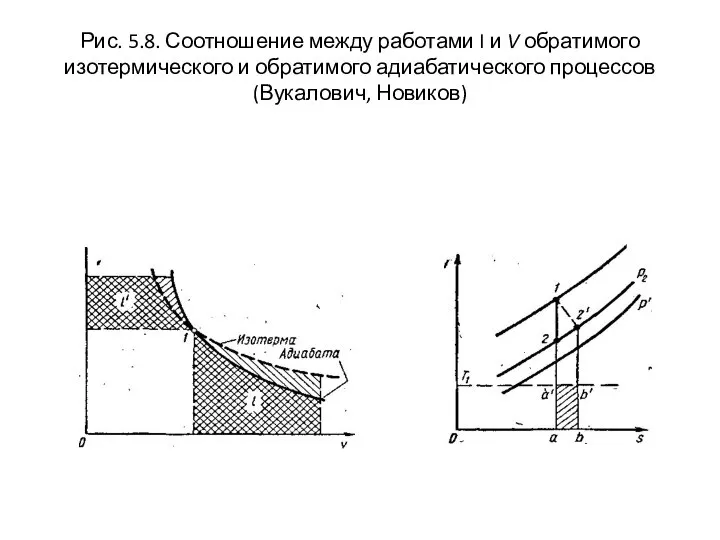
- 43. Рис. 5.8. Соотношение между работами I и V обратимого изотермического и обратимого адиабатического процессов (Вукалович, Новиков)
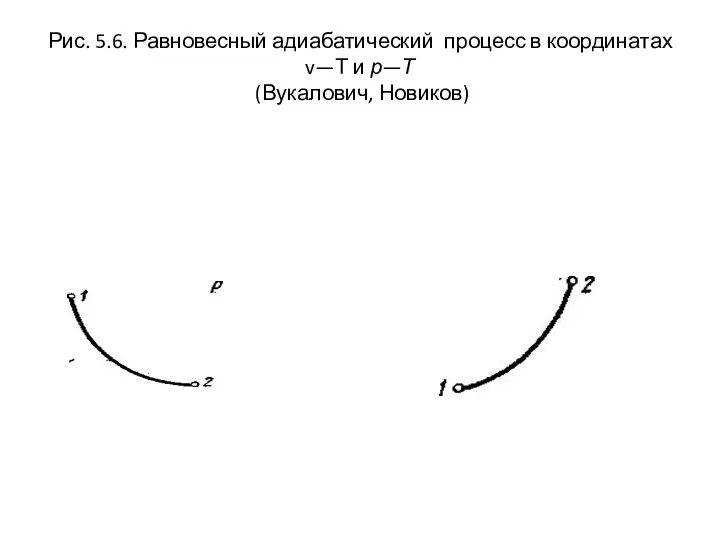
- 44. Рис. 5.6. Равновесный адиабатический процесс в координатах v—Т и р—Т (Вукалович, Новиков)
- 45. Рис. 5.2. Равновесный изотермический про- цесс в координатах р—Т и p—v
- 46. Рис. 5. Ц. Процесс адиабатического дросселирования
- 48. Скачать презентацию









































 Казанский университет. Институт физики
Казанский университет. Институт физики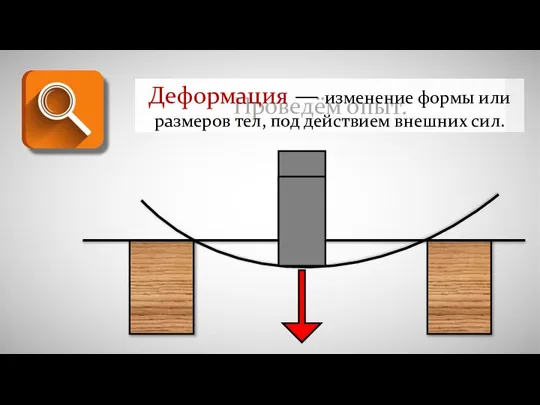 Деформация - изменение формы или размеров тел под действием внешних сил
Деформация - изменение формы или размеров тел под действием внешних сил Енергія електричного поля
Енергія електричного поля Полупроводниковые приборы
Полупроводниковые приборы Понятие термодинамики
Понятие термодинамики Проводники в электростатическом поле
Проводники в электростатическом поле Тема: Простые механизмы. Работа ученика 7 «в» СОШ №7 г.Якутска Филиппова Юры Руководитель проекта А.П.Филиппова
Тема: Простые механизмы. Работа ученика 7 «в» СОШ №7 г.Якутска Филиппова Юры Руководитель проекта А.П.Филиппова Теплота парообразования. Сжижение газов. Влажность воздуха
Теплота парообразования. Сжижение газов. Влажность воздуха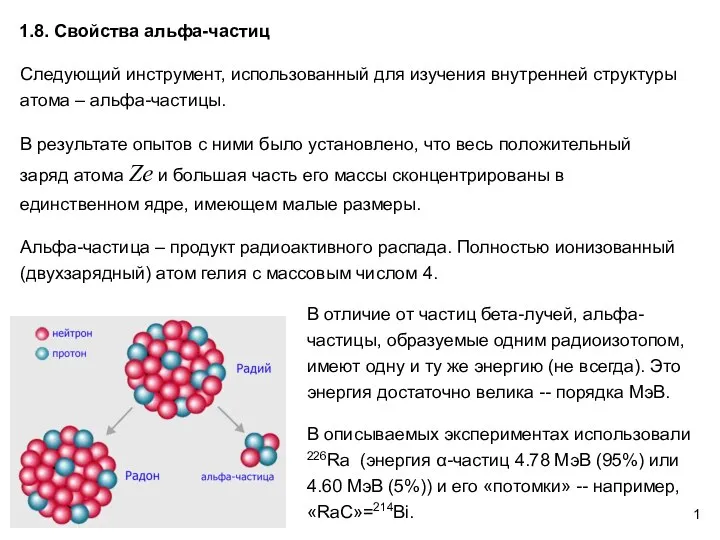 Свойства альфа-частиц. АФ1.8
Свойства альфа-частиц. АФ1.8 Нейтрон и его свойства
Нейтрон и его свойства מתקני הרמה ושינוע הרצאה :מתקני הרמה. כבלים ,חבלים ,שרשרות
מתקני הרמה ושינוע הרצאה :מתקני הרמה. כבלים ,חבלים ,שרשרות Команда «По» представляет: Закон сохранения импульса. Реактивное движение
Команда «По» представляет: Закон сохранения импульса. Реактивное движение Электростатика. Электрический заряд
Электростатика. Электрический заряд Электрическое поле. Законы постоянного тока
Электрическое поле. Законы постоянного тока Проект по физике на тему: «Экология, энергетика, человек»
Проект по физике на тему: «Экология, энергетика, человек» Модель атома Резерфорда Ядерная или Планетарная модель атома Вонс Диана и Тарамова Айза 10«Б»
Модель атома Резерфорда Ядерная или Планетарная модель атома Вонс Диана и Тарамова Айза 10«Б»  Лазер. История создания лазера. Устройство лазера. Применение лазера
Лазер. История создания лазера. Устройство лазера. Применение лазера Система и окружающая среда
Система и окружающая среда Контактные явления
Контактные явления Неньютоновские жидкости
Неньютоновские жидкости Дипломный проект. Ремонт, мотаж и эксплуатация домкратов
Дипломный проект. Ремонт, мотаж и эксплуатация домкратов Вычисления массы и массовой доли растворенного вещества (11 класс)
Вычисления массы и массовой доли растворенного вещества (11 класс) Презентация по физике "Радиация и её влияние на окружающую среду" - скачать
Презентация по физике "Радиация и её влияние на окружающую среду" - скачать  Теплообмен излучением между телами, разделённой прозрачной средой. Коэффициент облучённости. Теплообмен между телами
Теплообмен излучением между телами, разделённой прозрачной средой. Коэффициент облучённости. Теплообмен между телами Количественный анализ. Хроматографические методы
Количественный анализ. Хроматографические методы Тепловые процессы. Теплообменники. Нагрев острым паром
Тепловые процессы. Теплообменники. Нагрев острым паром Презентация по физике Электромагнитная индукция. Опыты Фарадея Подготовка к ГИА
Презентация по физике Электромагнитная индукция. Опыты Фарадея Подготовка к ГИА  Презентация Законы преломления.
Презентация Законы преломления.