Содержание
- 2. Цели урока: 1. Закрепление знаний об идеальном газе, изопроцессах. 2. Формирование умений решения задач на применение
- 3. Газовые законы Учебная презентация для 10 класса
- 4. Проверка P давление V объем T температура
- 5. Макроскопические параметры Параметры, характеризующие состояние газа без учета его молекулярного строения, называются макроскопическими. ? Назовите эти
- 6. Изопроцессы Процессы, протекающие в термодинамической системе при одном неизменном макроскопическом параметре когда два других изменяются, называются
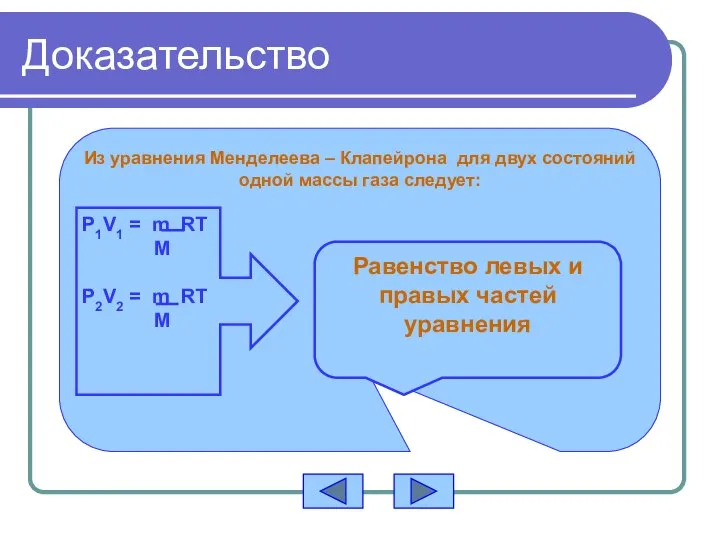
- 7. Доказательство Из уравнения Менделеева – Клапейрона для двух состояний одной массы газа следует: P1V1 = m
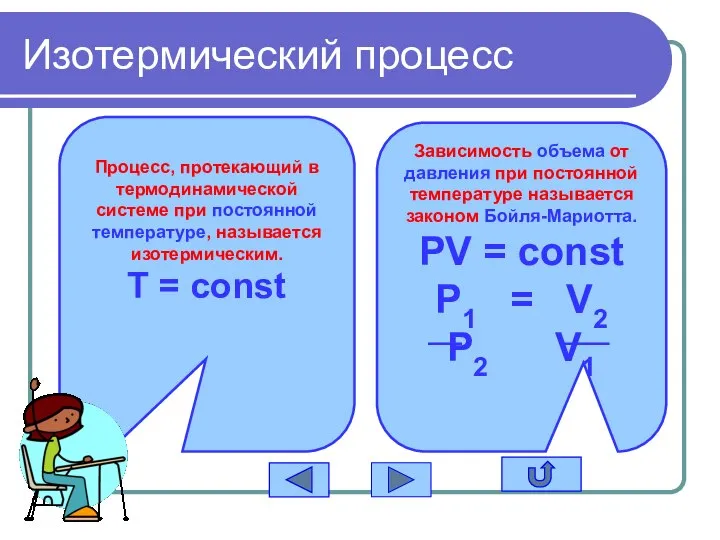
- 8. Изотермический процесс Процесс, протекающий в термодинамической системе при постоянной температуре, называется изотермическим. T = const Зависимость
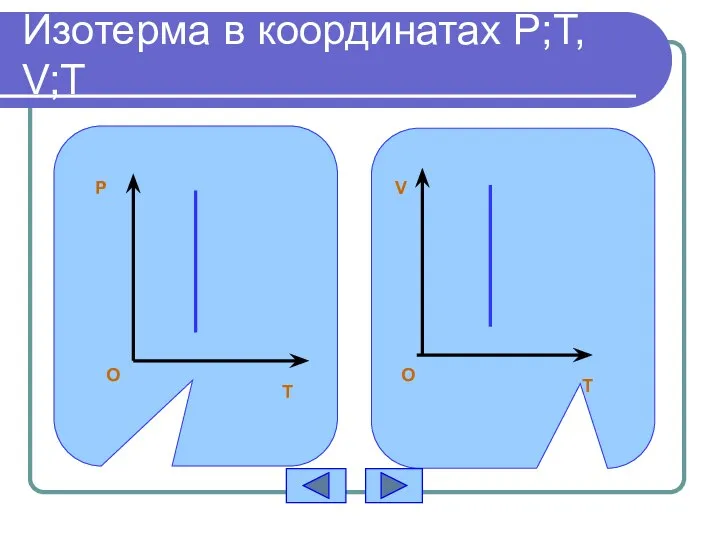
- 9. Изотерма в координатах P;T, V;T P T O T V O
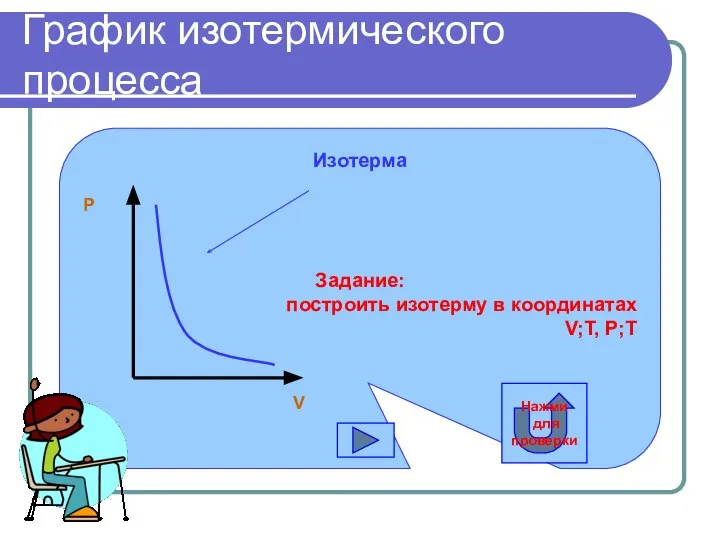
- 10. График изотермического процесса Изотерма Задание: построить изотерму в координатах V;T, P;T V P Нажми для проверки
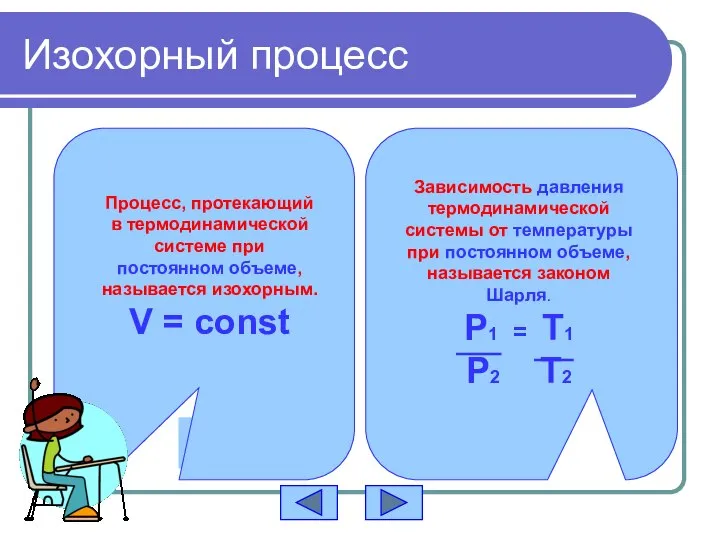
- 11. Изохорный процесс Процесс, протекающий в термодинамической системе при постоянном объеме, называется изохорным. V = const Зависимость
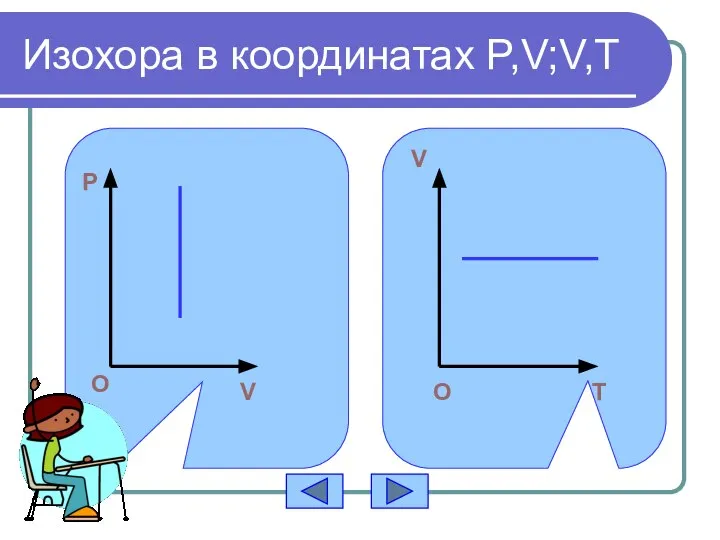
- 12. Изохора в координатах P,V;V,T О T V O O O
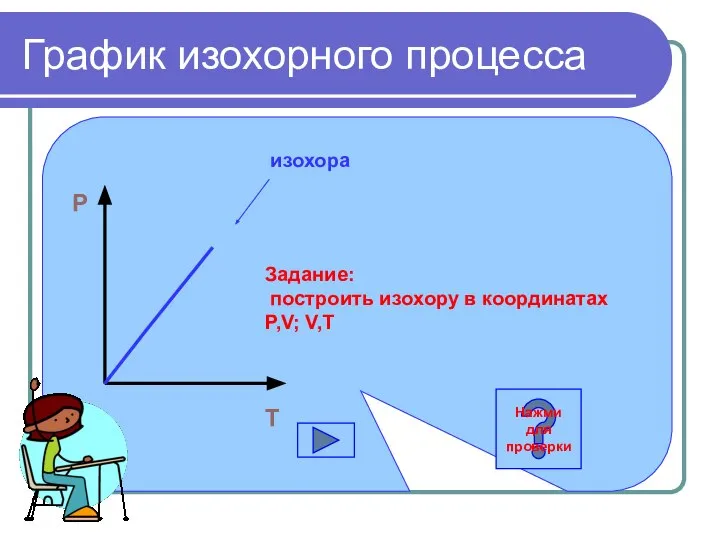
- 13. График изохорного процесса P O T изохора Задание: построить изохору в координатах P,V; V,T Нажми для
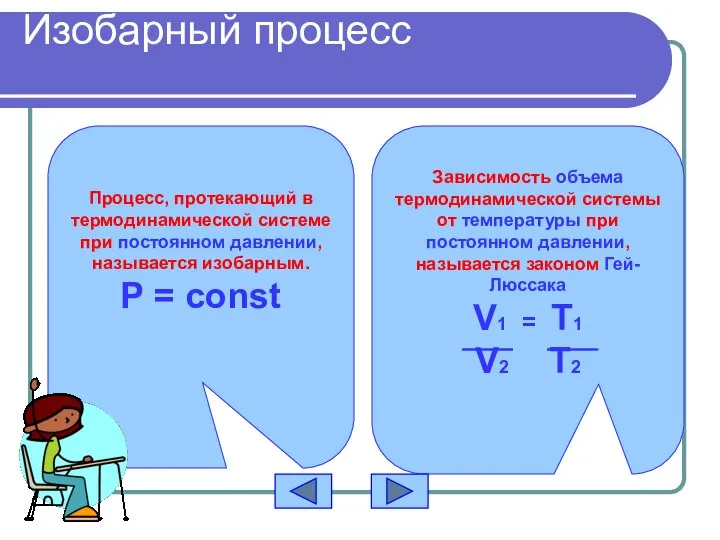
- 14. Изобарный процесс Процесс, протекающий в термодинамической системе при постоянном давлении, называется изобарным. Р = const Зависимость
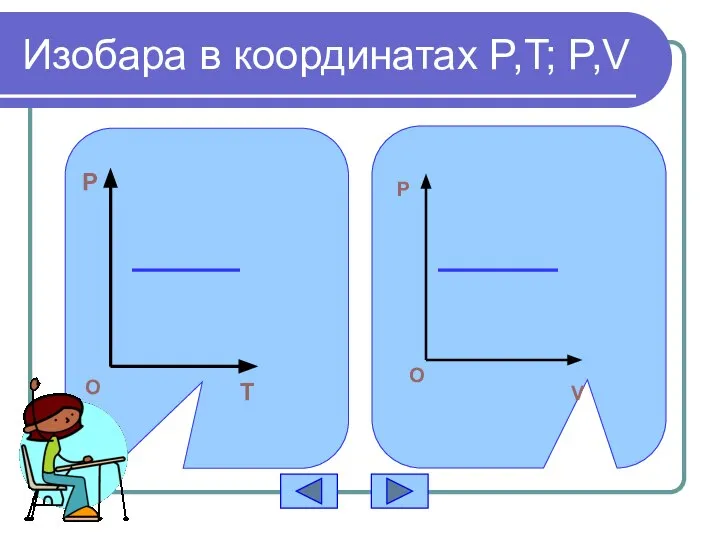
- 15. Изобара в координатах P,T; P,V P T O P O V
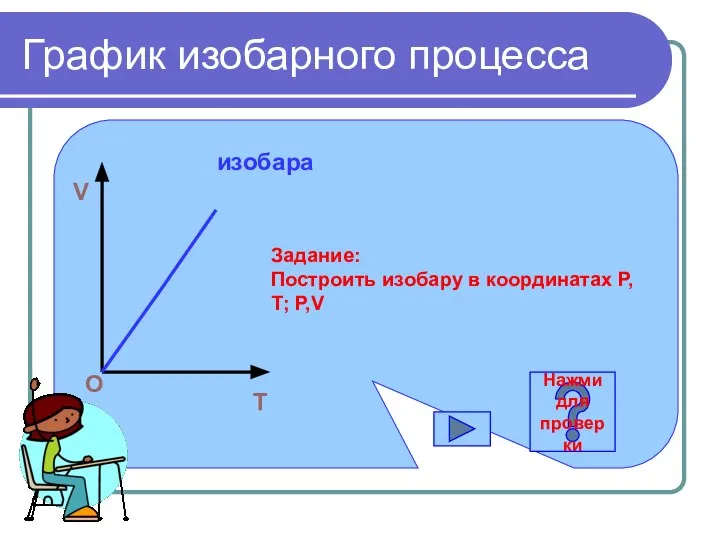
- 16. График изобарного процесса T V O изобара Задание: Построить изобару в координатах Р,Т; Р,V Нажми для
- 17. Подведем итог: P1 = V2 T = const, закон Бойля- Мариотта P2 V1 P1 = T1
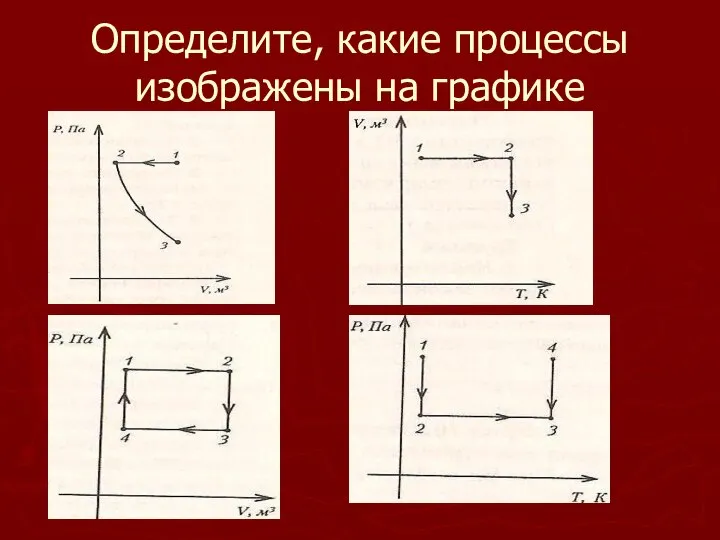
- 18. Определите, какие процессы изображены на графике
- 19. Графическое представление газовых процессов Базовый уровень 10 класс
- 20. Графики газовых процессов изображают в координатах p,V; p,T; V,T. Перед построением графика следует получить аналитическое выражение
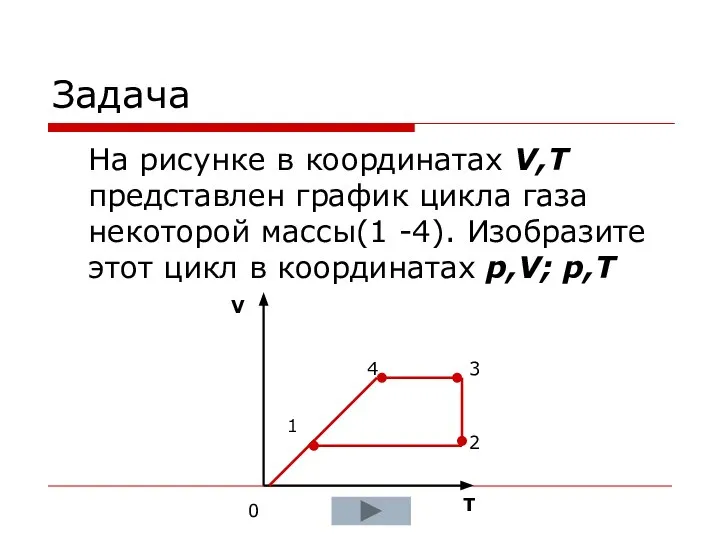
- 21. Задача На рисунке в координатах V,T представлен график цикла газа некоторой массы(1 -4). Изобразите этот цикл
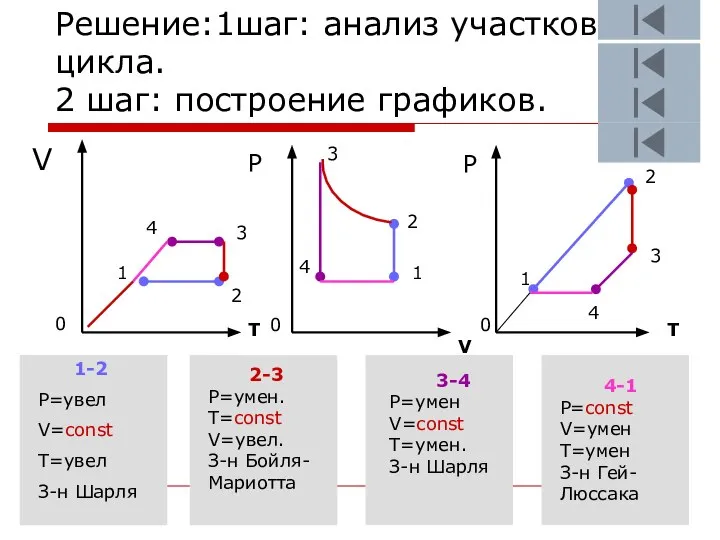
- 22. Решение:1шаг: анализ участков цикла. 2 шаг: построение графиков. V T V T Р Р 0 0
- 23. Участок 1-2 Перевод газа из состояния 1 в состояние 2 совершается при увеличении температуры и давления
- 24. Участок 2-3 Перевод газа из состояния 2 в состояние 3 совершается при постоянной температуре и если
- 25. Участок 3-4 Перевод газа из состояния 3 в состояние 4 совершается при уменьшении температуры и давления
- 26. Участок 4-1 Перевод газа из состояния 4 в состояние 1 совершается при уменьшении температуры и объема
- 27. Ученики школы Привидений: Каспер – водород, Микки – воздух, Олес – углекислый газ, Лулу – идеальный
- 28. Задача 1 Каспер решил отдохнуть и залез в банку объемом 20 л. Найдите давление Каспера, если
- 29. СИ: m= 4·10 -3 кг V= 2 ·10 -2 м3 T= 300 К M= 2·10 -3
- 30. Задача 2 Лулу, идеальную во всех отношениях, в темном коридоре подкараулили завидующие её фигуре Лоло и
- 31. Дано: Т1= Т Т2= 2Т р1= р Р2= 1,25р Решение:
- 32. Решение:
- 33. Задачи Задача Ивлевой Юли Задача о Марго Задача про трубку с ртутью Задача о Янеке Задача
- 34. Проверь свои знания по теме «Уравнение состояния идеального газа» Тренировочный тест
- 35. 1.Назови макроскопические параметры: Масса, давление, объем, температура давление, объем, температура
- 36. К макроскопическим параметрам идеального газа относятся: давление, объем и температура! P, V, T
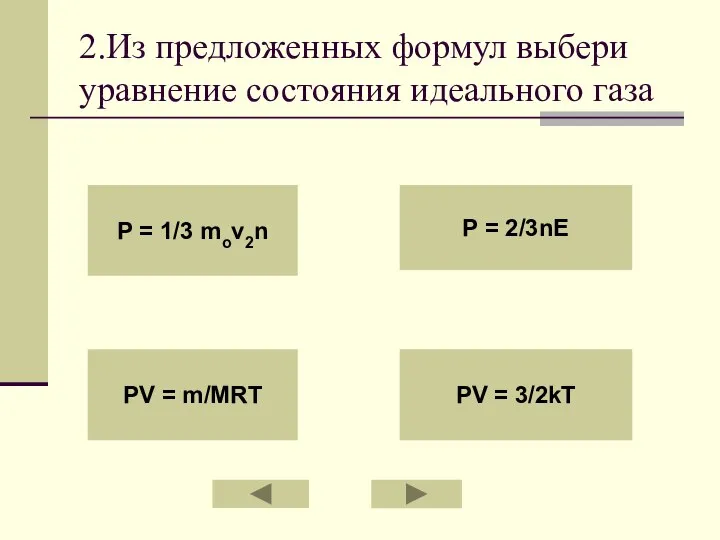
- 37. 2.Из предложенных формул выбери уравнение состояния идеального газа P = 1/3 mov2n PV = m/MRT P
- 38. Неправильно! Повтори теорию!
- 39. Молодец! Переходи к следующему вопросу
- 40. Неправильно! Повтори теорию!
- 41. Уравнением состояния идеального газа называется зависимость между макроскопическими параметрами: давлением, объемом и температурой! pv = m/MRT
- 42. Молодец! Переходи к следующему вопросу
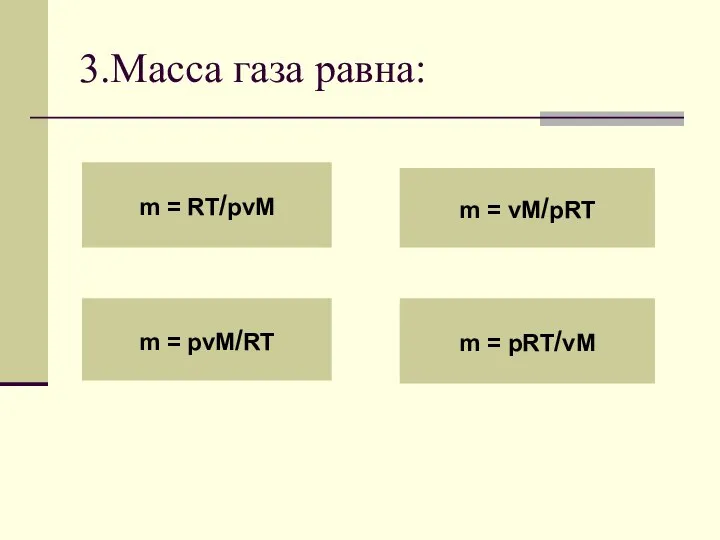
- 43. 3.Масса газа равна: m = RT/pvM m = pvM/RT m = vM/pRT m = pRT/vM
- 44. Молодец! Переходи к следующему вопросу
- 45. Неправильно! Повтори теорию!
- 46. Чтобы выразить неизвестную величину из уравнения Менделеева – Клапейрона, умножь левую и правую часть уравнения на
- 47. 4.Универсальная газовая постоянная равна: 6,022 *10 23 моль-1 1,38 * 10 – 23Дж/К 8,31 Дж/ (моль*К)
- 48. Неправильно! Повтори теорию!
- 49. Молодец! Переходи к следующему вопросу
- 50. Универсальной газовой постоянной называется произведение числа Авогадро и постоянной Больцмана: 6,02 * 1023 * 1,38 *
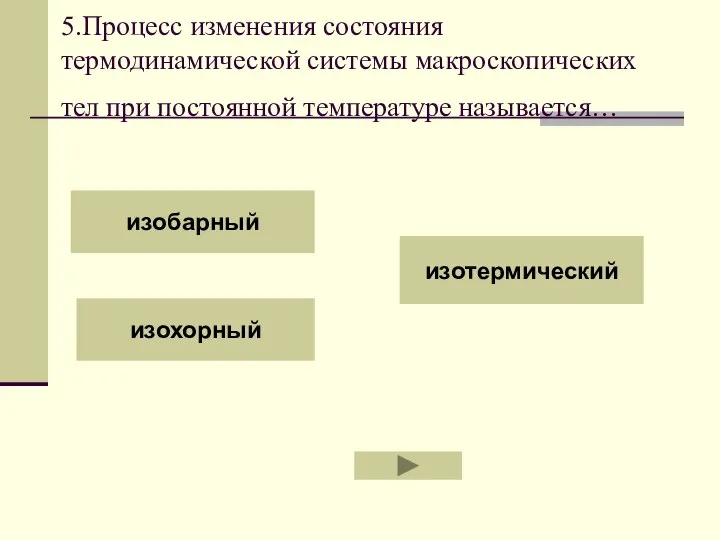
- 51. 5.Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называется… изобарный изохорный изотермический
- 52. Согласно уравнению состояния газа в любом состоянии с неизменной температурой произведение давления газа на его объем
- 53. Молодец! Переходи к следующему вопросу
- 54. Неправильно! Повтори теорию!
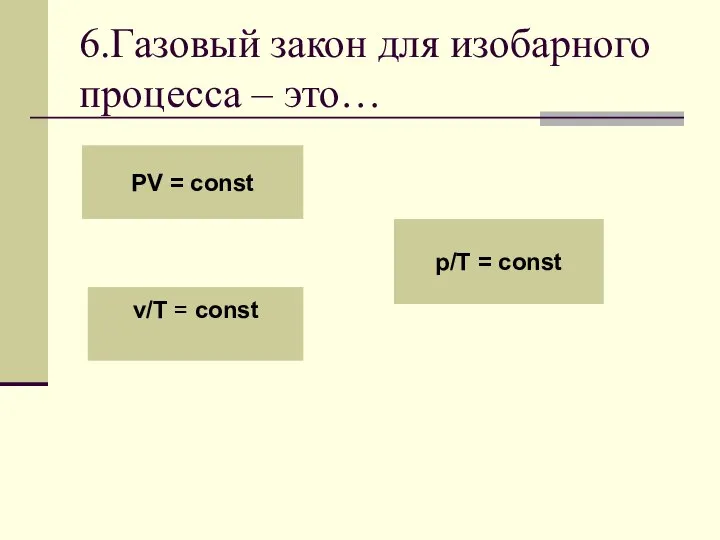
- 55. 6.Газовый закон для изобарного процесса – это… PV = const v/T = const p/T = const
- 56. Неправильно! Повтори теорию!
- 57. Молодец! Переходи к следующему вопросу
- 58. Для данной массы газа отношение объема к температуре постоянно, если давление газа не меняется. v/T =
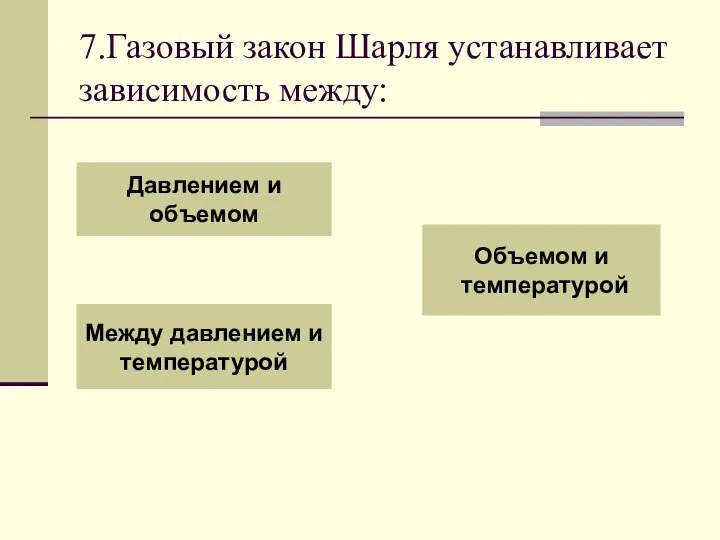
- 59. 7.Газовый закон Шарля устанавливает зависимость между: Давлением и объемом Между давлением и температурой Объемом и температурой
- 60. Повтори теорию! Неправильно!
- 61. Поздравляю! Переходи к следующему вопросу
- 62. Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным. Газовый закон Шарля. V = const.
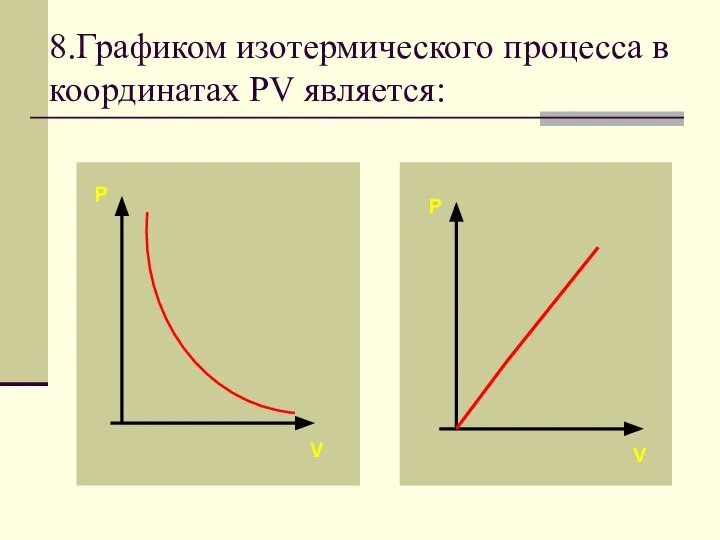
- 63. 8.Графиком изотермического процесса в координатах PV является: P P V V
- 64. Поздравляю! Переходи к следующему вопросу
- 65. Неправильно! Повтори теорию!
- 66. Зависимость между давлением и объемом в изотермическом процессе обратно пропорциональная. Графиком в координатах PV является изотерма
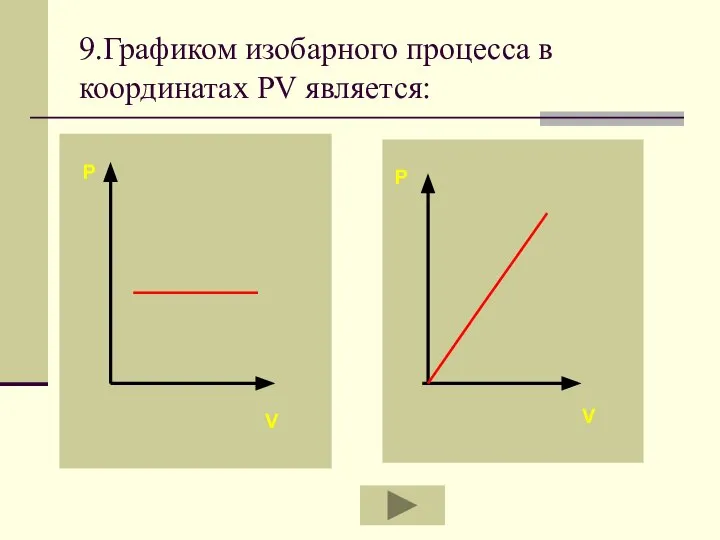
- 67. 9.Графиком изобарного процесса в координатах PV является: P V P V
- 68. Поздравляю! Переходи к следующему вопросу
- 69. Неправильно! Повтори теорию!
- 70. Если процесс изобарный давление постоянно, в координатах PV график прямая линия параллельная оси объема.
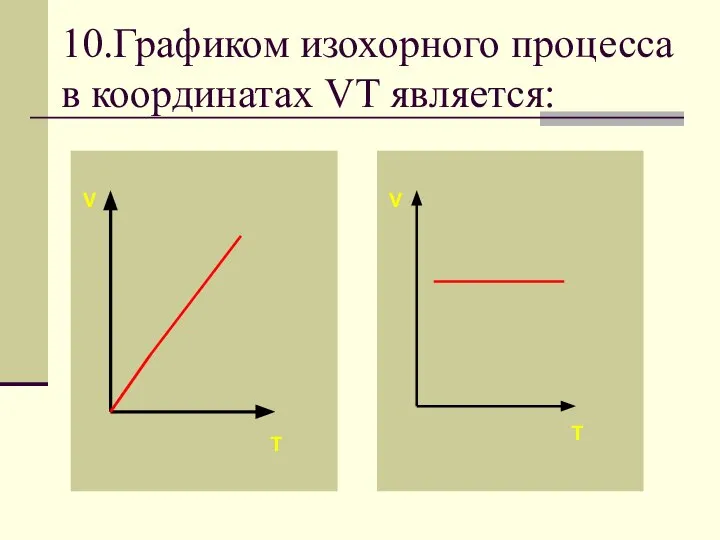
- 71. 10.Графиком изохорного процесса в координатах VT является: V V T T
- 72. Поздравляю! Переходи к следующему вопросу
- 73. Неправильно! Повтори теорию!
- 74. Если процесс изохорный объем постоянный, в координатах VT график - прямая линия параллельная оси температуры.
- 75. Реши задачу: Найди давление газа бутана (С4Н8) в баллоне для портативных газовых плит объемом 0,5 л
- 76. Поздравляю! Переходи к следующей задаче
- 77. Неправильно! Посмотри решение
- 78. Решение: Переведи единицы измерения объема, массы, температуры в СИ. Найди молярную массу бутана: M=(4*12 + 1*8)
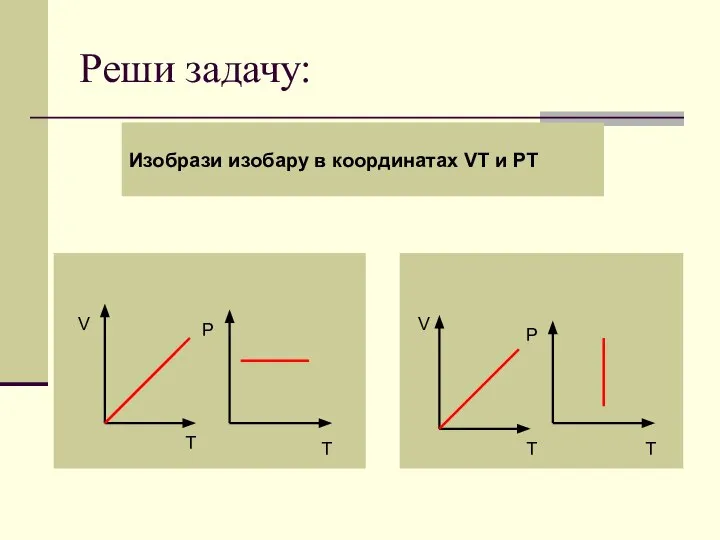
- 79. Реши задачу: Изобрази изобару в координатах VT и PT V T P T V T P
- 80. Поздравляю! Переходи к контрольному тесту
- 82. Скачать презентацию
















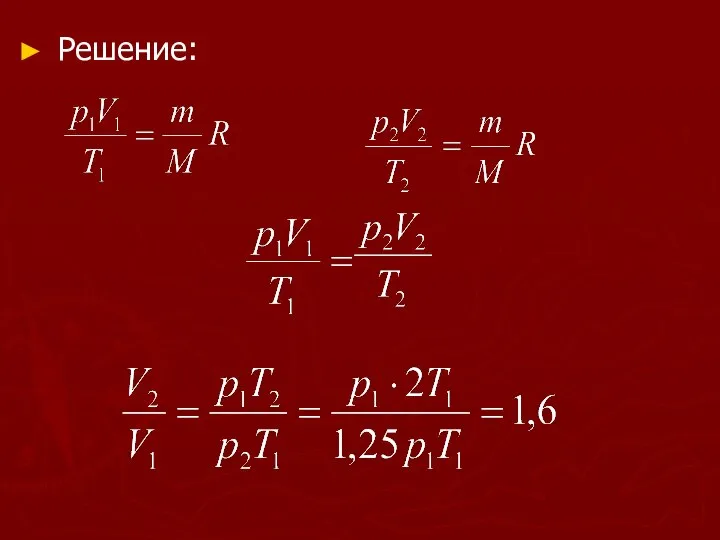







































 Свойства и применение радиоволн. (11 класс)
Свойства и применение радиоволн. (11 класс) Модели строения атома
Модели строения атома СТАТИКА Работу выполнили ученицы 10 класса А Средней школы № 288 Тимониной Галины, Скрылёвой Лины, Сев
СТАТИКА Работу выполнили ученицы 10 класса А Средней школы № 288 Тимониной Галины, Скрылёвой Лины, Сев Элементы специальной теории относительности
Элементы специальной теории относительности Электромагнитные явления
Электромагнитные явления Элементы механизации из КМ
Элементы механизации из КМ Презентация по физике "Понятие звука" - скачать
Презентация по физике "Понятие звука" - скачать  Изучение изображения предметов в тонкой линзе
Изучение изображения предметов в тонкой линзе Взаимодействие частиц и излучений с веществом
Взаимодействие частиц и излучений с веществом Непосредственные и косвенные измерения
Непосредственные и косвенные измерения Ортадан тепкіш сораптардың сипаттамалары
Ортадан тепкіш сораптардың сипаттамалары Северное сияние
Северное сияние Преломление света (11 класс)
Преломление света (11 класс) Elektriska piedzina. (№1)
Elektriska piedzina. (№1) Магнітний запис інформації
Магнітний запис інформації Ультрафиолетовое излучение
Ультрафиолетовое излучение Живой свет свечи
Живой свет свечи Рост наноструктур и микроскопия. Методы выращивания наноструктур
Рост наноструктур и микроскопия. Методы выращивания наноструктур Уравнение баланса мощности ВДК без аккумулирования
Уравнение баланса мощности ВДК без аккумулирования Лекция 02. Интерференция волн
Лекция 02. Интерференция волн Релейная защита электроэнергетических систем. Лекция 9
Релейная защита электроэнергетических систем. Лекция 9 Электротехника. Основные пояснения и термины
Электротехника. Основные пояснения и термины Физические основы телевидения
Физические основы телевидения  Расчет эквивалентных сопротивлений линейных бесконечных цепей
Расчет эквивалентных сопротивлений линейных бесконечных цепей Көміртекті нанотүтікше
Көміртекті нанотүтікше «Пітер ван Мушенбрук , та його винаходи»
«Пітер ван Мушенбрук , та його винаходи»  Проблемы прочности в технике
Проблемы прочности в технике Атомная физика
Атомная физика