Содержание
- 2. 5. Реальные газы.
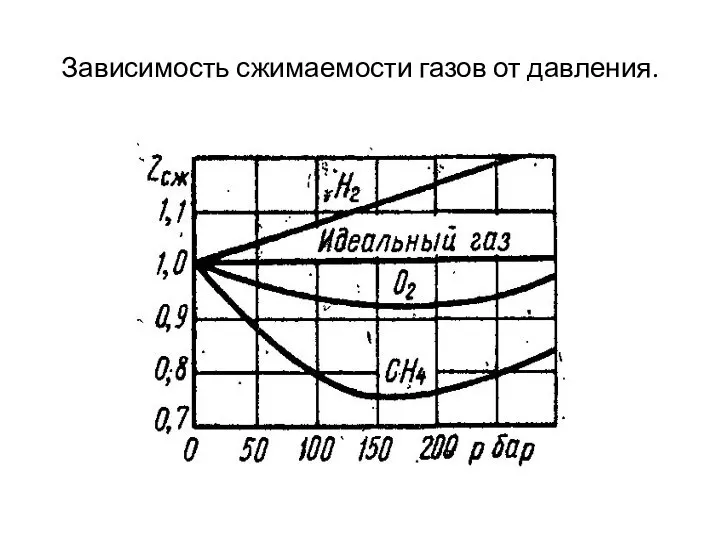
- 3. Зависимость сжимаемости газов от давления.
- 4. 5.2.Уравнение Ван-дер-Ваальса. Уравнение Менделеева-Клапейрона удовлетворительно описывает разряжённые газы. Это значит, новое уравнение должно для малых плотностей
- 5. Собственный объём молекул.
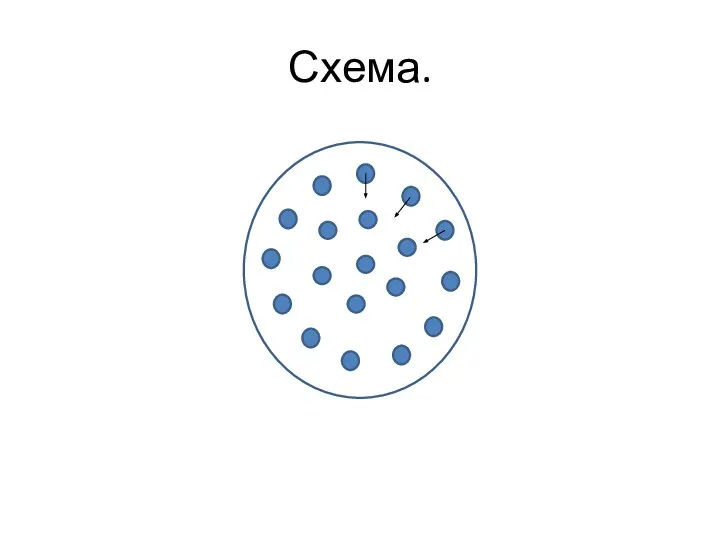
- 6. Схема.
- 7. Силы взаимодействия.
- 8. Уравнение Ван-дер-Ваальса.
- 9. Уравнение Ван-дер-Ваальса для любого количества вещества.
- 10. Коэффициент сжимаемости.
- 11. Сжимаемость газов по Ван-дер-Ваальсу.
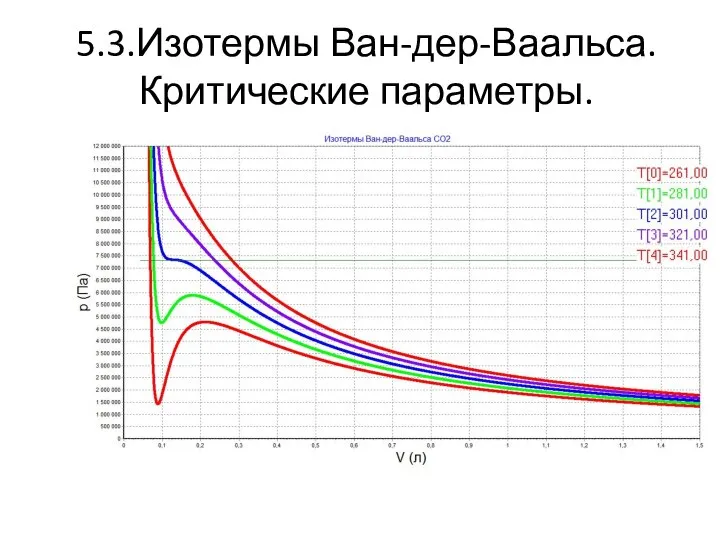
- 12. 5.3.Изотермы Ван-дер-Ваальса. Критические параметры.
- 13. Изотермы Вар-дер-Ваальса. Progr D: Progr E: Progr F: Progr G: Progr H:
- 14. Система уравнений для отыскания Критических параметров.
- 15. Преобразование системы.
- 16. Критический объём.
- 17. Критическая температура.
- 18. Критическое давление.
- 19. Безразмерные параметры.
- 20. Размерные параметры.
- 21. Уравнение Ван-дер-Ваальса с безразмерными параметрами.
- 22. Безразмерное уравнение Ван-дер-Ваальса.
- 23. 5.4.Изотермы Эндрюса. Изотермы Ван-дер-Ваальса – теоретические кривые.
- 24. Эксперименты Марума. Экспериментальные изотермы выглядят иначе. Марум обнаружил возможность сжижения газов. При 7 Атм. Давление преставало
- 25. Исследование Эндрюса. Английский химик Томас Эндрюс (1813 – 1885) исследовал углекислый газ. Заметил появление капелек жидкости,
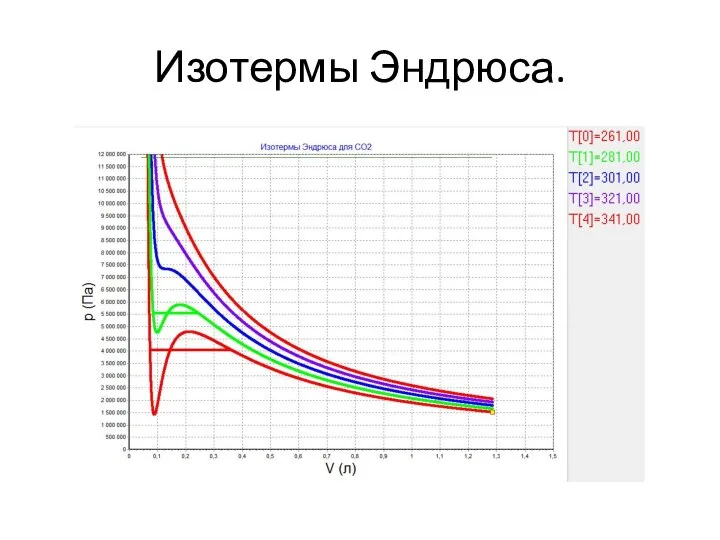
- 26. Изотермы Эндрюса.
- 27. Исследование изотерм Эндрюса. Progr D: Progr E: Progr F: Progr G: Progr H:
- 28. Правило Максвелла.
- 29. Условие сжижения газов. Чтоб сжидить газ его нужно охладить до температуры ниже критической. Этим объясняется неудача
- 30. Правило рычага. Обозначения.
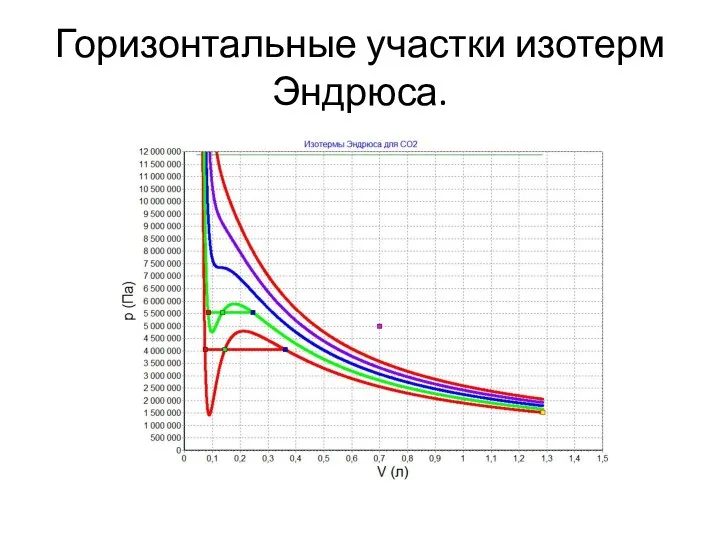
- 31. Горизонтальные участки изотерм Эндрюса.
- 32. Плотности жидкости и газа.
- 33. Правило рычага.
- 34. Отрезки на горизонтальном участке
- 35. Формулировка правила рычага. Таким образом, массы фаз, жидкой и газообразной, обратно пропорциональны величинам отрезков от текущей
- 36. 5.5. Внутренняя энергия газа Ван-дер-Ваальса.
- 37. Зависимость внутренней энергии от температуры.
- 38. Полная зависимость внутренней энергии
- 39. Функции двух переменных
- 40. 5.6.Эффект Джоуля-Томсона. Работы по сжижению газов. Опыты Джоуля и Томсона по дросселированию. Определение. Дросселированием называется процесс
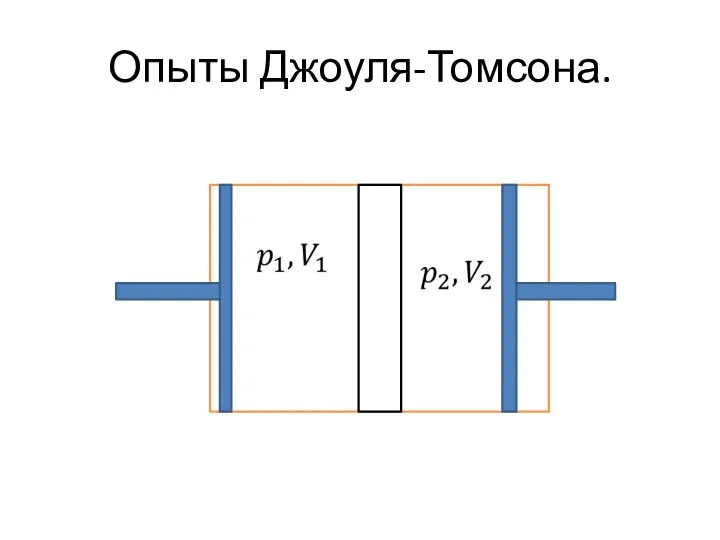
- 41. Опыты Джоуля-Томсона.
- 42. Определение эффекта Джоуля-Томсона. Эффектом Джоуля-Томсона называется явление изменения температуры газа при дросселировании.
- 43. Работа газа и над газом.
- 44. Изменение внутренней энергии.
- 45. Энтальпия.
- 46. Дифференциал энтальпии.
- 47. Производная температуры по давлению.
- 48. Теплоёмкость при постоянном давлении.
- 49. Естественные параметры. Определение. Естественными параметрами некоторой термодинамической функции состояния называются параметры, через дифференциалы которых выражается дифференциал
- 50. Для внутренней энергии.
- 51. Дифференциал внутренней энергии.
- 52. Преобразование первого начала термодинамики.
- 53. Дифференциал энтальпии в естественных параметрах.
- 54. Производная энтальпии по давлению
- 55. Формула эффекта Джоуля-Томсона.
- 56. Термодинамический потенциал Гиббса
- 57. Математическая формула дифференциала потенциала Гиббса.
- 58. Выражения для давления и энтропии.
- 59. Общая формула Эффекта Джоуля-Томсона.
- 60. Анализ формулы.
- 61. 5.7.Идеальный и реальный газы.
- 62. Газ Ван-дер-Ваальса
- 63. Производная от объёма по температуре.
- 64. Преобразование формулы.
- 65. Температура инверсии.
- 66. Положительный эффект.
- 67. Отрицательный эффект.
- 68. Отсутствие эффекта
- 70. Скачать презентацию















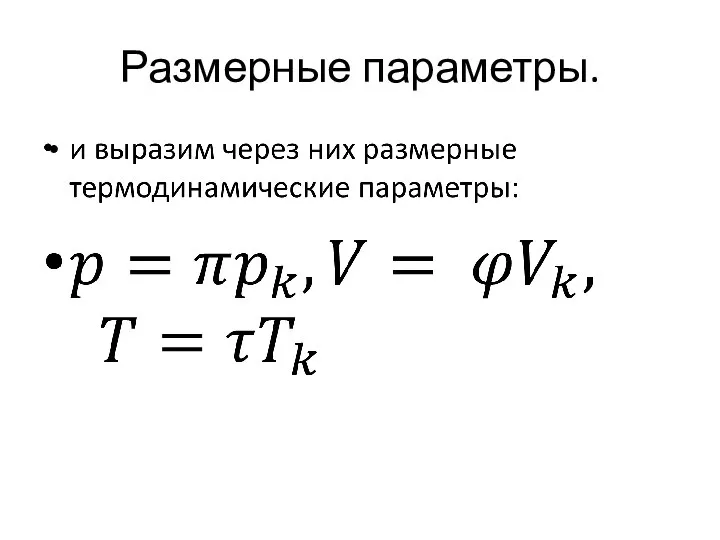













































 Реологические модели
Реологические модели Смеси идеальных газов. I закон термодинамики. Внутренняя энергия и работа
Смеси идеальных газов. I закон термодинамики. Внутренняя энергия и работа Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов. Учитель физики ГБОУ СОШ № 128 г.Санкт-Пете
Три состояния вещества. Различие в молекулярном строении твердых тел, жидкостей и газов. Учитель физики ГБОУ СОШ № 128 г.Санкт-Пете Termodünaamika. Entroopia. (Loeng 8)
Termodünaamika. Entroopia. (Loeng 8) Естественнонаучная картина мира в классической науке
Естественнонаучная картина мира в классической науке Проектирование МДП СБИС. Структуры МДП в СБИС
Проектирование МДП СБИС. Структуры МДП в СБИС Взаимное притяжение и отталкивание молекул
Взаимное притяжение и отталкивание молекул Выпрямители. Переменный ток
Выпрямители. Переменный ток Моя любимая профессия Техническое обслуживание и ремонт автомобилей
Моя любимая профессия Техническое обслуживание и ремонт автомобилей Кинематика точки
Кинематика точки Лекция 5 Динамика вращательного движения
Лекция 5 Динамика вращательного движения  Презентация по физике "Удельная теплота сгорания" - скачать бесплатно
Презентация по физике "Удельная теплота сгорания" - скачать бесплатно 实验五 功率放大电路
实验五 功率放大电路 Теоретическая механика
Теоретическая механика «Исследование сил Архимеда».
«Исследование сил Архимеда». Перемещение тела при прямолинейном равноускоренном движении без начальной скорости (по оси y) Учимся решать задачи (Для учащихся М
Перемещение тела при прямолинейном равноускоренном движении без начальной скорости (по оси y) Учимся решать задачи (Для учащихся М Испытания композитных материалов и конструкций
Испытания композитных материалов и конструкций Обеспечение повышения качества поверхности и эксплуатационных свойств деталей машин, работающих при циклическом нагружении
Обеспечение повышения качества поверхности и эксплуатационных свойств деталей машин, работающих при циклическом нагружении Источники света. Распространение света
Источники света. Распространение света Урок физики тема: «Интерференция света» 11 класс
Урок физики тема: «Интерференция света» 11 класс  Радиоактивность. Период радиоактивного распада и дифференциальные уравнения. Интегрированный урок
Радиоактивность. Период радиоактивного распада и дифференциальные уравнения. Интегрированный урок Структура методики обучения физике
Структура методики обучения физике Амплитудные и фазовые измерения ионосферы
Амплитудные и фазовые измерения ионосферы Презентация по физике "магнитное поле1" - скачать бесплатно
Презентация по физике "магнитное поле1" - скачать бесплатно Индукция магнитного поля
Индукция магнитного поля Уравнения теории упругости. Напряженное состояние в точке. Гипотеза Сен-Венана. (Лекции 1-2)
Уравнения теории упругости. Напряженное состояние в точке. Гипотеза Сен-Венана. (Лекции 1-2) Физика
Физика Наблюдение и опыт
Наблюдение и опыт