Содержание
- 2. Лекция № 4 Статистический метод описания. 1. Основная задача статистической физики. Микросостояние системы частиц. 2. Элементарные
- 3. Состояние системы детально охарактери-зованное на уровне каждой частицы называется микросостоянием. Микросостояния системы описываются заданием в каждый
- 4. Детальное описание состояний макроскопи-ческих систем, ввиду колоссальности числа частиц в них, не только невозможно осуще-ствить фактически,
- 5. Основная задача статистической физики: найти наиболее вероятные распределения молекул по скоростям, энергиям, импульсам и т.д. И
- 6. Элементарные сведения из теории вероятностей. С точки зрения атомно-молекулярного строения вещества величины, встречающиеся в макроскопической физике,
- 7. Статистические закономерности изучаются теорией вероятностей. Событиями или случаями в теории вероятностей называют всякие явления, относительно которых
- 8. Если событие произойти не может, то его называют невозможным. Событие называют случайным, если в результате испытания
- 9. Математическое определение вероятности: вероятность какого-либо события – это предел, к которому стремится отношение числа случаев, приводящих
- 10. По определению Лапласа, вероятность - отношение числа благоприятных случаев к числу возможных случаев. Если событие достоверно,
- 11. События несовместимы, если появление одного из них исключает появление любого из остальных. Теорема сложения вероятностей. Вероятность
- 12. Сумма вероятностей всех единственно возможных и несовместимых событий равна единице: - это утверж- дение является следствием
- 13. Это соотношение часто называют условием нормировки вероятностей. Теорема умножения вероятностей. Вероятность произведения двух событий А и
- 14. Если события А и В независимы (их вероятности не зависят от того, произош-ло второе событие или
- 15. либо зелёным, либо красным (событие А), равна по теореме сложения вероятностей: Если событие А произошло, то
- 16. Существует ещё одна интерпретация вероятности, применяющаяся в физике. Пусть в закрытом сосуде имеется одна моле-кула. Сталкиваясь
- 17. Важным понятием в теории вероятностей и её приложениях является понятие среднего значения. Пусть произведено N однотип-ных
- 18. Отношение , т.е. отношение числа наб-людений при которых величина x имеет значение , к общему числу
- 19. Введём понятие отклонения результатов отдельных измерений от среднего значения , т.е. , где i = 1,2,…,N
- 20. Распространим полученные результаты на случай когда характеризующая систему ве-личина x может принимать непрерывный ряд значений от
- 21. Вероятность того, что результат измерений окажется в интервале от нуля до а , равна: , в
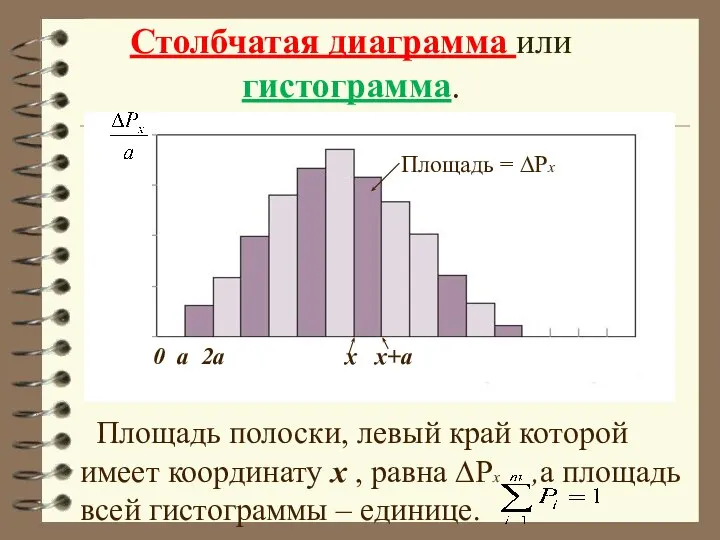
- 22. Столбчатая диаграмма или гистограмма. Площадь полоски, левый край которой имеет координату x , равна ∆Рx ,а
- 23. Гистограмма (столбчатая диаграмма) наг-лядно характеризует вероятность получения результатов измерений, заключающихся в различных интервалах одинаковой ширины а.
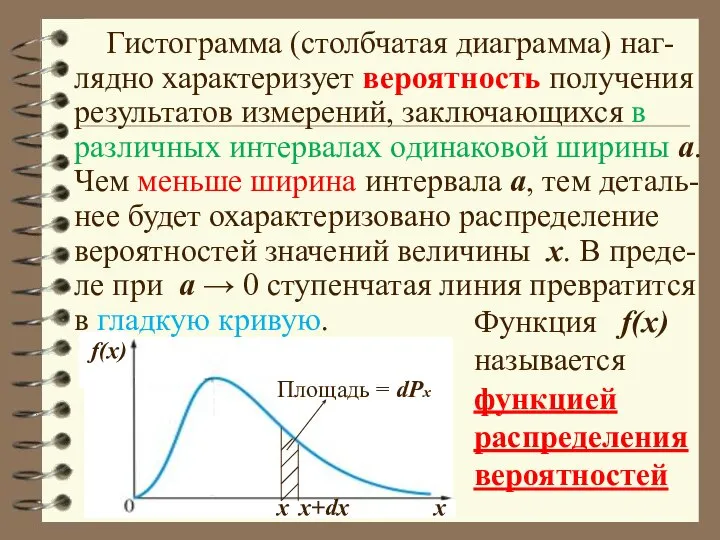
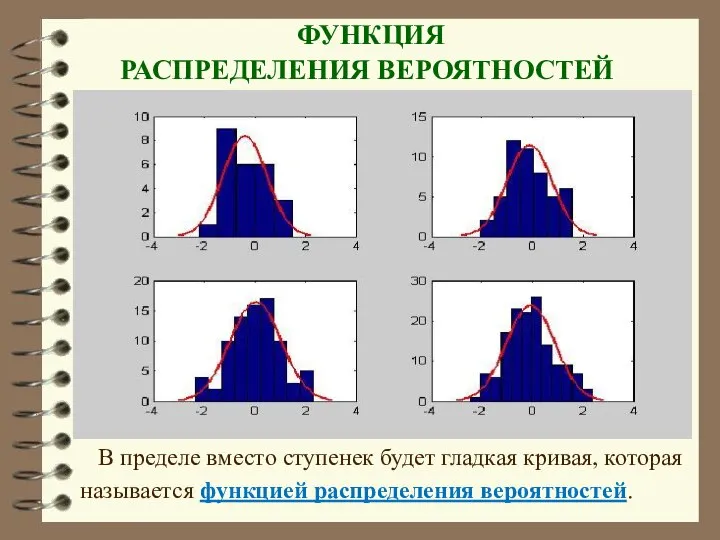
- 24. ФУНКЦИЯ РАСПРЕДЕЛЕНИЯ ВЕРОЯТНОСТЕЙ В пределе вместо ступенек будет гладкая кривая, которая называется функцией распределения вероятностей.
- 25. Площадь столбика ширины dx равна ве-роятности того, что результат измерения окажется в пределах от x до
- 26. Зная функцию распределения f(x) , можно найти среднее значение результатов измере-ния величины x . В случаях
- 27. Аналогичные рассуждения дают, что сред-нее значение некоторой функции φ(x) можно вычислить по формуле: Например:
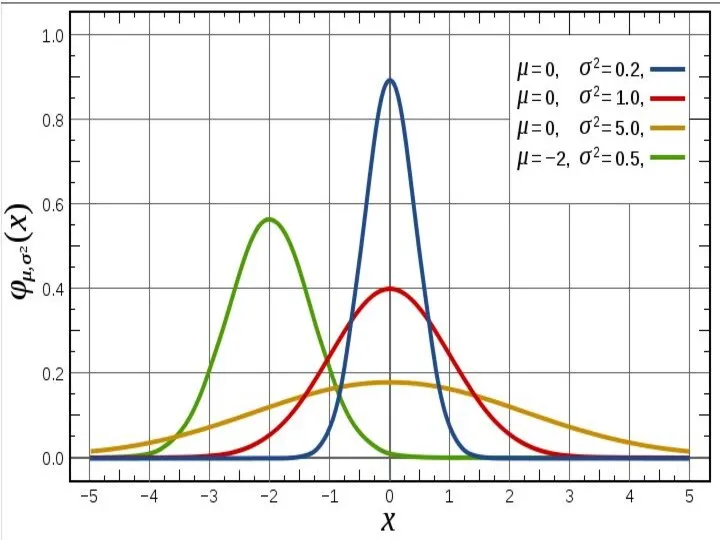
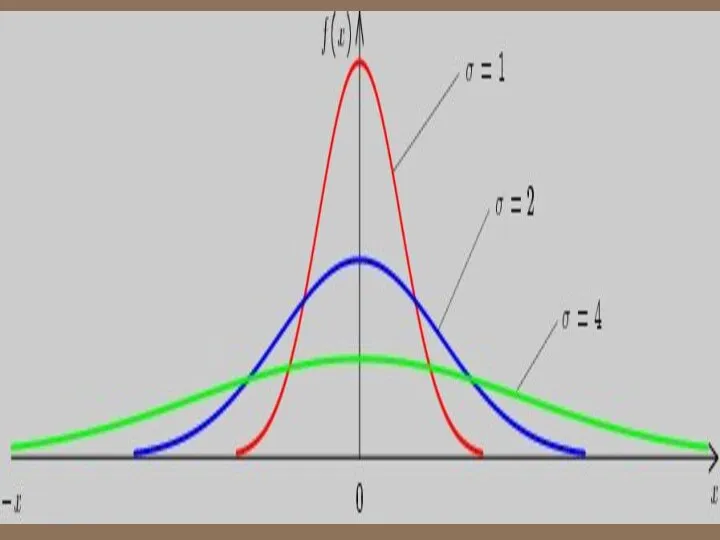
- 28. Закон распределения Гаусса. Нормальное распределение, также называ-емое гауссовским распределением или распре-делением Гаусса — распределение вероятнос-тей, которое
- 31. Гаусс (Gauss) Карл Фридрих (30.4.1777, Брауншвейг, - 23.2.1855, Гёттинген), немецкий математик, внёсший фундаментальный вклад также в
- 33. Закон распределения скоростей молекул при тепловом равновесии Возьмём газ, состоящий из очень большого числа N тождественных
- 34. друг друга всякие два противоположно направленные процесса. Скорости таких противоположно направленных процессов должны быть одинаковыми. Это
- 35. Закон распределения скоростей Максвелла. Возьмём в воображаемом пространстве, которое назовём υ – пространством (пространством скоростей), прямоуго-льные
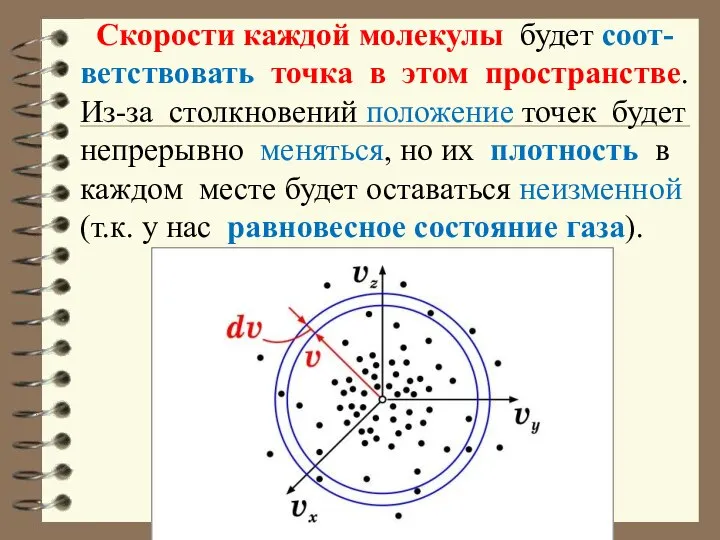
- 36. Скорости каждой молекулы будет соот-ветствовать точка в этом пространстве. Из-за столкновений положение точек будет непрерывно меняться,
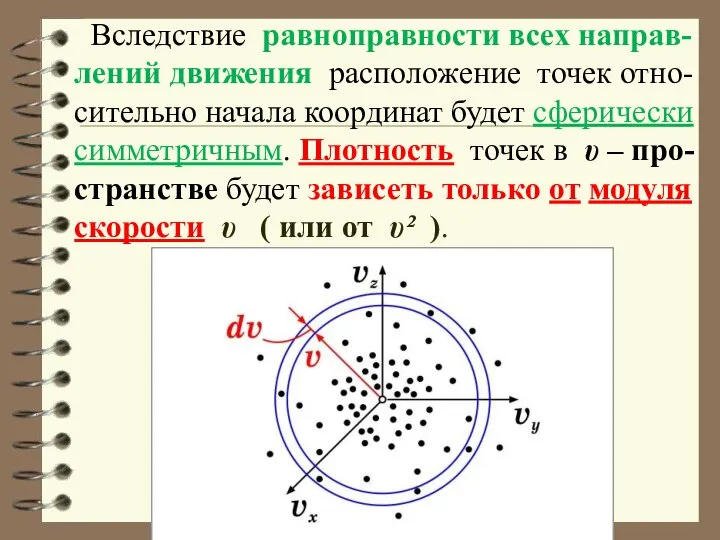
- 37. Вследствие равноправности всех направ-лений движения расположение точек отно-сительно начала координат будет сферически симметричным. Плотность точек в
- 38. Молекулы движутся хаотически. Среди них есть и очень быстрые, и очень медленные. Благодаря беспорядочному движению и
- 39. Мы будем искать число частиц (Δn) скорости которых лежат в определён-ном интервале значения скорости Δυ (
- 40. Ясно так же, что Δn должно быть пропорционально концентрации молекул n . Число Δn зависит и
- 41. Здесь f (υ) – функция распределения молекул по скоростям, n – концентрация молекул и Δυ -
- 42. Таким образом, f(υ) – имеет смысл вероятности, то есть показывает, какова вероятность любой молекулы газа в
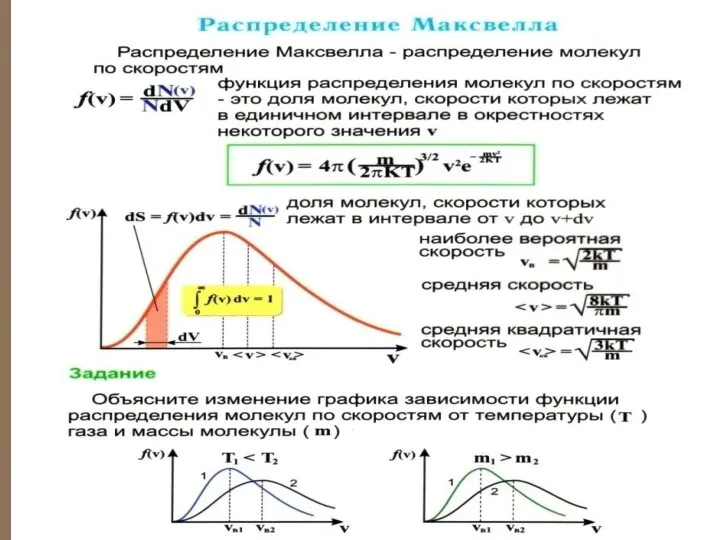
- 43. Функция распределения Максвелла Пусть имеется n тождественных молекул, находящихся в состоянии беспорядочного теплового движения при определенной
- 44. В результате каждого столкно-вения проекции скорости молекулы испытывают случайное изменение на Δυx, Δυy, Δυz, причем изменения
- 45. При этом, мы не можем ничего определенного сказать о точном значении скорости той или иной частицы
- 46. Максвелл Джеймс Клерк (1831 – 1879) – английский физик. Работы посвящены электродинамике, молекулярной физике, общей статике,
- 47. Скорость – векторная величина. Для проекции скорости на ось х (x-ой составляющей скорости ), имеем: или
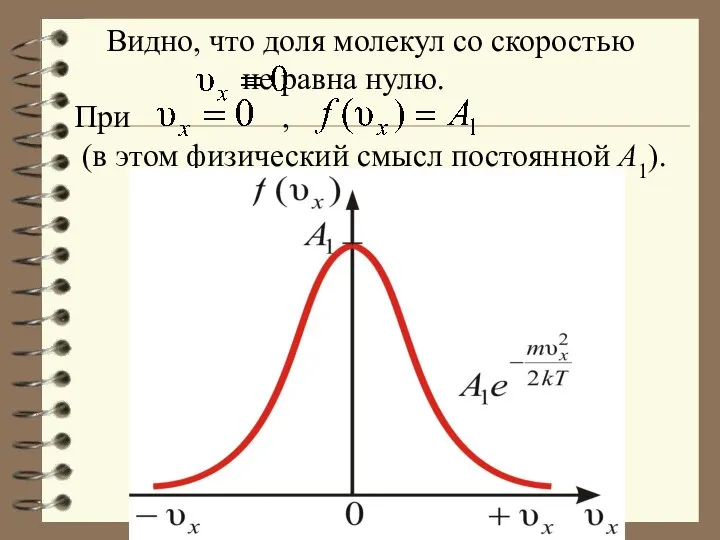
- 48. Видно, что доля молекул со скоростью не равна нулю. При , (в этом физический смысл постоянной
- 49. Приведённое выражение и график справедливы для распределения молекул газа по x-ым компонентам скорости. Очевидно, что и
- 50. Вероятность того, что скорость молекулы одновременно удовлетворяет трём условиям: x – компонента скорости лежит в интервале
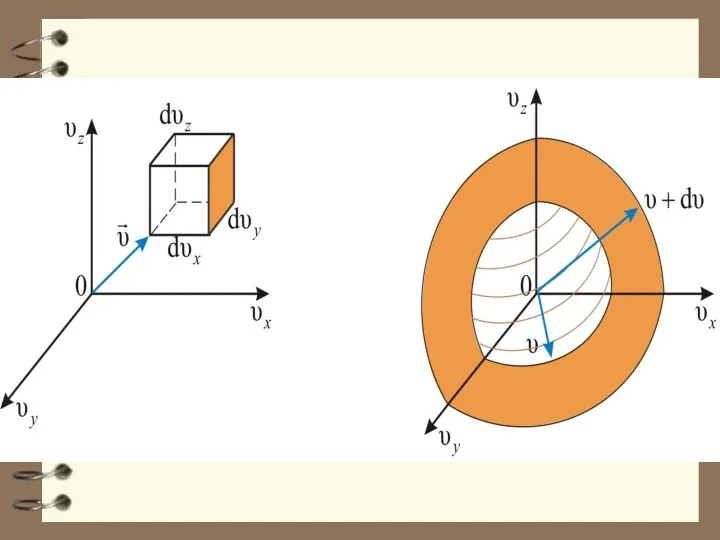
- 51. Или Этой формуле можно дать геометричес-кое истолкование: dnxyz – это число моле-кул в параллелепипеде со сторонами
- 52. Величина dnxyz не может зависеть от направления вектора скорости. Поэтому надо получить функцию распределения молекул по
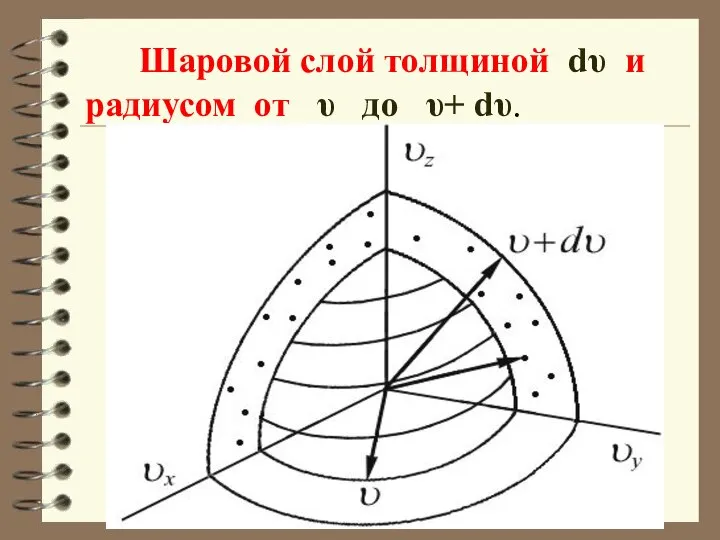
- 53. Шаровой слой толщиной dυ и радиусом от υ до υ+ dυ.
- 55. Этот шаровой слой складывается из тех параллелепипедов, о которых говорилось выше. Объём этого шарового слоя: Общее
- 56. Отсюда следует закон Максвелла – распределение молекул по абсолютным значениям скоростей: где – доля всех частиц
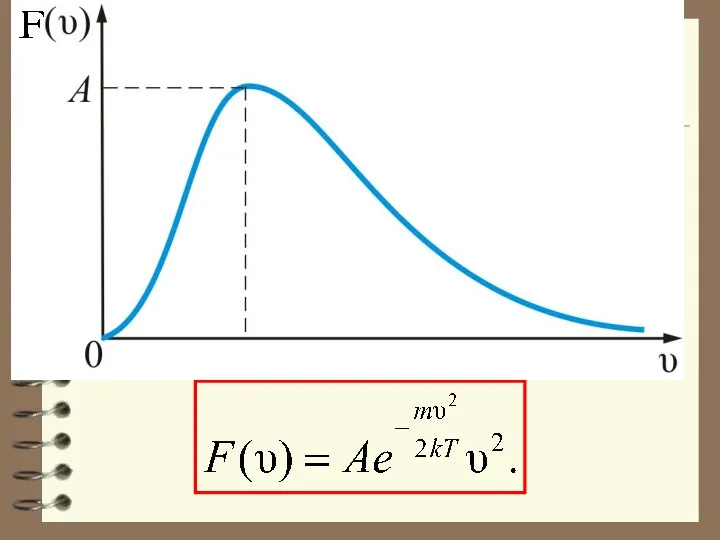
- 57. При получаем плотность вероятности, или функцию Максвелла распределения молекул по скоростям: Эта функция обозначает долю молекул
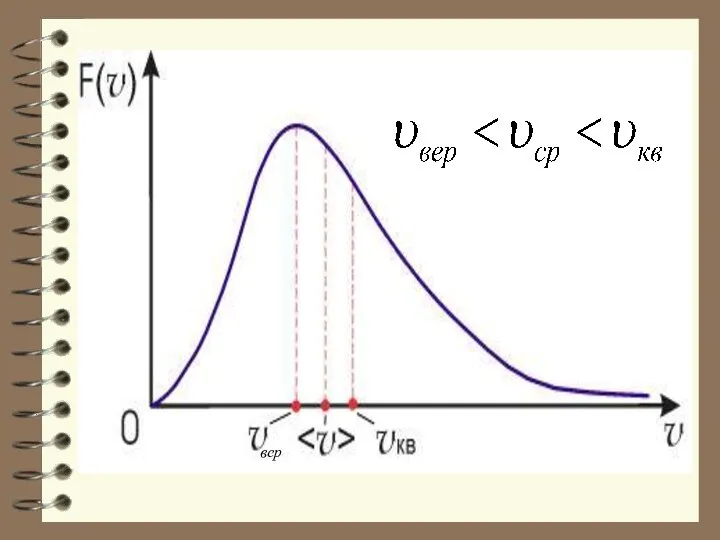
- 58. Обозначим тогда получим: График этой функции показан на рис.
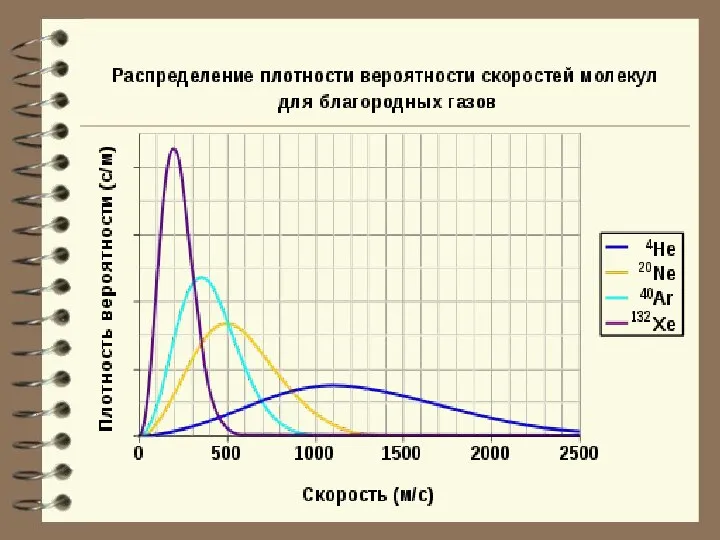
- 60. Выводы: - Вид распределения молекул газа по скоростям, для каждого газа зависит от рода газа (m)
- 61. Распределение Максвелла характеризует распределение молекул по значениям кинетической энергии (то есть показывает, какова вероятность при данной
- 62. Характерные скорости (наиболее вероятная, среднеквадратичная и средняя скорости молекул газа). Рассмотрим, как изменяется с абсолютной величиной
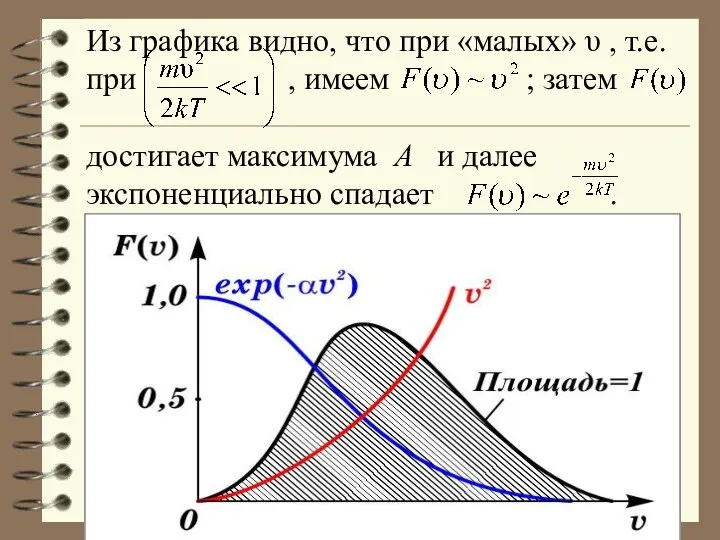
- 63. Из графика видно, что при «малых» υ , т.е. при , имеем ; затем достигает максимума
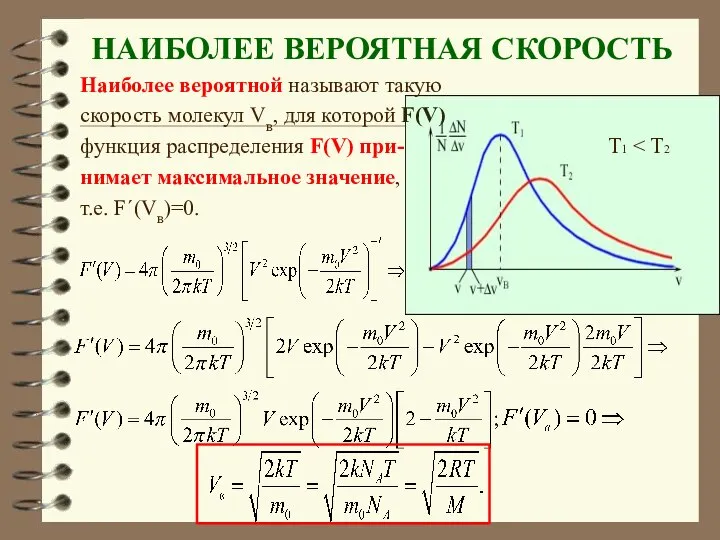
- 64. НАИБОЛЕЕ ВЕРОЯТНАЯ СКОРОСТЬ Наиболее вероятной называют такую скорость молекул Vв, для которой F(V) функция распределения F(V)
- 65. Величина скорости, на которую при-ходится максимум зависимости называют наиболее вероятной скоростью . Величину этой скорости находят
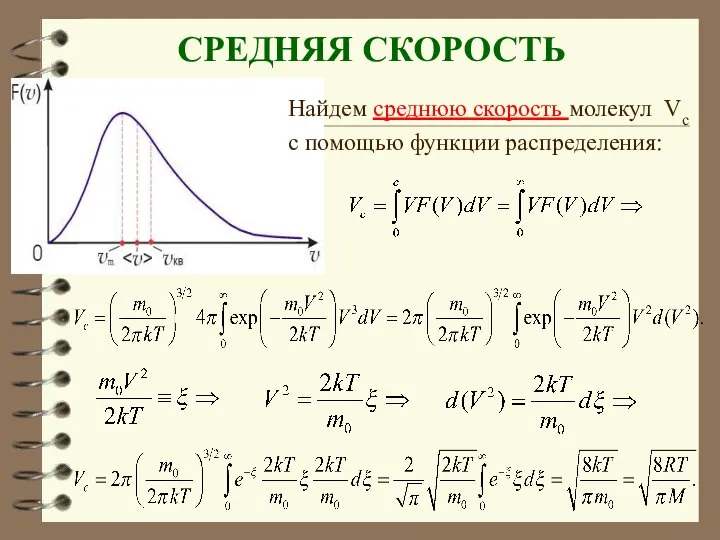
- 66. СРЕДНЯЯ СКОРОСТЬ Найдем среднюю скорость молекул Vc с помощью функции распределения:
- 67. Средняя скорость − υср где – число молекул со скоростью от υ до . Если подставить
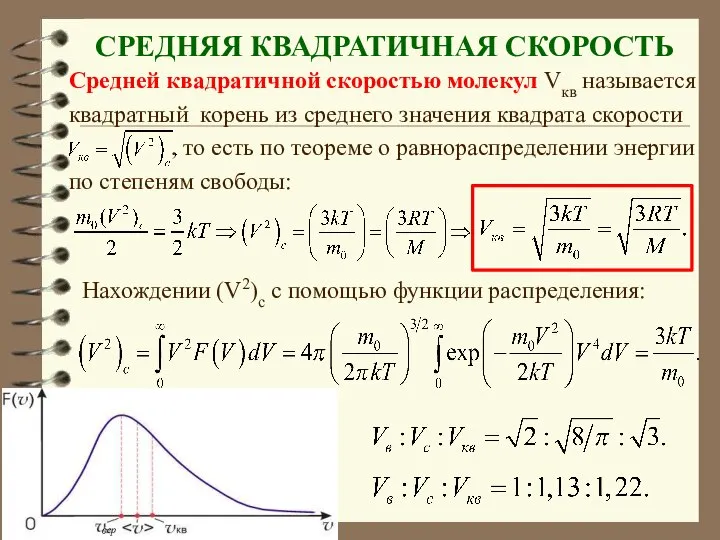
- 68. СРЕДНЯЯ КВАДРАТИЧНАЯ СКОРОСТЬ Средней квадратичной скоростью молекул Vкв называется квадратный корень из среднего значения квадрата скорости
- 69. Среднюю квадратичную скорость находят используя соотношение :
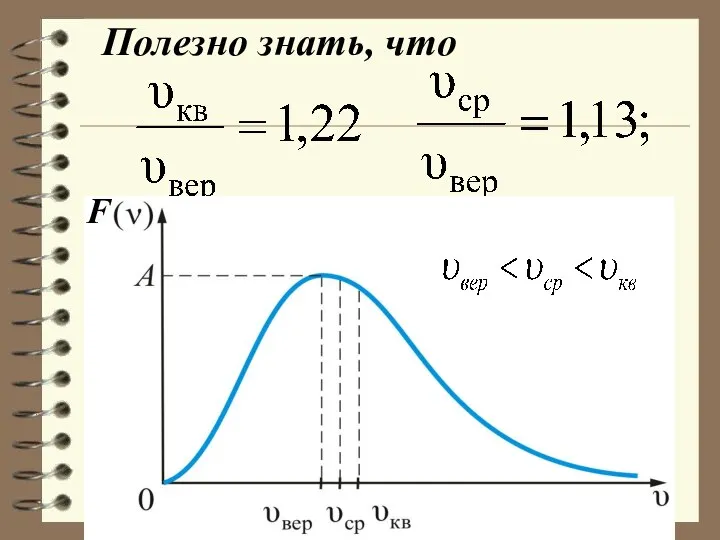
- 70. Полезно знать, что F
- 71. вер
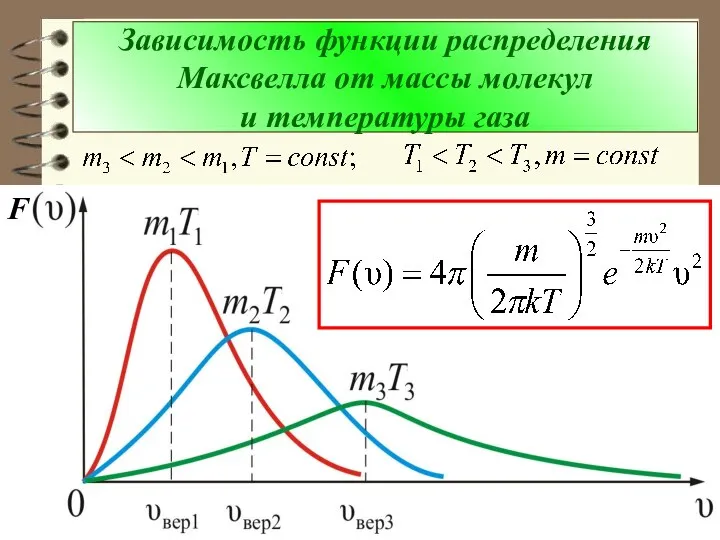
- 72. Зависимость функции распределения Максвелла от массы молекул и температуры газа F
- 73. Из рис. можно проследить за измене-нием при изменении m и T: (при ) или (при ).
- 77. Скачать презентацию






















































 Объем тела и его измерение
Объем тела и его измерение Примеры решения задач по теме Движение с постоянным ускорением свободного падения
Примеры решения задач по теме Движение с постоянным ускорением свободного падения Геометрическая оптика
Геометрическая оптика  Дифракция
Дифракция Презентация по физике Фотоэффект
Презентация по физике Фотоэффект Презентация Тепловые двигатели и их применение.
Презентация Тепловые двигатели и их применение.  Синтетические жидкие диэлектрики
Синтетические жидкие диэлектрики Антенный переключатель РЛС
Антенный переключатель РЛС Котельные установки и парогенераторы
Котельные установки и парогенераторы Давление света
Давление света Управление колебаниями системы маятник-тележка с приводом методом скоростного биградиента
Управление колебаниями системы маятник-тележка с приводом методом скоростного биградиента Магниторазведка. Вопросы госэкзамена. Лекция 2
Магниторазведка. Вопросы госэкзамена. Лекция 2 Великие физики
Великие физики Презентация по физике "Звуковые волны (8-9 класс)" - скачать
Презентация по физике "Звуковые волны (8-9 класс)" - скачать  Электромагнитная индукция
Электромагнитная индукция Интегрированный (физика + музыка) повторительно-обобщающий урок по теме: «Звуковые волны»
Интегрированный (физика + музыка) повторительно-обобщающий урок по теме: «Звуковые волны» Опыты в домашних условиях
Опыты в домашних условиях Биполярный транзистор. Проверка исправности
Биполярный транзистор. Проверка исправности Кинематика твердого тела
Кинематика твердого тела Свойства металлов. Учебная практика (занятие 1)
Свойства металлов. Учебная практика (занятие 1) Методы преподавания. Интеллектуальная минутка по теме: Физика 7 класс
Методы преподавания. Интеллектуальная минутка по теме: Физика 7 класс МОЛЕКУЛЯРНАЯ ФИЗИКА .
МОЛЕКУЛЯРНАЯ ФИЗИКА .  Механические волны
Механические волны Есть ли будущее у дирижаблей
Есть ли будущее у дирижаблей Электродинамика. Электростатика
Электродинамика. Электростатика Устройство и техническая характеристика бульдозера
Устройство и техническая характеристика бульдозера Увеличительные приборы. Строение растительной клетки
Увеличительные приборы. Строение растительной клетки Неразъёмные соединения
Неразъёмные соединения