Содержание
- 2. Молекулы вещества в жидком состоянии расположены почти вплотную друг к другу. Могут совершать тепловые колебания около
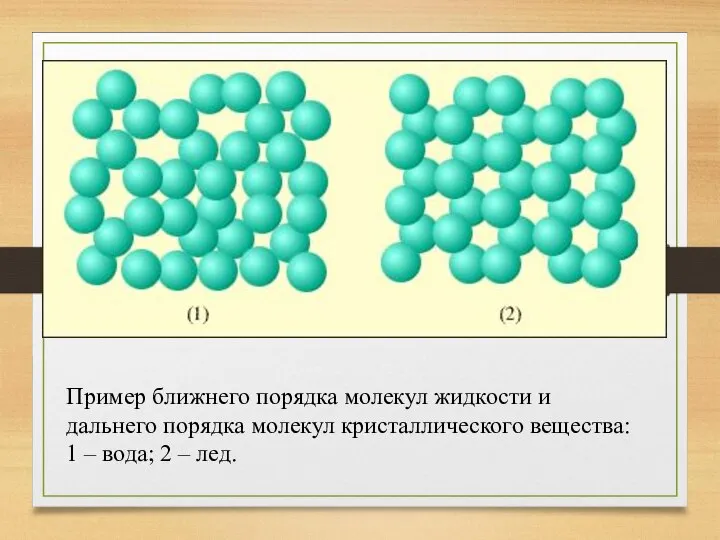
- 3. Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: 1 – вода; 2 –
- 4. Молекула воды H2O состоит из одного атома кислорода и двух атомов водорода, расположенных под углом 104°.
- 5. Молекулярный механизм поверхностного натяжения. Внутри жидкости результирующая сила притяжения, действующая на молекулу со стороны соседних молекул,
- 6. Капля масла в водном растворе спирта. Молекулы, находящиеся на поверхности под действием резуль- тирующей силы притяжения
- 7. В космическом корабле шарообразную форму принимает и достаточно большая масса жидкости.
- 8. Поверхностное натяжение – явление молекулярного давления на жидкость, вызванное притяжением молекул поверхностного слоя к молекулам внутри
- 9. Сила поверхностного натяжения – сила, направленная по касательной к поверхности жидкости, перпен- дикулярно участку контура, ограничивающего
- 10. Поверхностное натяжение жидкости зависит: 1) от природы жидкости, т. е. от сил притяжения между молекулами данной
- 11. Действие сил поверхностного натяжения Поверхностное натяжение жидкостей, находящихся в контакте с воздухом, мН/м.
- 12. Из-за действия сил поверхностного натяжения в каплях жидкости и внутри мыльных пузырей возникает избыточное давление Δp.
- 13. Избыточное давление внутри мыльного пузыря в два раза больше, так как пленка имеет две поверхности: Отсюда
- 15. Смачивание – искривление поверхности жидкости у поверхности твердого тела в результате взаимодействия молекул жидкости с молекулами
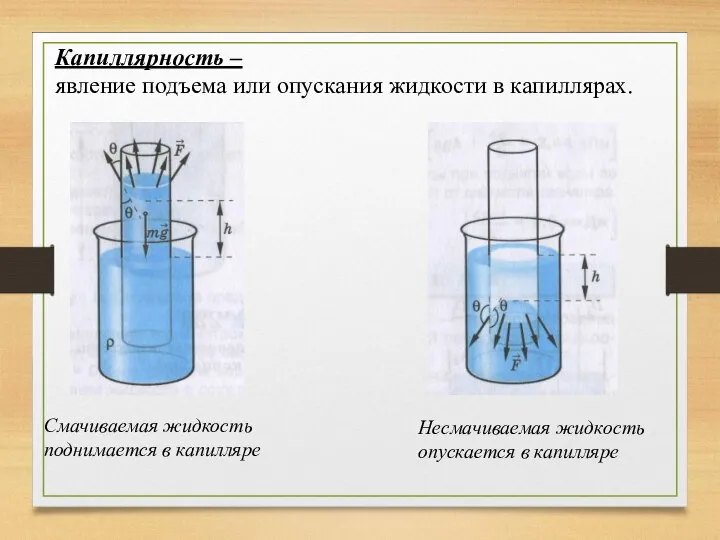
- 18. Капиллярность – явление подъема или опускания жидкости в капиллярах. Смачиваемая жидкость поднимается в капилляре Несмачиваемая жидкость
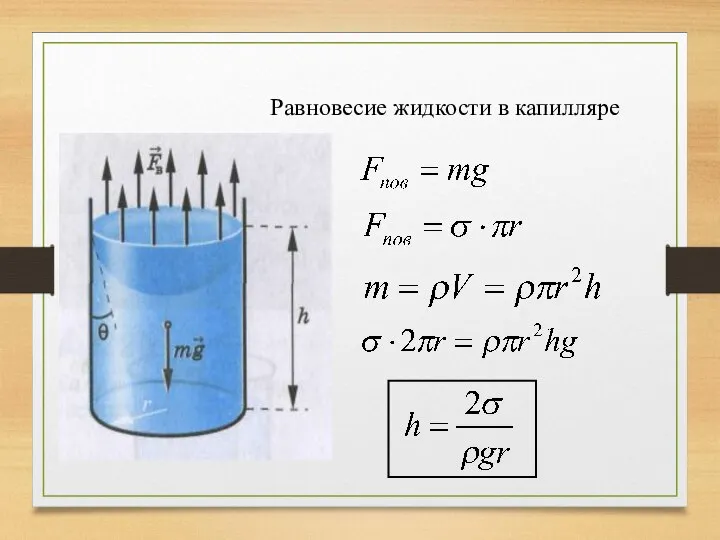
- 19. Равновесие жидкости в капилляре
- 20. Поднятие жидкости в капиллярах разного диаметра (D1 > D2, h1
- 22. Скачать презентацию
















 «Исаак Ньютон: «Я гипотез не измышляю…»
«Исаак Ньютон: «Я гипотез не измышляю…»  Гармонические колебания. Сложение гармонических колебаний
Гармонические колебания. Сложение гармонических колебаний Эфир в опыте Майкельсона-Морли
Эфир в опыте Майкельсона-Морли Радиоактивность. Строение атома
Радиоактивность. Строение атома Ионизирующее излучение. Радиация и здоровье
Ионизирующее излучение. Радиация и здоровье Сила тока. Повторение
Сила тока. Повторение Презентация по физике Нормативные требования к освещению рабочих мест.
Презентация по физике Нормативные требования к освещению рабочих мест. Сила Архимеда. Плавание тел
Сила Архимеда. Плавание тел Элементы машиноведения. Составные части машин
Элементы машиноведения. Составные части машин Презентация по физике Способы сохранения энергоресурсов Энергосберегающие машины
Презентация по физике Способы сохранения энергоресурсов Энергосберегающие машины  Қарастырылатын мәселелер
Қарастырылатын мәселелер Атомная физика
Атомная физика Тепловой двигатель. КПД теплового двигателя
Тепловой двигатель. КПД теплового двигателя Введение в нанотехнологии
Введение в нанотехнологии Характеристики основных компонент ГТУ
Характеристики основных компонент ГТУ Magnetic Resonance
Magnetic Resonance Презентация по физике "Вес тела. Единицы силы. Связь между силой тяжести и массой тела" - скачать
Презентация по физике "Вес тела. Единицы силы. Связь между силой тяжести и массой тела" - скачать  Макроскопическая намагниченность, прецессия
Макроскопическая намагниченность, прецессия Оптика. Явление полного внутреннего отражения света. Рефрактометрия
Оптика. Явление полного внутреннего отражения света. Рефрактометрия Приемники оптического излучения. Способы их крепления
Приемники оптического излучения. Способы их крепления Теорема о движении центра масс
Теорема о движении центра масс Упругое рассеяние в центральном поле
Упругое рассеяние в центральном поле Электрическое поле в веществе
Электрическое поле в веществе Слесарное дело
Слесарное дело Сейсмограф Физика 9 класс
Сейсмограф Физика 9 класс Движение тела, брошенного под углом к горизонту
Движение тела, брошенного под углом к горизонту Лекционный курс физические основы измерений и эталоны. Охлаждение при расширении газов. Эффект джоуля-томсона
Лекционный курс физические основы измерений и эталоны. Охлаждение при расширении газов. Эффект джоуля-томсона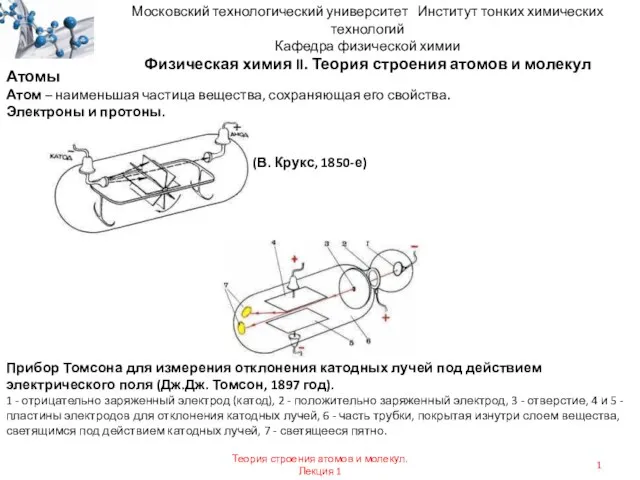 Теория строения атомов и молекул
Теория строения атомов и молекул