Содержание
- 2. Правила рейтинга по курсу термодинамика ника и теплопередачадля Максимальное количество рейтинговых баллов за работу по основной
- 3. Семестровый рейтинговый балл складывается из выполнения и защиты лабораторных работ (до 30 баллов), результатов двух контрольной
- 4. Индивидуальное задание состоит из двух домашних заданий и оценивается первая максимум в 10 баллов, вторая 5
- 5. К экзамену допускаются студенты получившие зачет по теплотехнике и включенные деканатом в экзаменационную ведомость. Экзамен состоит
- 9. Основные определения и понятия Термодинамическая система Под понятием системы подразумевается тело или совокупность тел . Система
- 10. Термодинамической системой принято называть закрытую систему, внутреннее состояние которой определяется значениями определенного количества независимых переменных, которые
- 11. Идеальным газом называется система, физическое состояние которой вполне определяется значением одной независимой переменной, а именно значением
- 12. Термодинамические процессы Изменение состояния системы называется процессом. Равновесный процесс - это непрерывная последо-вательность равновесных состояний системы.
- 13. Термодинамическая работа В простейшем случае элементарная термодинамическая работа L (Дж) простых тел определяется в зависимости от
- 14. Термодинамическая работа обратимого изменения объема
- 15. Поскольку термодинамическая работа зависит от пути (вида) процесса, для вычисления интегральных значений полной ( ), или
- 16. Потенциальная (техническая) работа Потенциальной (технической) работой называется работа по перемещению сплошных масс (газа, пара или жидкости)
- 17. Потенциальная работа обратимого изменения давления
- 18. Для определения интегральных значений полной ( ) или удельной ( ) работы надо знать уравнение процесса
- 19. Необратимые потери термодинамической ( ) и потенциальной ( ) работ превращаются в теплоту внутреннего теплообмена (
- 20. В условиях механических процессов (dEcz=G⋅c⋅dc+G⋅g⋅dz) уравнение распределения термодинамической и потенциальной работ формулируется следующим образом:
- 21. Внутренняя энергия тела Внутренняя энергия представляет собой полный запас энергии тела и состоит из энергии поступатель-ного
- 22. Теплота Теплота - количество энергии, передаваемой от одного тела к другому посредством теплопро-водности, конвективного или лучистого
- 23. Теплоемкость Истиной теплоемкостью называется количество теплоты, которое надо сообщить единице количества вещества в термодинамическом процессе (z=idem.),
- 24. Связь между массовой, молярной и объемной теплоемкостью представлена следующими соотношениями: Экспериментальное определение теплоемкости обычно проводится в
- 25. Теплоемкость реального газа зависит от температуры и давления. Теплоемкость идеального газа зависит только от температуры. Для
- 26. Для некоторых газов в определенном интервале температур истинная теплоемкость изменяется по линейному закону тогда сzm- первая
- 27. Различают три агрегатных состояния простых систем: твердое, жидкое и газовое. Линии фазовых превращений (испарение - I,
- 28. Диаграмма фазовых состояний чистого вещества
- 29. Критические параметры являются важнейшими термодинамическими постоянными вещества. Критическая температура – это температура, при которой и выше
- 30. Поэтому в принципе, для простых тел (однородных систем) должно существовать единое уравнение состояния , описывающее любое
- 31. где R – характеристическая постоянная газа; Т – абсолютная температура газа; ( Дж/кмоль К ) –
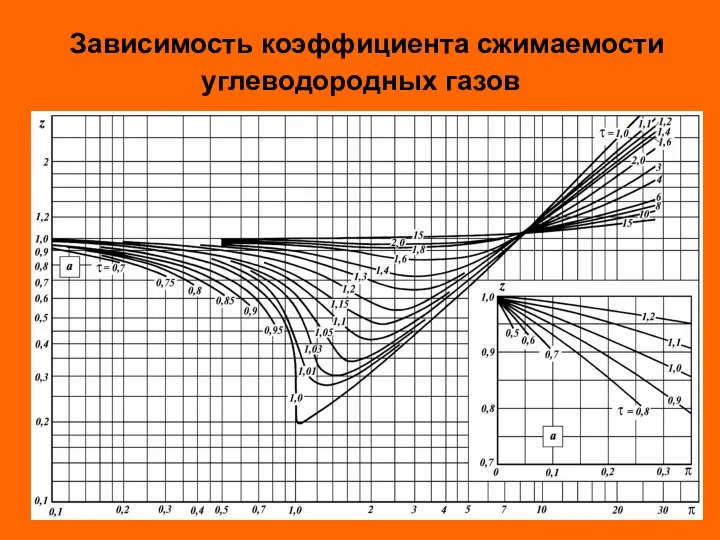
- 32. Для обобщения данных по коэффициентам сжимаемости различных газов был использован прин-цип «соответственных» состояний, сформулирован-ный Ван-дер-Ваальсом. Принцип
- 33. Степень удаления от критической точки определяется с помощью приведенных параметров: приведенного давления приведенной температуры приведенного объема
- 34. Зависимость коэффициента сжимаемости углеводородных газов
- 35. Смеси жидкостей, паров и газов Смесью называется термодинамическая система состоящая из n-компонентов химический не взаимодействующих между
- 36. Молярной концентрацией или молярной долей i-го компонента называется отношение количества киломолей этого компонента к общему числу
- 37. Средняя (кажущаяся) молярная масса смеси равна отношению массы смеси к количеству киломолей смеси и может быть
- 38. Зависимость между массовой и молярной концентрациями устанавливается соотношением Газовая постоянная смеси может быть вычислена по следующему
- 39. Схемы смешения при постоянном объеме (а) и при постоянном давлении (б)
- 40. где , – давление и температура смеси.
- 41. = =
- 42. где массовая и молярная концентрации i-го компо-нента смеси; - средние удельные массовая и молярная теплоемкости i-го
- 43. Смеси реальных газов , pк,i и Тк,i − критические давление и температура компонентов газовой смеси.
- 44. Первое начало термодинамики Первое начало термодинамики – это количественное выражение закона сохранения и превращения энергии. Закон
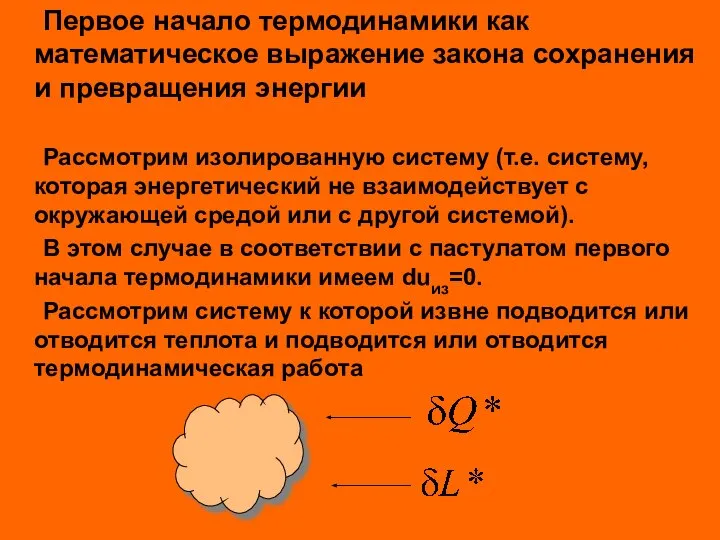
- 45. Первое начало термодинамики как математическое выражение закона сохранения и превращения энергии Рассмотрим изолированную систему (т.е. систему,
- 46. Таким образом изменение внутренней энергии системы равно алгебраической сумме подведенных извне теплоты и термодинамической работы (подведенная
- 47. - эффективная работа; - внешний теплообмен Полученные уравнения учитывают только внешние эффекты и справедливы только для
- 48. уравнения первого начала термодинамики по балансу рабочего тела, и справедливы для реальных процессов . В обратимых
- 49. Первое начало термодинамики для простых тел Для простых тел, то есть систем, состояние которых определяется двумя
- 50. Выражение удельной потенциальной работы можно представить в виде соотношения из которого следует, что ; и ,
- 51. Первое начало термодинамики для 1 кг простого тела по балансу рабочего тела в дифференциальной и интегральной
- 52. Аналитическое выражение первого начала термодинамики Значения удельных внутренней энергии и энтальпии простого тела однозначно определяются двумя
- 53. Подставляя выражения полных дифференциалов внутренней энергии и энтальпии в уравнение первого начала термодинамики имеем
- 54. Данное соотношение называется первым началом термодинамики для простых тел в аналитической форме. Выражения в квадратных скобках
- 55. – коэффициент Джоуля – Гей Люссака, – коэффициент Джоуля-Томсона, Коэффициенты Джоуля – Гей Люссака ( )
- 56. Калорические коэффициенты по физическому смыслу являются аналогами теплоемкостей в изотермическом процессе. Данную запись первого начала называют
- 58. С другой стороны из выражения первого начала термодинамики для простого тела С учетом того, что для
- 59. Из уравнения первого начала термодинамики для идеального газа из которого следует, что разность истинных теплоемкостей идеального
- 60. Уравнение может быть записано и для одного кмоля газа Разделив уравнение первого начала термодинамики на абсолютную
- 61. С учетом того, что для идеального газа, исходя уравнения Клапейрона, справедливы равенства: получим
- 62. Правая часть уравнения представляет собой сумму полных дифференциалов. Это значит, что и соотношение есть полный дифференциал
- 64. Скачать презентацию





































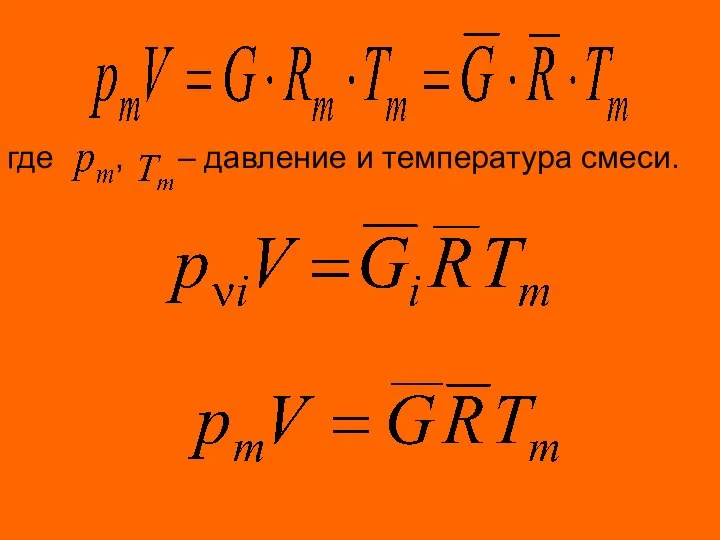





















 Гидравлика машин
Гидравлика машин Световые явления
Световые явления Давление твердых тел, жидкостей и газов
Давление твердых тел, жидкостей и газов Постулаты теории относительности
Постулаты теории относительности Вес тела и сила тяжести
Вес тела и сила тяжести Индукционные нагреватели. Перспективы и области применения
Индукционные нагреватели. Перспективы и области применения Теоретическая (техническая) механика. Статика
Теоретическая (техническая) механика. Статика Характеристики движения
Характеристики движения Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц
Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц Плоская система сил
Плоская система сил Магнитные подшипники
Магнитные подшипники Аморфні та склоподібні матеріали. (Лекція 2)
Аморфні та склоподібні матеріали. (Лекція 2) Реальные газы, жидкости и твердые тела
Реальные газы, жидкости и твердые тела Давление. Единицы давления
Давление. Единицы давления Закон всемирного тяготения
Закон всемирного тяготения Интеллектуальная игра «Физбой»
Интеллектуальная игра «Физбой» Тепловозы. Устройство тепловоза
Тепловозы. Устройство тепловоза Кристаллические тела (10 класс)
Кристаллические тела (10 класс) Квантовые методы в медицине. Ядерный магнитный резонанс. Электронный парамагнитный резонанс. (Лекция 14)
Квантовые методы в медицине. Ядерный магнитный резонанс. Электронный парамагнитный резонанс. (Лекция 14) Теоретическая механика как наука и ее место среди естественных наук
Теоретическая механика как наука и ее место среди естественных наук Сила упругости. Закон Гука
Сила упругости. Закон Гука Електричний струм у газах
Електричний струм у газах  Подготовила учитель физики МОУ СОШ №1 р.п. Степное Бейбулатова Е.А.
Подготовила учитель физики МОУ СОШ №1 р.п. Степное Бейбулатова Е.А. Механика. Наука о движении тел
Механика. Наука о движении тел Энергия движущейся воды и ветра
Энергия движущейся воды и ветра Работа силы тяжести
Работа силы тяжести Оценка угла места в системах локации метрового диапазона
Оценка угла места в системах локации метрового диапазона «Интерференция света»
«Интерференция света»