Содержание
- 2. Гипотеза о том, что вещества состоят из атомов, впервые была высказана Левкиппом и Демокритом примерно в
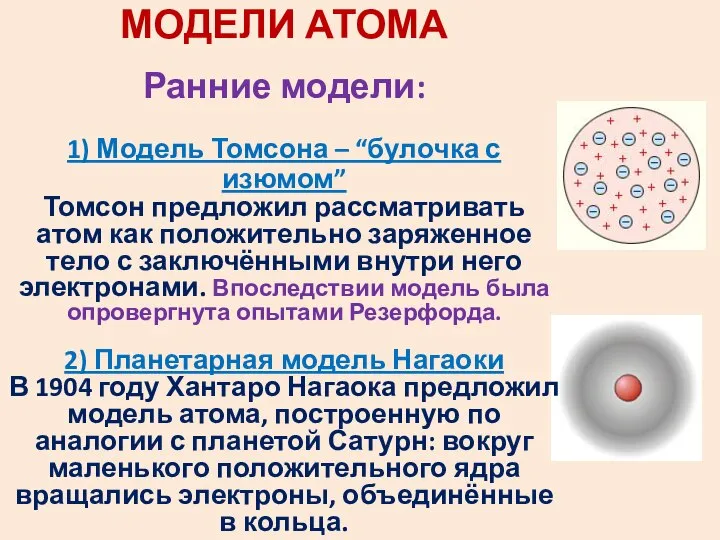
- 3. МОДЕЛИ АТОМА Ранние модели: 1) Модель Томсона – “булочка с изюмом” Томсон предложил рассматривать атом как
- 4. Опыт Резерфорда по рассеянию α-частиц Эрнст Резерфорд
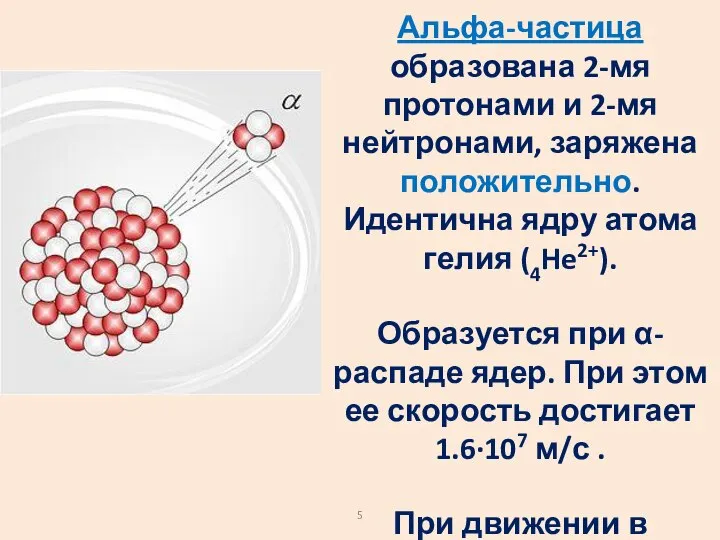
- 5. Альфа-частица образована 2-мя протонами и 2-мя нейтронами, заряжена положительно. Идентична ядру атома гелия (4He2+). Образуется при
- 6. Резерфорд направил поток α-частиц на золотую фольгу толщиной около 0,1 мкм. Большинство частиц пролетели сквозь фольгу,
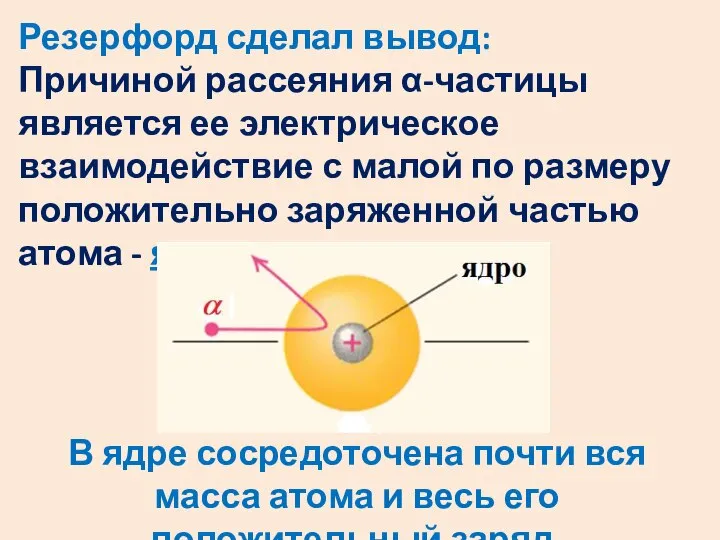
- 7. Резерфорд сделал вывод: Причиной рассеяния α-частицы является ее электрическое взаимодействие с малой по размеру положительно заряженной
- 8. Планетарная модель атома Резерфорда Атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам
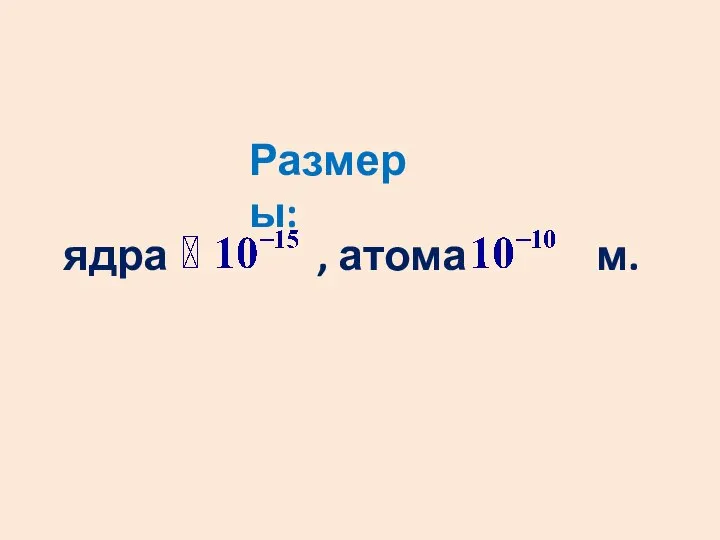
- 9. ядра , атома м. Размеры:
- 10. Неустойчивость атома Резерфорда Согласно классической электродинамике электрон при движении с центростреми-тельным ускорением должен излучать электромагнитные волны
- 11. Теория водородоподобного атома по Бору При построении теории Бор опирался на опыт Резерфорда и данные по
- 12. Водородоподобный атом – это атом с одним внешним электроном: Na, K, Rb, Cs. Спектр атома –
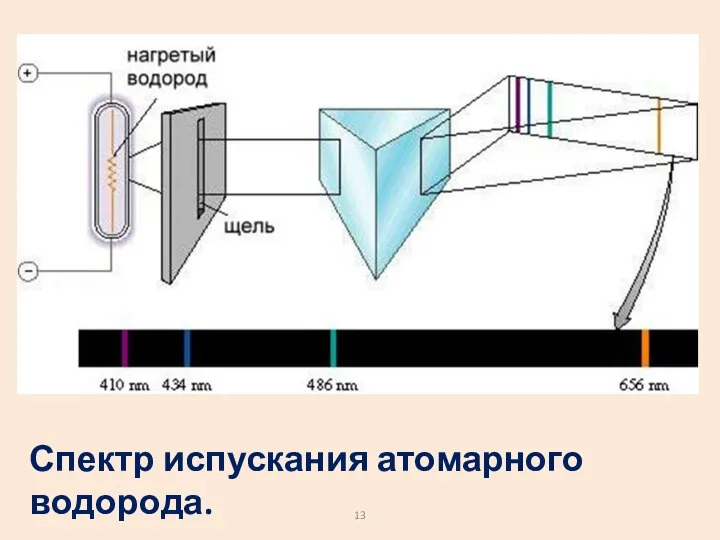
- 13. Спектр испускания атомарного водорода.
- 14. Спектр атома водорода образован сериями линий. Линии сгущаются к высокочастотной границе серии. В видимой области наблюдается
- 15. Бальмер подобрал формулу для частот спектральных линий: Для серии Бальмера m = 2, n = 3,
- 16. Постулаты Бора Атом может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует
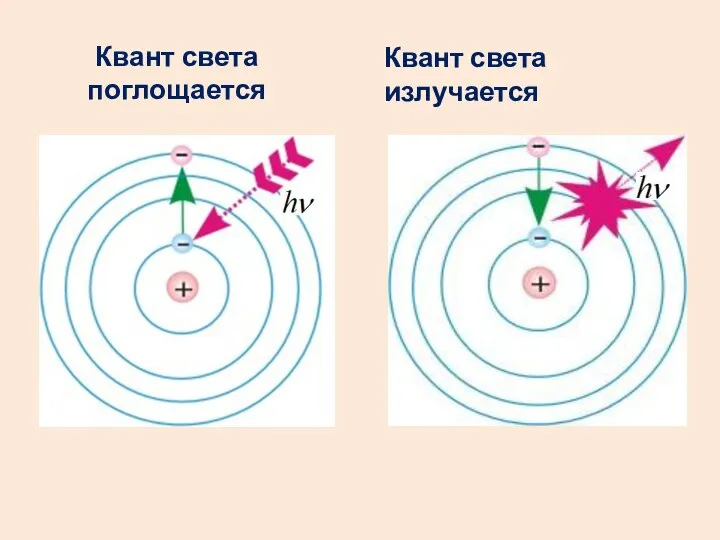
- 17. Второй постулат Бора (правило частот) При переходе атома из одного стационарного состояния с энергией Wn в
- 18. Квант света поглощается Квант света излучается
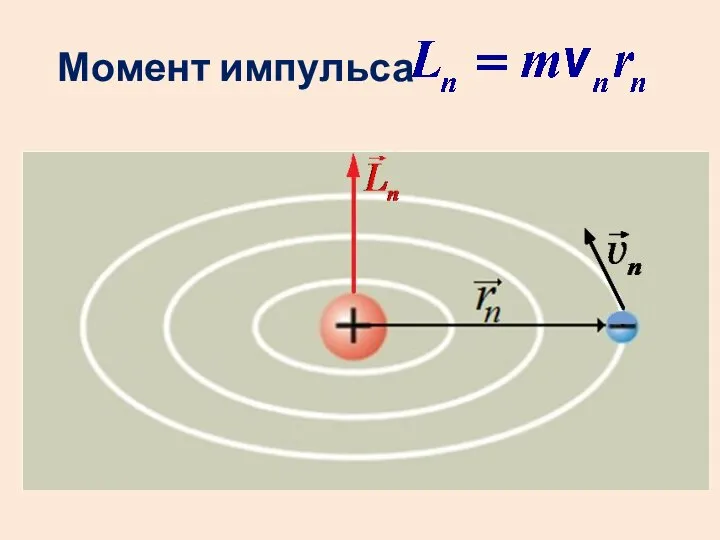
- 19. Третий постулат (квантование орбит) Момент импульса электрона в атоме принимает только дискретные значения, кратные постоянной Планка:
- 20. Момент импульса
- 21. На электрон действует кулоновская сила. По 2-му закону Ньютона
- 22. Радиус ближайшей к ядру орбиты называют первым боровским радиусом. заряд ядра,
- 23. Полная энергия электрона в атоме: Энергия электрона на первой боровской орбите в атоме водорода:
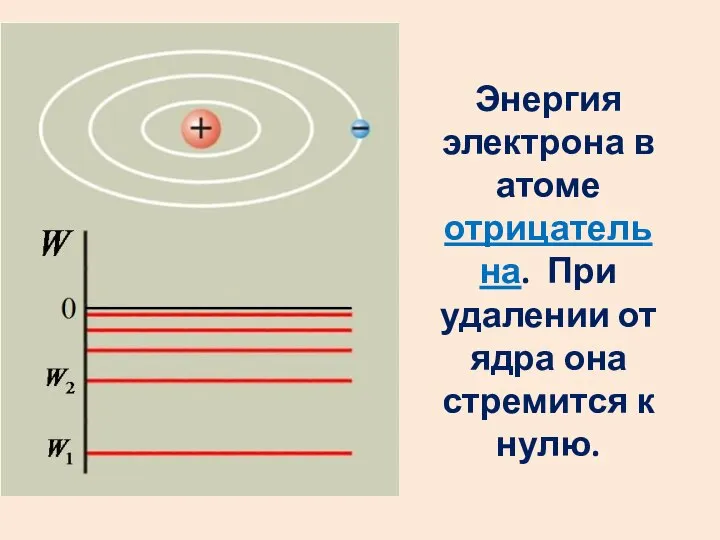
- 24. Энергия электрона в атоме отрицательна. При удалении от ядра она стремится к нулю.
- 25. Частота излучения при переходе с n-го на m-й уровень энергии: R=3,3∙1015 Гц - частотная константа Ридберга,
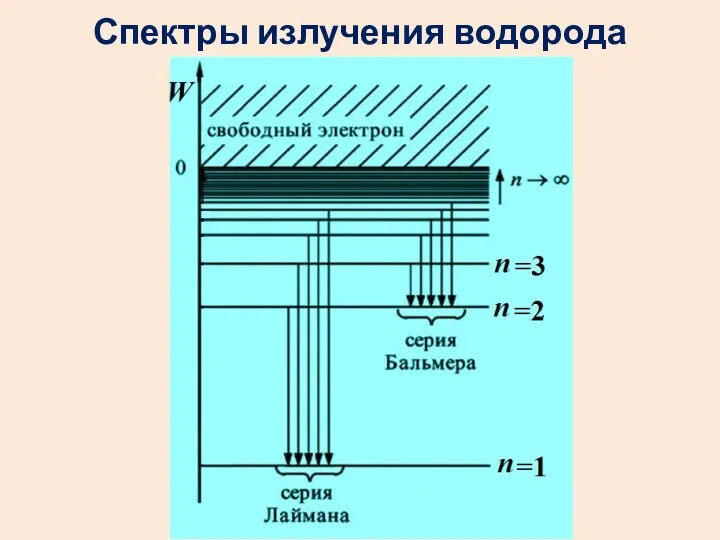
- 26. Спектры излучения водорода
- 27. Спектры поглощения водорода
- 28. Для серии Лаймана m=1, n=2, 3, 4,…. Бальмера m=2, n=3, 4, 5…. Пашена m=3, n=4, 5,
- 29. Опыт Франка и Герца Квантовые постулаты Бора нашли экспериментальное подтверждение в опыте Дж.Франка и Г. Герца.
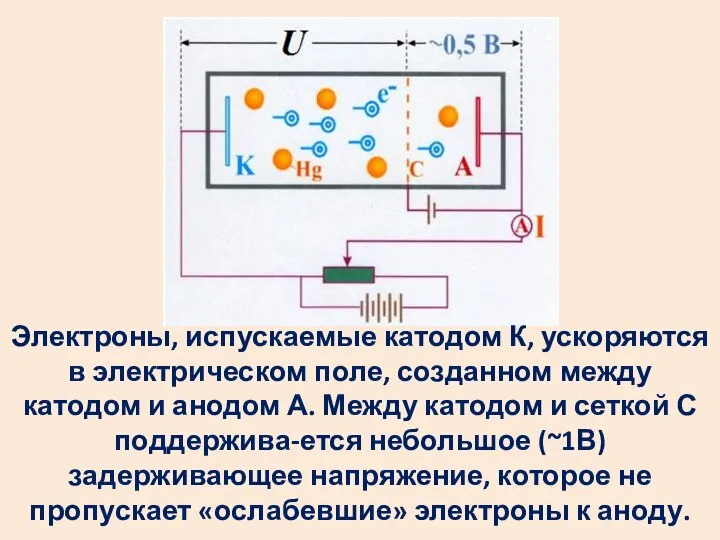
- 30. Электроны, испускаемые катодом К, ускоряются в электрическом поле, созданном между катодом и анодом А. Между катодом
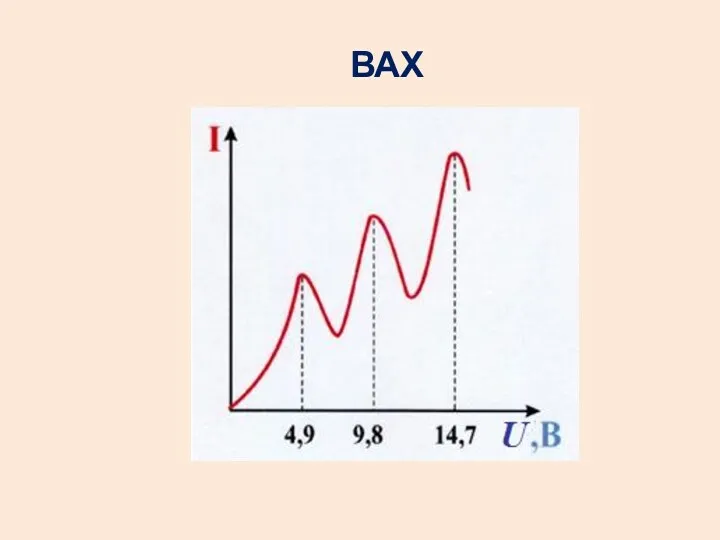
- 31. ВАХ
- 32. Опыт Франка - Герца показал, что спектр поглощаемой атомом энергии дискретен. Минимальная порция, которую может поглотить
- 33. Теория Бора дала не только качественное, но и количественное описание атомных спектров, а также опытов Франка
- 34. Достоинства и недостатки теории Бора Достоинства: 1. Объяснила линейчатый спектр атомов. 2. Предсказала значения частот. 3.
- 35. Квантовая теория атома
- 36. Электрон в атоме находится в потенциальной яме. Применим к нему уравнение Шредингера Решение уравнения дает дискретные
- 37. n=1, 2,… - главное квантовое число. Оно определяет энергию электрона, степень его удаленности от ядра, размеры
- 38. Квантование момента импульса l = 0, 1, 2, …, n-1 - орбитальное квантовое число. Модуль момента
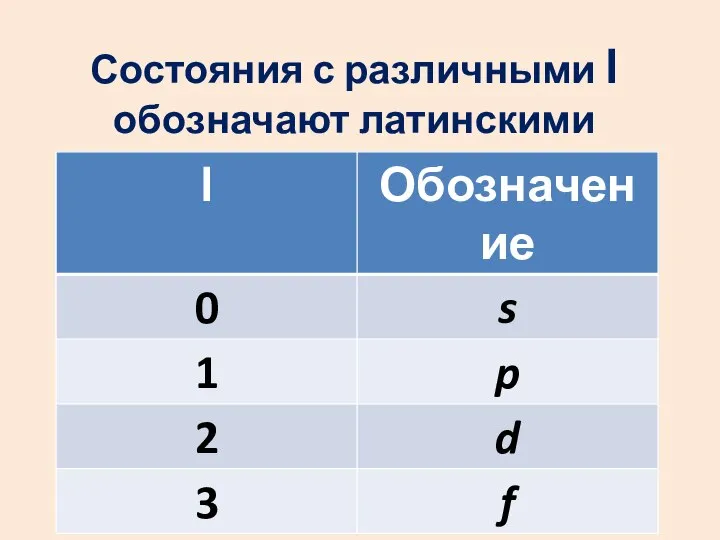
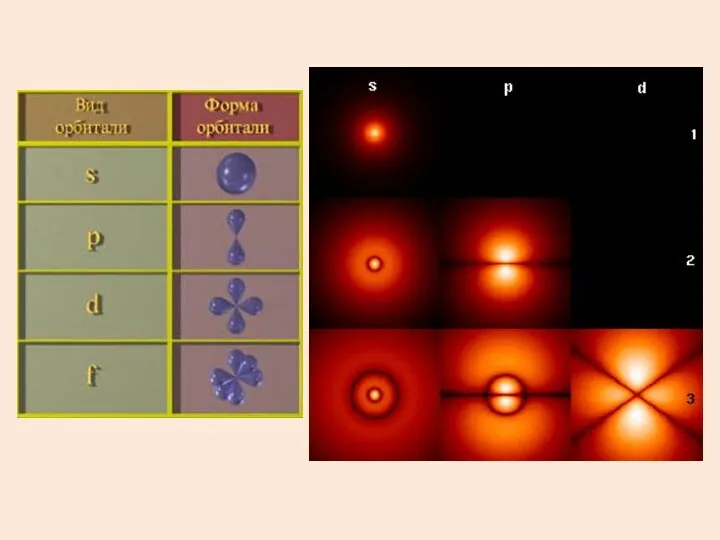
- 39. Состояния с различными l обозначают латинскими буквами
- 41. Выделим в пространстве какое-либо направление, например, направление магнитного поля. Проекция момента импульса электрона на это направление
- 42. Вектор момента импульса электрона прецессирует вокруг направления магнитного поля .
- 43. Проекция момента импульса на направ-ление z имеет дискретные значения: m – магнитное квантовое число Оно задает
- 45. Аналогично механическому моменту импульса квантуется орбитальный магнитный момент электрона:
- 48. Квантование спина Спин электрона – это его собственный момент импульса. Спин квантуется по закону: спиновое квантовое
- 49. Собственный магнитный момент электрона:
- 50. Проекция спина электрона на направление магнитного поля может принимать только одно из двух значений магнитное спиновое
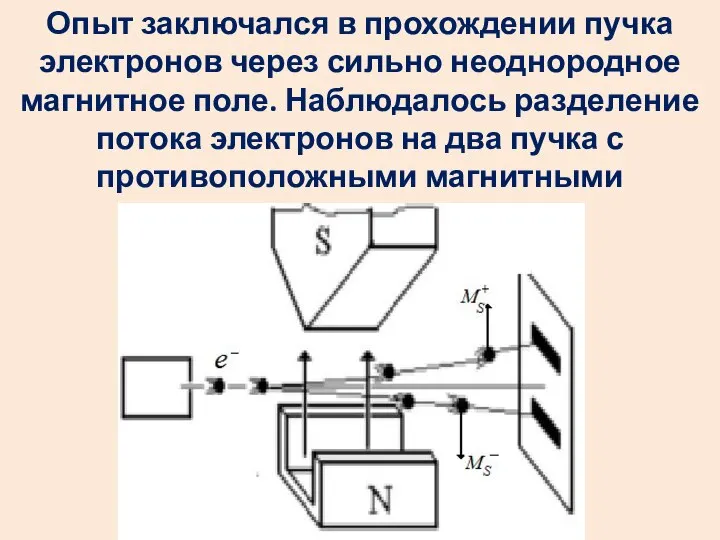
- 51. Квантование спина электрона экспериментально доказано опытами Штерна и Герлаха.
- 52. Опыт заключался в прохождении пучка электронов через сильно неоднородное магнитное поле. Наблюдалось разделение потока электронов на
- 53. Вывод: Состояние электрона в атоме определяется набором 4-х квантовых чисел: главного n, (n = 1, 2,
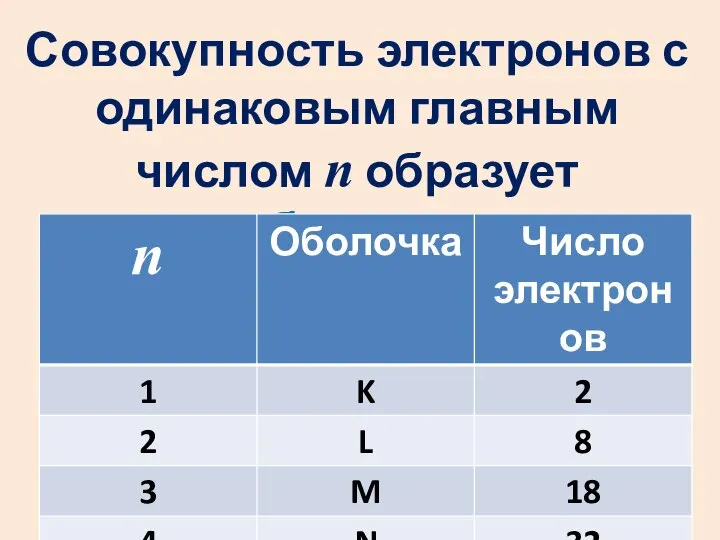
- 54. Число состояний на энергетичес-ком уровне с главным квантовым числом n: с учетом спина
- 55. Совокупность электронов с одинаковым главным числом n образует оболочку.
- 56. Правила отбора: возможны лишь такие переходы между состояниями, при которых
- 58. Скачать презентацию








































 Корпускулярные свойства рентгеновского излучения
Корпускулярные свойства рентгеновского излучения Внимательно изучите условие задачи, поймите физическую сущность явлений и процессов, рассматриваемых в задаче, уясните основной в
Внимательно изучите условие задачи, поймите физическую сущность явлений и процессов, рассматриваемых в задаче, уясните основной в Скалярное поле. Поверхности и линии уровня. Градиент скалярного поля. Лекция 30
Скалярное поле. Поверхности и линии уровня. Градиент скалярного поля. Лекция 30 Голограмма – чудо современной оптики
Голограмма – чудо современной оптики Колебания. Общие понятия
Колебания. Общие понятия Экспериментальные методы регистрации ионизирующих излучений 11 класс Подготовили: Гаськова М. Яремич В. учитель
Экспериментальные методы регистрации ионизирующих излучений 11 класс Подготовили: Гаськова М. Яремич В. учитель Простые механизмы. Рычаг. Равновесие сил на рычаге
Простые механизмы. Рычаг. Равновесие сил на рычаге Курс лекций. Электрический привод
Курс лекций. Электрический привод Тема 3. Движение квазичастиц электронов в электрическом поле
Тема 3. Движение квазичастиц электронов в электрическом поле Расчет на выносливость по контактным напряжениям
Расчет на выносливость по контактным напряжениям Способы установки и закрепления заготовок при обработке
Способы установки и закрепления заготовок при обработке Кинематика вращательного движения твёрдого тела
Кинематика вращательного движения твёрдого тела Презентация по физике на тему: «Двигатель внутреннего сгорания»
Презентация по физике на тему: «Двигатель внутреннего сгорания»  Презентация по физике "Электроизмерительные приборы" - скачать
Презентация по физике "Электроизмерительные приборы" - скачать  Становление механики © В.Е. Фрадкин, СПб АППО, 2006
Становление механики © В.Е. Фрадкин, СПб АППО, 2006 Тема: Решение задач по теме: «Давление твердых тел , жидкостей и газов»
Тема: Решение задач по теме: «Давление твердых тел , жидкостей и газов» Разряд в неоднородном электрическом поле. Корона. Сценарии разрядных процессов в коаксиале. (Лекция 3)
Разряд в неоднородном электрическом поле. Корона. Сценарии разрядных процессов в коаксиале. (Лекция 3) Кинематический анализ
Кинематический анализ Векторлар өрісінің циркуляциясы, роторы
Векторлар өрісінің циркуляциясы, роторы Принцип плавания судов
Принцип плавания судов Физика на кухне
Физика на кухне Теоретическая прочность в сравнении с реальной. Дислокации и дисклинации. Лекция 1
Теоретическая прочность в сравнении с реальной. Дислокации и дисклинации. Лекция 1 Системы, элементы, сигналы Составила Антонова Е.П. 2010г.
Системы, элементы, сигналы Составила Антонова Е.П. 2010г. Квалификационный экзамен по ПМ 04 Слесарь по ремонту дорожно-строительных машин и тракторов
Квалификационный экзамен по ПМ 04 Слесарь по ремонту дорожно-строительных машин и тракторов Изоляторы ЛЭП. Линейные изоляторы
Изоляторы ЛЭП. Линейные изоляторы Электричество. Электростатика
Электричество. Электростатика Термодинамика. Тепловая машина. (Лекция 7)
Термодинамика. Тепловая машина. (Лекция 7) Введение в физику. Механика
Введение в физику. Механика