Возникновение атомистической гипотезы строения вещества и ее экспериментальные доказательства. Идеальный газ
Содержание
- 2. Цель работы: сформировать представления о структуре и содержании новой физической теории, организовать усвоение основных положений МКТ
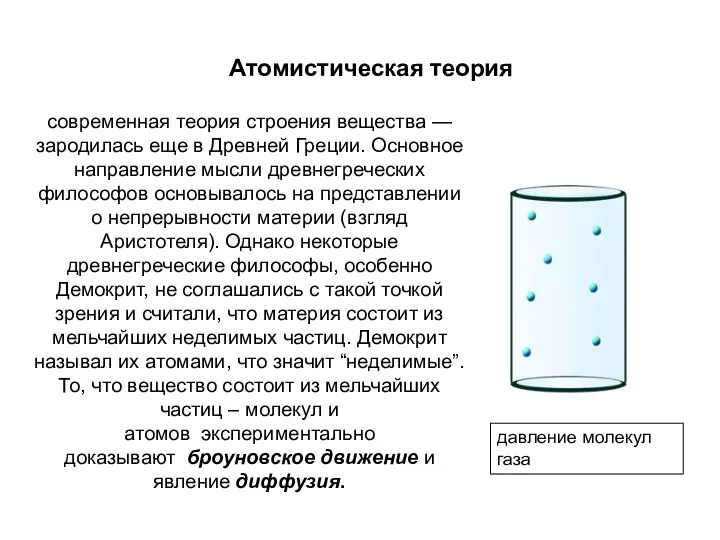
- 3. Атомистическая теория современная теория строения вещества — зародилась еще в Древней Греции. Основное направление мысли древнегреческих
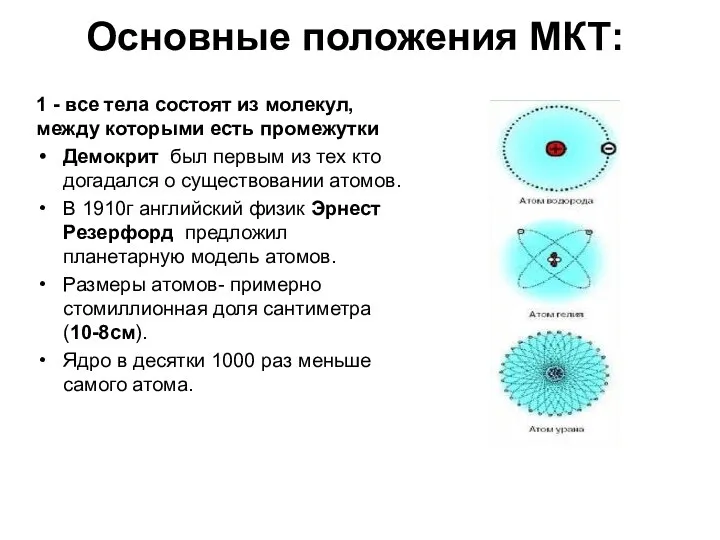
- 4. Основные положения МКТ: 1 - все тела состоят из молекул, между которыми есть промежутки Демокрит был
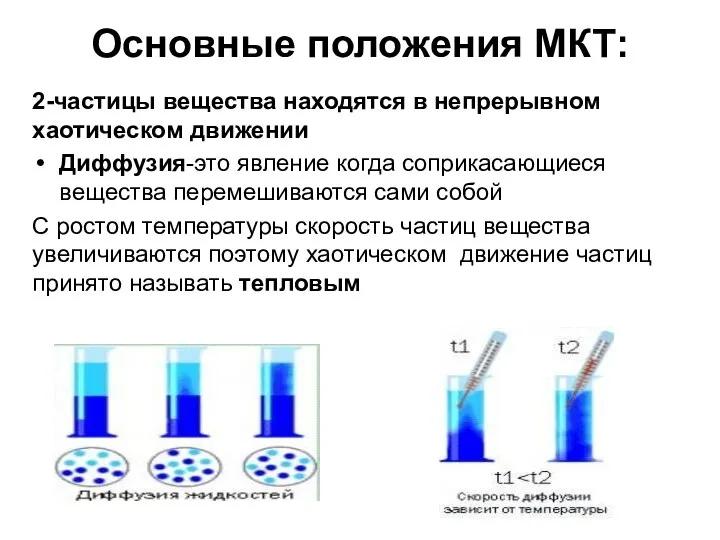
- 5. Основные положения МКТ: 2-частицы вещества находятся в непрерывном хаотическом движении Диффузия-это явление когда соприкасающиеся вещества перемешиваются
- 6. Основные положения МКТ: 3 - частицы вещества взаимодействуют друг с другом. Частицы вещества одновременно и притягиваются
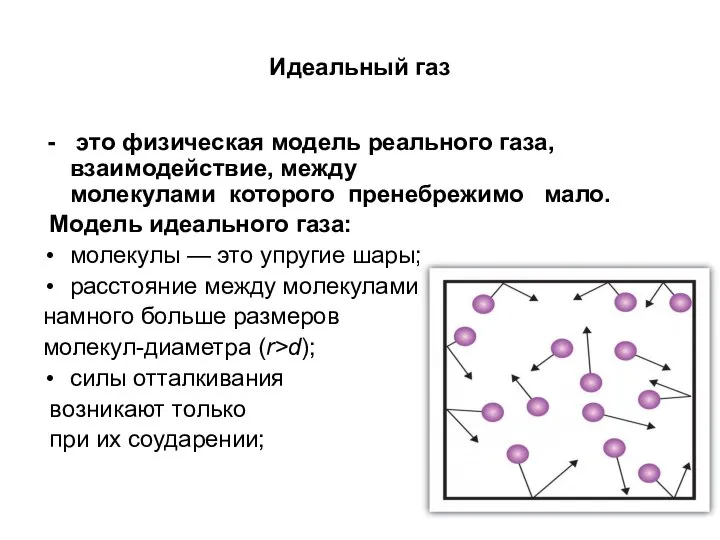
- 7. Идеальный газ это физическая модель реального газа, взаимодействие, между молекулами которого пренебрежимо мало. Модель идеального газа:
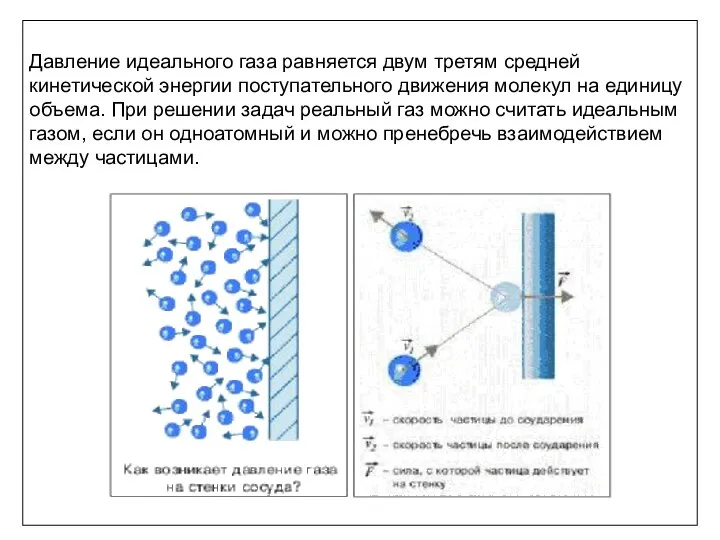
- 9. Основное уравнение молекулярно-кинетической теории При соприкосновении частицы с границей емкости проекция vx скоростного вектора на ось
- 10. Давление идеального газа равняется двум третям средней кинетической энергии поступательного движения молекул на единицу объема. При
- 11. Основное уравнение МКТ идеального газа -связывает микропараметры частиц ( массу молекулы, средний квадрат скорости молекул) с
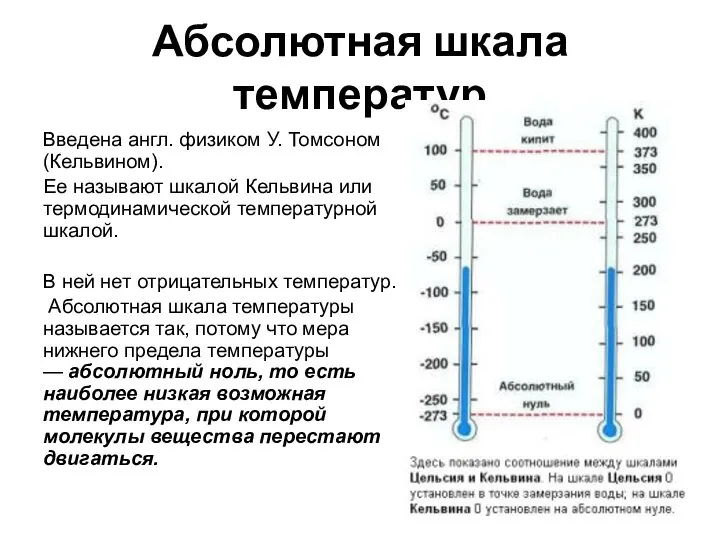
- 12. Абсолютная шкала температур Введена англ. физиком У. Томсоном(Кельвином). Ее называют шкалой Кельвина или термодинамической температурной шкалой.
- 13. Уи́льям То́мсон, барон Ке́львин (26 июня 1824 – 17 декабря 1907 гг.) британский физик и механик.
- 14. Единица абсолютной температуры в СИ: [T]=1K (Кельвин). Нулевая температура абсолютной шкалы – это абсолютный ноль 00К
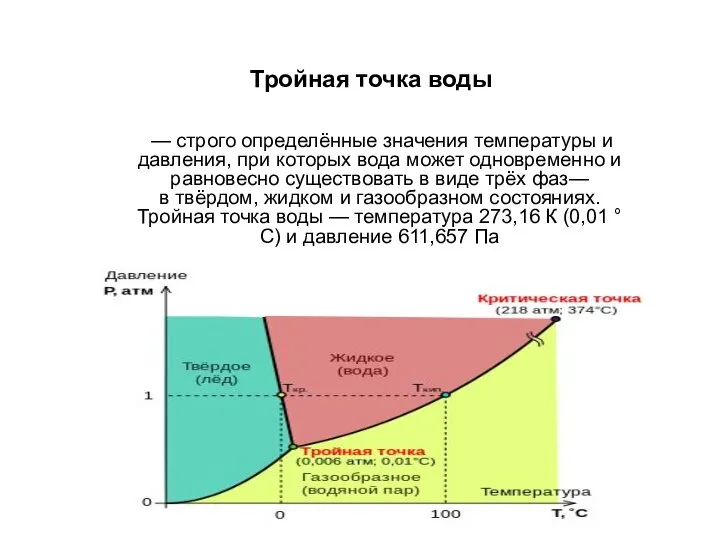
- 15. Тройная точка воды — строго определённые значения температуры и давления, при которых вода может одновременно и
- 16. Тройная точка воды как видно из параметров тройной точки воды, при нормальных условиях равновесное сосуществование льда,
- 18. Скачать презентацию






![Единица абсолютной температуры в СИ: [T]=1K (Кельвин). Нулевая температура абсолютной шкалы](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1468764/slide-13.jpg)

 ГЕОРГ СИМОН ОМ
ГЕОРГ СИМОН ОМ Презентация по физике "Первоначальные сведения о строении вещества" -
Презентация по физике "Первоначальные сведения о строении вещества" -  Техническая система и её элементы (6 класс)
Техническая система и её элементы (6 класс) Презентация по Физике на тему Электрический ток в различных средах
Презентация по Физике на тему Электрический ток в различных средах  Радиационный фон школьных помещений (ГБОУ школа №430
Радиационный фон школьных помещений (ГБОУ школа №430  Телескоп
Телескоп Машиностроение
Машиностроение Свободное падение
Свободное падение Схеми набираючої групи. (Заняття 29)
Схеми набираючої групи. (Заняття 29) Динамика материальной точки. Масса и импульс. Законы Ньютона
Динамика материальной точки. Масса и импульс. Законы Ньютона Термодинамика
Термодинамика Линзы. Оптическая сила линзы
Линзы. Оптическая сила линзы Вепольный анализ
Вепольный анализ Разделы физики
Разделы физики Ответы и решения.Решение задачи А1
Ответы и решения.Решение задачи А1 Кристаллические тела (10 класс)
Кристаллические тела (10 класс) Метод поиска решений творческих задач. Метод фокальных объектов
Метод поиска решений творческих задач. Метод фокальных объектов Элементы релятивистской механики. Специальная теория относительности. (Лекция 4.2)
Элементы релятивистской механики. Специальная теория относительности. (Лекция 4.2) Демонстрационный вариант контрольных измерительных материалов единого государственного экзамена 2010 года по физике
Демонстрационный вариант контрольных измерительных материалов единого государственного экзамена 2010 года по физике ЭЛЕКТРОМАГНИТНАЯ ПРИРОДА СВЕТА
ЭЛЕКТРОМАГНИТНАЯ ПРИРОДА СВЕТА  Активационные методы. (Лекция 6)
Активационные методы. (Лекция 6) Закони динаміки. Сили та види взаємодій
Закони динаміки. Сили та види взаємодій Ионосфера. Прохождение. Диапазоны Лекция радиоклуба МИЭТ
Ионосфера. Прохождение. Диапазоны Лекция радиоклуба МИЭТ Оптические приборы. Глаз
Оптические приборы. Глаз Попов Александр Степанович 1859-1905
Попов Александр Степанович 1859-1905 Монтаж, ремонт и обслуживание комплектных распределительных устройств
Монтаж, ремонт и обслуживание комплектных распределительных устройств СОВРЕМЕННЫЕ ТЕРМОМЕТРЫ. ТЕМПЕРАТУРНЫЕ ШКАЛЫ. ВЕТРОВА ЕЛЕНА, учащаяся МУСОШ № 37 г. Иваново, НАУМОВА ЛАРИСА ГЕННАДЬЕВНА , учитель фи
СОВРЕМЕННЫЕ ТЕРМОМЕТРЫ. ТЕМПЕРАТУРНЫЕ ШКАЛЫ. ВЕТРОВА ЕЛЕНА, учащаяся МУСОШ № 37 г. Иваново, НАУМОВА ЛАРИСА ГЕННАДЬЕВНА , учитель фи Взаимодействие тел. Масса
Взаимодействие тел. Масса