Содержание
- 2. Самопроизвольный процесс – процесс, который может протекать без затраты работы извне, причем в результате может быть
- 3. Несамопроизвольный (вынужденный) процесс – процесс, для протекания которого требуется затрата работы извне в количестве, пропорциональном производимому
- 4. Второе начало термодинамики дает возможность определить, 1 - какой из процессов будет протекать самопроизвольно (прямой или
- 5. Второе начало термодинамики дает возможность определить, какими должны быть условия, чтобы нужный процесс протекал в необходимом
- 6. Формулировки второго начала термодинамики: - Теплота не может самопроизвольно переходить от менее нагретого тела к более
- 7. Для КПД идеальной тепловой машины, работающей по циклу Карно: Максимальный КПД тепловой машины не зависит от
- 8. Для необратимо работающей тепловой машины уравнение преобразуется в неравенство: Для общего случая можем записать: Любая форма
- 9. Можно условно принять, что внутренняя энергии системы состоит из двух составляющих: "свободной" X энергий -причем "свободная"
- 10. Мерой связанной энергии является новая термодинамическая функция состояния, называемая Энтропией. Выражение является определением новой функции состояния
- 11. Если система обратимо переходит из состояния 1 в состояние 2, изменение энтропии будет равно: Подставляя в
- 12. Если рассматривать изолированную систему (δQ = 0), то для обратимого процесса dS = 0, для самопроизвольного
- 13. Выводы: 1. В изолированных системах самопроизвольно могут протекать только процессы, сопровождающиеся увеличением энтропии. 2. Энтропия изолированной
- 14. Статистическая интерпретация энтропии Классическая термодинамика рассматривает происходящие процессы безотносительно к внутреннему строению системы; поэтому в рамках
- 15. Количественная связь между энтропией S и термодинамической вероятностью Ω (омега) выражается формулой Больцмана: S = klnΩ
- 16. ТРЕТЬЕ НАЧАЛО ТЕРМОДИНАМИКИ Внутреннюю энергию системы можно условно представить в виде суммы двух величин "свободной" и
- 17. Основные положения тепловой теоремы: 1. При абсолютном нуле температуры свободная энергия X равна теплоте процесса. Xo=
- 18. Строго говоря, тепловая теорема Нернста и постулат Планка являются следствиями из второго начала термодинамики. Но независимо
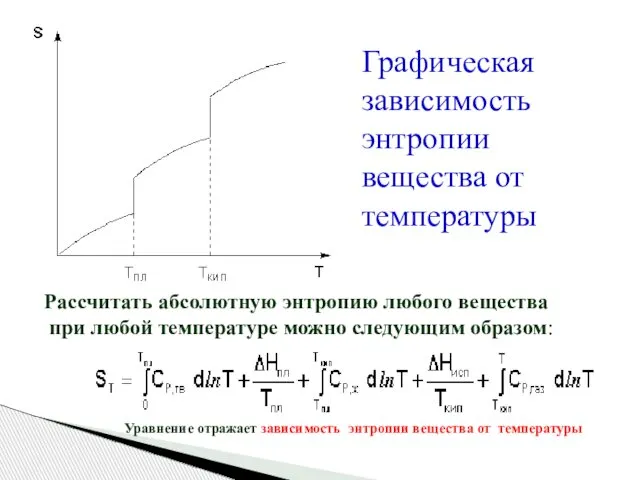
- 19. Расчет абсолютной энтропии. Рассчитаем изменение энтропии некоторой системы при нагревании её от абсолютного нуля до температуры
- 20. При T ⇒ 0 любое вещество может находиться только в твердом состоянии. При нагревании вещества возможен
- 21. Графическая зависимость энтропии вещества от температуры Рассчитать абсолютную энтропию любого вещества при любой температуре можно следующим
- 22. Поскольку энтропия есть функция состояния, изменение энтропии в ходе химического процесса определяется только видом и состоянием
- 23. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ Изменение энтропии однозначно определяет направление и предел самопроизвольного протекания процесса лишь для наиболее простых
- 24. Для характеристики процессов, протекающих в закрытых системах, были введены новые термодинамические функции состояния: изобарно-изотермический потенциал -
- 25. Поведение всякой термодинамической системы в общем случае определяется одновременным действием двух факторов – энтальпийного, отражающего стремление
- 26. Для изолированных систем (ΔН = 0) направление и предел самопроизвольного протекания процесса однозначно определяется величиной изменения
- 27. Для закрытых систем при температурах, не равных нулю, необходимо одновременно учитывать оба фактора. Направление и предел
- 28. Для закрытых систем, находящихся в изобарно-изотермических либо изохорно-изотермических условиях свободная энергия принимает вид изобарно-изотермического либо изохорно-изотермического
- 29. Рассмотрим закрытую систему, в которой осуществляется равновесный процесс при постоянных температуре и объеме. Выразим работу данного
- 30. Закрытую систему, находящуюся в изобарно-изотермических условиях, характеризует изобарно-изотермический потенциал G: Поскольку –ΔF = Amax, можно записать:
- 31. Основываясь на принципе минимума свободной энергии, сформулируем условия самопроизвольного протекания процесса в закрытых системах. Условия самопроизвольного
- 32. В химии наиболее часто используется изобарно-изотермический потенциал, поскольку большинство химических (и биологических) процессов происходят при постоянном
- 33. Основываясь на этом уравнении, можно оценить вклад энтальпийного и энтропийного факторов в величину ΔG и сделать
- 34. ХИМИЧЕСКОЕ РАВНОВЕСИЕ Протекание самопроизвольного процесса в термодинамической системе сопровождается уменьшением свободной энергии системы (dG 0. Условием
- 36. Скачать презентацию
































 Философские проблемы науки и техники. Классическая механика. (Лекция 5)
Философские проблемы науки и техники. Классическая механика. (Лекция 5) Магнитное поле Земли
Магнитное поле Земли Рычаг
Рычаг Уклон и конусность
Уклон и конусность Параллельная работа синхронных генераторов. Режим работы электропривода якорно-швартовных механизмов. (Билет 5)
Параллельная работа синхронных генераторов. Режим работы электропривода якорно-швартовных механизмов. (Билет 5) Расчет статически определимых систем на подвижную нагрузку
Расчет статически определимых систем на подвижную нагрузку Относительность движения
Относительность движения Магниторазведка
Магниторазведка Енергія електричного поля
Енергія електричного поля Зависимость силы тока от напряжения
Зависимость силы тока от напряжения Презентация Сила трения.
Презентация Сила трения. Точность различных методов базирования. Требования к деталям поступающим на сборку
Точность различных методов базирования. Требования к деталям поступающим на сборку Монтаж, техническая эксплуатация и ремонт холодильного шкафа для продуктов двухдверного
Монтаж, техническая эксплуатация и ремонт холодильного шкафа для продуктов двухдверного Атомная и ядерная физика
Атомная и ядерная физика Ядерный реактор
Ядерный реактор Перспективы развития атомной энергетики
Перспективы развития атомной энергетики Электрический ток в вакууме. Диод. Работу выполнили: Брюхов А., Нисов А.
Электрический ток в вакууме. Диод. Работу выполнили: Брюхов А., Нисов А.  Физика в военном деле
Физика в военном деле Свободное падение тел. Движение с ускорением свободного падения
Свободное падение тел. Движение с ускорением свободного падения Центр тяжести тела. Условия равновесия тел
Центр тяжести тела. Условия равновесия тел Классификация и параметры ДВС 1
Классификация и параметры ДВС 1 Физика как наука
Физика как наука Презентация по физике "Модели атома" - скачать
Презентация по физике "Модели атома" - скачать  Метрология, стандартизация и сертификация
Метрология, стандартизация и сертификация Амплитуда колебаний в звуковой волне
Амплитуда колебаний в звуковой волне Устройство и технические характеристики тягового двигателя ЭДП810 (СТК 810)
Устройство и технические характеристики тягового двигателя ЭДП810 (СТК 810) Уравнения распространения волн
Уравнения распространения волн Попов – основатель радиовещания
Попов – основатель радиовещания