Содержание
- 2. Все оксиды и гидроксиды по их химическим свойствам можно разделить на три вида: основные амфотерные кислотные
- 3. Если соединение реагирует с кислотой с образованием соли и воды, то оно обладает основными свойствами. Например:
- 4. Если соединение реагирует со щелочью с образованием соли и воды, то оно обладает кислотными свойствами. Например:
- 5. Но есть и вещества - «хамелеоны». При добавлении к таким веществам кислоты, они проявляют основные свойства,
- 6. К амфотерным соединениям относят оксиды и гидроксиды некоторых металлов (в них металл чаще всего имеет степень
- 7. Точно так же и при реакции гидроксида цинка с соляной кислотой образуются соль хлорид цинка и
- 8. Рассмотрим уравнения этих реакций. ZnO+2KOH=K2ZnO2+H2O Zn(OH)2+2KOH=K2ZnO2+2H2O Амфотерный оксид цинка в реакции со щелочью гидроксид калия образовал
- 9. Таким образом классификацию оксидов и гидроксидов можно представить следующей схемой:
- 10. Так как кислотность, основность или амфотерность химических свойств определяют экспериментальным образом, рассмотрим опыт, позволяющий доказать, что
- 11. Внимание! Если для нерастворимого основания не имел значения порядок смешивания растворов, для амфотерного гидроксида он принципиально
- 12. Полученный осадок амфотерного гидроксида алюминия нужно разделить пополам.
- 13. При добавлении к первому образцу гидроксида алюминия избытка кислоты исчезновение осадка доказывает наличие у него основных
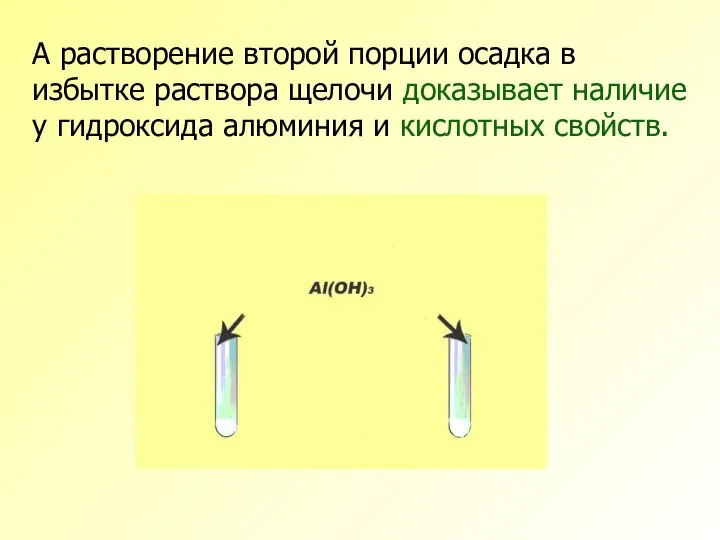
- 14. А растворение второй порции осадка в избытке раствора щелочи доказывает наличие у гидроксида алюминия и кислотных
- 15. Таким образом это исследование доказало кислотно-основную двойственность химических свойств гидроксида алюминия, то есть его амфотерность. Уравнениями
- 16. Реакция гидроксида алюминия с раствором кислоты: Al(OH)3+3HCl=AlCl3+3H2O Реакция гидроксида алюминия с избытком раствора щелочи: Al(OH)3+KOH=K[Al(OH)4] Полученный
- 18. Скачать презентацию














 Второе начало термодинамики. Направленность химических процессов
Второе начало термодинамики. Направленность химических процессов Apa în natură. Resursele de apă
Apa în natură. Resursele de apă Электрохимический ряд напряжений металлов
Электрохимический ряд напряжений металлов  Мое любимое химическое вещество: Серебро
Мое любимое химическое вещество: Серебро Кристаллические решетки
Кристаллические решетки Относительная атомная масса
Относительная атомная масса Мұнай құрамындағы тұздың мөлшерін анықтау
Мұнай құрамындағы тұздың мөлшерін анықтау Реакционная способность аренов
Реакционная способность аренов NiCl2 - Никель хлориді
NiCl2 - Никель хлориді Вчені - хіміки
Вчені - хіміки  Строение атома
Строение атома Плазма та її властивості. Практичне застосування плазми. (11 клас)
Плазма та її властивості. Практичне застосування плазми. (11 клас) Свойства покрытий на основе акрилового лака
Свойства покрытий на основе акрилового лака СОЕДИНЕНИЯ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ
СОЕДИНЕНИЯ ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ Презентация по Химии "Токсикологическая химия" - скачать смотреть
Презентация по Химии "Токсикологическая химия" - скачать смотреть  Нуклеиновые кислоты
Нуклеиновые кислоты Презентация по Химии "ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА" - скачать смотреть бесплатно
Презентация по Химии "ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА" - скачать смотреть бесплатно Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4)
Индол. Методы синтеза. Химические свойства. Биологически активные производные. (Лекция 4) Влияние этилового спирта на организм детей
Влияние этилового спирта на организм детей Тайна воды которую мы пьём
Тайна воды которую мы пьём L’introduction a la biochimie. La structure et les proprietes des proteines
L’introduction a la biochimie. La structure et les proprietes des proteines Гетероциклді қосылыстар. Алкалоидтар
Гетероциклді қосылыстар. Алкалоидтар Системы эвтектического типа
Системы эвтектического типа Тренировочный вариант заданий для подготовки к ГИА по химии
Тренировочный вариант заданий для подготовки к ГИА по химии Химическое строение рецепторов и лигандов. Агонисты и антогонисты, принцип структурной комплементарности
Химическое строение рецепторов и лигандов. Агонисты и антогонисты, принцип структурной комплементарности Презентация по химии Количество вещества
Презентация по химии Количество вещества Теория химического строения А. М. Бутлерова. Часть III
Теория химического строения А. М. Бутлерова. Часть III Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения
Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения