Содержание
- 2. Взаимное влияние атомов в молекуле может осуществляться по системе σ-связей (индуктивный эффект), по системе π-связей (мезомерный
- 3. Индуктивный эффект (I-эффект) – смещение электронной плотности по цепи σ -связей, которое обусловлено различиями в электроотрицательностях
- 4. Индуктивный эффект обозначают буквой I и графически изображают стрелкой, остриё которой направлено в сторону более ЭО
- 5. –I эффект проявляют заместители, которые содержат атомы с большей ЭО, чем у углерода: -F, -Cl, -Br,
- 6. +I эффект проявляют заместители, содержащие атомы с низкой электроотрицательностью: металлы (-Mg, -Li); насыщенные углеводородные радикалы (-CH3,
- 7. Мезомерный эффект – смещение электронной плотности по цепи сопряженных π-связей. Возникает только при наличии сопряжения связей.
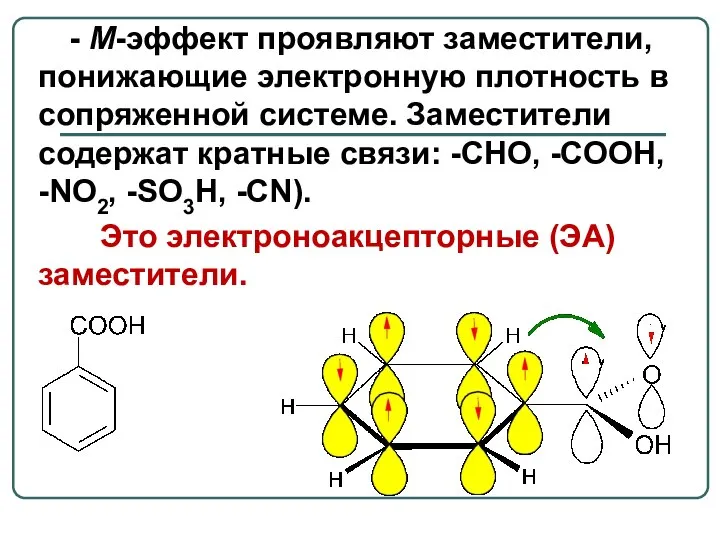
- 8. - М-эффект проявляют заместители, понижающие электронную плотность в сопряженной системе. Заместители содержат кратные связи: -CHO, -COOH,
- 9. +М-эффектом обладают заместители, повышающие электронную плотность в сопряженной системе. К ним относятся -OH, -NH2, -OCH3, -O-,
- 10. В молекулах органических соединений индуктивный и мезомерный эффекты заместителей, действуют одновременно.
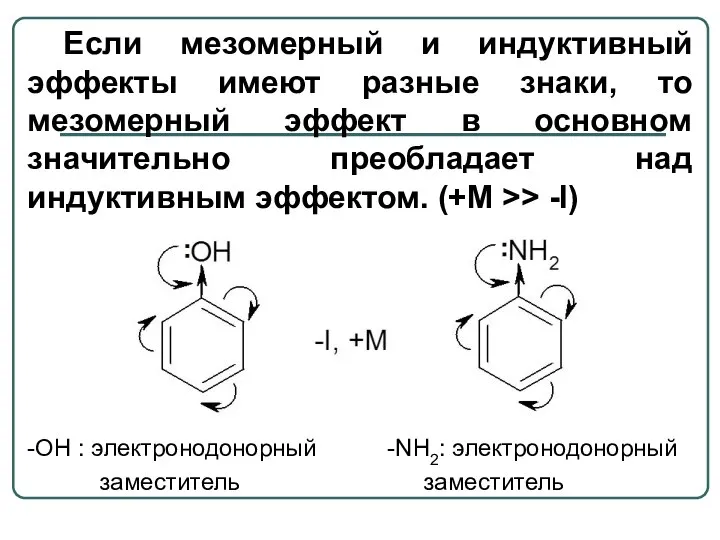
- 11. Если мезомерный и индуктивный эффекты имеют разные знаки, то мезомерный эффект в основном значительно преобладает над
- 12. -СООН, -СНО: электроноакцепторный заместитель
- 13. Таким образом, учитывая перераспределение электронной плотности в молекулах органических соединений можно прогнозировать их свойства.
- 14. Классификация заместителей -NH2, -NHR, -NR2 -OH -OR -NHCOCH3 -C6H5 -R -H -X -CHO, -COR -SO3H -COOH,
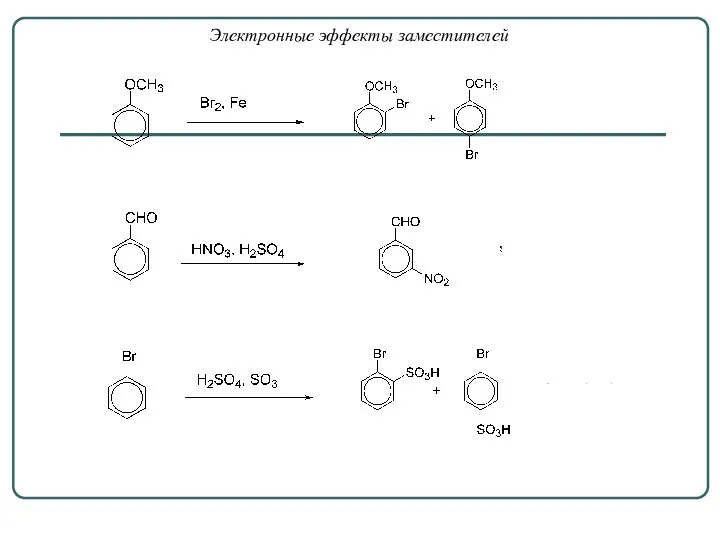
- 15. Электронные эффекты заместителей
- 16. 1. Общая характеристика спиртов. 2. Одноатомные спирты: физические и химические свойства, способы получения. 3. Многоатомные спирты.
- 17. 1. Общая характеристика спиртов. Номенклатура, классификация, изомерия.
- 18. Гидроксисоединения – это вещества, которые в своем составе содержат OH-группы. К ним относят спирты, фенолы, нафтолы
- 19. Спирты – это гидроксисоединения, в молекулах которых OH-группы связаны с насыщенным атомом углерода, находящимся в состоянии
- 21. Классификация спиртов I. По строению углеводородного радикала: - алифатические предельные и непредельные: пропанол-1, бутен-2-ол-1 - алициклические:
- 22. II. По числу OH-групп: a) одноатомные спирты этанол бензиловый спирт
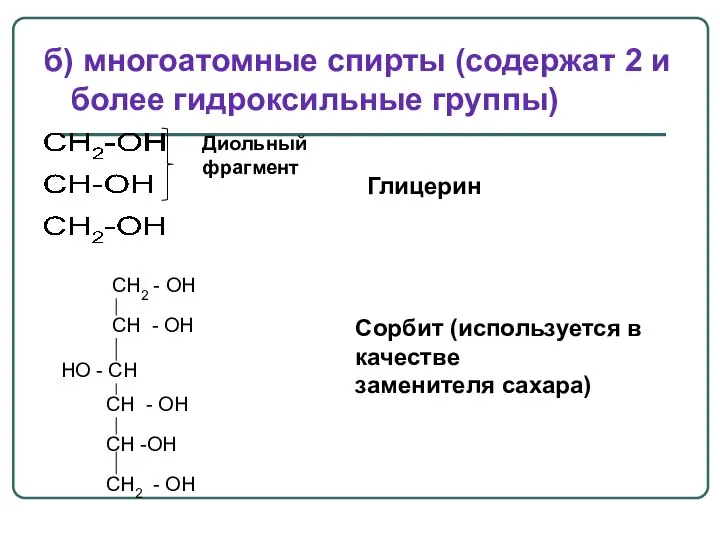
- 23. б) многоатомные спирты (содержат 2 и более гидроксильные группы) Глицерин Диольный фрагмент CH2 - OH CH
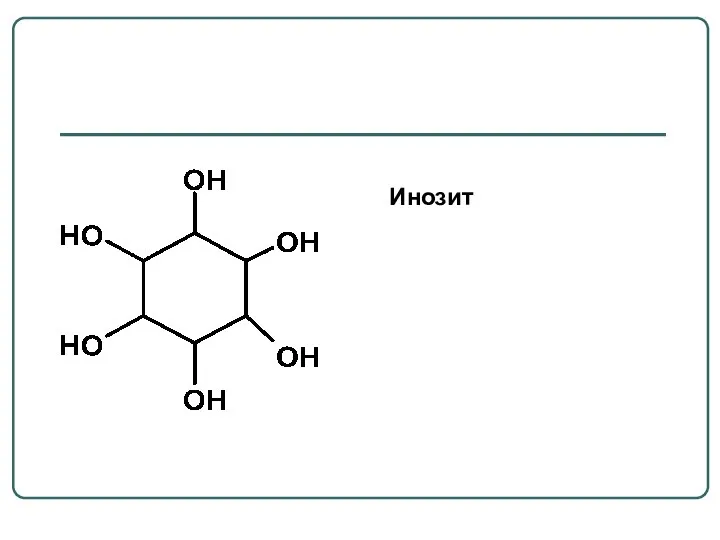
- 24. Инозит
- 25. III. По характеру атома углерода звена, с которым соединена OH-группа a) первичные спирты б) вторичные спирты
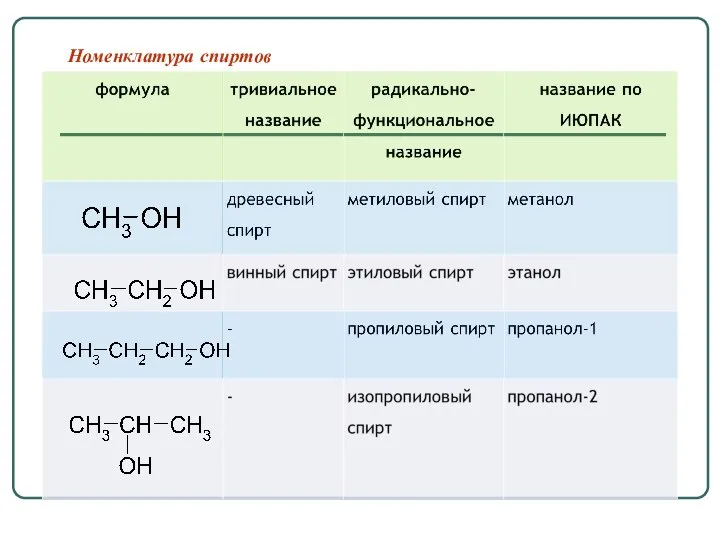
- 26. Номенклатура спиртов
- 27. 2. Одноатомные спирты: физические и химические свойства, способы получения.
- 28. Физические свойства спиртов Низшие члены гомологического ряда спиртов являются жидкостями и, начиная с C12, одноатомные спирты
- 29. Гидроксигруппа является сильно полярной группой, поэтому низшие спирты растворяются в воде неограниченно: метанол, этанол, пропанол смешиваются
- 30. Метиловый спирт считается самым ядовитым спиртом. Прием внутрь вызывает слепоту или смерть. НЕ ПЕЙ МЕТИЛОВЫЙ СПИРТ
- 31. В молекуле спиртов можно выделить несколько реакционных центров: О-Н кислотный центр, за счет полярности связи способный
- 32. 1 R CH CH2 O H 4 3 1 1. OH-кислотный центр 2. Нуклеофильный и n
- 33. Химические свойства Спирты проявляют слабые кислотные и слабые основные свойства, то есть являются амфолитами. I. Реакции
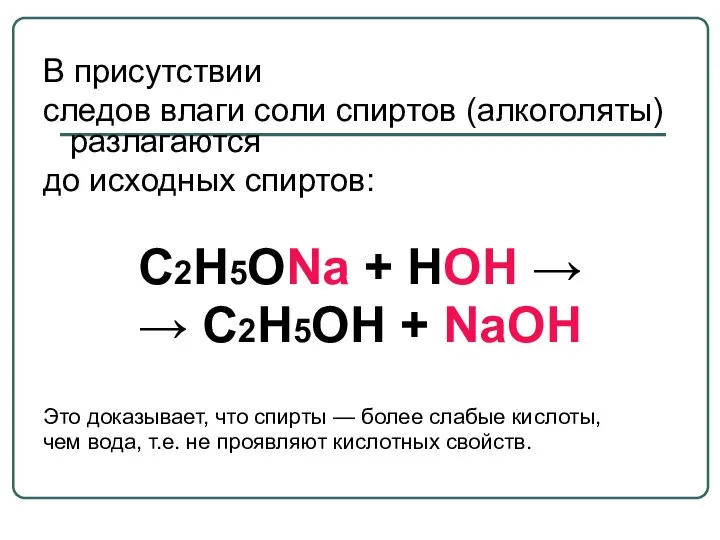
- 34. В присутствии следов влаги соли спиртов (алкоголяты) разлагаются до исходных спиртов: С2Н5ОNa + НОН → →
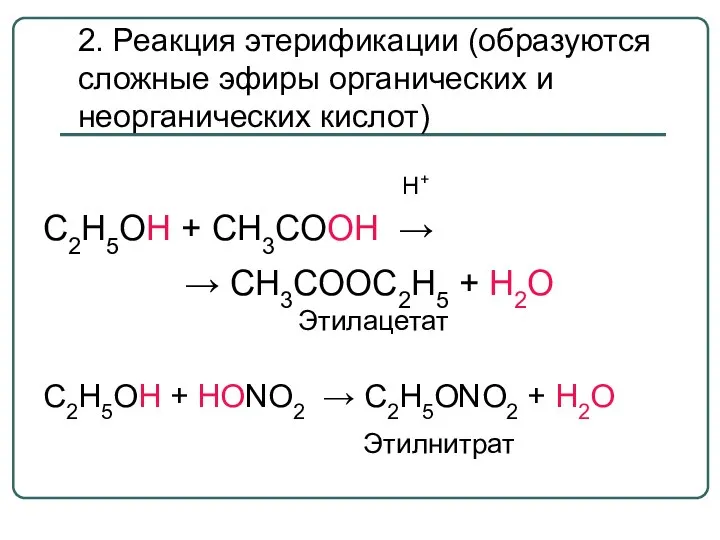
- 35. 2. Реакция этерификации (образуются сложные эфиры органических и неорганических кислот) Н+ С2Н5ОН + СН3СООН → →
- 36. 3. Замещение гидроксильной группы на галоген CH3-CH2-OH +НBr → C2H5-Br +H2O этанол бромэтан
- 37. 4. Замещение гидроксильной группы на аминогруппу Al2O3,t CH3-CH2-OH+Н-NН2 → C2H5-NН2 + H2O этанол аммиак этиламин
- 38. II. Реакции отщепления (элиминирования) Виды реакций отщепления: - межмолекулярная дегидратация - внутримолекулярная дегидратация - дегидрирование
- 39. При межмолекулярной дегидратации образуются простые эфиры, при внутримолекулярной – алкены. бутанол-2 бутен-2 этанол диэтиловый эфир
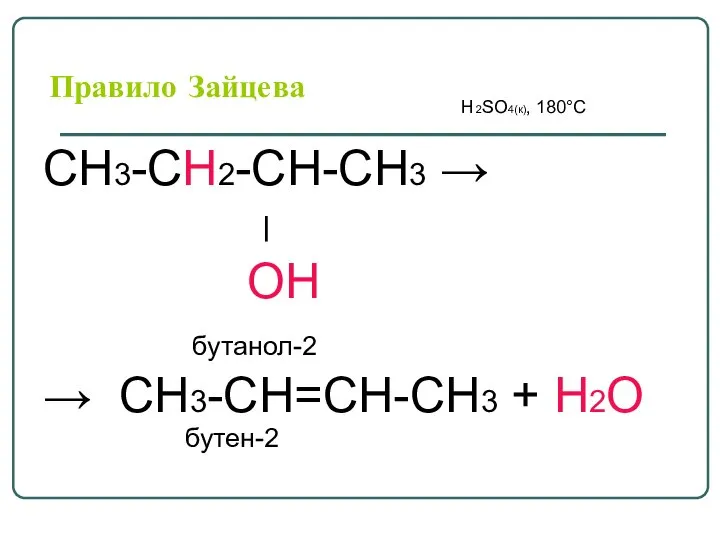
- 40. Правило Зайцева H2SO4(к), 180°С СН3-СН2-СН-СН3 → ׀ ОН бутанол-2 → СН3-СН=СН-СН3 + Н2О бутен-2
- 41. Дегидрирование (образуются альдегиды или кетоны) CH3-CH2-OH → → CH3-C=O + H2↑ ׀ H этаналь (уксусный альдегид)
- 42. СН3-СН-СН3 → (Cu,t) ׀ ОН → CH3-C-СH3 + H2↑ ׀ ׀ O этанон (ацетон, диэтилкетон)
- 43. III. Реакции окисления Горение C2H5-OH +3О2→ → 2CO2 + 3H2O+ Q
- 44. Неполное окисление. t CH3-CH2-OH +CuO → → CH3-C=O +Cu +H2О ׀ H этаналь (уксусный альдегид)
- 45. Способы получения спиртов Гидратация алкенов Щелочной гидролиз галогеноалканов (в присутствии водного раствора щелочи) Гидрирование альдегидов и
- 46. Специфические способы получения метанола и этанола 1. Синтез метанола из водяного газа (катализатор, давление, температура): СО+
- 47. 3. Многоатомные спирты
- 48. Многоатомные спирты Присутствие в молекулах многоатомных спиртов двух и более гидроксильных групп обуславливает некоторые отличия в
- 49. Химические свойства CH2 - OH CH - OH CH2 - OH Cu(ОН)2 +2ОН- -4Н2О CH2 -
- 51. Данная реакция используется для качественного обнаружения многоатомных спиртов. В реакцию при этом вступает α-диольный фрагмент.
- 52. 2. Реакция этерификации с органическими и неорганическими кислотами
- 53. Способы получения Получение гликолей 1. Окисление алкенов перманганатом калия в нейтральной среде (гидроксилирование) Щелочной гидролиз дигалогеналканов
- 54. Физические свойства Этиленгликоль и глицерин при обычных условиях представляют собой бесцветные вязкие жидкости, легко смешивающиеся с
- 55. 4. Фенолы: характеристика, способы получения, свойства, применение
- 56. Фенолы По количеству OH-групп различают: фенол a) Одноатомные фенолы Фенолы – гидроксисоединения, в молекулах которых OH-группы
- 58. пирокатехин резорцин гидрохинон пирогаллол б) многоатомные фенолы
- 59. Физические свойства фенола Фенол- кристаллическое вещество, антисептик.
- 60. Химические свойства фенолов 1. Кислотные свойства: фенол фенолят натрия
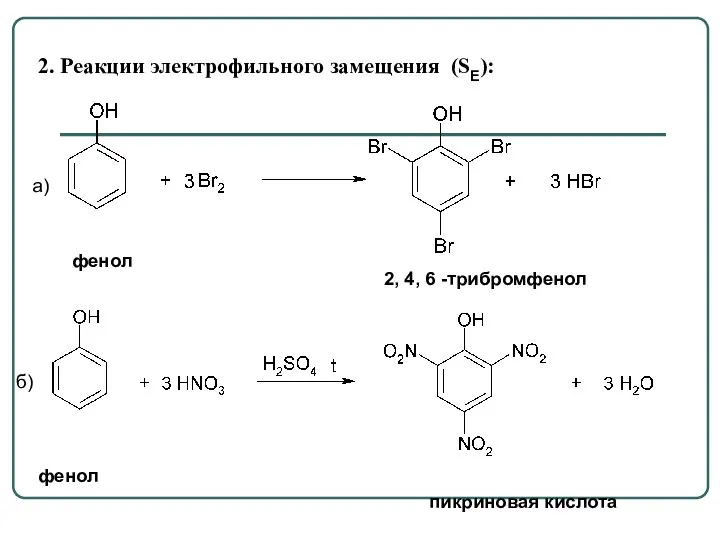
- 61. 2. Реакции электрофильного замещения (SE): а) б) фенол пикриновая кислота фенол 2, 4, 6 -трибромфенол
- 62. 3. Окисление фенолов: гидрохинон хинон
- 63. 4. Реакции присоединения (гидрирование) с образованием алициклических спиртов (циклогексанол) 5. Качественная реакция с хлоридом железа (III):
- 64. 6. Реакции поликонденсации. Фенол + формальдегид →катализатор→ фенолформальдегидная смола :
- 66. Скачать презентацию





















































 Вирощування кристалів в додомашніх умовах
Вирощування кристалів в додомашніх умовах Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Определение валентности элементов
Определение валентности элементов V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады) Альдегидтер және кетондар
Альдегидтер және кетондар Кристаллические решетки
Кристаллические решетки Получение и установление состава кристаллогидрата фосфата цинка
Получение и установление состава кристаллогидрата фосфата цинка Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Теоретические основы органической химии
Теоретические основы органической химии Железо и его соединения.
Железо и его соединения. Beryllium. The physical properties of beryllium
Beryllium. The physical properties of beryllium Физический процесс и химическая реакция.
Физический процесс и химическая реакция. Общая и неорганическая химия
Общая и неорганическая химия Химические свойства алканов
Химические свойства алканов Расчёт равновесного состава
Расчёт равновесного состава Викторина. Дмитрий Иванович Менделеев
Викторина. Дмитрий Иванович Менделеев Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары
Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары Уран. Получение урана
Уран. Получение урана Значение основных химических элементов в жизни человека
Значение основных химических элементов в жизни человека Сведения о воде
Сведения о воде Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs
Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs Буровые технологические жидкости для бурения и крепления горизонтальных скважин
Буровые технологические жидкости для бурения и крепления горизонтальных скважин Имеет ли вода форму
Имеет ли вода форму Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Кислород. Получение кислорода и его физические свойства
Кислород. Получение кислорода и его физические свойства