Содержание
- 2. Sn, Pb Аллотропия олова: α-Sn (порошок) ⮀ 13,2 °С β-Sn (металл) ⮀ γ-Sn ⮀ 173 °С
- 3. Sn, Pb Cплавы припой (30-70)% Sn, Pb бронза Cu+Sn, Al, Be, Pb баббит Sn+Sb, Cu; Pb+Sb,
- 4. Получение металлов SnO2(т) + C(т) = Sn(ж) + CO2(г) 2PbS(т) + 3O2(г) = 2PbO(т) + 2SO2(г)
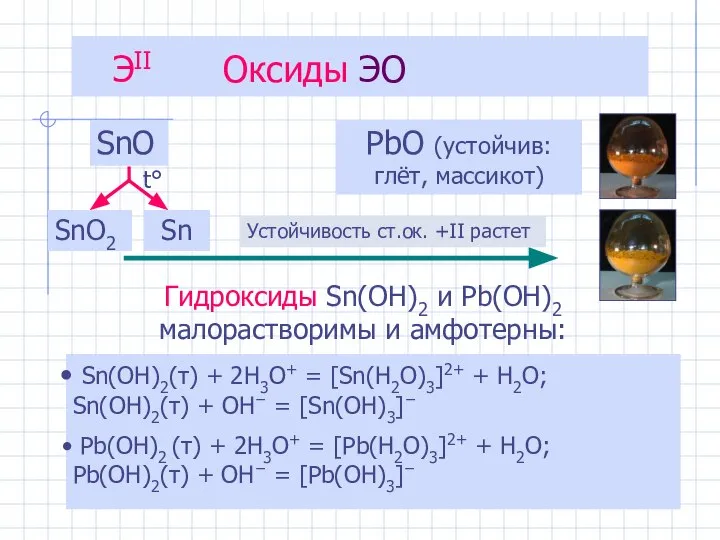
- 5. ЭII Оксиды ЭО SnO PbO (устойчив: глёт, массикот) Sn(OH)2(т) + 2H3O+ = [Sn(H2O)3]2+ + H2O; Sn(OH)2(т)
- 6. Аквакатионы ЭII [Э(H2O)3]2+ + H2O ⮀ [Э(H2O)2(OH)]+ + H3O+ SnII – сильный комплексообразователь (координирует ионы Cl–
- 7. [Pb2+]: PbSO4 > PbCrO4 > PbS PbSO4(т) + CrO42– = PbCrO4(т) + SO42– белый желтый PbCrO4(т)
- 8. амфотерн. с преобладанием кислотн. св-в полигидраты ЭO2.n H2O (уст. при рН ЭO2.n H2O + 2OH− =
- 9. Окислительно-восстановительные свойства Sn2+ – мягкий восстановитель рН ϕ° = +0,14 B рН > 7: [Sn(OH)3]− +
- 10. Окислительно-восстановительные свойства PbO2 – сильный окислитель рН рН > 7: PbO2 + 2H2O +2e − =
- 12. Скачать презентацию



![Аквакатионы ЭII [Э(H2O)3]2+ + H2O ⮀ [Э(H2O)2(OH)]+ + H3O+ SnII –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408014/slide-5.jpg)
![[Pb2+]: PbSO4 > PbCrO4 > PbS PbSO4(т) + CrO42– = PbCrO4(т)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1408014/slide-6.jpg)



 Особенности технологий обработки жидкостей и газов
Особенности технологий обработки жидкостей и газов Сплави металів
Сплави металів Өтмө металлдар
Өтмө металлдар Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов Uses of chlorine and its compounds
Uses of chlorine and its compounds Origin of petroleum dilemma
Origin of petroleum dilemma Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе
Аттестационная работа. Проектно-исследовательская деятельность учащихся на уроках химии и во внеурочной работе Строение атома
Строение атома Липиды
Липиды Презентация Химические свойства кислот в свете теории электролитической диссоциации 9 Класс
Презентация Химические свойства кислот в свете теории электролитической диссоциации 9 Класс Жидкостная хроматография
Жидкостная хроматография Химиялык кару
Химиялык кару Разбор заданий #ОВРновый, #реакционно и #соточка
Разбор заданий #ОВРновый, #реакционно и #соточка Алюминий. История получения. Свойства алюминия. Корунд, бокситы
Алюминий. История получения. Свойства алюминия. Корунд, бокситы Химическая лаборатория
Химическая лаборатория Неорганическая химия. Соединение химических элементов
Неорганическая химия. Соединение химических элементов Исследование растворимости в системе уксусная кислота-этиловый спирт-этилацетат-вода методом изотермического титрования при 60˚C
Исследование растворимости в системе уксусная кислота-этиловый спирт-этилацетат-вода методом изотермического титрования при 60˚C Классификация терпенов
Классификация терпенов Презентация по Химии "Метали" - скачать смотреть бесплатно
Презентация по Химии "Метали" - скачать смотреть бесплатно Теория гибридизации. (Лекция 3)
Теория гибридизации. (Лекция 3) Оружие массового поражения. Биологическое оружие
Оружие массового поражения. Биологическое оружие  Organic Compounds
Organic Compounds Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов
Углеводороды и их природные источники. Гомологический ряд алканов. Строение алканов Трансформация соединений азота
Трансформация соединений азота Карбоновые кислоты
Карбоновые кислоты Спирты. Физические свойства
Спирты. Физические свойства Коррозия железа в различных средах Проект по химии: Авторы: ученица 10б класса
Коррозия железа в различных средах Проект по химии: Авторы: ученица 10б класса  Сульфатна кислота і сульфати
Сульфатна кислота і сульфати