Содержание
- 2. Литература 1. Тиноко И, Зауэр К, Вэнг Дж., Паглиси Дж. Физическая химия. (Принципы и применение в
- 3. Вопросы 1. Предмет, задачи и разделы физической и коллоидной химии. 2. Химическая термодинамика. Первый закон термодинамики.
- 4. 1. Предмет, задачи и разделы физической химии Термин «физическая химия» впервые ввел М. В. Ломоносов в
- 5. При решении основных задач физическая химия пользуется следующими теоретическими методами физики: Термодинамический метод – применяется для
- 6. Термодинамический метод: не учитывает конкретную природу веществ, квантование энергии, не опирается ни на какие модельные представления
- 7. Физическая химия включает несколько разделов: Термодинамика Химическая кинетика и катализ Электрохимия
- 8. 2. Химическая термодинамика. Первый закон термодинамики Химическая термодинамика – наука, изучающая условия устойчивости систем и законы.
- 9. Тепловые балансы составляют на основе первого закона термодинамики. На основе второго и третьего законов проводят анализ
- 11. Система – тело или несколько тел, находящихся во взаимодействии между собой (диффузия, теплообмен, химическая реакция) и
- 12. Термодинамическая система – совокупность тел, которые могут энергетически взаимодействовать между собой и с другими телами и
- 13. По способу взаимодействия системы с окружающей средой (иначе, по пропускной способности граничной поверхности) или другими системами
- 14. Термодинамические параметры – физические величины, характеризующие состояние термодинамической системы: Температура Объем Плотность Давление Масса Намагниченность электрическая
- 15. Величины, количественно выражающие термодинамические свойства (параметры), называют также термодинамическими переменными. Поскольку все они взаимосвязаны, их разделяют
- 16. В любой ТДС обязательно протекают процессы, которые могут быть: равновесными, неравновесными, обратимыми, необратимыми.
- 17. Если в ТДС определенное свойство системы не будет изменяться во времени, т. е. оно будет одинаковым
- 18. Функции могут зависеть от пути процесса. Функции, которые зависят от начального и конечного состояний системы и
- 19. Экстенсивное свойство системы прямо пропорционально массе системы и обладает аддитивностью (можно складывать): V, H, Uвн, S,
- 20. Уравнение, связывающее термодинамические параметры системы в равновесном состоянии, – уравнение состояния. Вследствие взаимосвязи между свойствами системы
- 21. Пусть дан изолированный сосуд, который разделен полупроницаемой перегородкой. В первой части сосуда температура Т1, во второй
- 22. Работа процесса – это энергия, передаваемая одним телом другому при их взаимодействии, не зависящая от температуры
- 23. Внутренняя энергия системы Uвн складывается из энергии поступательного и вращательного движения молекул, энергии внутримолекулярного колебательного движений
- 24. Существование не изменяющихся во времени термодинамических систем вводится постулатом о термодинамическом равновесии (первое исходное положение термодинамики).
- 25. Фаулер в 1931 г. сформулировал принцип термического равновесия или постулата о температуре: если две системы А
- 26. Иногда функциональную связь энергии и температуры основывают на постулате: при заданных внешних параметрах энергия системы является
- 27. Энергия (от греческого energeia – действие, деятельность) – общая количественная мера движения и взаимодействия всех видов
- 28. Внутренняя энергия U является внутренним параметром системы, и при равновесии ее величина будет определяться внешними параметрами
- 29. Система обладает определенным запасом энергии. Теплота же и работа проявляются только при процессе, когда происходит обмен
- 30. Первый закон термодинамики является математическим выражением закона сохранения и превращения энергии в применении к термодинамическим системам.
- 31. Формулировки первого закона термодинамики: Общий запас энергии в изолированной системе остается постоянным. Разные формы энергии переходят
- 32. В термодинамике применяется следующая формулировка закона сохранения энергии: Существует аддитивная функция состояния термодинамической системы – внутренняя
- 33. W = PdV Рассмотрим изохорный процесс (V=const): В изохорном процессе, когда системой выполняется только работа расширения,
- 34. В изобарном процессе (Р=const) и работа расширения не равна нулю: Если система – идеальный газ, то
- 35. Для адиабатического процесса и уравнение первого закона термодинамики принимает вид т. е. положительная работа будет совершаться
- 36. Джоуль установил, что внутренняя энергия идеального газа является функцией только температуры и не зависит от объема
- 37. Теплоемкость идеального газа не зависит от температуры, а Сv – молярная теплоемкость, получим для адиабатического процесса
- 38. Для изотермического процесса (Т=const) работа расширения идеального газа, для которого PV = nRT, будет равна
- 39. Внутренняя энергия простой закрытой системы (система может выполнять только работу расширения) является функцией двух независимых переменных
- 40. (∂Q/∂V)T называют теплотой изотермического расширения тела; величина (∂Q/∂T)V есть теплоемкость
- 41. Энтальпия (Н) определяется тождеством Рассматривая Н как функцию независимых переменных Т и Р, получим выражение для
- 42. Величину (∂Q/∂Р)T называют теплотой изотермического сжатия. Теплоемкости СР и СV -важнейшие термодинамические параметры, с помощью которых
- 43. Отношение количества теплоты δQ, полученной системой (веществом) при бесконечно малом изменении его состояния в каком-либо процессе,
- 44. 3. Термохимия. Закон Гесса При химических реакциях происходит изменение внутренней энергии, так как в ходе реакции
- 45. В химии чаще совершаются процессы при постоянном давлении, чем при постоянном объеме. Если при этом совершается
- 46. Если реакция протекает необратимо при постоянном давлении или постоянном объеме, а продукты реакции имеют ту же
- 47. Энтальпия реакции ∆rH может быть больше нуля (∆rH>0) – такие реакции называются эндотермическими реакциями (с поглощением
- 48. Первое следствие из закона Гесса. Энтальпия реакции (тепловой эффект химической реакции) равен сумме энтальпий (теплот) образования
- 49. Состояние системы, при котором значение термодинамической функции принимается за начало ее отсчета, называют стандартным состоянием. Стандартное
- 50. Для проведения термодинамических расчетов необходимы данные о термодинамических свойствах веществ при любой температуре, поэтому удобно задать
- 51. Второе следствие из закона Гесса. Энтальпия реакции равна разности между суммой теплот сгорания исходных веществ и
- 52. Третье следствие из закона Гесса. Тепловой эффект разложения химического соединения равен по величине и противоположен по
- 53. Четвертое следствие из закона Гесса. Если из различных исходных веществ получаются одни и те же продукты,
- 54. Пятое следствие из закона Гесса. Тепловой эффект реакции, протекающей в газовой фазе, равен сумме энергий связи
- 55. 4. Второй закон термодинамики Процессы, происходящие спонтанно без внешних воздействий, называются самопроизвольными. Они обладают определенными характерными
- 56. Хотя общая энергия остается постоянной, при самопроизвольном процессе происходит перераспределение энергии, ее диссипация – переход части
- 57. Второй закон термодинамики гласит: существует аддитивная функция состояния системы – энтропия (S), которая следующим образом связана
- 58. Объединенный первый и второй законы термодинамики и называется фундаментальным уравнением термодинамики: Третий закон термодинамики, установленный в
- 59. Третий закон термодинамики равносилен условию: энтропия всех тел в состоянии равновесия стремится к нулю по мере
- 60. значение стандартной энтропии вещества увеличивается при повышении массы частицы (у частиц с большей массой больше возможных
- 61. 5. Процессы в неизолированных системах. Энергии Гельмгольца и Гиббса. Система может совершать различные виды работы, как
- 62. Необходимо найти функцию состояния, изменение которой бы соответствовало работе изотермического процесса системы при любых условиях. Объединим
- 63. и система может совершать максимальную работу, если протекает равновесный процесс. Для того чтобы найти функцию состояния,
- 64. Выражение, стоящее в круглых скобках, имеет свойства функции состояния и носит название энергия Гельмгольца. т.е. максимальная
- 68. 6. ФАЗОВЫЕ РАВНОВЕСИЯ В ОДНОКОМПОНЕНТНЫХ СИСТЕМАХ. УРАВНЕНИЕ КЛАПЕЙРОНА – КЛАУЗИУСА Фаза в термодинамике определяется как совокупность
- 69. Компоненты – индивидуальные вещества, концентрации которых независимы и могут выразить изменение в составе любой фазы данной
- 70. Рассмотрим однокомпонентную закрытую систему, состоящую из двух фаз: фаза 1 и фаза 2. Пусть G1 и
- 71. Но так как система закрытая, то Если в системе при Т,Р=const устанавливается равновесие, то но по
- 72. Если в системе не установилось равновесие (происходит направленный переход вещества из одной фазы в другую), то
- 73. Если изменить температуру и давление равновесной системы, то молярные энергии Гиббса фаз также изменятся и станут
- 74. Уравнения полных дифференциалов молярных энергий Гиббса в равновесных фазах 1 и 2: Превращение фаз рассматривалось как
- 75. Изменение молярного объема при переходе 1 моля вещества из одной фазы в другую равно: Уравнение является
- 76. Фазовые превращения или фазовые переходы – это переходы вещества из одного фазового состояния в другое при
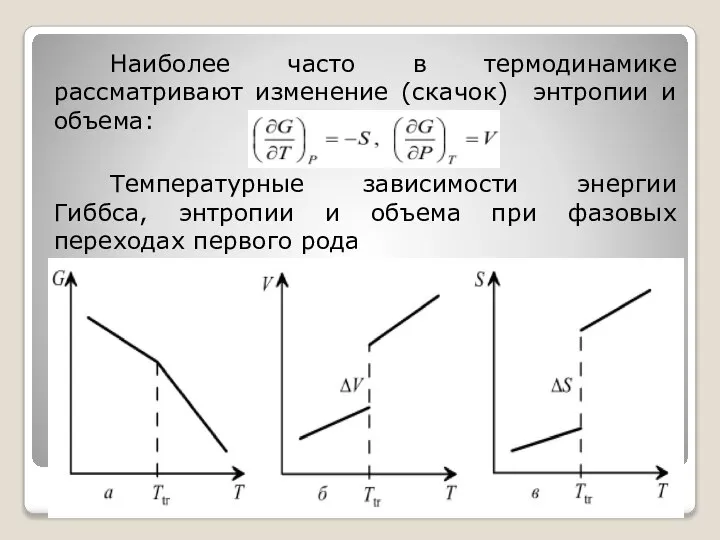
- 77. Наиболее часто в термодинамике рассматривают изменение (скачок) энтропии и объема: Температурные зависимости энергии Гиббса, энтропии и
- 78. При фазовых переходах первого рода в единице массы выделяется или поглощается определенное количество теплоты, называемое теплотой
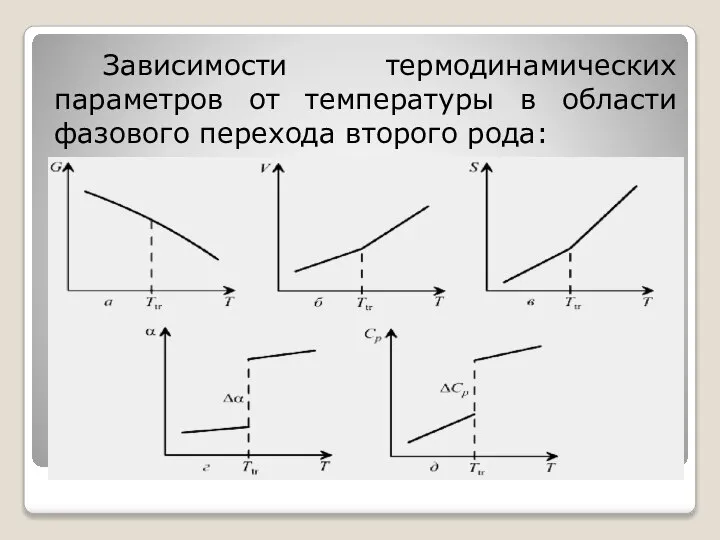
- 79. При фазовых переходах второго рода первые производные энергии Гиббса по температуре и давлению (энтропия, объем) непрерывны,
- 80. Зависимости термодинамических параметров от температуры в области фазового перехода второго рода:
- 82. Скачать презентацию













































































 Дослідження розчинності речовин природознавство
Дослідження розчинності речовин природознавство Францій БІОЛОГІЧНА РОЛЬ
Францій БІОЛОГІЧНА РОЛЬ  Электрохимические анализаторы медицинского назначения
Электрохимические анализаторы медицинского назначения Природні джерела вуглеводнів і їх переробка
Природні джерела вуглеводнів і їх переробка Составы и температуры плавления смесей
Составы и температуры плавления смесей Химическая коррозия
Химическая коррозия Валентность. Порядок действий при составлении химической формулы
Валентность. Порядок действий при составлении химической формулы Химия өнеркәсібіндегі энергетикалық ресурстар
Химия өнеркәсібіндегі энергетикалық ресурстар Что такое полупроводники
Что такое полупроводники Направление окислительно-восстановительного процесса
Направление окислительно-восстановительного процесса Приготовление основного и рабочих растворов хлорной извести
Приготовление основного и рабочих растворов хлорной извести Презентация по Химии "Вклад Д.И. Менделеева в развитие агрохимии. Значение его вклада в современном сельском хозяйстве" - скач
Презентация по Химии "Вклад Д.И. Менделеева в развитие агрохимии. Значение его вклада в современном сельском хозяйстве" - скач Гибридизация атомных орбиталей
Гибридизация атомных орбиталей Растворение. Растворимость веществ в воде. 8 класс
Растворение. Растворимость веществ в воде. 8 класс гетероциклич
гетероциклич Железо-углеродистые сплавы
Железо-углеродистые сплавы Изомерия - презентация_
Изомерия - презентация_ Презентация по Химии "Избранные главы металлоорганической химии" - скачать смотреть
Презентация по Химии "Избранные главы металлоорганической химии" - скачать смотреть  Сшивка и контролируемая деструкция полиолефинов
Сшивка и контролируемая деструкция полиолефинов Типы химических реакций
Типы химических реакций Периодический закон и Периодическая система химических элементов
Периодический закон и Периодическая система химических элементов Оксиды азота
Оксиды азота Российские химические технологии
Российские химические технологии Хімічні властивості кислот
Хімічні властивості кислот Получение водорода с использованием технологии газификации угля и отходов угольной промышленности
Получение водорода с использованием технологии газификации угля и отходов угольной промышленности Гетероциклдік қосылыстар
Гетероциклдік қосылыстар Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Состояние радионуклидов в различных фазах и методы его изучения
Состояние радионуклидов в различных фазах и методы его изучения