Содержание
- 2. Окислительно-восстановительными реакциями называют реакции, сопровождающиеся изменением степени окисления элементов.
- 3. Почему одни из окислительно - восстановительных протекают, а другие нет? Почему один и тот же окислитель
- 4. Ox + ne ⇔ Red Окисл. Восстан. форма форма Ox и Red взаимосвязаны и это есть
- 5. Общая схема процесса: Ox1+Red2 ⇔ Red1+Ox2 окислитель I+ восстановитель II= восстановитель I + окислитель II Окислительно-восстановительные
- 6. Стандартный (нормальный) окислительно-восстановительный потенциал пар, которые являются растворимыми формами, - это разница потенциалов, которая возникает между
- 8. Электродвижущая сила ЭДС = Е⁰ок-Е⁰вост ЭДС>0 процесс протекает самопроизвольно в прямом направлении, при ЭДС Чем больше
- 9. Опыт 1. Сравнение химической активности железа и меди. Предварительно обезжиренную и протравленную в соляной кислоте железную
- 10. Сu + FeSO4→ реакция не идет; ∆Е= E(Fe+2\Fe)- E(Cu2+\Cu)= -0,44-0,34= -0,78 В, реакция невозможна, ЭДС‹0 Fe
- 11. Опыт 2. Взаимодействие раствора соли железа (III) с иодидом калия, с бромидом натрия. К подкисленному раствору
- 12. KJ + FeCl3 → FeCl2 + KCl + J2 2J- - 2e → J20 EJ2\2J-= 0,536
- 13. KBr + FeCl3 → 2Br- - 2e → Br20 EBr2\2Br-= 1,065 восстановитель Fe+3 + 1e →
- 14. Задание 1. Какая из приведенных ниже систем будут восстановителем, если в качестве окислителя использовать кислый раствор
- 15. Fe3+ е = Fe2+ Е=0,771 В F2 +2e =2F- Е=2,87 В S +2H+ +2e =H2S Е=0,17
- 16. MnO4- +8H+ +5е =Мn2+ +4Н2О E=1,507 Восстановителем могут быть системы, где электродный потенциал меньше электродного потенциала
- 17. МnО4- + 8Н+ +5е = Мn2++ 4 Н2О в кислой S042- +2Н+ +2е= S032- + Н2О
- 18. Вывод: а)МnО4- + 8Н+ +5е = Мn2++ 4 Н2О E=1,507 B S042- +2Н+ +2е= S032- +
- 19. Все три реакции протекают самопроизвольно, т.к. ЭДС›0. Окислительные свойства иона МпО4- выражены сильнее в кислой среде,
- 20. Опыт 3. Окислительные свойства перманганата калия. В три отдельные пробирки с раствором перманганата калия добавьте разбавленную
- 21. 2KMnO4 + H2O+3Na2SO3= 2MnO2↓ + 2K2SO4 +3Na2SO4+2KOH бурый 2KMnO4 +2 KOH+Na2SO3= 2K2MnO4+Na2SO4+H2O зеленый р-р 2KMnO4 +
- 22. Опыт 4. Влияние среды на окислительно-восстановительный потенциал. В две пробирки внесите дихромат калия (желтого цвета) и
- 23. CrO42- + 2H+ = Cr2O7 2- +H2O желтая оранжевая Cr2O7 2-+ 2OH- = CrO4 2- +
- 24. Cr2O7 2-+ 14H+ +6e = 2Cr3+ + 7H2O E Cr2O72-/ Сr3+ = 1,33B 2J- - 2e
- 25. 2K2CrO4 + H2SO4=К2Cr2O7+ K2SO4 +H2O K2Cr2O7+ 2KOH=2K2CrO4 + H2O K2Cr2O7 + 6KI + 7H2SO4 → 3I2
- 26. Ограничено ли прогнозирование окислительно-восстановительных реакций? Можно ли предсказать точно, будет ли протекать реакция или нет? Можно
- 27. Реакция горения ацетилена: С2Н2 + О2 = 5/2 СО2 + Н2О + 1300 кДж Картина «Вечерний
- 28. Черный порох: +5 0 0 0 +4 -2 2 KNO3 + 3 C + S =
- 30. Скачать презентацию



























 Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1)
Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1) Штучні і синтетичні волокна
Штучні і синтетичні волокна  Химиялық реакция белгілерін атаңыз
Химиялық реакция белгілерін атаңыз Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Физические и химические явления
Физические и химические явления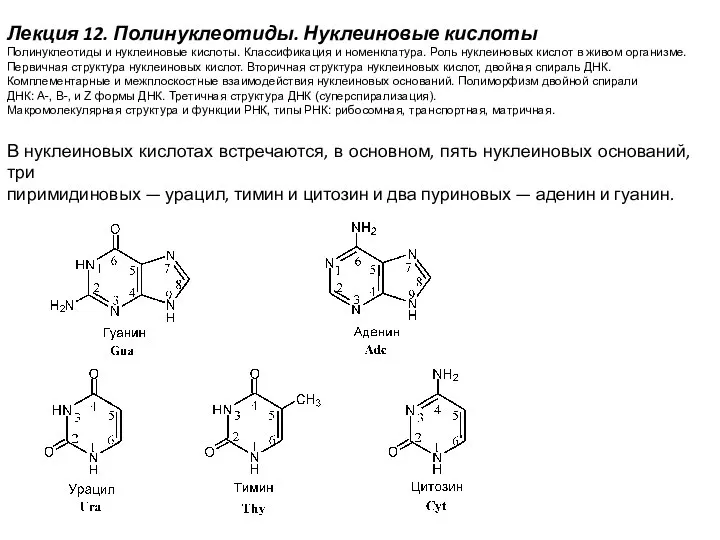 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Выдающиеся ученые - химики и их заслуги
Выдающиеся ученые - химики и их заслуги Классификация моющих средств
Классификация моющих средств Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы Молярный объём газообразного вещества
Молярный объём газообразного вещества Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Тыңайтқыштар
Тыңайтқыштар Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат
Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат Неидеальные растворы
Неидеальные растворы Introduction to metabolism
Introduction to metabolism Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов. Алкены
Алкены Презентация Лекарства дома
Презентация Лекарства дома Химия (Органическая химия)
Химия (Органическая химия) Цикли трикарбонових кислот
Цикли трикарбонових кислот Алкадиены
Алкадиены Оксиды азота.
Оксиды азота. Общая химия, понятия
Общая химия, понятия Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Основні класи неорганічних сполук
Основні класи неорганічних сполук Общая и неорганическая химия
Общая и неорганическая химия Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще
Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии
Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии