Содержание
- 2. Цели урока: организовать деятельность учащихся по изучению особенностей строения атома фосфора на основании его положения в
- 3. Мотивационно-ориентационный этап. Академик А.Е.Ферсман назвал этот элемент « элементом мысли и жизни», без него невозможно существование
- 4. Какие сведения о фосфоре вам были известны до сегодняшнего урока? ФОСФОР
- 5. История открытия фосфора 1669 г- Х.Бранд-первооткрыватель фосфора 1682г- Р.Бойль в химической лаборатории при работе с фосфором.
- 6. период Фосфор как химический элемент 3 группа 5 валентных электронов 5 степени окисления -3,0,+3,+5 высший оксид
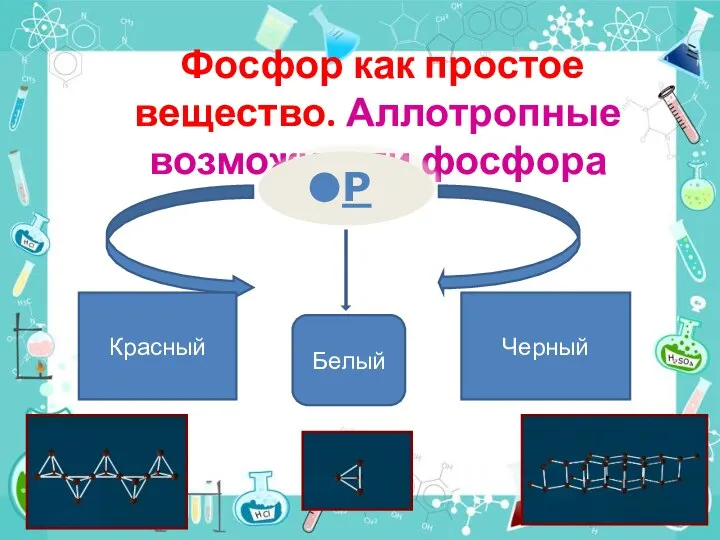
- 7. Фосфор как простое вещество. Аллотропные возможности фосфора Р Красный Белый Черный
- 8. Аллотропия фосфора
- 9. Прокомментируйте отрывок из романа А.Конан-Дойля « Собака Баскервилей». Попытайте определить, где правда, а где вымысел автора?
- 10. Химические свойства фосфора. ( Работа с учебником стр.160 и дополнительной литературой)
- 11. с бертолетовой солью при ударе взрывается, воспламеняется: 5KClO3 +6 P =3 P2O5 +5 KCl
- 12. « Сжигание красного фосфора и исследование продуктов его сгорания»
- 13. Видеоролик «Сгорание фосфора в хлоре» 2 Р + 3Cl2 ( нед) →2 PCI3 2 Р +
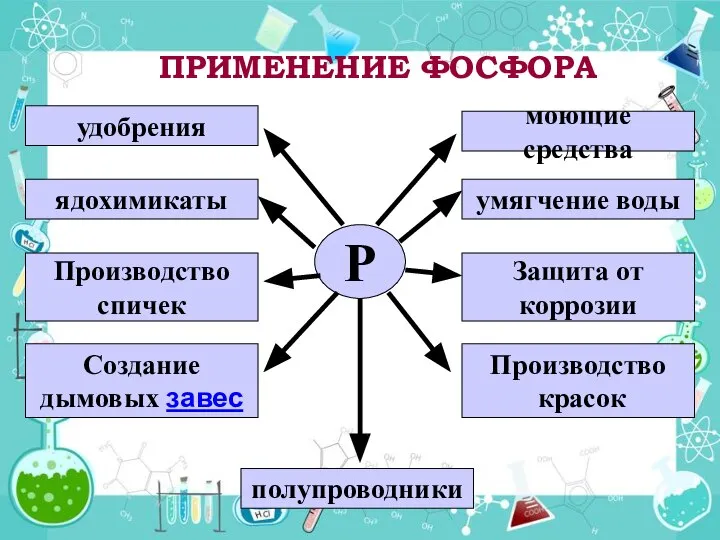
- 14. ПРИМЕНЕНИЕ ФОСФОРА Р удобрения ядохимикаты Производство спичек Создание дымовых завес полупроводники Производство красок Защита от коррозии
- 15. Войска США использовали фосфорные Бомбы в Ираке, 2004 г.
- 16. Первичное закрепление полученных знаний. Тест с использованием для голосования интерактивные индивидуальные устройства.
- 17. Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4
- 18. Тест 5. Причина свечения белого фосфора…. а)изменение агрегатного состояния вещества б) химическое явление в) физическое явление
- 19. Домашнее задание: Учащиеся выбирают для выполнения задания разных уровней сложности: 1 уровень: упр. №1 стр. 163
- 20. Итоги урока. Рефлексивно- оценочный этап. 1.Почему академик Ферсман назвал фосфор «элементом жизни и мысли? 2.Как ты
- 21. СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ И ИСТОЧНИКОВ Учебник О.С.Габриеляна « Химия- 9», изд.» Дрофа», 2007 год. Виртуальная лаборатория.
- 23. Скачать презентацию


















 Алкалоидтар. Алкалоидтар негіздік қасиет
Алкалоидтар. Алкалоидтар негіздік қасиет Применение фенола
Применение фенола Химический процесс. Практические занятия
Химический процесс. Практические занятия Коислоты
Коислоты Кристаллохимические радиусы
Кристаллохимические радиусы Жаңа дәрілерді жасау
Жаңа дәрілерді жасау Презентация по Химии "Алюминий как химический элемент и как простое вещество" - скачать смотреть
Презентация по Химии "Алюминий как химический элемент и как простое вещество" - скачать смотреть  Метаморфизм
Метаморфизм Гидролиз неорганических вещесв
Гидролиз неорганических вещесв АТФ (Аденозинтрифосфат)
АТФ (Аденозинтрифосфат) Презентация по Химии "Жёсткость воды" - скачать смотреть
Презентация по Химии "Жёсткость воды" - скачать смотреть  Ртуть и здоровье
Ртуть и здоровье Классификация химических веществ
Классификация химических веществ Беттік активті заттарды өндіру
Беттік активті заттарды өндіру Наукові напрямки практичної реалізації принципів «Зеленої» хімії
Наукові напрямки практичної реалізації принципів «Зеленої» хімії Химические и физические явления
Химические и физические явления Соли «Na2SO4»
Соли «Na2SO4» Инфракрасная спектроскопия. Спирты и фенолы
Инфракрасная спектроскопия. Спирты и фенолы Природные соединения кремния
Природные соединения кремния Жартылый өткізгіштікке ие химиялық элементтер
Жартылый өткізгіштікке ие химиялық элементтер Получение каталитического слоя на основе углеродных нанотрубок с наночастицами платины для водородно–воздушных топливных элеме
Получение каталитического слоя на основе углеродных нанотрубок с наночастицами платины для водородно–воздушных топливных элеме Изменения свойств химических элементов и их соединений в группах и периодах
Изменения свойств химических элементов и их соединений в группах и периодах Химические свойства металлов
Химические свойства металлов Конструкционные функциональные волокнистые композиты. Углеродные волокна
Конструкционные функциональные волокнистые композиты. Углеродные волокна Термодинамика силикатов и оксидных соединений. Теплоёмкость и закон Кирхгофа. (Тема 2)
Термодинамика силикатов и оксидных соединений. Теплоёмкость и закон Кирхгофа. (Тема 2) Морские льды. Их классификация и закономерности движения
Морские льды. Их классификация и закономерности движения Алюминий. Сплавы алюминия. Учитель: Белозерова Татьяна Анатольевна Учени
Алюминий. Сплавы алюминия. Учитель: Белозерова Татьяна Анатольевна Учени Современные системы фильтрации воды
Современные системы фильтрации воды