Содержание
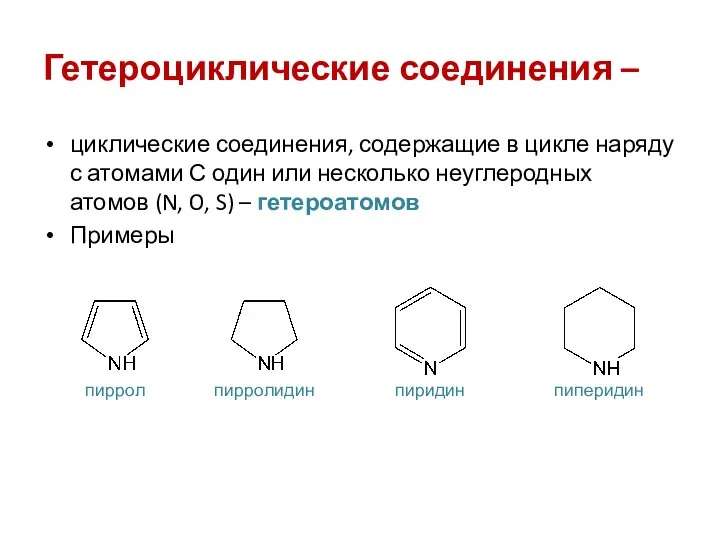
- 2. Гетероциклические соединения – циклические соединения, содержащие в цикле наряду с атомами С один или несколько неуглеродных
- 3. Классификации гетероциклов
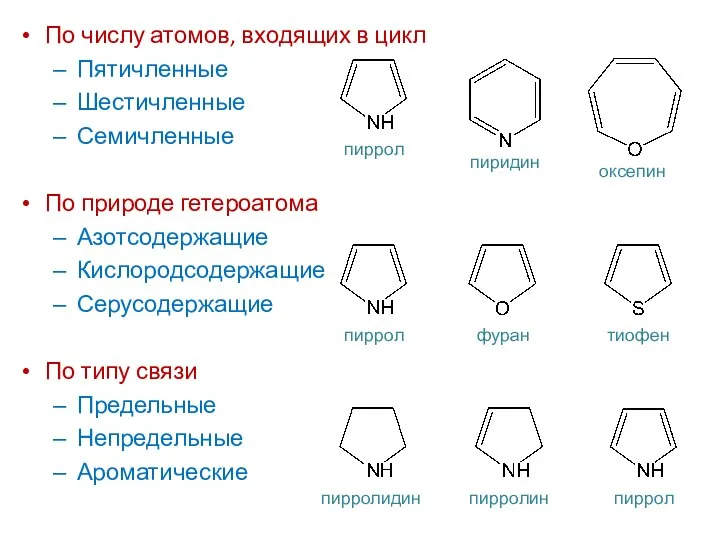
- 4. По числу атомов, входящих в цикл Пятичленные Шестичленные Семичленные По природе гетероатома Азотсодержащие Кислородсодержащие Серусодержащие По
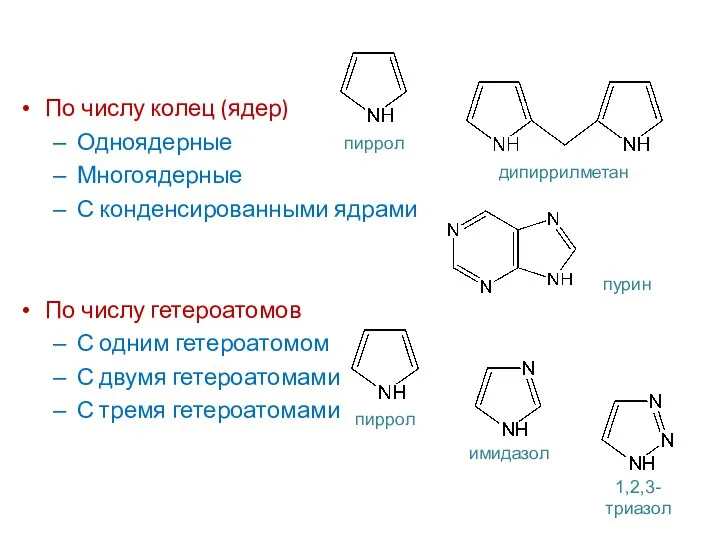
- 5. По числу колец (ядер) Одноядерные Многоядерные С конденсированными ядрами По числу гетероатомов С одним гетероатомом С
- 6. Пятичленные гетероциклы с одним гетероатомом
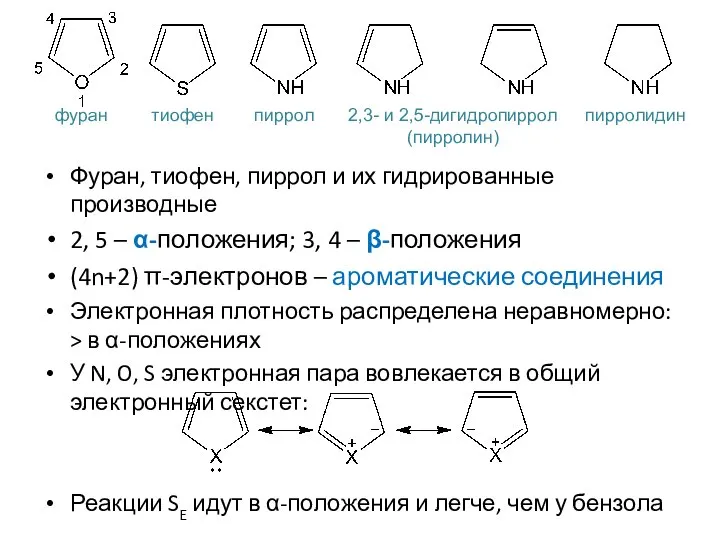
- 7. Фуран, тиофен, пиррол и их гидрированные производные 2, 5 – α-положения; 3, 4 – β-положения (4n+2)
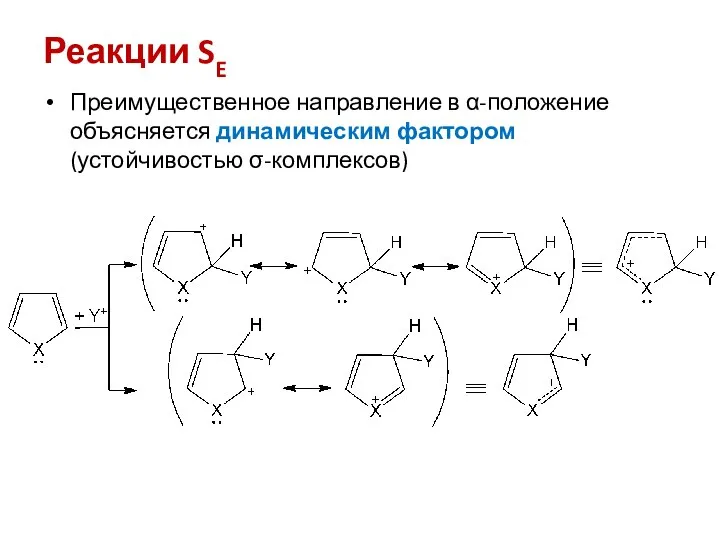
- 8. Реакции SE Преимущественное направление в α-положение объясняется динамическим фактором (устойчивостью σ-комплексов)
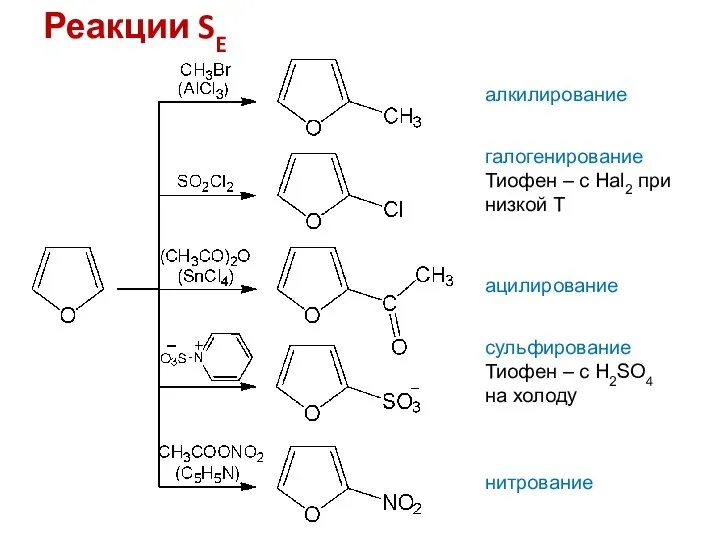
- 9. Реакции SE алкилирование галогенирование Тиофен – с Hal2 при низкой Т ацилирование сульфирование Тиофен – с
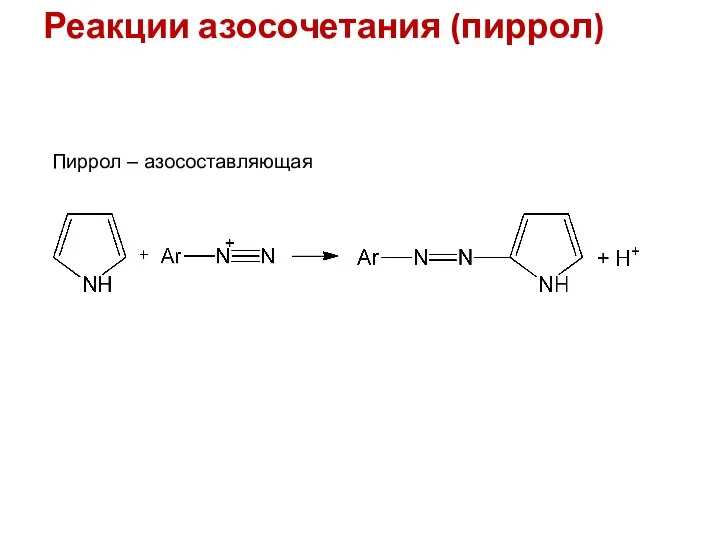
- 10. Реакции азосочетания (пиррол) Пиррол – азосоставляющая
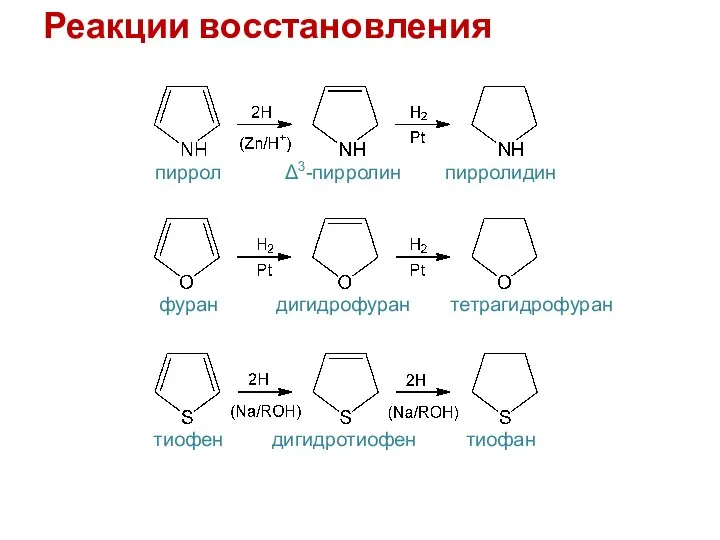
- 11. Реакции восстановления пиррол Δ3-пирролин пирролидин фуран дигидрофуран тетрагидрофуран тиофен дигидротиофен тиофан
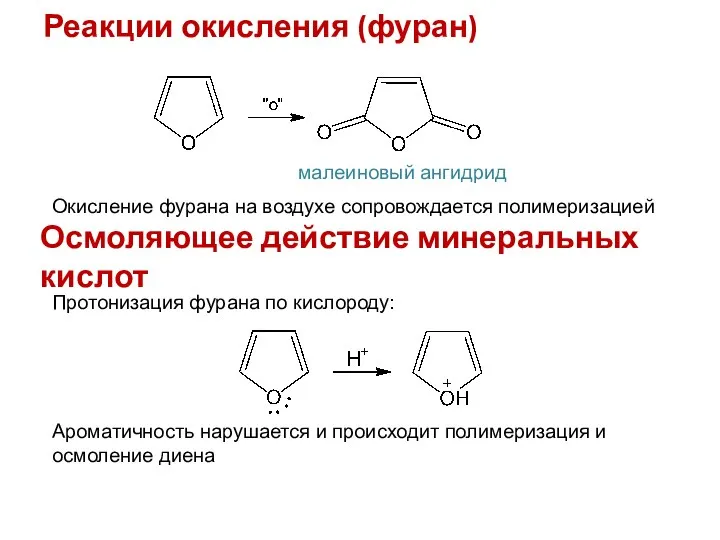
- 12. Реакции окисления (фуран) малеиновый ангидрид Окисление фурана на воздухе сопровождается полимеризацией Осмоляющее действие минеральных кислот Протонизация
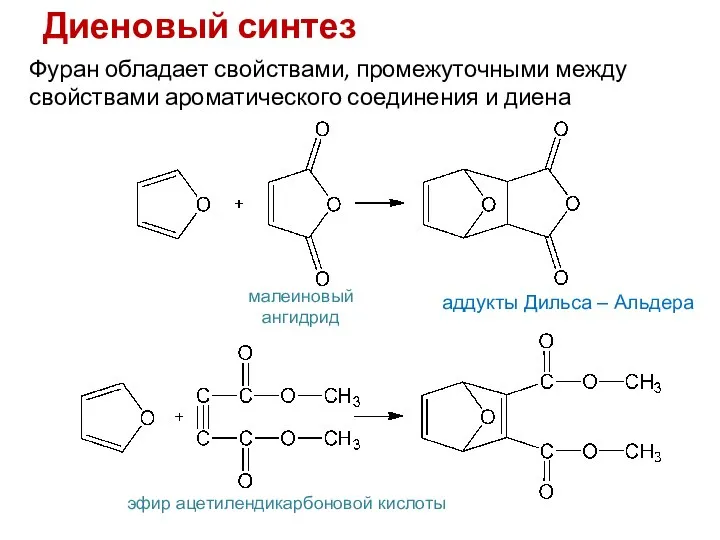
- 13. Диеновый синтез Фуран обладает свойствами, промежуточными между свойствами ароматического соединения и диена малеиновый ангидрид эфир ацетилендикарбоновой
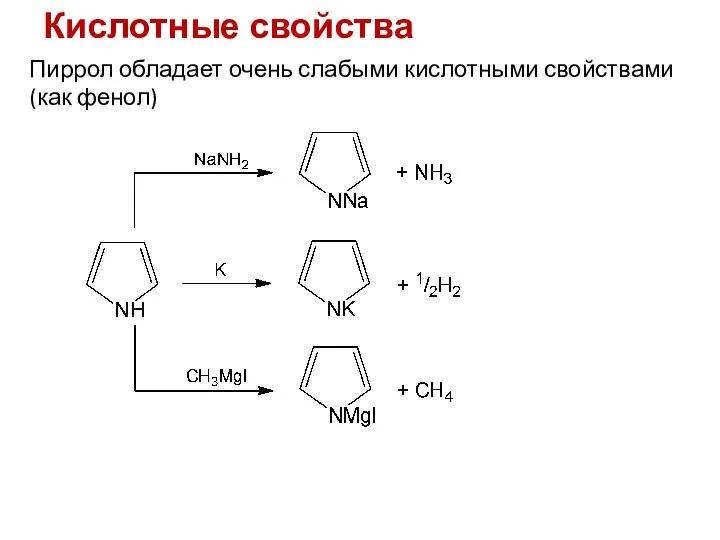
- 14. Кислотные свойства Пиррол обладает очень слабыми кислотными свойствами (как фенол)
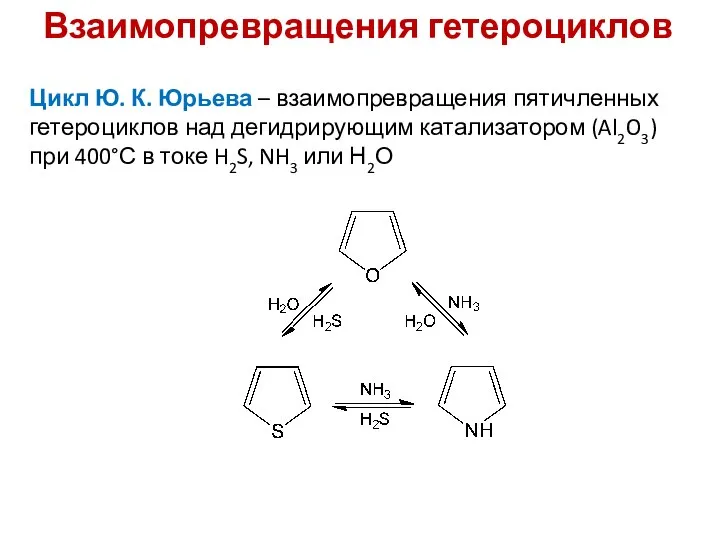
- 15. Взаимопревращения гетероциклов Цикл Ю. К. Юрьева – взаимопревращения пятичленных гетероциклов над дегидрирующим катализатором (Al2O3) при 400°С
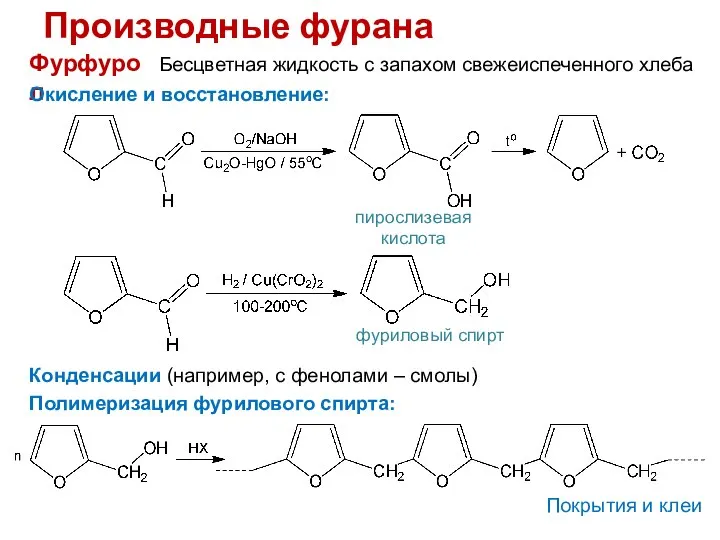
- 16. Производные фурана Фурфурол Бесцветная жидкость с запахом свежеиспеченного хлеба Окисление и восстановление: пирослизевая кислота фуриловый спирт
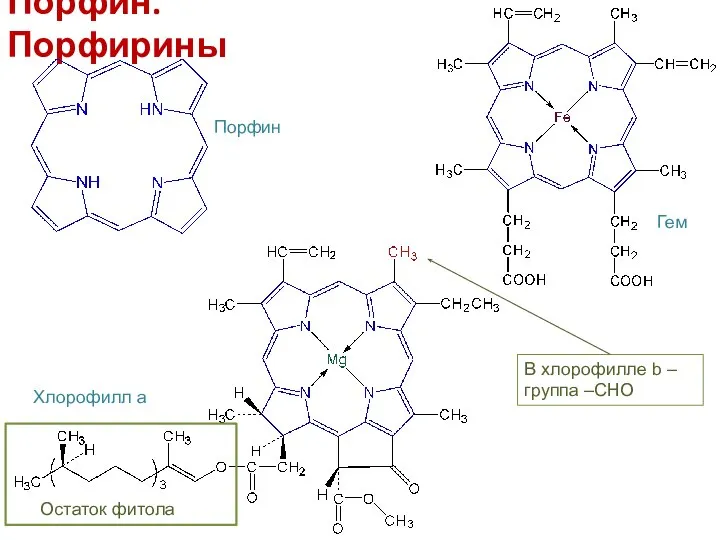
- 17. Порфин. Порфирины Порфин Гем Хлорофилл а Остаток фитола В хлорофилле b – группа –СНО
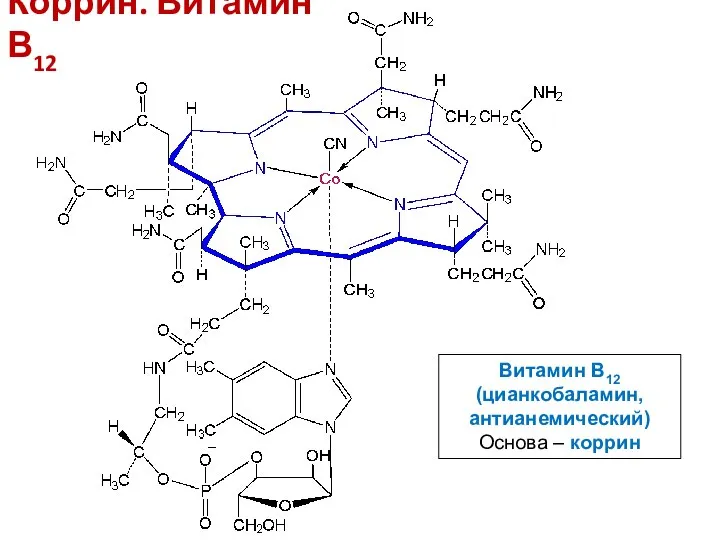
- 18. Коррин. Витамин В12 Витамин В12 (цианкобаламин, антианемический) Основа – коррин
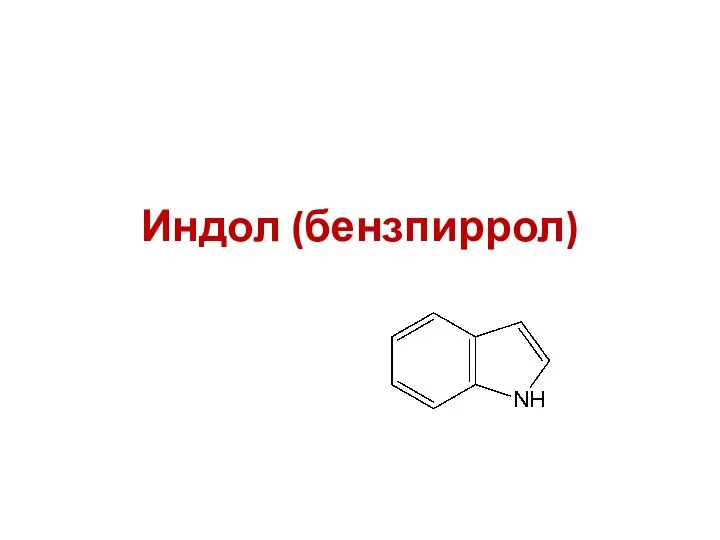
- 19. Индол (бензпиррол)
- 20. Получение Реакция Чичибабина Пропускают смесь паров анилина и ацетилена через раскаленные трубки Реакция Э. Фишера (гомологи
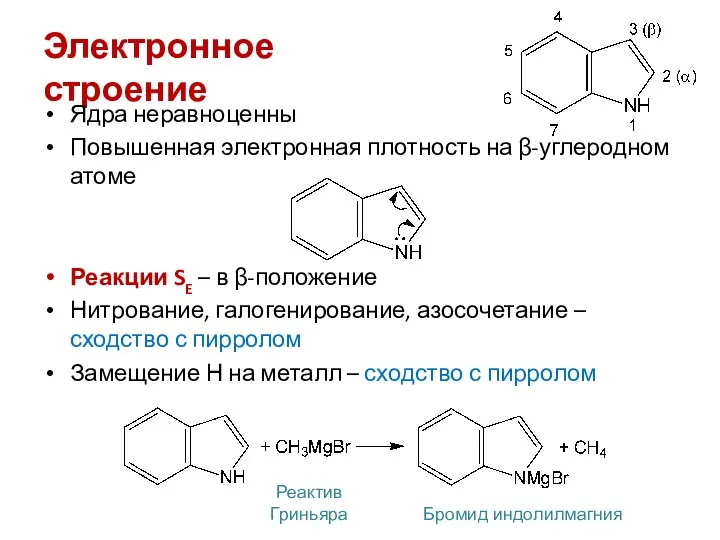
- 21. Электронное строение Ядра неравноценны Повышенная электронная плотность на β-углеродном атоме Реакции SE – в β-положение Нитрование,
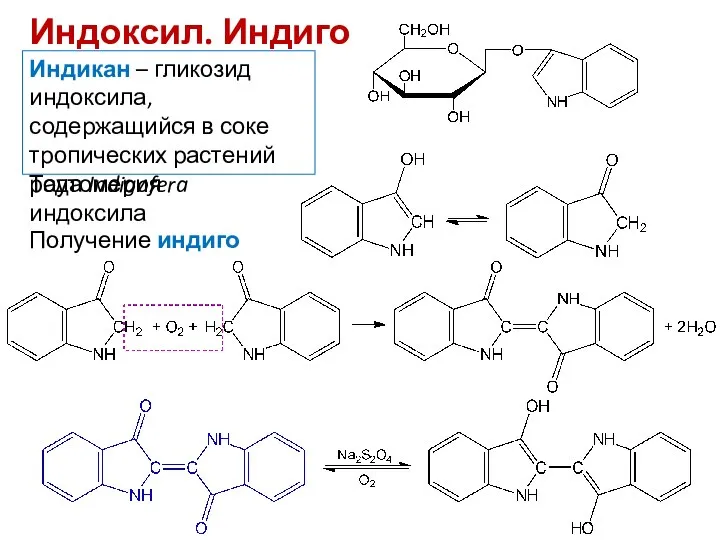
- 22. Индоксил. Индиго Индикан – гликозид индоксила, содержащийся в соке тропических растений рода Indigofera Таутомерия индоксила Получение
- 23. Индигокармин. Античный (тирский) пурпур 5,5'-индигосульфокислота 6,6'-диброминдиго
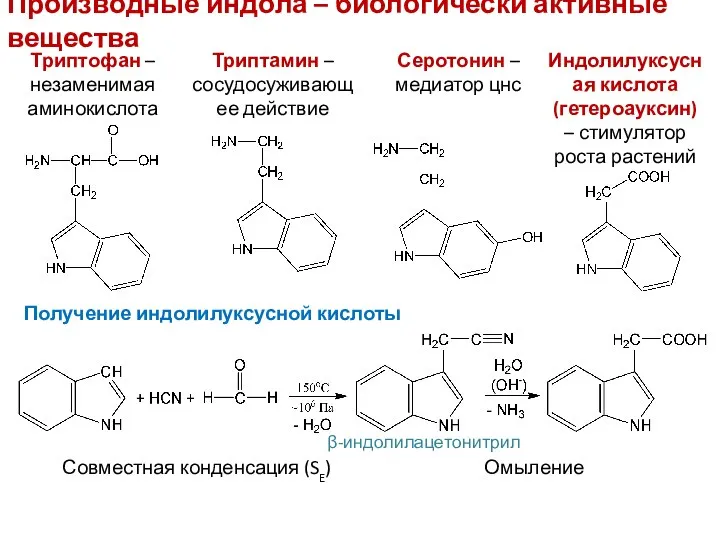
- 24. Производные индола – биологически активные вещества Триптофан – незаменимая аминокислота Триптамин – сосудосуживающее действие Серотонин –
- 25. Шестичленные гетероциклы с одним гетероатомом. Пиридин
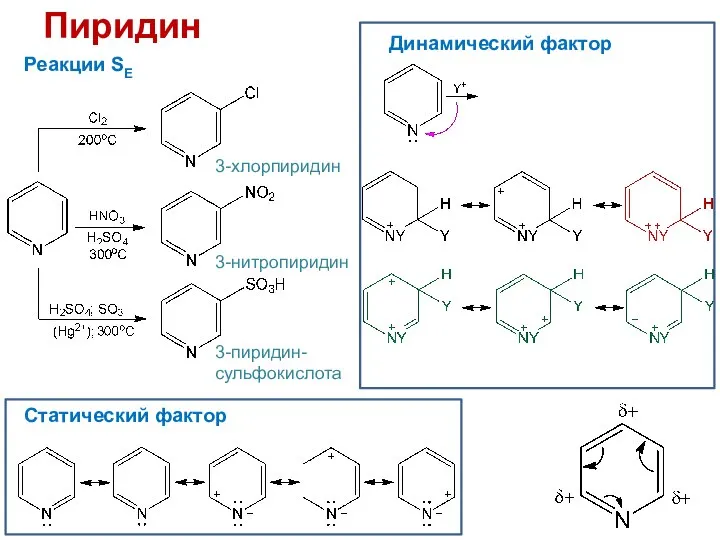
- 26. Пиридин Реакции SE 3-хлорпиридин 3-нитропиридин 3-пиридин-сульфокислота Статический фактор Динамический фактор
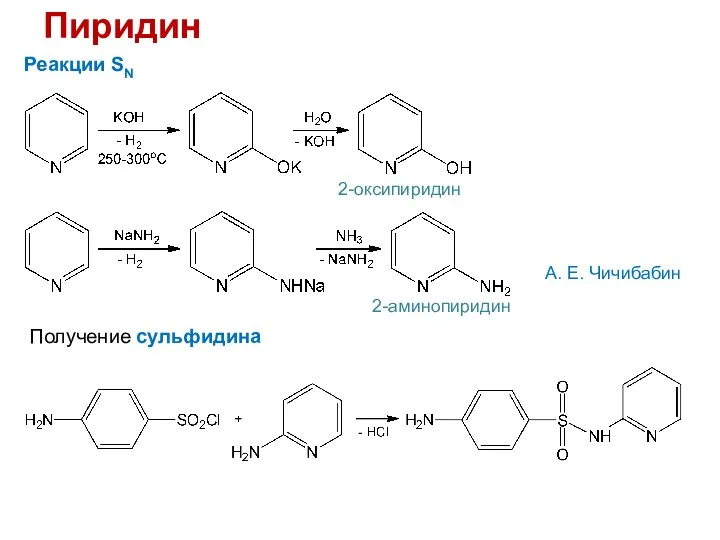
- 27. Пиридин Реакции SN 2-оксипиридин А. Е. Чичибабин 2-аминопиридин Получение сульфидина
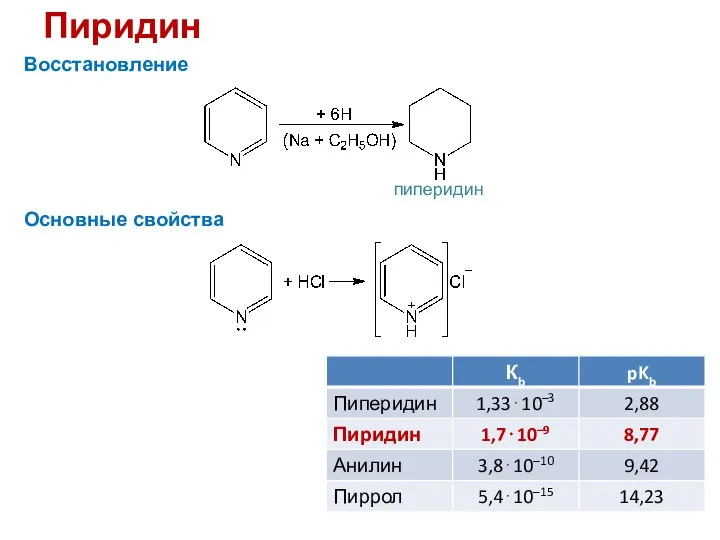
- 28. Пиридин Восстановление Основные свойства пиперидин
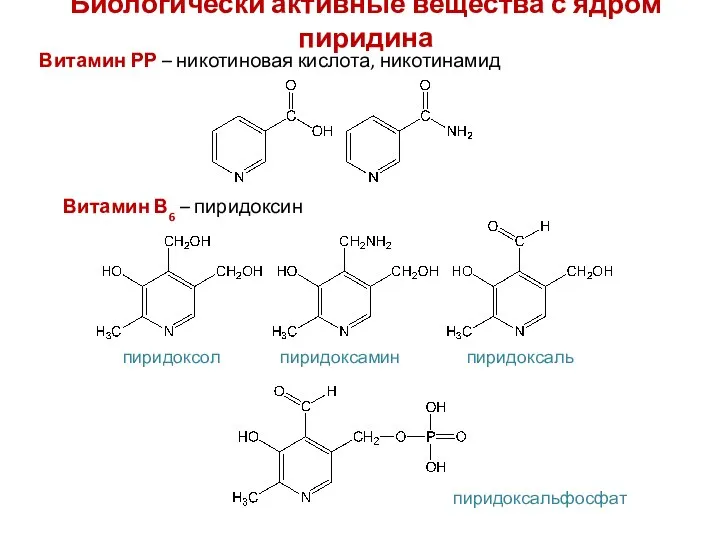
- 29. Биологически активные вещества с ядром пиридина Витамин РР – никотиновая кислота, никотинамид Витамин В6 – пиридоксин
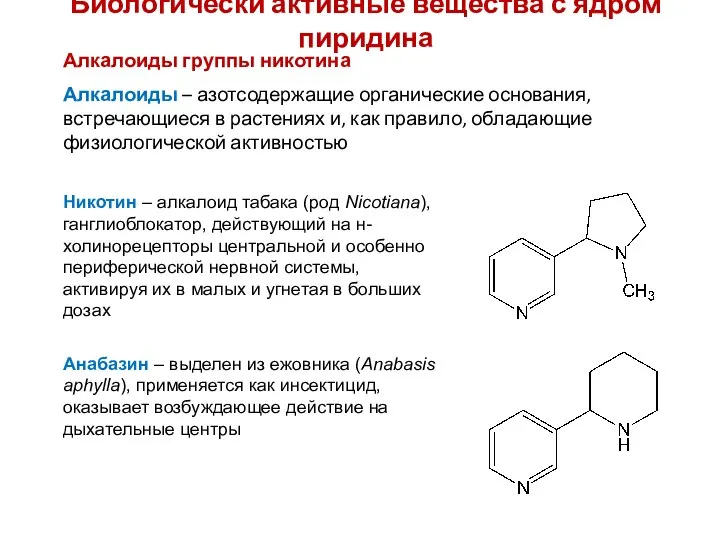
- 30. Биологически активные вещества с ядром пиридина Алкалоиды группы никотина Алкалоиды – азотсодержащие органические основания, встречающиеся в
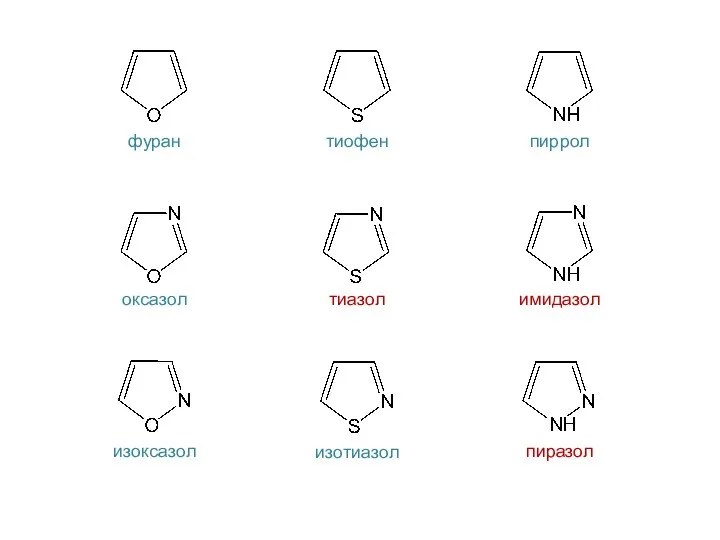
- 31. Пятичленные гетероциклы с двумя гетероатомами
- 32. фуран тиофен пиррол оксазол тиазол имидазол изоксазол изотиазол пиразол
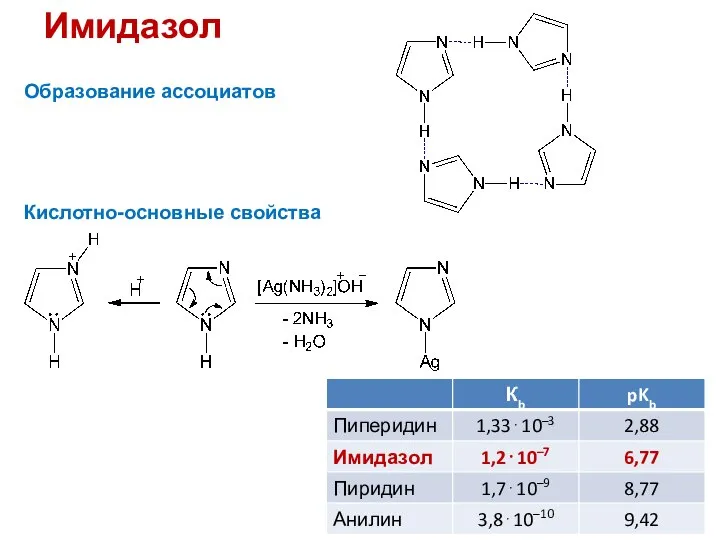
- 33. Имидазол Образование ассоциатов Кислотно-основные свойства
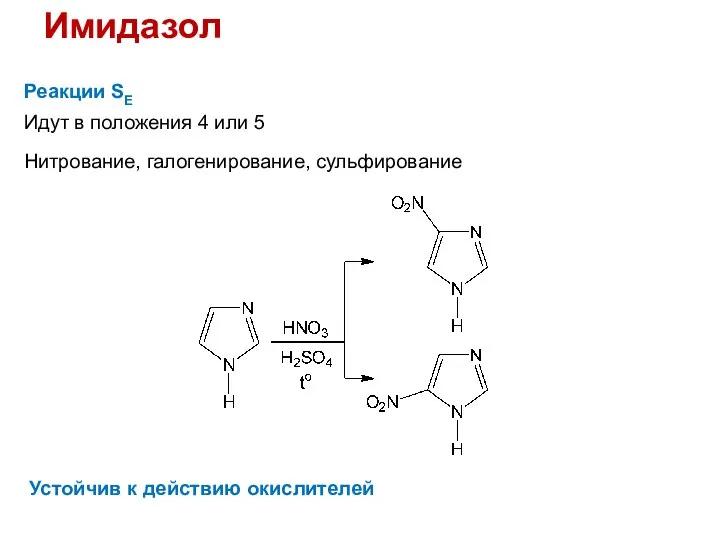
- 34. Имидазол Реакции SE Идут в положения 4 или 5 Нитрование, галогенирование, сульфирование Устойчив к действию окислителей
- 35. Производные имидазола – биологически активные вещества Гистидин – белковая аминокислота Гистамин – понижает кровяное давление, расширяет
- 36. Производные тиазола – биологически активные вещества Витамин В1 – тиамин Антибиотики Пенициллин G – бензилпенициллин Сульфаниламидные
- 37. Шестичленные гетероциклы с двумя гетероатомами
- 38. пиридазин пиразин пиримидин Диазины Азины оксазин тиазин
- 39. Пиримидиновые и пуриновые основания
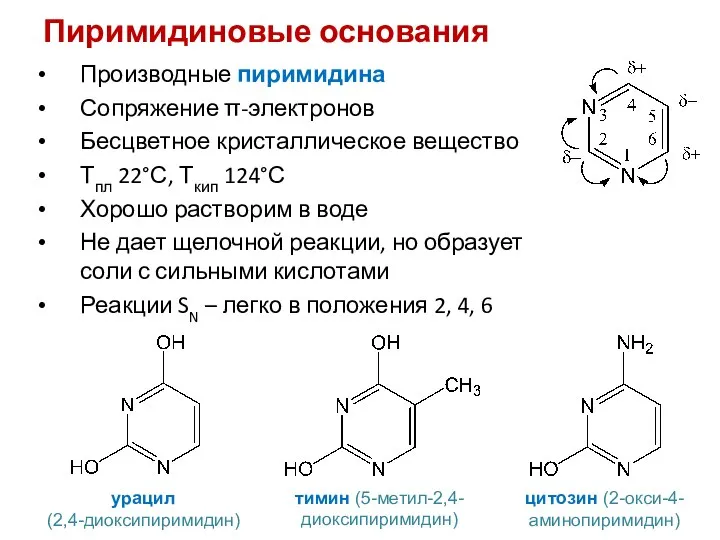
- 40. Пиримидиновые основания Производные пиримидина Сопряжение π-электронов Бесцветное кристаллическое вещество Тпл 22°С, Ткип 124°С Хорошо растворим в
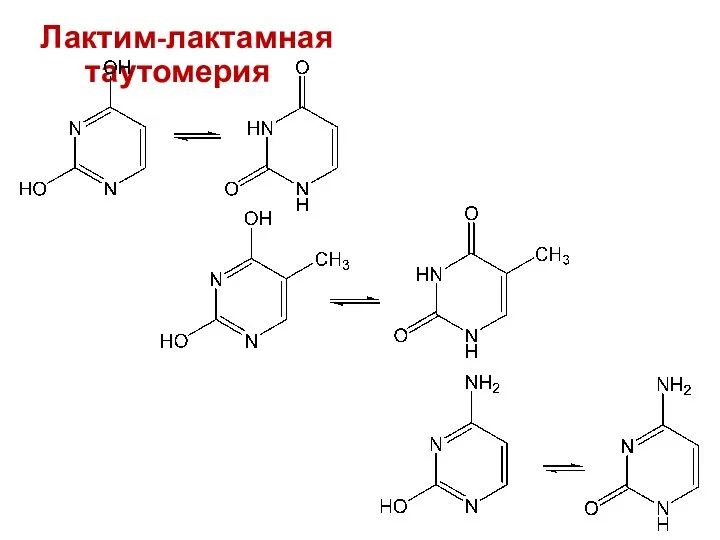
- 41. Лактим-лактамная таутомерия
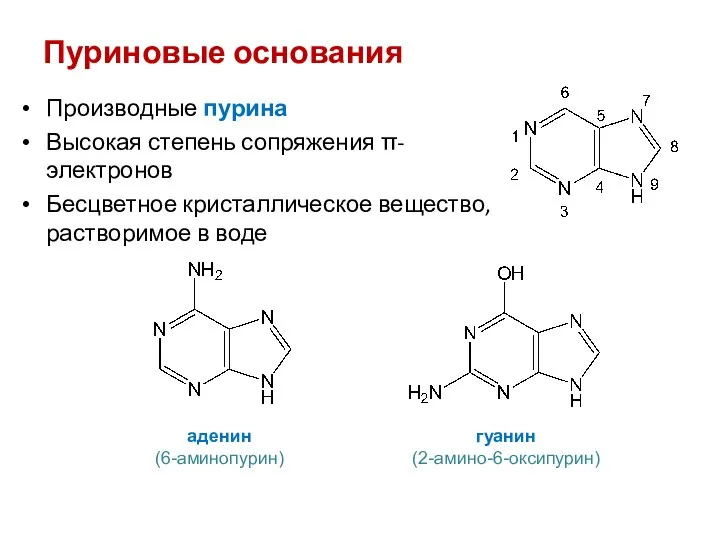
- 42. Пуриновые основания Производные пурина Высокая степень сопряжения π-электронов Бесцветное кристаллическое вещество, растворимое в воде аденин (6-аминопурин)
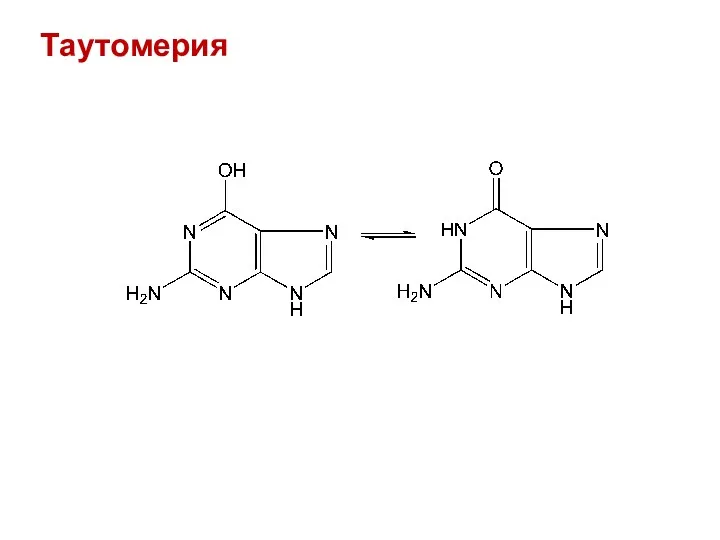
- 43. Таутомерия
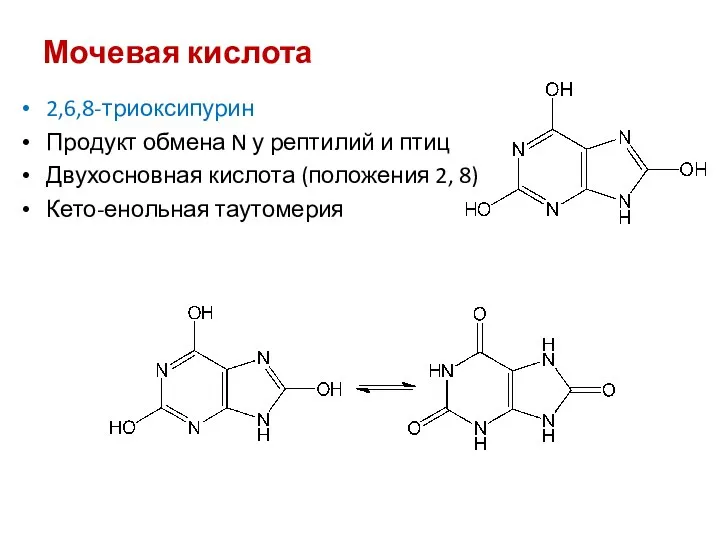
- 44. Мочевая кислота 2,6,8-триоксипурин Продукт обмена N у рептилий и птиц Двухосновная кислота (положения 2, 8) Кето-енольная
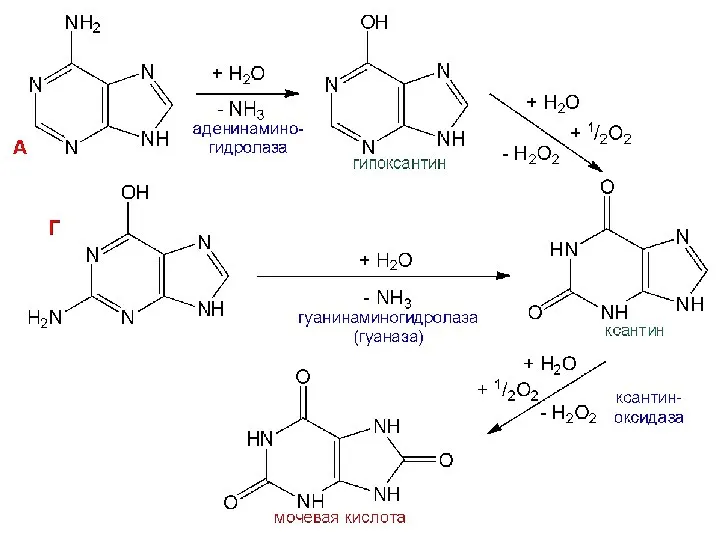
- 45. Распад пуриновых оснований Синтез мочевой кислоты
- 47. Распад пиримидиновых оснований
- 49. Скачать презентацию













 Фенолы Простые эфиры
Фенолы Простые эфиры Н2, NaCl, Ca, HCl
Н2, NaCl, Ca, HCl A laboratory examination of double replacement reaction
A laboratory examination of double replacement reaction Кремнийдің құрамы, құрылысы және қасиеттері
Кремнийдің құрамы, құрылысы және қасиеттері Химиялык байланыстар
Химиялык байланыстар Аттестационная работа. Химические опыты с лекарственными веществами и лабораторный практикум
Аттестационная работа. Химические опыты с лекарственными веществами и лабораторный практикум Основы органической химии. Кислородсодержащие органические соединения
Основы органической химии. Кислородсодержащие органические соединения Химия гетероциклических соединений
Химия гетероциклических соединений Ленгмюр адсорбциясының мономолекулярлық теориясы. Дәріс 11
Ленгмюр адсорбциясының мономолекулярлық теориясы. Дәріс 11 Химия в быту
Химия в быту Химическая картина мира
Химическая картина мира Особенности решения практикоориентированного задания №26 ГИА-11
Особенности решения практикоориентированного задания №26 ГИА-11 Азот в природе
Азот в природе Аттестационная работа. Мини-проекты на уроках химии. 8 класс
Аттестационная работа. Мини-проекты на уроках химии. 8 класс Характеристика высших гидроксидов по положению в ПСХЭ
Характеристика высших гидроксидов по положению в ПСХЭ Органические соединения и их классификация
Органические соединения и их классификация Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные
Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные  Классификация химических реакций в органической и неорганической химии
Классификация химических реакций в органической и неорганической химии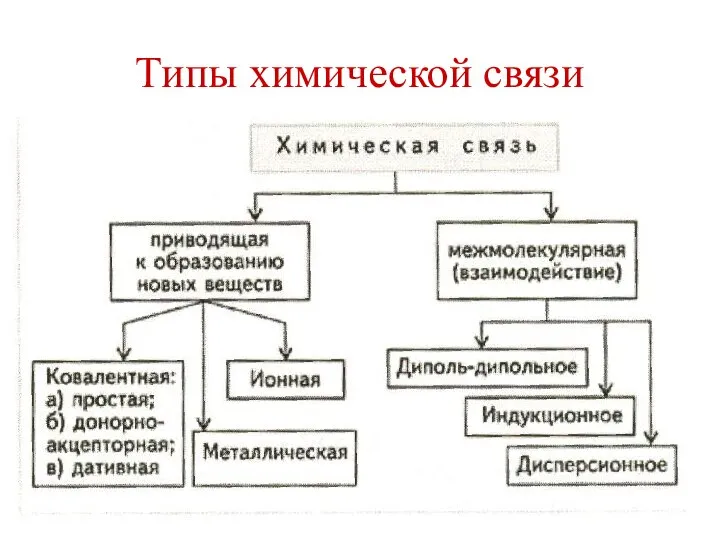 Типы химической связи
Типы химической связи  Общая фармакопейная статья
Общая фармакопейная статья Сероводород. Сульфиды
Сероводород. Сульфиды Строение и химические свойства кислот
Строение и химические свойства кислот Весь смысл жизни заключается в бесконечном завоевании неизвестного, в вечном усилии познать больше Эмиль Золя
Весь смысл жизни заключается в бесконечном завоевании неизвестного, в вечном усилии познать больше Эмиль Золя  Воздух- разделение на компоненты
Воздух- разделение на компоненты Галогены. Фтор, хлор, бром, йод, астат
Галогены. Фтор, хлор, бром, йод, астат Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Лекарственное растительное сырье, содержащее витамины
Лекарственное растительное сырье, содержащее витамины ПРЕЗЕНТАЦИЯ КАБИНЕТА ХИМИИ
ПРЕЗЕНТАЦИЯ КАБИНЕТА ХИМИИ