Содержание
- 2. Частицы растворенного вещества в воде окружены гидратной оболочкой. В некоторых случаях это приводит к химическому взаимодействию
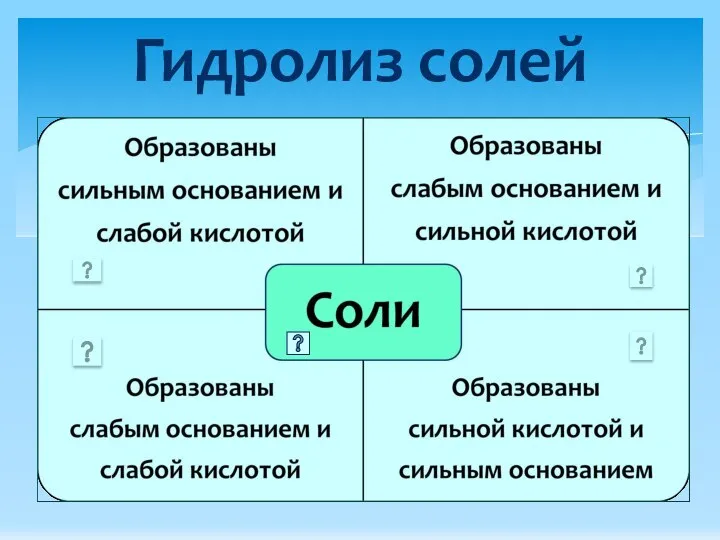
- 3. Гидролиз солей
- 4. Определение реакций среды растворов солей универсальным индикатором
- 5. Алгоритм составления уравнений гидролиза солей 1. Записать уравнение диссоциации соли; 2. Выбрать слабый ион; 3. Записать
- 6. Гидролиз солей, образованных слабым основанием и слабой кислотой: Al2 (CO3)3 ↔ 2Al3+ + 3CO32─ H2O ↔
- 7. Необратимый гидролиз солей, образованных слабым основанием и слабой кислотой: 3Na2CO3 + 2AlCl3 → Al2(CO3)3 + 6NaCl
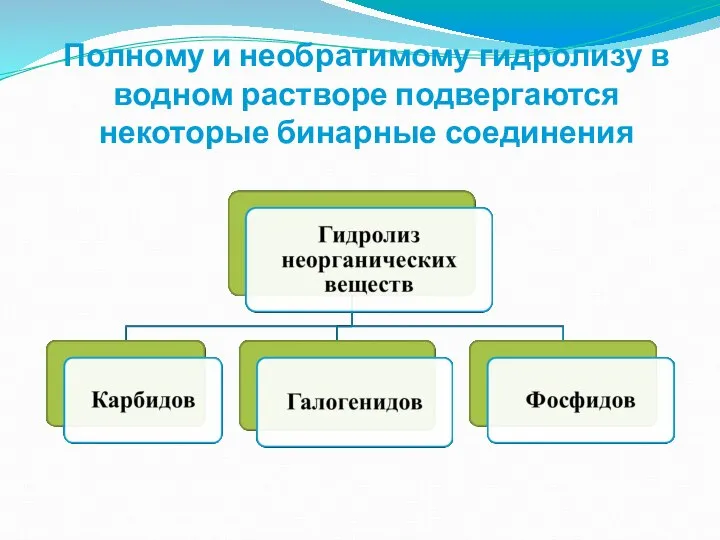
- 8. Полному и необратимому гидролизу в водном растворе подвергаются некоторые бинарные соединения
- 9. Гидролиз бинарных соединений Гидролиз фосфидов: Са3P2 + 6H2O = 3Са(OH)2 + 2PH3↑ фосфид фосфин кальция Гидролиз
- 10. Факторы, влияющие на условия протекания гидролиза 1. Химическая природа соли 2. Температура 3. Концентрация соли 4.
- 12. Условия смещения реакций обратимого гидролиза (согласно принципу Ле Шателье) Усилить гидролиз соли можно следующими способами: Добавить
- 13. Тест 1.Гидролизу по катиону и аниону подвергается соль : А) K2S, Б) KCl, В)(NH4)2CO3 , Г)
- 14. Ответы к тесту. 1. 1-3 2. А-2 Б-3 В-1 3. А-4 Б-1 В-2 Г-2 4. А-1
- 15. Роль гидролиза: В природе: преобразование земной коры; обеспечение слабощелочной среды морской воды. В народном хозяйстве: выработка
- 17. Скачать презентацию












 Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно
Презентация по Химии "Вода для жизни!" - скачать смотреть бесплатно Тема: “Обобщение сведений об основных классах неорганических соединений”.
Тема: “Обобщение сведений об основных классах неорганических соединений”. Коррозия (лат. corrosio — жегіде)- қоршаған ортаның әсерінен метал бетінің бүлінуі
Коррозия (лат. corrosio — жегіде)- қоршаған ортаның әсерінен метал бетінің бүлінуі Основные понятия и законы химии. Эквивалент. Закон эквивалентов. Закон титрования
Основные понятия и законы химии. Эквивалент. Закон эквивалентов. Закон титрования Пресная природная вода
Пресная природная вода Күкірт қышқылы
Күкірт қышқылы Синтетические каучуки и их применение
Синтетические каучуки и их применение Вольфрам. Знаходження в періодичній системі
Вольфрам. Знаходження в періодичній системі Презентация Алкины Ацетилен
Презентация Алкины Ацетилен Единица количества вещества - моль
Единица количества вещества - моль Жёсткость воды
Жёсткость воды Миючі засоби Виконала учениця 9-А класу, Велітченко Юлія
Миючі засоби Виконала учениця 9-А класу, Велітченко Юлія  Фосфор. Строение и свойства
Фосфор. Строение и свойства Элемент цинк
Элемент цинк Л3.12 Композицитонные материалы
Л3.12 Композицитонные материалы Хроматофокусирование: новые подходы в концентрировании и разделении
Хроматофокусирование: новые подходы в концентрировании и разделении Глицерин. Основные способы получения
Глицерин. Основные способы получения Химический состав клетки
Химический состав клетки Кислоты: названия, получение, свойства, применение
Кислоты: названия, получение, свойства, применение Сплавы металлов. Жиляев Дмитрий МОБУ СОШ №2 октябрь 2012
Сплавы металлов. Жиляев Дмитрий МОБУ СОШ №2 октябрь 2012  Пестициды. Классификация ядохимикатов в клинической фармации
Пестициды. Классификация ядохимикатов в клинической фармации Давайте повторим Заключительный урок в 8 классе
Давайте повторим Заключительный урок в 8 классе  Горение топлива
Горение топлива Введение в органическую химию. 10 класс
Введение в органическую химию. 10 класс ГИДРОЛИЗ СОЛЕЙ 9 класс
ГИДРОЛИЗ СОЛЕЙ 9 класс Презентация по Химии "Техника безопасности на уроках химии" - скачать смотреть
Презентация по Химии "Техника безопасности на уроках химии" - скачать смотреть  Диагенез и катагенез горных пород
Диагенез и катагенез горных пород Опис технологічного процесу отримання смол бекелітових рідких марок
Опис технологічного процесу отримання смол бекелітових рідких марок