Содержание
- 2. Химия элементов IVA группы
- 3. Электронные конфигурации в основном и возбужденном состоянии ns2np2 CH4, CS2, CO2, CH3CH2OH CO, CN- Валентность =
- 4. Распространенность и минералы C – 11 место, CO2, CaCO3 (известняк, кальцит, мрамор), уголь, нефть, природный газ
- 5. Открытие элементов C – известен с древнейших времен; лат. «карбон» – уголь Si – 1883 г.,
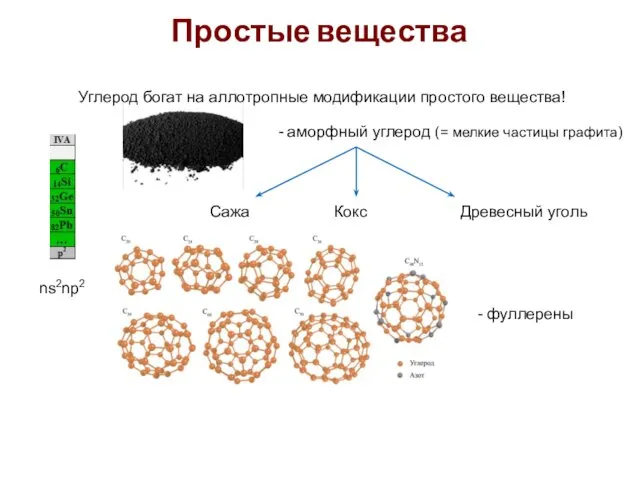
- 7. Простые вещества ns2np2 Углерод богат на аллотропные модификации простого вещества! - графит (2d полимер) - алмаз
- 8. ns2np2 Углерод богат на аллотропные модификации простого вещества! - аморфный углерод (= мелкие частицы графита) Сажа
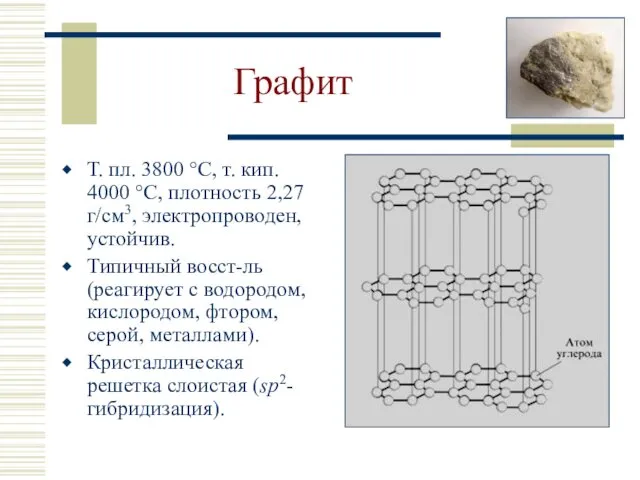
- 9. Графит Т. пл. 3800 °С, т. кип. 4000 °С, плотность 2,27 г/см3, электропроводен, устойчив. Типичный восст-ль
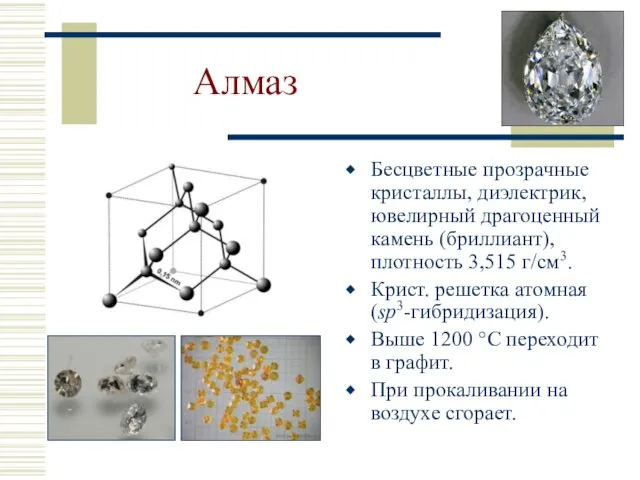
- 10. Алмаз Бесцветные прозрачные кристаллы, диэлектрик, ювелирный драгоценный камень (бриллиант), плотность 3,515 г/см3. Крист. решетка атомная (sp3-гибридизация).
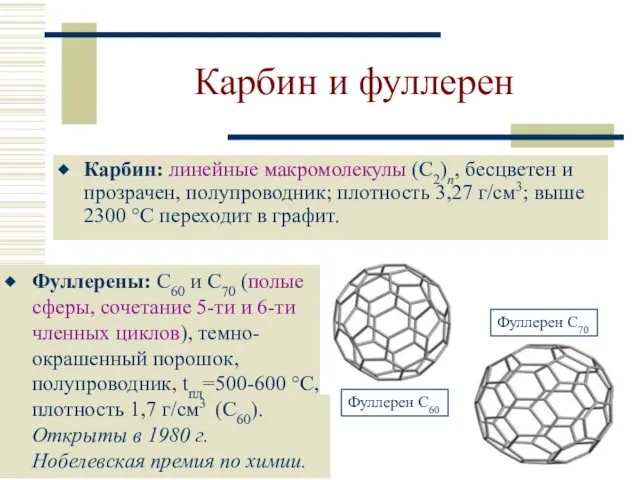
- 11. Карбин и фуллерен Карбин: линейные макромолекулы (С2)n, бесцветен и прозрачен, полупроводник; плотность 3,27 г/см3; выше 2300
- 14. Основные степени окисления +4 CO2, COCl2, CCl4, SCN-, Na2CO3, KHCO3 +2 CN–, CO 0 C –1
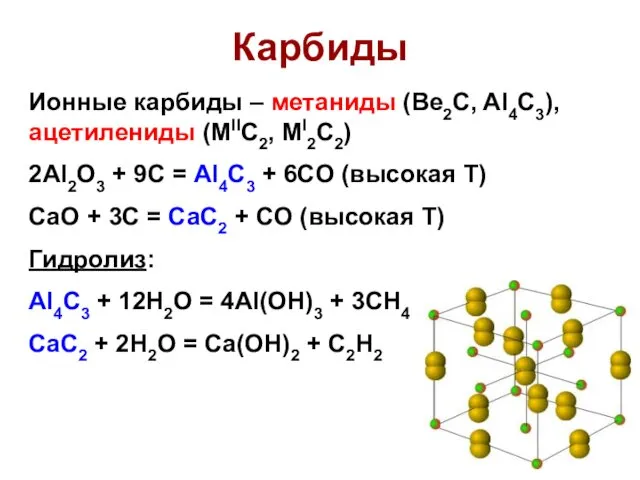
- 17. Карбиды Карбиды подразделяются на следующие виды: 1) ионные / солеобразные (CaC2, Al4C3); 2) молекулярные; 3) ковалентные
- 18. Карбиды Ионные карбиды – метаниды (Be2C, Al4C3), ацетилениды (MIIC2, MI2C2) 2Al2O3 + 9C = Al4C3 +
- 19. СО 1) Получение в промышленности: CO2 + C кокс = 2CO (при Т) С + H2O
- 20. Свойства СО 1) При н.у. нерастворим в воде, кислотах и щелочах (несолеобразующий) 2) Но солеобразующий при
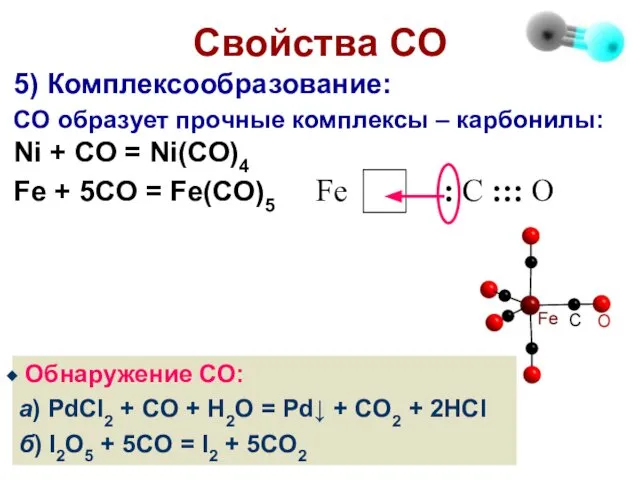
- 21. Свойства СО 5) Комплексообразование: CO образует прочные комплексы – карбонилы: Ni + CO = Ni(CO)4 Fe
- 22. СO2 1) Получение в промышленности: СaCO3 = CaO + CO2 (Т) С + O2 = CO2
- 23. Свойства СO2 1) Не поддерживает горение 2) Окислитель: а) активные металлы (Mg, Na, K) горят в
- 24. Моногидрат CO2 . H2O и угольная кислота H2CO3 В водном растворе: CO2 (г) + H2O ⮀
- 26. Галогениды и оксогалогениды углерода CX4: X = F, Cl, Br, I (газ ? твердое), не реагируют
- 27. Соединения С с S CS2 – сероуглерод, tкип. = 44 оС, легко возгорается, растворитель для P4,
- 28. Соединения с N HCN – циановодород, tкип. = 26 оС, ядовит, растворим в воде Таутомерия: H–C≡N
- 29. Получение кремния: SiO2 +2C = 2CO + Si (1900oC) SiO2 + 2Mg = 2MgO + Si
- 30. Свойства кремния 1) Реакции с простыми веществами: Si + O2 = SiO2 (при Т) Si +
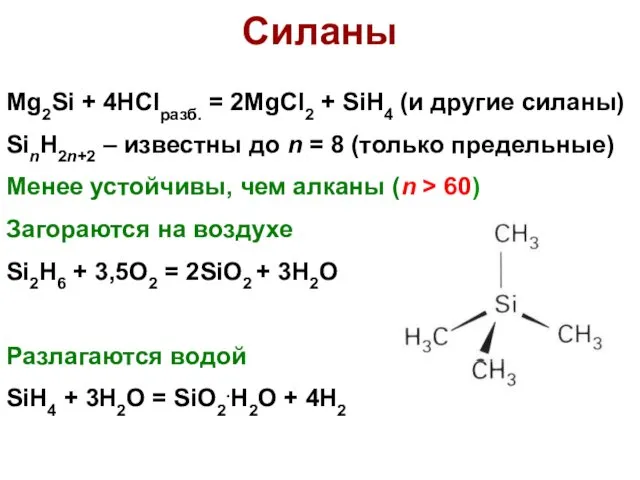
- 31. Cиланы Mg2Si + 4HClразб. = 2MgCl2 + SiH4 (и другие силаны) SinH2n+2 – известны до n
- 32. Связи Si–O–Si SiO2 Аметист, агат, сердолик оникс, яшма E = O, NH Cиликоновые полимеры
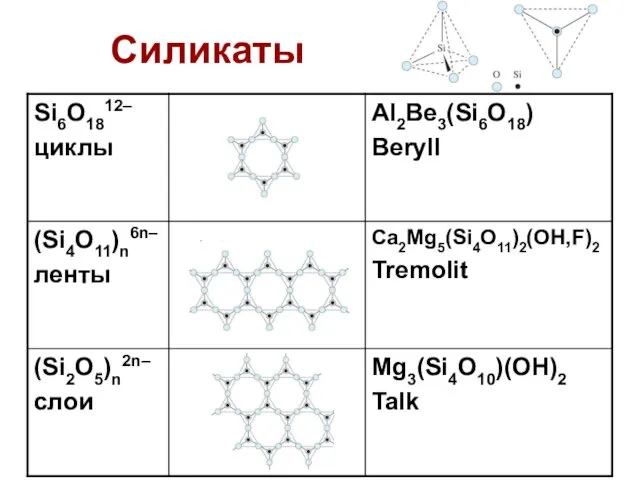
- 34. Силикаты (тысячи минералов)
- 35. Силикаты
- 36. SiO2 Свойства SiO2: Н/р в воде, минеральных кислотах, растворах щелочей SiO2 + 6HF = H2[SiF6] +
- 37. Кремневые кислоты Получение: действие минеральных к-т на р-ры силикатов; гидролиз галогенидов: Na2SiO3 + HCl xSiO2·yH2O +
- 38. Ge, Sn, Pb Увеличение металлических свойств в ряду Ge–Sn–Pb Простые вещества: Ge – структура алмаза, по
- 39. Получение Ge, Sn, Pb
- 40. Свойства Ge, Sn, Pb 1) С кислотами неокислителями: Ge нет реакции. Sn + 2HCl = SnCl2
- 41. Pb + 3H2SO4 конц. = Pb(HSO4)2 + SO2 + 2H2O 3) С щелочами: Ge – нет
- 42. ЭО2 (Э = Ge, Sn, Pb) GeO2 + 4HClконц. = GeCl4 + 2H2O GeO2 + 2NaOHр-р
- 43. Кислоты Э4+ (Э = Ge, Sn) xЭО2·yH2O – неопределенный состав. α и β-формы xЭО2·yH2O (x Растворы
- 44. Оловянные кислоты xSnО2.yH2O α: x Sn(OH)4 + 2H2SO4 разб. = Sn(SO4)2 + 4H2O Sn(OH)4 + 2KOHр-р
- 45. Соединения Pb4+ Pb(OAc)2 + CaOCl2 + H2O = PbO2↓+ CaCl2 + 2HOAc PbO2 + H2SO4 конц.
- 46. Свинцовый сурик 6PbO + O2 = 2Pb3O4 (400-500 oC) красно-оранжевый PbII2PbIVO4 (ортоплюмбат свинца) 2Pb3O4 = 6PbO
- 47. Соединения Э2+ (Э = Ge, Sn, Pb) Ox-Red свойства Уменьшение восстановительных свойств в ряду Ge–Sn–Pb (для
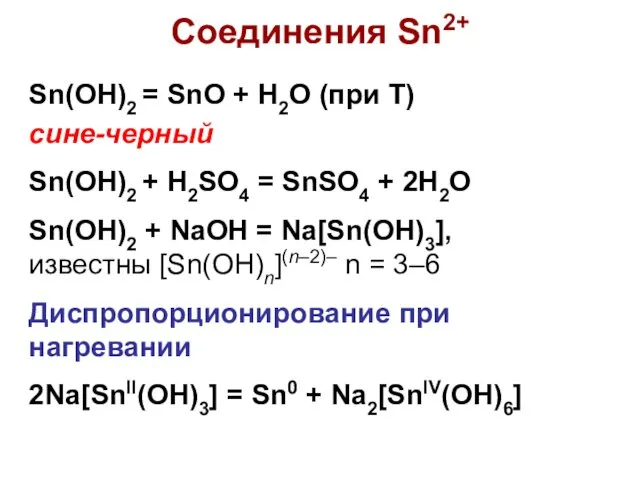
- 48. Соединения Sn2+ Sn(OH)2 = SnO + H2O (при Т) сине-черный Sn(OH)2 + H2SO4 = SnSO4 +
- 49. Растворимые соли SnX2: X = Cl, Br, I, NO3, ½SO4 Гидролиз: Sn2+ + H2O = Sn(OH)+
- 50. Соединения Pb2+ PbO – желтый или красный 2Pb + O2 = 2PbO (в расплаве свинца) PbO2
- 51. Примеры Ox-Red Sn2+ – удобный мягкий восстановитель 2MnO4– + 5Sn2+ + 16H+ = 2Mn2+ +5Sn4+ +
- 53. Скачать презентацию








































 Фтор (Fluorum), F
Фтор (Fluorum), F Введение. Основные понятия химии
Введение. Основные понятия химии Органічні сполуки в побуті Виконав Учень 11-Т класу ЗОШ №1 Новак Сергій
Органічні сполуки в побуті Виконав Учень 11-Т класу ЗОШ №1 Новак Сергій  Интеллектуальная викторина по химии для учащихся 8-9 классов
Интеллектуальная викторина по химии для учащихся 8-9 классов Хімічні явища в природі
Хімічні явища в природі Алканы
Алканы Ферменти. Історія вчення про ферменти
Ферменти. Історія вчення про ферменти Презентация Лекарства дома
Презентация Лекарства дома Липиды. Строение, свойства, функции. (Лекция 6)
Липиды. Строение, свойства, функции. (Лекция 6) Свойства живого вещества
Свойства живого вещества Применение нитратов
Применение нитратов  Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Исторические аспекты возникновения и развития. Теории химического строения
Исторические аспекты возникновения и развития. Теории химического строения Химия в косметике
Химия в косметике Кристаллическая структура и магнитные свойства нестехиометрических кобальтитов RBaCo4O7+x (x=0,0.1,0.2)
Кристаллическая структура и магнитные свойства нестехиометрических кобальтитов RBaCo4O7+x (x=0,0.1,0.2) “ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман
“ КОРОЗІЯ МЕТАЛІВ. ЗАХИСТ ВІД КОРОЗІЇ ” Підготував: Учень 10-А класу ЗОШ №25 м. Луцька Матвійчук Роман  Геологические условия формирования месторождений полезных ископаемых. (Лекция 3)
Геологические условия формирования месторождений полезных ископаемых. (Лекция 3) Фармацевтические суспензии и эмульсии
Фармацевтические суспензии и эмульсии Геохимия техногенеза
Геохимия техногенеза Кристаллическая решетка
Кристаллическая решетка Сера
Сера Комбинированные задачи. 11 класс. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Комбинированные задачи. 11 класс. Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  ЕГЭ по химии Технология подготовки учащихся
ЕГЭ по химии Технология подготовки учащихся педагогический стаж -11 лет, год окончания вуза - 2000, вуз - Бирский государственный педагогический институт, факультет -биолого
педагогический стаж -11 лет, год окончания вуза - 2000, вуз - Бирский государственный педагогический институт, факультет -биолого Методы определения подлинности лекарственного растительного сырья
Методы определения подлинности лекарственного растительного сырья Алканы. Получение и применение алканов
Алканы. Получение и применение алканов Виды и свойства текстильных материалов из химических волокон. 6 класс
Виды и свойства текстильных материалов из химических волокон. 6 класс Оксиды: получение, свойства, применение
Оксиды: получение, свойства, применение